Структурно-функциональная характеристика бактериального консорциума, выделенного из техногенных почв Верхнекамского месторождения солей
Автор: Ястребова О.В., Кошелева И.А., Плотникова Е.Г.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 3, 2016 года.
Бесплатный доступ
Из почвы района солеразработок (г. Березники, Пермский край), выделен бактериальный консорциум SMB1, способный к эффективному росту на нафталине в качестве единственного источника углерода и энергии в присутствии до 10% NaCl. В его состав входят два галотолерантных деструктора нафталина рода Arthrobacter (штаммы SMB145 =ВКМ Ac-2551, SMB11 =ВКМ Ac-2552), а также галотолерантный штамм Brevibacterium permense SMB14 (=ВКМ Ас-2280Т =LMG 22207Т) и галофильный штамм Chromohalobacter sp. SMB17, не утилизирующие нафталин. При совместном культивировании трех штаммов: Arthrobacter sp. SMB145, Brevibacterium permense SMB14 и Chromohalobacter sp. SMB17 на нафталине при повышенной минерализации среды (7% NaCl) наблюдались более высокие ростовые показатели штамма-деструктора Arthrobacter sp. SMB145 по сравнению с аналогичными данными, полученными при его культивировании индивидуально. Интенсивность дыхания бактериального консорциума SMB1 также была выше таковой штамма SMB145 при выращивании на нафталине в присутствии 5%-ного NaCl. Выделенный бактериальный консорциум SMB1 может быть рекомендован для разработки новых биотехнологий очистки загрязненных почв и стоков в условиях засоления.
Биодеградация, полициклические ароматические углеводороды, ассоциации бактерий, галотоле-рантные и галофильные бактерии
Короткий адрес: https://sciup.org/147204779
IDR: 147204779 | УДК: 579.262:57.083.18
Structural and functional characteristics of bacterial consortium, isolated from technogenic soils of the Verkhnekamsk salt deposit
The consortium of microorganisms SMB1, capable of efficient growing on naphthalene as a sole source of carbon and energy in the presence of 10% NaCl has been isolated from soil of potassium salt mining region (Berezniki, Perm krai). The consortium consists of two halotolerant bacterial strains-destructors of naphthalene, namely Arthrobacter sp. (strains SMB145 =ВКМ Ac-2551, SMB11 =ВКМ Ac-2552), halotolerant strain Brevibacterium permense SMB14 (=ВКМ Ас-2280Т =LMG 22207Т) and halophile strain Chromohalobacter sp. SMB17 incapable of naphthalene utilization. During co-cultivation of the three strains Arthrobacter sp. SMB145, Brevibacterium permense SMB14 and Chromohalobacter sp. SMB17 on naphthalene at 7% NaCl higher growth parameters of the strain destructor Arthrobacter sp. SMB145 have been observed compared to individual strain cultivation. The bacterial consortium SMB1 respiration rate was higher in comparison to the individual strain SMB145 cultivation on naphthalene at 5% NaCl. Isolated bacterial consortium SMB1 can be recommended for the development of new biotechnologies for the treatment of polluted soils and wastewater under the conditions of salinization.
Текст научной статьи Структурно-функциональная характеристика бактериального консорциума, выделенного из техногенных почв Верхнекамского месторождения солей
Полициклические ароматические углеводороды (ПАУ) относят к числу наиболее распространенных, экологически опасных, устойчивых соедине ний, накапливающихся в окружающей среде как в результате природных процессов, так и в результате промышленной деятельности человека. Способ-
(С Ястребова О. В., Кошелева И. А., Плотникова Е Г., 2016
ность к утилизации или трансформации ди- и три-кольцевых ароматических углеводородов (нафталин, фенантрен) обнаружена у многих природных бактерий [Cemiglia 1992; Habe, Omori, 2003]. В ряде случаев загрязнение почв и водоемов промышленными отходами. содержащими токсичные соединения сопровождается другими неблагоприятными факторами, в частности, повышенной концентрацией солей. В таких условиях возможность биодеградации ПАУ определяется устойчивостью бактерий к повышенной минерализации среды и способностью проявлять при этом биодеградатив-ные свойства.
Из высокоминерализованных сред, таких как моря, лиманы, солончаковые болота, морские осадки, пластовые воды нефтедобычи выделены галотолерантные и галофильные бактерии, способные разлагать алканы, моно- и полиароматические углеводороды в условиях повышенной солености среды (1.0-10%) [Dalvi et al.. 2012; Feng et al., 2012; Al-Mailem et al., 2013]. В литературе приводятся данные о способности штаммов родов ^г- hodom onas, Мarinobacter, Haiom on as, Cbrom o-halobacter к деструкции моноароматических углеводородов (бензола. толуола. фенола, бензоата, салицилата) в присутствии 1-10%^ного NaCl в среде культивирования [Kim et at. 2008: Berlendis ct at, 2010; Dalvi et aL 2012: Bonfa ct al.. 2013]. Бактериальная деструкция ПАУ, в частности нафталина, фенантрена и антрацена, при высокой солености среды (до 9% NaCl) описана для бактерий родов Micrococcus, Pseudomonas, Mannobacter, Marteleda, Arthrobacter [Плотникова и др,. 2001: Ashok et al.. 1995; Feng et al., 2012: Al-Mailem et al.. 2013].
В ряде исследований показано, что сообщества микроорганизмов, выделенные из засоленных почв, солончаковых болот, прибрежных зон, более эффективно утилизируют ПАУ в условиях высокого засоления среды, чем индивидуальные штаммы-деструкторы [Таш, 2002; Dastgheib et al., 2012; Moghadam ct al., 2014]. В составе бактериального консорциума Qplie, растущего на фенантрене в присутствии до 17% NaCl, выявлен штамм-деструктор фенантрена рода A/flrtrtoZwcter и штамм Halomonas sp., утилизирующий метаболиты фенантрена [Dastgheib et al., 2012]. На примере нафталин- и фенантрен- утилизирующих сообществ показано влияние повышенного засоления среды на филогенетический состав и активность ферментов ШТаММОБ-ДССТруКТОрОБ микробного КОНСОр-циума [Castle ct al.. 2006; Guo ct aL 2016].
Из почв района разработок Верхнекамского месторождения солей (г. Березники, Пермский край) нами были выделены и описаны галотолерантные бактерии родов Rhodococcus, Bacillus, Arthrobacter и Pseudomonas, способные к активной деструкции ПАУ (нафталина. фенантрена) при содержании 6-9% NaCl в ростовой среде [Плотникова и др., 2001. 2011]. Из образца засоленной почвы методом на копительного культивирования получена ассоциация бактерий (именуемая далее SMB1). растущая на нафталине как единственном источнике углерода и энергии б присутствии до 10% NaCl [Плотникова и др., 2001].
Цель настоящей работы - структурно-функциональная характеристика ассоциации бактерий SMB1, а также изучение влияния повышенных концентраций хлорида натрия на ростовые характеристики ассоциации и составляющих ее бактерий.
Материалы и методы исследования
Ассоциация бактерий, условия культивирования. Объектом исследования являлась ассоциа ция микроорганизмов SMB1, которая была изолирована методом накопительного культивирования из образца почвы, отобранной в районе солеразработок (г. Березники, Пермский край) [Плотникова и др., 2001]. Культивирование ассоциации проводили аэробно в 100 мл минеральной среды Раймонда [Розанова, Назина, 1982], содержащей нафталин (1 г/л) и 6% (вес/объем) NaCl, на термостатируемой качалке (100 об/мин) при 28°С. Последовательные пассажи ассоциации осуществляли каждые 2-3 недели путем выращивания при описанных выше условиях. Исследование данной ассоциации проводили после 2 месяцев культивирования.
Рост бактерий поддерживался в минеральной среде Раймонда с нафталином (штаммы SMB11 и SMB145), в полноценной среде Раймонда (штаммы SMB14 и SMB17X где в качестве субстратов использовались триптон («Sigma». Германия) и дрожжевой экстракт («Sigma». Германия) в концентрации 5 г/л и 2.5 г/л. соответственно. Содержание хлорида натрия в средах составляло 3%.
ДНК-1 инн рован не штаммов проводили методом REP-ПЦР (полимеразная цепная реакция повторяющихся экстрагенетических палиндромных последовательностей ДНК. как описано Vcrsalovic с соавт. [Vcrsalovic ct al., 1994].
Идентификация бактерии. Выделение то тальной ДНК бактерий проводили согласно работе М. Ferrero et al. [2002]. Для амплификации нуклеотидных последовательностей гена 16S рРНК использовали бактериальные праймеры 27F и 1492К а ПЦР проводили при условиях, описанных ЕЮ. Гавриш с соавт. [Гавриш и др., 2004]. Нуклеотидные последовательности гена 16S рРНК определяли с применением набора реактивов DYEiiamic ЕТ Dye Terminator Cy cle sequencing Kit на автоматическом секвенаторе Genetic analyser 35OOXL (Applied Biosystems. США) и сравнивали с таковыми типовых штаммов близкородственных видов из базы данных GenBank с помощью программы CLUSTAL W.
Параметры роста бактерии в составе ассоциации SMB1 и индивидуально оценивали при выра щивании их в жидкой минеральной среде Раймонда при 2 8 °C с нафталином в качестве субстрата (1 г/л). При инкубировании бактерий на минеральной агаризованной среде (1.5%) нафталин добавляли в крышку перевернутой чашки Петри. Оптическую плотность (ОП) культуральной жидкости определяли на спектрофотометре UV-Visible BioSpec-mini («Shimadzu», Япония) при 600 нм и толщине кюветы 0.5 см. Количество колониеобразутощих единиц (КОЕ) определяли методом серийных разведении с последующим высевом и подсчетом колоний бактерий на чашках с агаризованной богатой средой Раймонда* Количество хлорида натрия в средах культивирования варьировали от 0 до 10%.
Для изучения взаимного влияния штаммов на характер роста в составе ассоциации проводились эксперименты по их совместному культивированию в жидкой минеральной среде Раймонда с нафталином (1 г/л) в качестве единственного источника углерода и энергии в присутствии 3, 5 и 7% NaCl. В качестве посевного материала исполыювали суспензии штаммов Arthrobacter sp. SMB 145* В. permense SMB 14 и SMB 17 в экспоненциальной фазе роста с тигром клеток около 104 КОЕ. Морфологические различия колоний штаммов позволили исследовать особенности роста отдельных штаммов в составе ассоциации. КОЕ каждого штамма определяли методом серийных раз-ведений с последующим высевом и подсчетом колоний бактерий на чашках с агаризованной полноценной средой Раймонда.
Интенсивность дыхания бактерий измеряли с использованием респирометра Micro-Oxymax respirometer (Columbus Instruments International Corp. Columbus* ОН). Накопление CO? и потребление O2 измерялось сенсорами одновременно через определенные интервалы времени. В ходе эксперимента использовались 250-мл флаконы. содержащие 100 мл минеральной среды Раймонда и нафталин в качестве субстрата в концентрации 0*5 мг/мл. Содержание хлорида натрия в среде культивирования составляло 0 и 5%* В качестве посевного материала использовали суспензии штаммов Arthrobacter sp. SMB 145, В. permease SMB 14 и SMB 17 в экспоненциальной фазе роста с титром клеток около К)4 КОЕ.
Результаты и их обсуждение
Выделение и состав бактериального сообщества SMB1. Сообщество микроорганизмов SMBL выделенное из почвы района солеразработок (г. Березники, Пермский край), способно к эффективное росту на нафталине в качестве единственного источника углерода и энергии в присутствии до 10% NaCl. Установлен состав консорциума SMB1: грамположительные бактерии-деструкторы нафталина - Arthrobacter sp. SMB 11 и Arthrobacter sp SMB 145. а также штаммы Brevibacterium sp. SMB 14 и Chromohaiohacier sp. SMB 17. не способные утилизировать нафталин*
Грамположительный штамм SMB14 образовывал матовые колонии, которые на свету приобретали ярко-оранжевую окраску. На основании проведенных исследований штамм SMB14 был описан как новый вид Brevibacterhun permease (=ВКМ Ас-2 2 801) [Гавриш и др*. 2004]* Данный штамм способен к росту на бензойной и пара-оксмбензойнои кислотах как единственном источнике углерода и энергии. В. permease SMB 14 растет на полноценной среде Раймонда как без добавления NaCl, так и при повышенной концентрации соли - до 12% (таблица).
Рост микробного сообщества SMB1 и индивидуальных штаммов на агаризованной минеральной среде Раймонда в присутствии разных концентраций NaCl
|
Штамм |
Рост на минеральной среде с нафталином |
Рост на полноценной среде |
||||||||||
|
Без NaCl |
3% |
7% |
10% |
14% |
Без NaCl |
3% |
6% |
12% |
18% |
24% |
29% |
|
|
SMBll |
+ |
+ |
+ |
— |
— |
+ |
+ |
+ |
+ |
— |
— |
— |
|
SMB 145 |
+ |
+ |
— |
— |
+ |
+ |
+ |
+ |
— |
— |
— |
|
|
SMB14 |
— |
— |
— |
— |
— |
+ |
+ |
+ |
+ |
— |
— |
— |
|
SMB17 |
— |
— |
— |
— |
— |
— |
+ |
+ |
+ |
4- |
± |
+ |
|
SMI* |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
± |
+ |
Примечание. «+» - рост (колонии размером 1-3 мм); «±» - слабый рост (колонии размером менее 1 мм); «-» -отсутствие роста бактерий
Штамм SMB17 при росте на полноценной агаризованной среде образует прозрачные, плоские колонии желтоватого цвета. Клетки - подвижные палочки. Грамотрицательный, аэроб, катал азо- и оксидазоположителен. Растет на средах при 3-29% NaCl и не растет в отсутствии соли, те. является га лофильным микроорга низмом [Ка шнер, 1981] (таблица). Сравнительный анализ нуклеотидной последовательности 16S рДНК (около 1470 п.н.) показал, что штамм входит в филогенетический кластер, включающий представителей рода Chro-mohaiobacter, наиболее близок (около 99%) к Chromohalobacter canadensis АТСС 43984т [Arahal et al.. 2001 ], Ch rom oh alobacter b eijermckt / ATCC 19372T [Pe^onek et al, 2006] и Chromohalobacter japonic us [Sanchez-Porro et* al*. 2007]. Дан- ный штамм растет в минеральной среде с бензойной и /1<7/?<7-оксибензойной кислотами в качестве субстрата*
Штаммы SMB11 и SMB145 на коринс-бак-тсриальном агаре образовывали круглые ровные* выпуклые, блестящие светло-желтые колонии. Изучение физиолого-биохимических и генетических характеристик позволили отнести вышеперечисленные штаммы к роду Arthrobacter (группе «А. globijormis») [Определитель..., 1997], Анализ нуклеотидных последовательностей гена 16S рРНК штаммов (около 1400 п.н.) выявил 99.7%-ное сходство со штаммом A. crvsiaUopoletes DSM 20117т [Ensign. Rittenberg, 19631. В то же время, штаммы SMB11 и SMB145 отличались морфологическими характеристиками (цвет, размер колоний при выращивании на полноценной среде Раймонда). Проведенный анализ REP-ПЦР профилей показал различия в организации геномов этих штаммов, что указывают на неидентичность изо-лятов(рис. 1).
М 1 2
Рис. L Электрофореграмма продуктов амплификации REP-ПЦР штаммов Arthrobacter spp, выделенных из сообщества микроорганизмов SMB1:
М - маркер 1 kb («Силекс», Россия), 1 -SMB145, 2 - SMB11
Штаммы-деструкторы Arthrobacter spp. SMB 11 и SMB 145 являются галотолерантными микроорганизмами: растут на полноценной среде как в отсутствии, так и в присутствии NaCl (до 12%) [Кашнср, 1981]. На полноценной среде Раймонда данные штаммы способны к росту при концентрации NaCl от 0 до 12% (таблица).
Кроме того, штаммы Arthrobacter sp. SMB11, SMB 145 растут на нафталине и фенантрене в качестве единственного источника углерода и энергии при концентрации до 7% NaCl. Данные штаммы способны использовать в качестве субстрата также салицилат, бензоат, л^^-гидроксибензоат, орто- фталевую кислоту* ацетат.
К настоящему времени имеются ограниченные сведения о микроорганизмах, осуществляющих дс-струкцию ПАУ в условиях высокой минерализа ции среды* Большинство подобных микроорганизмов-деструкторов было выделено из нефтезагрязненных морских отложений и воды И ОТНОСЯТСЯ к грамотрицательным бактериям [Dastghcib et al*, 2012; Feng ct al** 2012; Al-Mailein ct al** 2013]. Описаны га л ого лерантные грам положительные бактерии родов Bacillus, Paembaciilus, Micrococcus, утилизирующие ПАУ* в частности нафталин, при солености среды 0-10%, [Ashok et al., 1995; Kumar et al., 2007]. Ранее нами были обнаружены и охарактеризованы бактерии-деструкторы нафталина и фенантрена родов Rhodococcus, Bacillus, Arthrobacter и Pseudomonas. утилизирующие ПАУ в присутствии NaCl до 6% [Плотникова и др., 2001; Ястребова и др., 2008; Anan'ina et al., 2 011].
Рост ассоциации бактерий SMB1 и штам-мов-дсструкторов на нафталине при повышенной солености среды* При росте ассоциации на агаризоваиной минеральной среде в парах нафталина наблюдалось формирование биопленки на агаре при содержании хлорида натрия до 14% (таблица). В то же время, эффективный рост сообщества в жидкой минеральной среде на нафталине как единственном источнике углерода и энергии был зафиксирован при содержании соли не более 8%. Наибольшие показатели роста сообщества были установлены в отсутствие NaCl в ростовой среде (ОД54о=0.66 оптических единиц), тогда как в присутствии 5, 7 и 8%-ного NaCl оптическая плотность культуры уменьшалась и достигала 0.25, 0.19 и 0.11 оптических единиц, соответственно.
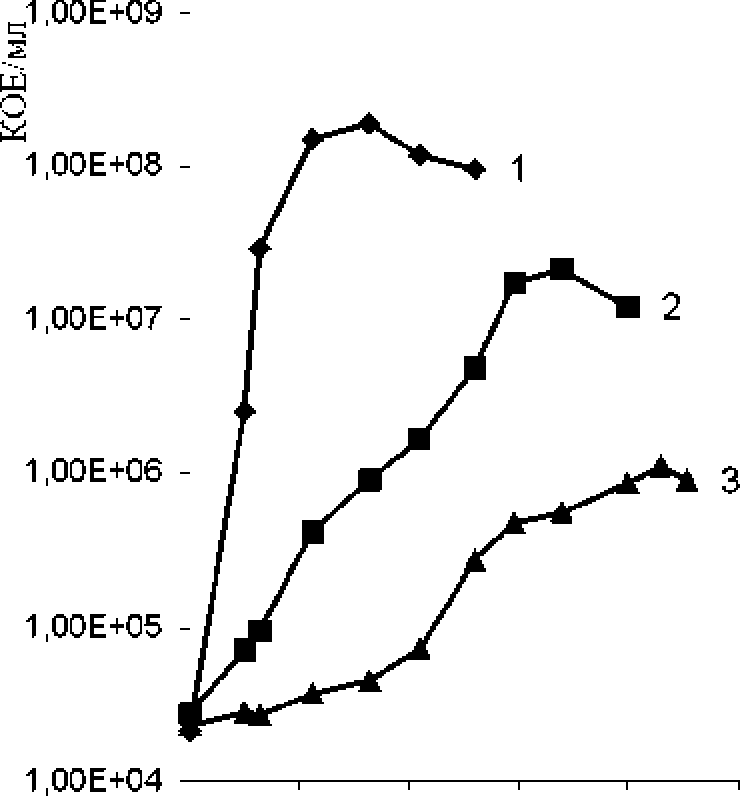
Штаммы Arthrobacter sp. SMB 11 и SMB 145 растут на агаризоваиной и в жидкой минеральных средах с нафталином в качестве субстрата, как без соли, так и при содержании до 7% NaCl в среде культивирования (таблица). Кривые роста штамма Arthrobacter sp* SMB 145 на среде с нафталином в присутствии различных концентраций хлорида натрия представлены на рис* 2. Наибольший титр клеток (l*9xlOs) достигается при отсутствии соли в среде культивирования, тогда как при 5%-ного NaCl максимальное число КОЕ - 2.1-1O7. а при 7% - l.lxlO6* Максимальная скорость роста в отсутствие соли наиболее высокая и составляет 0*15 ч"1* тогда как в присутствии 5 и 7%-ного NaCl достигает 0*024 и 0*02 ч"1* соответственно. Таким образом, повышение концентрации соли в среде отрицательно влияет на ростовые характеристики Arthrobacter sp. SMB 145 при выращивании на нафталине. Негативное влияние высокой солености среды на бактериальную деструкцию ПАУ может объясняться снижением растворимости ароматических углеводородов и доступности кислорода, а также ингибированием метаболических процессов бактериальных клеток при высокой минерализации среды [McGenity, 2010; Martins, Peixoto, 2012; Guo et al, 2016].
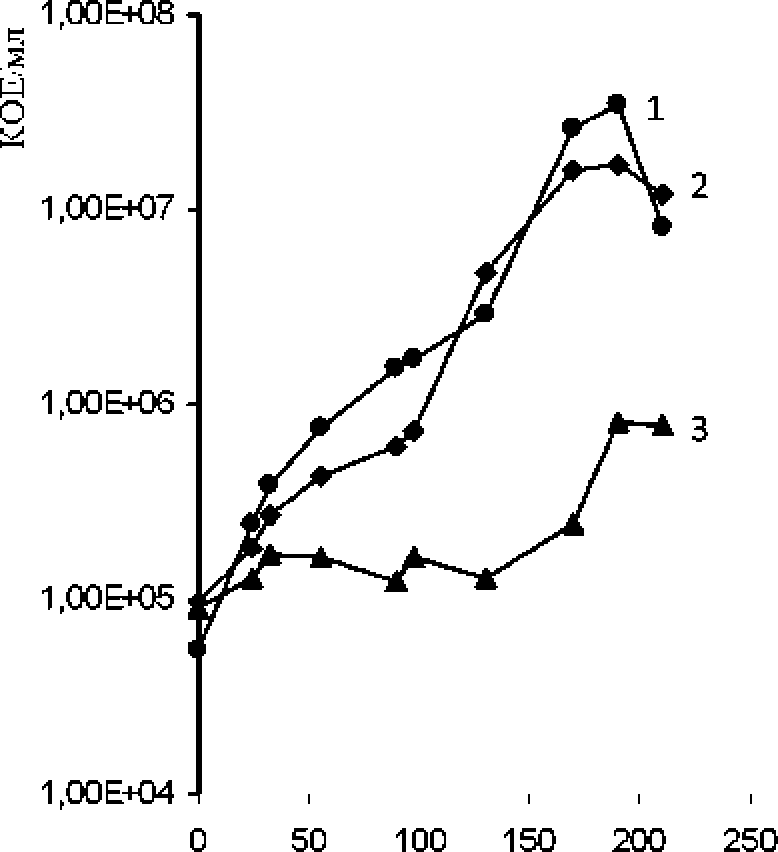
Рост штаммов на нафталине в составе ассоциации (модельный эксперимент). Изучены ростовые характеристики штаммов микробной ассоциации Arthrobacter sp. SMB 145, Brevibacterium per-mense SMB 14 и Chranohalobacter sp. SMB 17 при культивировании в минеральной среде Раймонда на нафталине в качестве единственного источника углерода и энергии в присутствии 7% соли. Установлено, что у штамма Arthrobacter sp. SMB 145 происходило увеличение ростовых параметров при культивировании в сообществе, по сравнению с ростом чистой культуры при тех же условиях (рис. 2. 3). Максимальное значение КОЕ штамма достигало 3.4x107 за 190 ч. культивирования в сообществе (рис. 3). в то время как при росте индивидуальной культуры -1. 1х Ю6 за 215 ч. (рис. 2).
0 50 1 00 1 50 200 250
Время, ч
Рис. 2, Рост штамма.4 rihrobacier sp.
SMB 145 в минеральной среде Раймонда на нафталине в присутствии различных концентраций NaCk
1 - без соли, 2 - 5% NaCI, 3 - 7% NaCI
В ряде исследований показана более эффективная деструкция ПАУ бактериальными сообществами, чем индивидуальными штаммами-деструкторами в тех же условиях вследствие более широкой субстратной специфичности и снижения концентрации токсичных метаболитов в процессе ко-метаболизма бактерий микробных сообществ [Casellas et al., 1998; Moghadam et ak, 2014].
Интересно, что в эксперименте со смешанной культурой у В. perntense SMB 14 происходило увеличение значения КОЕ с 9.8x10" до 1.7x10' (рис. 3), в то время как при индивидуальном культивировании штамма на нафталине, как единственном источнике углерода и энергии, роста не наблюдалось.
Бремя, ч
Рис. 3* Рост штаммов бактериального сообщества SMB1 в минеральной среде Раймонда на нафталине в присутствии 7%-ного
NaCI:
1 -Arthrobacter sp. SMB 145,2 -Brevibactenum permense SMB 14; 3 - Chrotnohalobacter sp. SMB 17
Количество клеток галофильного штамма Chromuhalubacter sp. SMB 17 увеличивалось не более чем на порядок: с 9.1х104до 8.0x10^ (рис. 3). Данный штамм не способен к деструкции нафталина. однако стабильно поддерживается в данной наспал ин-деградирующей микробной ассоциации. Как показали Tagger с соавторами. в состав наф-талин-утилизирующего м икробного сообщества входят бактерии, способные к росту на нафталине, а также бактерии, использующие в качестве ростового субстрата ряд органических кислот образующихся штаммами-деструкторами при росте на на^палине [Tagger el ak. 1990]. Можно предположить. что клетки галофильного штамма Chronto-halobacler sp. SMB 17 из исследуемого консорциума поддерживают свое существование в сообществе за счет продуктов метаболизма, накапливаемых в среде культивирования штаммами-деструкторами при росте на нафталине. а также лизиса клеток бактерий.
Интенсивность дыхания бактерий. В ряде исследований показана положительная корреляция между уровнем накопления углекислого газа и такими параметрами, как степень и скорость утилизации ПАУ [Bouchez et ak, 1997; Zaidi, Imam, 1999]. Как показывает суммарное накопление углекислого газа (рис. 4), бактериальное сообщество SMB1 осуществляет более интенсивную деструкцию нафталина, по сравнению с индивидуальной ку лыурой Arthrobacter sp. SMB145.
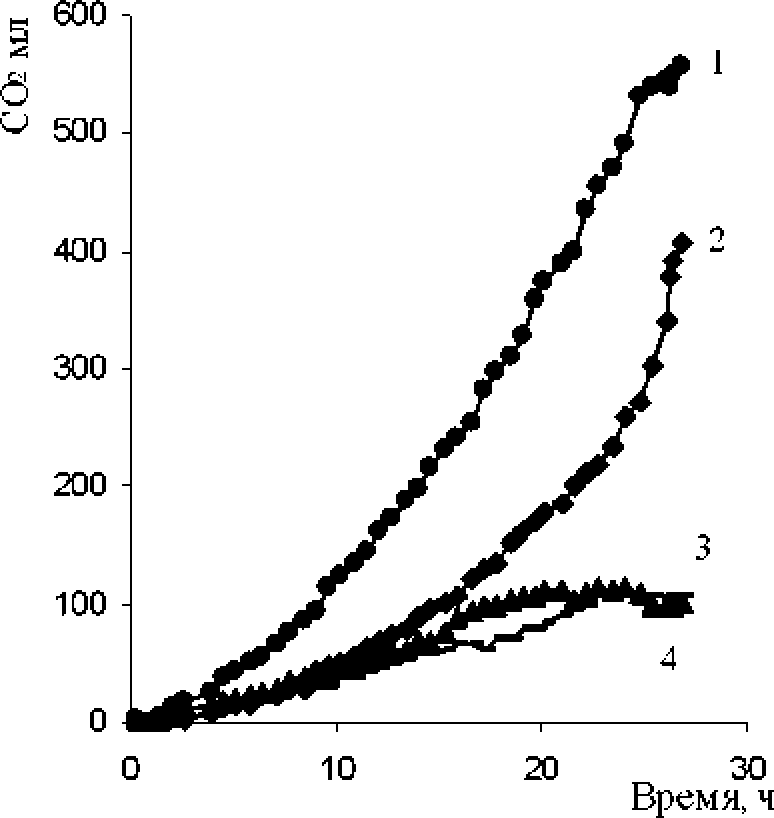
Рис. 4. Суммарное накопление СО2 (мл) при выращивании бактериального сообщества SMB1 и чистых культур в минеральной среде Раймонда с нафталином (0,5 мг/мл) в присутствии 5%-ного NaCL
1 - SMB1; 2 - SMB145; 3 - SMB14; 4 - контроль (среда Раймонда, нафталин)
При выращивании штамма Brevibacienum рег-mense SMB 14 накопление углекислого газа остается на уровне контроля. ЧТО свидетельствует об отсутствии деструкции нафталина данной культурой.
Время, ч
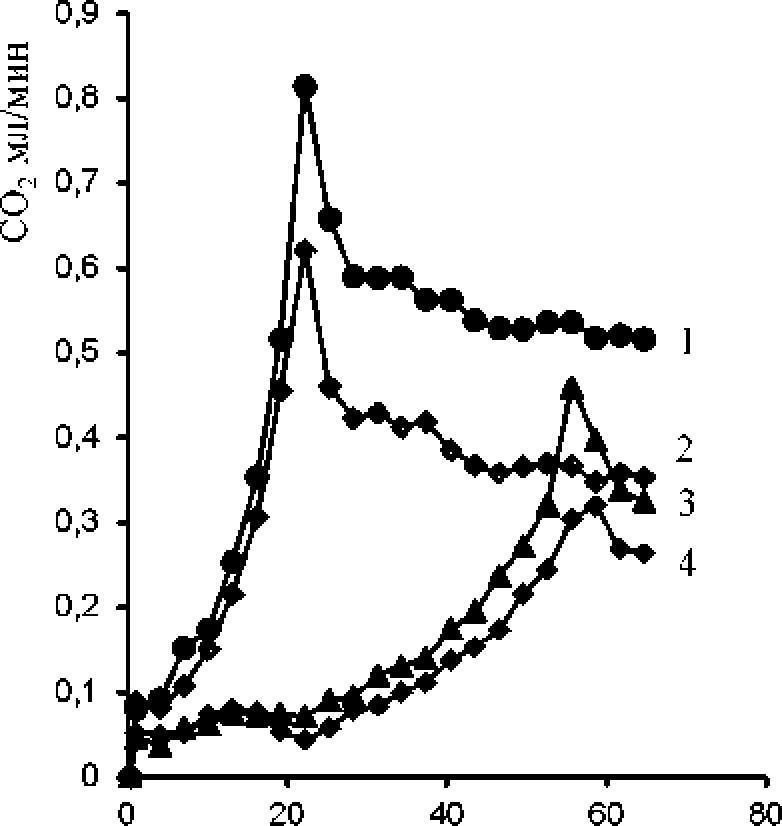
Рис. 5. Удельная скорость выделения СО2 бактериального сообщества SMB1 и штамм-ма SMB145 при выращивании в минеральной среде Раймонда с нафталином (0.5 мг/мл) и разной концентрацией NaCl:
1 - SMB1 (0% NaCl); 2 - SMB 145 (0% NaCl); 3 -SMB1 (5% NaCl); 4 - SMB 145 (5% NaCl)
Удельная скорость выделения CO2 бактериального сообщества SMB1 была на 24% выше таковой штамма SMB145 в среде без добавления соли и на 30% выше в среде с 5%-ного NaCl (рис. 5), что также свидетельствует о более эффективной деструкции нафталина сообществом SMB1 по сравнению со штаммом-деструктором Arthrobacter sp. SMB145.
Заключение
Выделенный бактериальный консорциум SMB1, растущий на нафталине как единственном источнике углерода в присутствии до 10% NaCl, включает два галоголерантных штамма-деструктора нафталина рода^гйго^^с/е/* (штаммы SMB11, SMB145), а также галотолерантный штамм Brevibacterium perntense SMB 14 и галофил ьный штамм Chromohatobacter sp. SMB 17. не утилизирующие нафталин. В результате исследований установлено. что штамм-деструктор Arthrobaaer sp. SMB 145 менее эффективно растет на нафталине в условиях повышенного засоления Среды при культивировании индивидуально, чем в составе бактериального сообщества SMBL Можно предположить положительное влияние экзо-метаболитов галофильного штамма обладающих осмопротекторными свойствами, таких как сахара, аминокислоты и их производные [Келлэм et al, 199SJ. на способность штаммов-деструкторов к росту и утилизации нафталина при повышенном засолении среды. В то же время штаммы сообщества, не утилизирующие нафталин, могут использовать в качестве субстрата метаболиты нафталина, выделяемые штаммами-деструкторами в среду ку л ьтивирова ния
Помимо вышеописанной микробной ассоциации, из образцов почв, отобранных в районе солеразработок, было выделено еще несколько сообществ микроорганизмов, также деградирующих ПАУ при повышенных концентрациях хлорида натрия. В состав этих сообществ также входили га-лотолерантные бактерии-деструкторы ПАУ и сопутствующие галофильные и/или галотолерантные бактерии [Ананьина и др., 2005: Ананьина и др., 2007]. прослеживается закономерность формирования в экосистемах с повышенным содержанием солей устойчивых аэробных микробных ассоциаций, способных использовать как источник углерода и энергии сложные органические соединения (нафталин) в условиях засоления. Изучение таких микробных сообществ, имеющих большой потенциал для использования их при биоремедиации засоленных почв, загрязненных полициклическими ароматическими углеводородами, внесет существенный вклад в понимание механизмов взаимоотношений отдельных штаммов микробного сообщества.
Работа поддержана грантом РФФИ-Урал № 16-44-590968 р_а.
Список литературы Структурно-функциональная характеристика бактериального консорциума, выделенного из техногенных почв Верхнекамского месторождения солей
- Ананьина Л.Н., Алтынцева О.В., Плотникова Е.Г. Изучение сообщества микроорганизмов, выделенного из района солеразработок//Bестник Пермского университета. 2005. Bi>ni. 6. Биология. С. 109-114
- Ананьина Л.Н. и др. Salinicola socius gen. nov., sp. nov. -новая умеренно галофильная бактерия из ассоциации микроорганизмов, утилизирующей нафталин//Микробиология. 2007. Т. 76, № 3. С. 369-376
- Гавриш Е.Ю. и др. Три новых вида бревибактерий -Brevibacterium antiquum sp. nov., Brevibacterium aurantiacum sp. nov. и Brevibacterium permense sp. nov.//Микробиология. 2004. Т. 73, № 2. C. 218-225
- Кашнер Д. Жизнь микробов в экстремальных условиях. М.: Мир. 1981. 365 с
- Определитель бактерий Берджи: пер. с англ./под ред. Дж. Хоулта и др. М.: Мир. 1997. Т. 1, 2
- Плотникова Е.Г. и др. Бактерии-деструкторы полициклических ароматических углеводородов, выделенные из почв и донных отложений района солеразработок//Микробиология. 2001. Т. 70, № 1. С. 61-69
- Плотникова Е.Г. и др. Галотолерантные бактерии рода Arthrobacter -деструкторы полициклических ароматических углеводородов//Экология. 2011. № 6. С. 459-466
- Розанова Е.П., Назина Т.Н. Углеводородокисляю-щие бактерии и их активность в нефтяных пластах//Микробиология. 1982. Т. 51. С. 324-348
- Ястребова О.В., Ананьина Л.Н., Плотникова Е.Г. Бактерии рода Bacillus, выделенные из почв района солеразработок//Bестник Пермского университета. 2008. Bi>ni. 9 (25). Биология. С. 58-62
- Anan'ina L.N. et al. Naphthalene-degrading bacteria of the genus Rhodococcus from the Verkhne-kamsk salt mining region of Russia//Antonie Van Leeuwenhoek. 2011. Vol. 100, Is. 2. P. 309316
- Al-Mailem D.M., Eliyas M., Radwan S.S. Oil-bioremediation potential of two hydrocarbonoclas-tic, diazotrophic Marinobacter strains from hy-persaline areas along the Arabian Gulfcoasts//Extremophiles. 2013. Vol. 17. P. 463-470
- Arahal D.R. et al. Transfer of Halomonas canadensis and Halomonas israelensis to the genus Chromo-halobacter as Chromohalobacter canadensis comb. nov. and Chromohalobacter israelensis comb. nov.//Int J Syst Evol Microbiol. 2001. Vol. 51. P. 1443-1448
- Ashok, T., Saxena, S., Musarrat J. Isolation and char acterization of four polycyclic aromatic hydrocarbon degrading bacteria from soil near an oil refinery//Lett. Appl. Microbiol. 1995. Vol. 21, Is. 4. P. 246-248
- Berlendis S. et al. First evidence of aerobic biodegra-dation of BTEX compounds by pure cultures of Marinobacter//Appl. Biochem. Biotechnol. 2010. Vol. 160. P. 1992-1999
- Bonfa M.R.L. et al. Phenol degradation by halophilic bacteria isolated from hypersaline environments//Biodegradation. 2013. Vol. 24. P. 699-709
- Bouchez M., Blanchetl D., Vandecasteele J.-P. An interfacial uptake mechanism for the degradation of pyrene by a Rhodococcus strain//Microbiology. 1997. Vol. 143. P. 1087-1093
- Casellas M. et al. Isolation and characterization of a fluorine-degrading bacterial strain and its role in synergistic degradation of fluorene by a consortium//Can. J. Microbiol. 1998. Vol. 44. P. 734742
- Castle D.M., Montgomery M.T., Kirchman D.L. Effects of naphthalene on microbial community composition in The Delaware estuary//FEMS Microbiol. Ecol. 2006. Vol. 56. P. 55-63
- Cerniglia C.E. Biodegradation of polycyclic aromatic hydrocarbons//Biodegradation. 1992. Vol. 3. P. 351-368
- Dalvi S., Azetsu S., Patrauchan M.A., Aktas D.F., Fa-thepure B.Z. Proteogenomic elucidation of the initial steps in the benzene degradation pathway of a novel halophile, Arhodomonas sp. Strain Rozel, isolated from a hypersaline environment//Appl. Environ. Microbiol. 2012. Vol. 78. P. 7309-7316
- Dastgheib S.M.M. et al. Biodegradation of polycyclic aromatic hydrocarbons by a halophilic microbial consortium//Appl. Microbiol. Biotechnol. 2012. Vol. 95. P. 789-798
- Ensign J.C., Rittenberg S.C. A crystalline pigment produced from 2-hydro-xypridine by Arthrohacter crvstallopoites n.sp.//Arch.Mikrobiol. 1963. Vol. 47. P. 137-153
- Ferrero M. et al.. Coexistence of two distinct copies of naphthalene degradation genes in Pseudomonas strains isolated from the western mediterranean region//Appl. Environ. Microbiol. 2002. Vol. 68. P. 957-962
- Guo G. et al. Effect of salt contents on enzymatic activities and halophilic microbial community structure during phenanthrene degradation//International Biodeterioration & Biodegradation. 2016. Vol. 110. P. 8-15
- Habe H., Omori T. Genetics of Polycyclic Aromatic Hydrocarbon Metabolism in Diverse Aerobic Bacteria//Biosci. Biotechnol. Biochem. 2003. Vol. 67, № 2. P. 225-243.
- Kim, D. et al. Molecular cloning and functional characterization of the genes encoding benzoate and p-hydroxybenzoate degradation by the halophilic Chro-mohalobacter sp. strain HS-2//FEMS Microbiol. Lett. 2008. Vol. 280. P. 235-241
- Kumar M. et al. A halotolerant and thermotolerant Bacillus sp. degrades hydrocarbons and produces tensionactive emulsifyingagent//World J. Microbiol. Biotechnol. 2007. Vol. 23. P. 211-220
- Martins L.F., Peixoto R.S. Biodegradation of petroleum hydrocarbons in hypersaline environments//Brazilian Journal of Microbiology. 2012. P. 865872
- McGenity T.J. Halophilic hydrocarbon degraders. In: K. N. Timmis (ed). Handbook of Hydrocarbon and Lipid Microbiology. Berlin: Springer-Verlag, 2010. P. 1939-1951
- Moghadam M.S. et al. Biodegradation of polycyclic aromatic hydrocarbons by a bacterial consortium enriched from mangrove sediments//Journal of Environmental Health Science & Engineering. 2014. 12:114 URL: http://www.ijehse.com/content/12/1/114
- Pec,onek J. et al. Reclassification of Pseudomonas beijerinckii Hof 1935 as Chromohalobacter bei-jerinckii comb. nov., and emended description of the species//Int. J. Syst. Evol. Microbiol. 2006. Vol. 56. P. 1953-1957.
- Sanchez-Porro C. et al. Chromohalobacter japonicus sp. nov., a moderately halophilic bacterium isolated from a Japanese salty food//Int. J. Syst. Evol. Microbiol. 2007. Vol. 57. P. 2262-2266
- Tagger S., Truffaut N., Le Petit J. Preliminary study on relationship among strains forming a bacterial community selected on naphthalene from a marine sediment//Can. J. Microbiol. 1990. Vol. 36. P. 676-681
- Ventosa A., Nieto J. J., Oren A. Biology of moderately halophilic aerobic bacteria//Microbiology and Molecular biology reviews. 1998. Vol. 62, № 2. P. 504-544
- Versalovic J., Schneider M., de Bruijn F.J. Genomic fingerprinting of bacteria using repetitive sequence based polymerase chain reaction//Meth. Mol. Cell. Biol. 1994. Vol. 5. P. 25-40
- Zaidi B.R., Imam S.H. Factors afecting microbial degradation of Polycyclic Aromatic Hydrocarbon phe-nanthrene in the Caribbean Coastal Water//Marine Pollution Bulletin. 1999. Vol. 38, № 8. P. 737-742
- Feng T.-C. et al. Phenanthrene biodegradation by halophilic Martelella sp. AD-3//Journal of Applied Microbiology. 2012. Vol. 113. P. 779-789.
- Tam N.F. et al. Preliminary study on biodegradation of phenanthrene by bacteria isolated from mangrove sediments in Hong Kong.//Mar. Pollut. Bull. 2002. Vol. 45. P. 316-324


