Структурно-функциональная характеристика фотосинтетического аппарата галофитов, отличающихся по типу накопления солей
Автор: Розенцвет Ольга Анатольевна, Нестеров Виктор Николаевич, Богданова Елена Сергеевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Наземные экосистемы
Статья в выпуске: 3-7 т.15, 2013 года.
Бесплатный доступ
Исследовали структурные (состав и содержание липидов) и функциональные (концентрация хлорофиллов a и b, каротиноидов, соотношение хлорофиллов a/b, соотношение хлорофиллы/каротиноиды, доля хлорофиллов в ССК) особенности фотосинтетического аппарата эвгалофитов, криногалофитов и гликогалофитов. Установлено, что разделение растений по соленакапливающему признаку поддерживается различным соотношением содержания пигментов и липидов, а вариации в их содержании позволяют судить об экологической пластичности фотосинтетического аппарата галофитов в условиях засушливого климата и высокого содержания солей в почве.
Галофиты, регуляция солевого обмена, пигменты, липиды, вариативность
Короткий адрес: https://sciup.org/148202183
IDR: 148202183 | УДК: 577.125.528
The structurally functional characteristic of the photosynthetic device of halophytes, differing by salts accumulation
Investigated structural (structure and the maintenance of lipids) and functional (concentration of a chlorophyll a and b, carotenoids, a ratio of a chlorophyll of a/b, a ratio a chlorophyll/carotenoids, a share of a chlorophyll in LHC) features of the photosynthetic device of halophytes. It is established that division of plants on a salt accumulation sign is supported by various ratio of the maintenance of pigments and lipids, variations in their contents allow to judge about ecological plasticity of the photosynthetic device of halophytes in the conditions of droughty climate and the high content of salts in the soil.
Текст научной статьи Структурно-функциональная характеристика фотосинтетического аппарата галофитов, отличающихся по типу накопления солей
О дним из главных экологических факторов, который лимитирует рост и продуктивность многих растений является засоление почв [6, 23]. Известно, что ионы солей в высоких концентрациях могут дезинтегрировать клеточные мембраны, подавлять активность ферментов и приводить к нарушению таких жизненно важных функций как клеточное деление, ассимиляция углерода, поглощение элементов минерального питания и др. [2]. Галофиты, как правило, успешно растут и развиваются даже при высоком содержании солей в почве, благодаря молекулярно-генетическим особенностям, обуславливающим специфичные защитные механизмы [9, 19].
Основой биопродуктивности растений является хорошо функционирующий процесс фотосинтеза, неразрывно связанный с мембранами хлоропластов. Функциональная активность пигмент-белковых комплексов фотосинтетического аппарата (ФА), зависит от организации мембран тилакоидов, в которые они погружены [28]. Критериями оценки функционирования ФА являются содержание и соотношение хлорофиллов (Хл) a и b , доля хлорофиллов в ССК, содержание каротиноидов [18]. Основными компонентами мембран тилакоидов являются галактолипиды - монога-лактозилдиацилглицерол (МГДГ) и дигалакто-зилдиацилглицерол (ДГДГ), сульфолипид суль-фохиновозилдиацилглицерол (СХДГ) и фосфати-дилглицерол (ФГ) [13, 25, 28].
Исследованиями последних лет установлена специфичность состава липидов отдельных субъединиц фотосистем (ФС) I и II, а также специализированная роль отдельных классов липидов в процессе фотосинтеза [10, 15, 16, 28]. Например,
МГДГ создает условия для функционирования виолаксантин-деэпоксидазы – фермента, осуществляющего на свету превращение виолаксантина в зеаксантин [14]; а ФГ способствует тримериза-ции мономеров светособирающего комплекса (ССК), что влияет на формирование гран; ДГДГ поддерживает структуру полипептидных комплексов реакционного центра ФС II [11, 26]; сульфолипид стабилизирует белковые комплексы, участвующие в транспорте электронов, и АТФ-синтазы, осуществляющей синтез АТФ [20, 22, 24].
Эффективность работы пигментной системы зависит от соответствия ее структуры и функций климатическим и/или экологическим условиям. Тесное взаимодействие пигмент-белковых комплексов с липидным окружением дает основание предполагать, что существует определенная связь между количественным содержанием гликолипидов (ГЛ) и пигментов в листьях растений, обусловленная как совокупным действием абиотических факторов внешней среды, так и особенностями вида растений. Сведения об изменениях, происходящих в пигментном и липидном комплексе дикорастущих галофитов, различающихся типом регуляции солевого обмена, практически отсутствуют. С этой точки зрения представляют интерес галофиты, произрастающие в регионах с экстремальными условиями обитания. Таким регионом, в частности, является бассейн оз. Эльтон (Приэльтонье), климатические условия которого отличаются широкой амплитудой температурного режима (от –50°С зимой до +50°С – летом), а также крайне низким количеством осадков.
Цель настоящей работы – изучить структурнофункциональные особенности фотосинтетического аппарата галофитов, отличающихся по механизмам регуляции солевого обмена, в связи с условиями произрастания.
МАТЕРИАЛ И МЕТОДИКА
Район исследования расположен на территории Волгоградской области, характеризуется близостью залегания грунтовых вод, засоленностью почвогрунтов, что обуславливает формирование солончаковости и солонцеватости почв и определенного типа растительности [3]. Растительный материал отбирали в первой половине дня в середине июня 2012 г. Было заложено 5 площадок (20 х 20 м), расположенных в устьевых участках рек Чернавка (49°12´с.ш., 44°40´в.д.), Ланцуг (49°12´с.ш., 46°38´в.д.), Хара (49°12´с.ш., 46°39´в.д.), Солянка (49°10´с.ш., 46°35´в.д.), Большая Смарогда (49°07´с.ш., 46°50´в.д.).
Объектами исследования были выбраны представители эвгалофитов – Suaeda salsa (L.) Pall. и Salicornia perennans Willd. из семейства Cheno-podiaceae , криногалофитов – Limonium gmelinii (Willd.) O. Kuntze из семейства Plumbaginaceae , гликогалофитов – Artemisia santonica L. из семейства Asteraceae .
Для биохимических анализов использовали 10–12 листьев среднего яруса из 15–20 растений (в случае S. perennans – среднюю часть побега), произрастающих в пределах одного биотопа. Из объединенной биомассы растений одного вида составляли три независимых биологических пробы и использовали для анализов. Одновременно отбирали пробы почвы на глубине 15–20 см для определения кислотности, влажности и минерального остатка почвенной вытяжки [1].
Экстракцию, идентификацию, анализ липидов и пигментов проводили, как описано ранее [4]. В таблицах и рисунках использованы средние арифметические значения из трех независимых биологических проб для каждого биотопа. Статистическую обработку результатов анализов проводили с использованием программ Statistica 6.0 for Windows, Microsoft Excel 2007 и Statgraphics Centurion XV.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Условия произрастания исследованных видов галофитов в устьевых участках пяти рек различались по температурному режиму, содержанию влаги в почве, кислотности и содержанию солей (табл. 1).
Наибольшая амплитуда изменчивости характерна для влажности и солености водной вытяжки почвы – минимальные и максимальные значения различались в 10–20 раз. Вариации температурного режима на поверхности почвы на момент сбора растений и кислотности почвы были менее выражены.
Как известно, первичными фоторецепторами в процессе фотосинтеза являются пигменты [8]. Среднее содержание суммы Хл а и b в надземной части галофитов уменьшалось в ряду L. gmelinii – S. salsa – S. perennans – A. santonica (4,9; 4,5; 3,1 и 2,5 мг/г сухой массы, соответственно) (табл. 2). Учитывая неоднородность условий обитания, был рассчитан коэффициент вариации ( K v ) содержания зеленых и желтых пигментов в зависимости от условий произрастания. Оказалось, что у эвгалофитов S. perennans и S. salsa содержание зеленых пигментов варьировало в равной степени ( K v = 31%), у криногалофита L. gmelinii – отличалось стабильностью ( K v = 13%), а у A. santonica – большей вариабельностью ( K v = 43%) и меньшим их количеством в сравнении с другими видами.
Содержание каротиноидов было примерно равным у двух видов S. salsa и L. gmelinii (0,98 и 0,91 мг/г) и выше, чем у растений S. perennans и A. santonica , (0,70 и 0,63 мг/ г сухой массы, соответственно). Размах вариабельности в содержании каротиноидов был аналогичным размаху вариабельности суммы хлорофиллов, то есть наибольший у гликогалофита A. santonica (35%), а наименьший у криногалофита L. gmelinii (21%). Концентрация каротиноидов по отношению к Хл убывала в том же порядке, что и сумма Хл а + b , то есть в ряду L. gmelinii – S. salsa – S. perennans – A. santonica , что, вероятно, связано с видовыми морфологическими особенностями. Так, растения L. gmelinii отличаются от остальных видов самыми крупными размерами листьев и в тоже время меньшим содержанием каротиноидов в пигментном фонде (наибольшими значениями отношения Хл a + b /Кар). Известно, что каротиноиды защищают реакционные центры ФА от фотоингибирования и фотоокисления Хл [17, 18]. Известна также способность каротиноидов осуществлять функцию дополнительных светосбор-щиков. Более высокое содержание каротиноидов в растениях с более мелкими листьями ( S. salsa , S. perennans и A. santonica ), отличающихся более высоким содержанием каротиноидов, вероятно, способствует более эффективному использованию солнечный света по сравнению с L. gmelinii.
Таблица 1 . Физико-химические характеристики условий в местах отбора растений.
|
Место произрастания, река |
Орографические параметры |
Температура воздуха, о С |
||
|
Влажность, % |
Содержание солей, мг/мл |
Кислотность |
||
|
Чернявка |
46,0–48,0 |
0,6–0,8 |
9,2–9,3 |
30,0 |
|
Ланцуг |
33,0–35,0 |
1,0–1,2 |
8,9–9,1 |
35,0 |
|
Хара |
2,3–36,0 |
0,1–1,0 |
8,6–9,7 |
35,0 |
|
Солянка |
37,8–39,8 |
0,5–0,7 |
9,7–9,8 |
35,0 |
|
Б. Смарогда |
13,3–17,4 |
0,8–0,9 |
9,0–9,8 |
31,0 |
|
Таблица 2. Некоторые фотосинтетические характеристики надземной части галофитов в зависимости от места произрастания |
|||||||
|
Место произрастания, река |
Хл a , мг/г сух. массы |
Хл b , мг/г сух. массы |
Кар, мг/г сух. массы |
Хл a + b , мг/г сух. массы |
Хл a / b |
(Хл a + b )/Кар |
Доля Хл в ССК, % |
|
Чернавка |
3,14 |
0,68 |
1,02 |
Suaeda salsa 3,82 |
4,62 |
3,75 |
39,2 |
|
Ланцуг |
3,94 |
1,01 |
1,21 |
4,95 |
3,90 |
4,09 |
44,9 |
|
Хара |
3,31 |
1,13 |
0,92 |
4,44 |
2,93 |
4,83 |
56,0 |
|
Солянка |
1,94 |
0,72 |
0,58 |
2,66 |
2,69 |
4,59 |
59,5 |
|
Б. Смарогда |
4,83 |
1,61 |
1,15 |
6,44 |
3,00 |
5,60 |
55,0 |
|
Чернавка |
2,94 |
1,01 |
Sa 0,83 |
icornia perenn 3,95 |
ans 2,91 |
4,76 |
56,3 |
|
Ланцуг |
1,62 |
0,43 |
0,51 |
2,05 |
3,77 |
4,02 |
46,1 |
|
Хара |
1,51 |
0,56 |
0,48 |
2,07 |
2,70 |
4,31 |
59,5 |
|
Солянка |
2,55 |
1,36 |
0,91 |
3,91 |
1,88 |
4,30 |
76,5 |
|
Б. Смарогда |
2,56 |
1,05 |
0,75 |
3,61 |
2,44 |
4,81 |
64,0 |
|
Чернавка |
3,84 |
1,32 |
L 1,00 |
imonium gmelin 5,16 |
ii 2,91 |
5,16 |
56,3 |
|
Ланцуг |
2,87 |
0,96 |
0,77 |
3,83 |
2,99 |
4,97 |
55,1 |
|
Хара |
4,11 |
1,27 |
1,16 |
5,38 |
3,24 |
4,64 |
51,9 |
|
Солянка |
3,67 |
1,25 |
0,93 |
4,92 |
2,94 |
5,29 |
55,9 |
|
Б. Смарогда |
3,36 |
1,96 |
0,68 |
5,32 |
1,71 |
7,82 |
61,1 |
|
Чернавка |
2,59 |
0,8 |
Ar 0,78 |
temisia santoni 3,39 |
ca 3,24 |
4,35 |
51,9 |
|
Ланцуг |
2,75 |
0,83 |
0,86 |
3,58 |
3,31 |
4,16 |
51,0 |
|
Хара |
1,23 |
0,42 |
0,49 |
1,65 |
2,93 |
3,37 |
56,0 |
|
Солянка |
0,89 |
0,29 |
0,32 |
1,18 |
3,07 |
3,69 |
54,1 |
|
Б. Смарогда |
1,87 |
0,66 |
0,69 |
2,53 |
2,83 |
3,67 |
57,4 |
Примечание. Стандартная ошибка составляет 5-7%.
Для нормальной работы ФА важно не только абсолютное значение содержания пигментов, но и их соотношение, которое указывает на взаимодействие комплексов реакционных центров ФС и ССК в хлоропластах. Полагают, что увеличение содержания Хл а приводит к снижению содержание ССК и нарушению упаковки гран [27]. Средние значения отношение Хл а/b для всех исследованных видов растений варьировали в пределах 2,7-3,4. Вариативность этого признака ( K v ) в зависимости от условий произрастания у трех видов галофитов S. salsa , L. gmelinii и S. perennans составила 22-25%, а у A. santonica - лишь 7%, что может свидетельствовать о более стабильном состоянии гран данного гликогалофита. Дополнительным аргументом стабильности состояния тилакоидов этого вида является и наименьшая вариативность показателя доли хлорофиллов в ССК (K v = 5%) в сравнении с другими видами ( K v = 1720%).
Как отмечалось выше, функциональная активность ФА зависит от структурной организации мембран тилакоидов. Известно, что у фотосинтезирующих растений тилакоидные мембраны превалируют над цитоплазматическими. В результате главные липиды хлоропластов - ГЛ, как правило, доминируют среди общих липидных (ОЛ) экстрактов растений [5]. В наших исследованиях содержание ОЛ в надземной части растений различалось как у отдельных видов галофитов, так и внутри вида в зависимости от места их произрастания (рис. 1). Наибольшее содержание ОЛ в расчете на 1 г сухой массы отмечено у гликогалофита A. santonica - 66-159, а наименьшее - у эвгалофита S. perennans - 38-50 мг. Галофиты L. gmelinii и S. salsa в этом отношении занимали промежуточное положение - 53-123 и 46-80 мг/г, соответственно. Концентрация ОЛ в листьях L. gmelinii отличалась большей степенью вариации (Kv =38%), что, вероятно, связано с анатомоморфологическими свойствами, поскольку листья этого растения отличаются от остальных большими размерами и площадью листовой поверхности. В надземной массе A. santonica содержания ОЛ варьировало в пределах 32%, S. salsa -24%, S. perennans - 14%. В целом, очевидно, что содержание липидов зависело от действия факторов внешней среды и индивидуальных особенностей вида.
Доля ГЛ, которые имеют непосредственное отношение к структуре ФА, в пуле ОЛ составляла в среднем от 26 до 32%, а по отношению к мембранным липидам (МЛ) - от 65 до 85% (рис. 2). Например, листья A. santonica содержали наибольшее количество ГЛ - до 55 мг/г сух. массы (табл. 3), или 80-84% от МЛ (рис. 2).
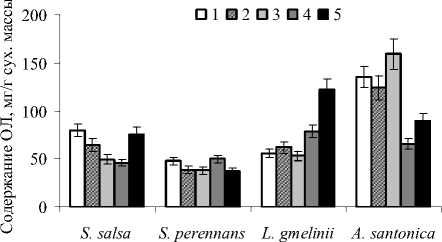
Рис. 1 . Содержание общих липидов в надземной части галофитов в зависимости от места произрастания. Место произрастания, река: 1 - Чернавка, 2 -Ланцуг, 3 - Хара, 4 - Солянка, 5 - Б. Смарогда.
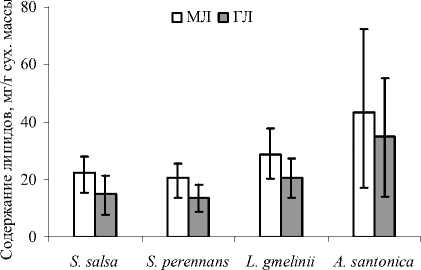
Рис. 2 . Содержание мембранных и гликолипидов в надземной части галофитов, собранных на 5 исследованных участках. Представлены минимальные, средние и максимальные величины.
Вариация этой группы липидов была выше, чем ОЛ. Самый высокий K v был зафиксирован у A. santonica (54%). Далее в порядке уменьшения следовали: S. salsa (40%), L. gmelinii и S. peren-nans (26%). Отметим, что у A. santonica была самая высокая вариация в содержании, как пигментов, так и ГЛ, что может быть связано со способностью регулировать интенсивность фотосинтеза за счет изменения числа хлоропластов.
Была проанализирована также структура пула ГЛ и вариации индивидуальных классов липидов тилакоидных мембран. В количественном отношении МГДГ доминировал у всех образцов растений S. salsa (39-48% от суммы липидов тилакоидных мембран) независимо от места произрастания (табл. 3). В других видах в равном или большем, чем МГДГ количестве, было отмечено содержание другого класса галактолипидов -ДГДГ (34-43%). Относительное содержание СХДГ составляло в среднем 7-16%. Еще меньшим был вклад ФГ (2-16%) (табл. 3).
Отношение МГДГ/ДГДГ имеет особое значение для работы ФА [28]. Считают, что данные липиды играют важную роль в стабилизации сильно искривленных участков мембраны [21]. Обычно соотношение МГДГ/ДГДГ в хлоропластах высших растений бывает около 1,5. По нашим данным, средние значения отношения МГДГ/ДГДГ у всех исследованных видов составили 1,0-1,3. Из литературных источников известно, что у некоторых чувствительных к засолению почвы видов, например, у томата Lycoper-sicum esculentum Mill. и огурца Curcumis sativus L., данное отношение составляет 1,8-2,0, а у солеустойчивых с Salicornia europaea и Atriplex gmelinii стремится к 1, т.е. является более низким [12]. По-видимому, устойчивость галофитов к засолению почвы достигается, в том числе, за счет большего содержания ДГДГ, что подтверждается и результатами наших исследований.
В отличие от суммарных ГЛ относительное содержание (% от суммы) индивидуальных классов в надземной части всех исследованных видов растений было более стабильным: Kv для МГДГ имел диапазон варьирования 6-14%, для ДГДГ -6-12%, для СХДГ - 12-27%. Можно видеть, что вариация сульфолипида несколько выше, чем галактолипидов. В отличие от галакто- и сульфолипидов относительное содержание ФГ имело большую степень изменчивости (Kv = 21-45%), что в сравнении с суммарными и индивидуальными ГЛ является самым высоким показателем. Например, для A. santonica Kv содержания ФГ составил 77%. Отметим, что минимальное значение Kv для содержания ФГ (16%) зафиксировано у L. gmelinii. Как ФГ, так и СХДГ, являются липидами, несущими отрицательный заряд, что, по-видимому, и обуславливает их участие в стабилизации комплексов АТФ- синтазы и ССК [22]. Повышенная вариация СХДГ в составе мембран хлоропластов исследованных галофитов может быть связана с необходимостью регуляции энергетических процессов в разных условиях произрастания, в то время как большая степень изменчивости ФГ - с изменением структуры тилакоидов за счет изменения количества гран. Это особенно характерно для фотосинтезирующих органов A. santonica, у которых к тому же была наиболее высокая вариабельность содержания зеленых пигментов. По имеющимся в литературе данным [7], структура хлоропластов - длина гран и количество стопок в гране, может быть демонтирована и сформирована вновь в течение нескольких минут. Этот эффект отмечен для растений в условиях повышенной инсоляции. Возможно, что у растений гликогалофита A. santonica, для которых характерно ограничение поступления солей в надземные органы, существует аналогичный эффект - динамичность структуры гран, поддерживаемая модуляцией липидов тилакоидных мембран.
Для выявления связи количественного содержания ГЛ и пигментов в надземной части растений, было проведено сравнение структурных и функциональных характеристик ФА. Оказалось, что отношение ГЛ/пигменты было самым высо- ким у соленепроницаемого вида A. santonica 9,2– 13,0 в сравнении с соленакапливающими S. salsa (1,6–6,4), S. perennans (2,7–6,0) и солевыделяющим L. gmelinii (2,8–4,5). Кроме того, для A. san- tonica была обнаружена прямая зависимость между содержанием пигментов и гликолипидов (рис. 3). У остальных видов подобная связь была менее выражена.
Таблица 3. Содержание ГЛ в надземной части галофитов в зависимости от места произрастания.
|
Место произрастания, река |
Липиды, мг/г сух. массы (% от суммы ГЛ и ФГ) |
|||
|
ФГ 1 |
МГДГ ! |
ДГДГ ! |
СХДГ |
|
|
Чернавка |
1,40 (16) |
Suaed 3,60 (39) |
a salsa 2,95 (33) |
1,08 (12) |
|
Ланцуг |
1,37 (6) |
9,99 (44) |
8,46 (38) |
2,76 (12) |
|
Хара |
1,04 (8) |
5,53 (44) |
4,14 (34) |
1,71 (14) |
|
Солянка |
1,31 (6) |
10,78 (48) |
8,55 (39) |
1,53 (7) |
|
Б. Смарогда |
2,24 (14) |
6,78 (42) |
4,50 (28) |
2,51 (16) |
|
Чернавка |
1,83 (12) |
Salicornia 5,60 (38) |
perennans 5,38 (37) |
1,86 (13) |
|
Ланцуг |
0,91 (6) |
7,69 (47) |
5,58 (34) |
2,11 (13) |
|
Хара |
0,91 (9) |
3,18 (33) |
3,96 (42) |
1,59 (16) |
|
Солянка |
1,45 (7) |
7,34 (37) |
8,02 (42) |
2,82 (14) |
|
Б. Смарогда |
2,33 (15) |
5,63 (37) |
5,27 (36) |
1,88 (12) |
|
Чернавка |
1,44 (6) |
Limonium 10,48 (40) |
gmelinii 10,16 (40) |
3,56 (14) |
|
Ланцуг |
1,45 (10) |
5,87 (38) |
5,57 (37) |
2,35 (15) |
|
Хара |
1,57 (7) |
10,41 (46) |
8,23 (36) |
2,45 (11) |
|
Солянка |
1,62 (9) |
6,10 (34) |
7,85 (42) |
2,66 (15) |
|
Б. Смарогда |
2,07 (7) |
11,95 (40) |
11,28 (39) |
3,94 (14) |
|
Чернавка |
2,67 (5) |
Artemisia 26,63 (46) |
santonica 20,94 (37) |
6,59 (12) |
|
Ланцуг |
2,17 (4) |
25,99 (45) |
23,78 (42) |
5,28 (9) |
|
Хара |
0,37 (2) |
8,63 (41) |
9,18 (43) |
2,95 (14) |
|
Солянка |
0,46 (4) |
5,89 (41) |
6,06 (42) |
1,88 (13) |
|
Б. Смарогда |
1,06 (3) |
13,21 (42) |
12,97 (41) |
4,33 (14) |
Примечание. Стандартная ошибка составляет 5–7 %.
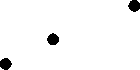
Содержание пигментов, мг/г сух. массы
Рис. 3. Зависимость содержания гликолипидов и пигментов в надземной части A. santonica , произрастающей на 5 исследованных участках.
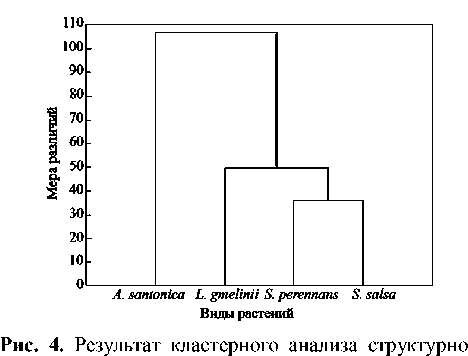
функциональных показателей исследуемых видов галофитов.
С помощью кластерного анализа удалось выявить сходство (различия) структурных и функциональных признаков у разных типов галофитов, отличающихся по типу накопления солей, с использованием всех характеристик, проанализированных в данной работе (рис. 4). Было установлено, что соленакапливающие виды S. salsa и S. perennans объединены в одну группу, затем за ними следует солевыделяющий вид L. gmelinii и соленепроницаемый вид A. santonica. При этом, криногалофит L. gmelinii имеет большее «родство» с эвгалофитами S. salsa и S. perennans, что может быть связано, в том числе с тем, что вместе эти 3 вида образуют группу облигатных галофитов в отличие от факультативного галофита A. santonica.
Изучение количественных характеристик пигментного и липидного комплекса 4-х видов дикорастущих галофитов, различающихся типом регуляции солевого обмена, показало, что разделение растений по соленакапливающему признаку имеет четкую биохимическую основу – более высокое суммарное содержание хлорофиллов на фоне низкого уровня суммарных мембранных липидов характерно для эвгалофитов и криногалофита в сравнении с гликогалофитом.
На основании данных по изменчивости исследуемых параметров в зависимости от места произрастания установлено, что общее содержание мембранных липидов, отвечающих за структуру ФА, в основном менялось сильнее ( K v = 26–54%), чем содержание зеленых пигментов ( K v = 13– 43%). В то же время соотношение индивидуальных компонентов ГЛ было более жестко детерминировано ( K v = 6–27 %). Следовательно, эффективное функционирование ФА галофитов в условиях засушливого климата и высокого содержания солей в почве обеспечивается сочетанием экологически пластичных и экологически стабильных компонентов.
Работа выполнена при поддержке гранта РФФИ № 12-04-0111-а.
Список литературы Структурно-функциональная характеристика фотосинтетического аппарата галофитов, отличающихся по типу накопления солей
- Аринушкина Е.В. Руководство по химическому анализу почв. Изд. Московского Университета, 1970. 489 с.
- Балнокин Ю.В., Строганов Б.П. Солевой обмен и проблема солеустойчивости растений. Новые направления в физиологии растений. М.: Наука, 1985. С. 199-213.
- Лысенко Т.М., Митрошенкова А.Е., Шарпило Н.И., Круглов А.А. Материалы к флоре Приэльтонья//Фиторазнообразие восточной Европы. 2010. № 8. С. 97-107.
- Нестеров В.Н., Розенцвет О.А., Мурзаева С.В. Изменение состава липидов у пресноводного растения Hydrilla verticillata (L. fil.) Royle в условиях аккумуляции и элиминации ионов тяжелых металлов//Физиология растений. 2009. Т. 56. № 1. С. 85-93.
- Санина Н.М. Мембранообразующие липиды. Физико-химические основы термоадаптации морских беспозвоночных и макрофитов/Автореферат дисс… Владивосток, 2006. С. 22-27.
- Строганов Б.П. Физиологические основы солеустойчивости растений (при разнокачественном засолении почвы). М.: АН СССР, 1962. 336 с.
- Anderson J.M., Chow W.S., Rivas J.L. Dynamic flexibility in the structure and function ofphotosystem II in higher plant thylakoid membranes: the grana enigma//Photosynth. Res. 2008. V. 98. P. 575-587.
- Blankenship R.E. Molecular mechanisms of photosynthesis. Oxford: Blackwell Science Ltd, UK. 2002. 321 p.
- Flowers T.J., Colmer T.D. Salinity tolerance in halophytes//New Phytol. 2008. V. 179. P. 945-963.
- Guskov A., Kern J., Gabdulkhakov A. et al. Cyanobacteria photosystem II at 2.9 A resolution: role of quinones, lipids, channels and chloride//Nat. Struct. Mol. Biol. 2009. V. 16. P. 334-342.
- Hagio M., Sakurai I., Sato S. et al. Phosphatidylglycerol is essential for the development of thylakoid membranes in Arabidopsis thaliana//Plant Cell Physiol. 2002. V. 43. P. 1456-1464.
- Hirayama O., Mihara M. Characterization of Membrane Lipids of Higher Plants Different in Salt Tolerance//Agric. Biol. Chem. 1987. V. 51. P. 3215-3221.
- Hölzl G., Dörman P. Structure and Function of Glycerolipids in Plants and Bacteria//Prog. Lipid res. 2007. V. 46. P. 225-243.
- Jahns P., Latowski D., Strzalka K. Mechanism and regulation of violaxanthin cycle: The role of antenna proteins and membrane lipids//Biochim. Biophys. Acta. 2009. V. 1787. P. 3-14.
- Jordan P., Fromme P., Witt H.T. et al. Three-dimensional structure of cyanobacterial photosystem I at 2.5 A resolution//Nature. 2001. V. 411. P. 909-917.
- Kern J., Loll B., Luneberg C. et al. Purification, characterization and crystallization of photosystem II from Thermosynechococcus elongatus cultivated in a new type of photobioreactor. Biochim Biophys Acta. 2005. V. 1706. P. 147-157.
- Lichtenthaller H.K. Chlorophylls and Carotenoids: Pigments of Photosynthetic Biomembranes//Methods in enzymology. 1987. V. 148. Р. 350-382.
- Lichtenthaller H.K., Buschmann C. Chlorophylls and Carotenoids: Measurement and Characterization by UV-VIS Spectroscopy//Current Protocols in Food Analytical Chemistry. 2001. F4.3.1-F4.3.8.
- Lokhande V.H., Suprasanna P. Prospects of Halophytes in Understanding and Managing Abiotic Stress Tolerance. In: Ahmad P., Prasad M.N.V. (eds.), Environmental adaptations and Stress Tolerance of Plants in the Era of Climate Change. Springer science + Business Media, 2012. P. 29-56.
- Minoda A., Sato N., Nozaki H. et al. Role of sufoquinovosyl diacylglycerol for the maintenance of photosystem II in Chlamydomonas reinhardtii//Eur. J.Biochem. 2002. V. 269. P. 2353-2358.
- Murata N., Hoshi H. Sulfoquinovosyl diacylglycerols in chilling sensitive and chilling resistant plants//Plant Cell Physiol. 1984. V. 25. №. 7. P. 1241-1245.
- Okanenko A.A., Taran N.Yu., Kosyk O.I. Plant sulfolipid. 1. Functions. Бiополiмери i клiтина. 2008. Т. 24. № 6. С. 431-440.
- Parida A.K., Das A.B. Effects of NaCl stress on nitrogen and phosphorus metabolism in a true mangrove Bruguiera parviflora grown under hydroponic culture//J. Plant Physiol. 2004. V. 161. P. 921-928.
- Ramani B., Papenbrock J., Schmidt A. Connecting sulfur metabolism and salt tolerance mechanisms in the halophytes Aster tripolium and Sesuvium portulacastrum//Trop. Ecol. 2004. V. 45. № 1. P. 173-182.
- Rawyler A., Sieganthaler P.A. Transversal localization of monogalactosyldiacylglycerol and digalactosyldiacylglycerol in spinach thylakoid membranes//Biochim. Biophys. Acta. 1985. V. 815. P. 287-298.
- Siegenthaler P.A., Trémolières A. Role of acyl lipids in the function of photosynthetic membranes in higher plants. In: Siegenthaler P.A., Murata N. (eds.), Lipids in photosynthesis: structure, function and genetics. Advances in photosynthesis and respiration. Dordrecht: Springer, 1998. V. 6. Р. 79-98.
- Sui N., Li M., Li K. et al. Increase in unsaturated fatty acids in membrane lipids of Suaeda salsa L. enhances protection of photosystem II under high salinity//Photosynthetica. 2010. V. 48. P. 623-629.
- Wada H., Murata N. Lipids in Thylakoid membranes and Photosynthetic Cells. In: Wada H., Murata N. (eds.), Lipids in Photosynthesis: Essential and Regulatory Function. N. Dordrecht: Springer, 2009. P. 1-9.


