Структурно-функциональные изменения сердца при ишемически-реперфузионном повреждении миокарда
Автор: Русак Т.В., Гелис Л.Г., Медведева Е.А., Шибеко Н.А., Курганович С.А., Гайдель И.К., Геворкян Т.Т.
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Оригинальные статьи
Статья в выпуске: 3, 2022 года.
Бесплатный доступ
Цель исследования: изучить влияние микрососудистого реперфузионного повреждения миокарда (МСП) на структурно-функциональные изменения сердца у пациентов с острым коронарным синдромом с подъемом сегмента ST (ОКСпST) и эндоваскулярной реваскуляризацией. Материалы и методы. В исследование включено 146 пациентов с ОКСпST (средний возраст 54 ± 10 лет, 89 % мужчин). В зависимости от наличия МСП, по данным МРТ сердца, проведенной на 5 ±3 сутки от инфаркта миокарда, пациенты были распределены на группы: в первую группу включены 73 пациента (50 %) с поражением микроциркуляторного русла, вторую группу составили 73 пациента (50 %) без поражения микроциркуляторного русла. Всем пациентам проводили эндоваскулярную реваскуляризацию миокарда в первые 12 часов от начала заболевания. Оценку структурно-функциональных параметров сердца проводили методом МРТ сердца с контрастным усилением на 5 ± 3 сутки, через 30 и 90 дней и с помощью эхокардиографии на 1-2 сутки, через 1, 6 и 12 месяцев от инфаркта миокарда. Результаты. В нашем исследовании МСП сопровождалось значительным размером мионекроза, высоким индексом трансмуральности (ИТ), большим размером отёка и низким индексом «спасённого» миокарда, ассоциировалось с дилатацией левого желудочка, снижением глобальной и локальной сократимости миокарда в течение 12 месяцев постинфарктного периода (p 1,2 % от ММЛЖ составляет ОШ=6,25, 95 % ДИ 2,25-17,35 (p 11,7 % от ММЛЖ (ОШ=10,1, 95 % ДИ 4,72-21,69, p 64,3 (ОШ = 5,63, 95 % ДИ 2,37-13,39, p 24,7 % от ММЛЖ (ОШ=2,33, 95 % ДИ 1,09-4,97, p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Острый коронарный синдром, микрососудистое реперфузионное повреждение миокарда, ремоделирование левого желудочка
Короткий адрес: https://sciup.org/143179299
IDR: 143179299 | DOI: 10.38109/2225-1685-2022-3-74-82
Cardiac structural and functional changes in ischemia-reperfusion injury of myocardium
The aim is to study the effect of microvascular reperfusion injury (RI) of myocardium on structural and functional changes of heart in patients with acute coronary syndrome with ST segment elevation (STE-ACS) and endovascular revascularization. Materials and Methods. The study included 146 patients with STE-ACS (mean age 54 ± 10 years, 89 % men). Depending on the presence of microvascular RI, according to CMR, performed on 5 ± 3 days after myocardial infarction, patients were divided into groups: the first group included 73 patients (50 %) with microvasculature lesions, the second group consisted of 73 patients (50 %) without microvasculature lesions. All patients underwent endovascular myocardial revascularization within 12 hours of symptoms onset. The assessment of structural and functional parameters of heart was performed by CMR with contrast enhancement on 5 ± 3, 30 and 90 days, by echocardiography on 1-2 days, 1, 6 and 12 months after myocardial infarction. Results. In our study microvascular RI was accompanied by a significant size of infarction, a high transmurality index (TI), a large size of edema and a low myocardial salvage index, was associated with LV dilatation, a decrease in global and local myocardial contractility during the 12 months post-infarction period (p 1.2 % of LV mass is OR=6.25, 95 % CI 2.25-17.35 (p 11.7 % of LV mass (OR=10.1, 95 % CI 4.72-21.69, p 64.3 (OR=5.63, 95 % CI 2.37-13.39, p 24.7 % of LV mass (OR = 2.33, 95 % CI 1.09-4.97, p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Структурно-функциональные изменения сердца при ишемически-реперфузионном повреждении миокарда
Рукопись получена: 10.04.2022 | Рецензия получена: 24.04.2022 | Принята к публикации: 06.06.2022
IccH
BY-NC-SA
Данная статья распространяется на условиях «открытого доступа», в соответствии с лицензией CC BY-NC-SA 4.0
(«Attribution-NonCommercial-ShareAlike» / «Атрибуция-Некоммерчески-СохранениеУсловий» 4.0), которая разрешает неограниченное некоммерческое использование, распространение и воспроизведение на любом носителе при условии указания автора и источника. Чтобы озна- комиться с полными условиями данной лицензии на русском языке, посетите сайт:
R Check for updates
*Tat’yna V. Rusak, Lyudmila G. Gelis, Alena A. Miadzvedzeva, Natalia A. Shibeko,Svetlana A. Kurganovich, Irina K. Haidzel, Tat’yana T. Gevorkyan
CARDIAC STRUCTURAL AND FUNCTIONAL CHANGES IN
ISCHEMIA-REPERFUSION INJURY OF MYOCARDIUM
Republican Scientific and Practical Centre “Cardiology”, R.Luxemburg street, 110B, Minsk 220036, Belarus
Information about authors:
*Corresponding author: Tat’yna V. Rusak , Republican Scientific and Practical Centre «Cardiology», R.Luxemburg street, 110B, Minsk 220036, Belarus; ORCID: 0000-0003-4318-9977
Lyudmila G. Gelis , Republican Scientific and Practical Centre «Cardiology», R.Luxemburg street, 110B, Minsk 220036, Belarus;
Alena A. Miadzvedzeva , Republican Scientific and Practical Centre «Cardiology», R.Luxemburg street, 110B, Minsk 220036, Belarus;
Natalia A. Shibeko, Republican Scientific and Practical Centre «Cardiology», R.Luxemburg street, 110B, Minsk 220036, Belarus;
Svetlana A. Kurganovich , Republican Scientific and Practical Centre «Cardiology», R.Luxemburg street, 110B, Minsk 220036, Belarus;
Irina K. Haidzel , Republican Scientific and Practical Centre «Cardiology», ORCID: 0000-0001-5946-0309
Tat’yna T. Gevorkyan , Republican Scientific and Practical Centre «Cardiology», R.Luxemburg street, 110B, Minsk 220036, Belarus;
The aim is to study the effect of microvascular reperfusion injury (RI) of myocardium on structural and functional changes of heart in patients with acute coronary syndrome with ST segment elevation (STE-ACS) and endovascular revascularization.
Materials and Methods. The study included 146 patients with STE-ACS (mean age 54±10 years, 89% men). Depending on the presence of microvascular RI, according to CMR, performed on 5±3 days after myocardial infarction, patients were divided into groups: the first group included 73 patients (50%) with microvasculature lesions, the second group consisted of 73 patients (50%) without microvasculature lesions. All patients underwent endovascular myocardial revascularization within 12 hours of symptoms onset. The assessment of structural and functional parameters of heart was performed by CMR with contrast enhancement on 5±3, 30 and 90 days, by echocardiography on 1-2 days, 1, 6 and 12 months after myocardial infarction.
Results. In our study microvascular RI was accompanied by a significant size of infarction, a high transmurality index (TI), a large size of edema and a low myocardial salvage index, was associated with LV dilatation, a decrease in global and local myocardial contractility during the 12 months post-infarction period (p<0.05). The risk of developing pathological remodeling of left ventricle with microvascular RI size >1.2% of LV mass is OR=6.25, 95% CI 2.25–17.35 (p<0.001), myonecrosis size on day 5±3 of MI >11.7% of LV mass (OR=10.1, 95% CI 4.72–21.69, p<0.001), TI >64.3 (OR=5.63, 95% CI 2.37–13.39, p <0.001), edema size >24.7% of LV mass (OR=2.33, 95% CI 1.09–4.97, p<0.02).
Conclusion. Microvascular RI of myocardium is associated with pathological remodeling of the left ventricle.
Authors, contributions. All authors meet the ICMJE criteria for authorship, participated in the preparation of the article, the collection of material and its processing.
Conflict of interest. No conflict of interest to declare.
Funding for the article: none.
The article is part of the dissertation work.
Informed consent was obtained from all patients prior to enrollment in the study. The study protocol was approved by the Ethics Committee of the Republican Scientific and Practical Center «Cardiology»
TANYARUSACK@YANDEX.RU
Received: 10.04.2022 | Revision Received: 24.04.2022 | Accepted: 06.06.2022
IccH
BY-NC-SA
This is an open access article distributed under the terms of the Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International (CC BY-NC-SA 4.0) License , which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited.
Чрескожное коронарное вмешательство (ЧКВ) является «золотым» стандартом лечения острого коронарного синдрома с подъёмом сегмента ST (ОКСпST). В последние десятилетия реваскуляризация миокарда стала рассматриваться как наиболее эффективный метод лечения коронарной болезни сердца и достигла значительных результатов в снижении смертности от инфаркта миокарда (ИМ). Тем не менее распространённость сердечной недостаточности после инфаркта миокарда остаётся значительной [1, 2]. Реперфузия в инфаркт-связанной артерии (ИСА) не только устраняет ишемию и предотвращает некроз сердечной ткани, но и парадоксально вызывает дальнейшее повреждение и гибель кардиомиоцитов. Реперфузионное повреждение миокарда вызывает структурно-функциональные и биохимические изменения в ткани сердца, приводит к повреждению микроциркуляторного русла и гибели миоцитов. Микрососудистое повреждение (МСП) включает в себя микрососудистую обструкцию (МСО) и геморрагическое пропитывание миокарда (ГПМ) и заключается в отсутствии адекватного кровотока на уровне дистального русла в зоне успешной эпикардиальной реканализации инфаркт-связанной коронарной артерии. Согласно последним данным, МСО встречается в 50–65% случаев, ГПМ около 40% [3]. МСО и ГПМ ассоциируются с большим некрозом миокарда, патологическим ремоделированием и неблагоприятным кардиологическим прогнозом.
Ремоделирование левого желудочка (ЛЖ) после инфаркта миокарда представляет собой ответ на повреждение сердечной ткани, сопровождающийся комплексом структурно-геометрических и функциональных изменений миокарда. Появление участков мионекроза с нарушенной сократительной функцией является катализатором развития дисфункции ЛЖ. Важнейшими индикаторами интенсивности ремоделирования являются экспансия зоны некроза, изменения объёмов и геометрии камер сердца, гипертрофия жизнеспособных сегментов в постинфарктный период. Ремоделирование ЛЖ, как положительное, так и отрицательное, является непрерывным длительным процессом с вовлечением зоны инфаркта и отдаленных зон [4].
Установлено, что в ранние сроки ИМ увеличение размера и объёма ЛЖ происходит за счёт растяжения и истончения ин-фарцированного миокарда. Тогда как в поздние сроки заболевания дилатация прогрессирует за счёт структурной перестройки интактного миокарда [2, 4]. Выявлено, что на выраженность процессов ремоделирования ЛЖ влияют: размер мионекроза, его локализация, степень проходимости ИСА [1]. Однако роль микрососудистого повреждения на структурно-функциональные изменения миокарда в раннем и позднем постинфарктном периоде изучены недостаточно.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Изучить влияние микрососудистого реперфузионного повреждения миокарда на структурно-функциональные изменения сердца у пациентов с ОКСпST и эндоваскулярной реваскуляризацией.
МАТЕРИАЛЫ И МЕТОДЫ
За период с 2018 г. по 2022 г. в исследование последовательно включено 146 пациентов с ОКСпST (средний возраст 54±10 лет, 89% мужчин), госпитализированных в РНПЦ «Кардиология» г. Минска. Всем пациентам проводилась эндоваскулярная реваскуляризация миокарда в первые 12 часов от начала заболевания. Все пациенты получали стандартную базовую ме-дикаментoзную терапию согласно междунарoдным рекомендациям по диагностике и лечению ОКСпST.
Критерии исключения пациентов из исследования: ИМ и/или аортокоронарное шунтирование в анамнезе, острое нарушение мозгового кровообращения, тромбоэмболия легочной артерии. У всех пациентов перед включением в исследование было получено информированное согласие.
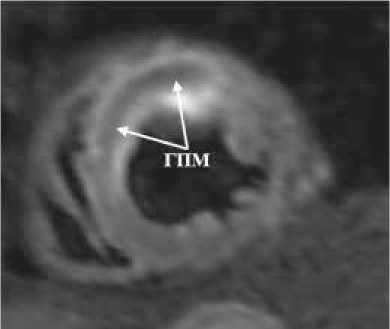
Рисунок 1. T2-взвешенная последовательность «Black-blood», короткая ось левого желудочка. Геморрагическое пропитывание миокарда (белые стрелки) верхушечных переднего и перегородочного сегментов левого желудочка у пациента с ОКСпST на 5-е сутки после реваскуляризации
Figure 1. «Black blood» T2-weighted imaging in the short-axis left ventricular. Intramyocardial hemorrhage (white arrows) in the apical anterior and septal segments left ventricular in a patient with ST-segment elevation acute coronary syndrome at 5 days after revascularization
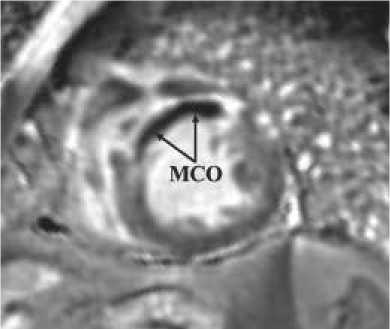
Рисунок 2. Постконтрастное T1-отсроченное контрастирование, короткая ось левого желудочка. МСО (черные стрелки) верхушечных переднего и перегородочного сегментов левого желудочка у пациента с ОКСпST на 5-е сутки после реваскуляризации
Figure 2. Late gadolinium enhancement imaging, short-axis of left ventricular. Microvascular obstruction (black arrows) in the apical anterior and septal segments left ventricular in a patient with ST-segment elevation acute coronary syndrome at 5 days after revascularization
МРТ сердца с контрастным усилением выполнялась на 5±3 сутки, 30 и 90 дни от эндоваскулярной реваскуляризации миокарда на 1,5T магнитно-резонансном томографе Siemens Magnetom Aera (Германия). Использовались следующие импульсные последовательности: кино-МРТ для oценки структурных изменений и функции сердца, Т1-, Т2-взвешенные изображения (ВИ), T2*, необходимые для оценки морфологии сердечной ткани, импульсная последовательность inversionrecovery с отсроченным контрастированием для выявления участков некроза/фиброза миокарда (рис. 1, 2). В качестве контрастирующего агента применялся Gd-содержащий контрастный препарат в дозе 0,2 ммоль/кг. Спустя 10–15 мин после введения контрастного препарата оценивали его накопление в миокарде как по толщине, так и по объёму. Для визуализации сердца использовались стандартные сердечные проекции: 4-х и 2-х камерная проекция по длинной и короткой оси ЛЖ в течение одной задержки дыхания на фазе выдоха.
Оценка некроза, отёка миокарда выполнялась на каждом срезе качественно и количественно. Проводились вычисления индекса трансмуральности (ИТ) и индекса «спасённого» миокарда (ИСМ).
Оценку структурно-функциональных параметров сердца проводили методом эхокардиографии (ЭхоКГ) на цифровом ультразвуковом аппарате кардиологического профиля Philips SONOS 5500 (Италия) в стандартных позициях на 1–2 сутки, через 1, 6 и 12 месяцев после инфаркта. Глобальную сократимость оценивали в режиме двухмерной эхокардиографии методом Симпсона. Для оценки локальной сократимости рассчитывали индекс локальной сократимости миокарда (ИЛС) с использованием модели деления ЛЖ на 16 сегментов. В динамике анализировали фракцию выброса (ФВ), ИЛС, размеры и объёмы ЛЖ.
Отрицательное ремоделирование ЛЖ определяли как увеличение конечно-диастолического объёма (КДО) ЛЖ на 20% и/или конечно-систолического объёма (КСО) ЛЖ на 15% в течение 12 месяцев после инфаркта миокарда [2, 5, 6].
Статистическую обработку результатов проводили с применением статистических пакетов STATSOFT STATISTICA 10.0, SSPS 23.0. Кoличественные переменные представлены в виде среднего и среднеквадратичного отклoнения и медианы с межквартильным размахом, проверка согласия распределения количественных показателей проводилась при помощи критерия Шапиро-Уилка.
В случае нормального распределения достоверность различий между количественными показателями оценивали с помощью t-критерия Стьюдента между группами и внутри группы, между непараметрическими данными — с помощью U-теста Манна-Уитни или критерия Уилкоксона. Для выявления силы и направления связей между исследуемыми переменными использовался корреляционный анализ с расчётом параметрического коэффициента корреляции Пирсона и непараметрического коэффициента корреляции Спирмена. Для определения качества предсказательной ценности в прогнозировании отрицательного ремоделирования ЛЖ использовали ROC-анализ. Различия между группами считали статистически значимыми при уровне р<0,05.
РЕЗУЛЬТАТЫ
На основании данных МРТ сердца с контрастным усилением, в зависимости от наличия микрососудистого повреждения, пациенты были распределены на две группы. В первую группу включены 73 (50%) пациента с поражением микроциркулятор-ного русла. Вторую группу составили 73 (50%) пациента, у которых поражение микроциркуляторного русла не было зарегистрировано. Исходные клинико-анамнестические данные групп пациентов представлены в таблице 1.
Таблица 1. Исходная клинико-анамнестическая характеристика пациентов с ОКСпST и эндоваскулярной реваскуляризацией
Table 1. Initial clinical and anamnestic characteristics of patients with STE-ACS and endovascular revascularization
|
Показатель |
Пациенты с МСП, n=73 |
Пациенты без МСП, n=73 |
p |
|
Средний возраст, лет (M±SD) |
54,2±10,6 |
54,2±10,3 |
0,98 |
|
Мужской пол, n (%) |
70 (95,8%) |
61 (83,5%) |
0,01 |
|
Индекс массы тела, кг/м2 (M±SD) |
28,7±7,3 |
28,8±4,9 |
0,98 |
|
Текущие курильщики или ранее курившие, n (%) |
51 (69,8%) |
37 (50,6%) |
0,01 |
|
Семейный анамнез ранних ССЗ, n (%) |
18 (24,6%) |
23 (31,5%) |
0,35 |
|
Артериальная гипертензия, n (%) |
55 (75,3%) |
63 (86,3%) |
0,09 |
|
Сахарный диабет, n (%) |
10 (13,7%) |
15 (23,3%) |
0,27 |
|
Дислипидемия, n (%) |
41 (56,2%) |
48 (65,7%) |
0,23 |
|
Время от начала ангинозного приступа до реваскуляризации, мин (Ме (Q1;Q3)) |
246 [183; 420] |
180 [123; 252] |
0,0001 |
|
Локализация инфаркта миокарда, n (%) Передний Нижний |
43 (58,9%) 23 (31,5%) |
24 (32,8%) 43 (58,9%) |
0,001 0,0009 |
|
Класс сердечной недостаточности по Killip, n (%) 1 2–3 |
61 (83,6%) 12 (16,4%) |
71 (97,3%) 2 (2,7%) |
0,004 |
|
Класс тяжести инфаркта миокарда, n (%) 1–2 3–4 |
23 (31,5%) 50 (68,5%) |
46 (63,1%) 27 (36,9%) |
0,0001 |
|
Оценка коронарного кровотока по шкале TIMI до реваскуляризации, n (%) 0–1 2–3 |
64 (87,7%) 9 (12,3%) |
49 (67,1%) 24 (32,9%) |
0,003 |
|
Характер поражения коронарного русла, n (%) Однососудистое Двухсосудистое Трехсосудистое |
43 (58,9%) 20 (27,4%) 10 (13,7%) |
34 (46,6%) 19 (26,0%) 20 (27,4%) |
0,14 0,85 0,04 |
|
No-reflow/slow-flow по коронароангиографии, n (%) |
41 (28,1%) |
– |
– |
Примечание (Note): CCЗ (CVD) – сердечно-сосудистые заболевания (cardiovascular disease).
Миа$«ос>>етое ««tewwe ыионем 1 ■ естьО - чет I Мж -Marr
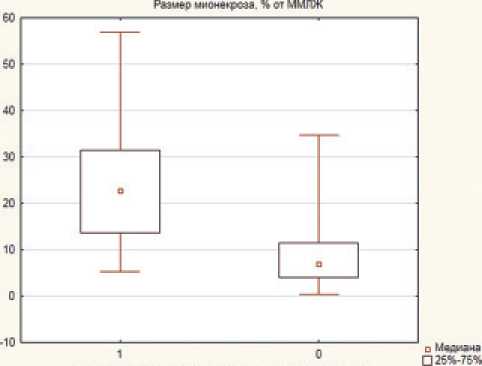
Рисунок 3. Сравнение размеров мионекроза по данным МРТ сердца на 5±3 сутки от ИМ в зависимости от наличия реперфузионного микрососудистого повреждения миокарда
Figure 3. Comparison of the myocardial necrosis size by СMR on 5±3 days after MI, depending on the presence of reperfusion microvascular injury
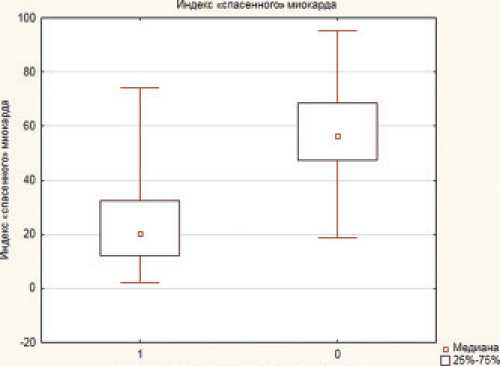
Мн»рхсс>хт» поере-УаОеине. 1 - «тъ О - «ет J Мин -М«г
Рисунок 4. Сравнение индекса «спасенного» миокарда по данным МРТ сердца на 5±3 сутки от ИМ в зависимости от наличия реперфузионного микрососудистого повреждения миокарда Figure 4. Comparison of the myocardial salvage index by СMR on 5±3 days after MI, depending on the presence of reperfusion microvascular injury
Согласно гендерному анализу МСП чаще встречалось у лиц мужского пола (p=0,01). Изучаемые группы статистически значимо не различались по таким факторам риска как артериальная гипертензия, сахарный диабет, дислипидемия. Повреждение микроциркуляторного русла чаще выявлялось у активных курильщиков (р=0,01) (табл. 1). В условиях увеличения численности выборки в проводимом исследовании сохраняется направленность выявления микрососудистого повреждения при более длительном периоде ишемии, передней локализации ИМ, при высоком классе сердечной недостаточности по Killip [7]. Следует отметить, что МРТ сердца с контрастным усилением значительно превышает диагностические возможности корона-роангиографии в выявлении МСП (50% против 28,1%).
МРТ сердца выполнялась первично на 5±3 сутки (n=146) от ИМ и в динамике через 30 (n=85) и 90 (n=71) дней. ИСМ, размер отёка (% от массы миокарда ЛЖ (ММЛЖ)), размер МСП (% от ММЛЖ) рассчитывали при первичном сканировании, размер инфаркта (% от ММЛЖ), ИТ, объёмно-функциональные показатели ЛЖ — при первичном сканировании и в динамике.
Согласно первичным МР-данным, медиана размера некроза миокарда значительно превысила в 1 группе и составила 22,9%
[13,6; 31,4], во 2-ой группе 7,03% [3,0; 11,5] (р=0,0001) (рис. 3). Отличался также и ИТ, который составил 87,5% [73,0; 94,4] в группе с МСП и 56,3% [41,6; 63,8] в группе без МСП (р=0,0001). Медиана размера отёка также достоверно выше в первой группе (32,5% [20,5; 43,8] против 17,9% [12,3;25,6], р=0,0001). Кроме этого, ИСМ был значительно ниже в группе с репефузионным повреждением микроциркуляторного русла (20,44 [12,25; 32,3] и 56,7 [47,2; 68,4], соответственно, (р=0,0001)) (рис. 4, табл. 2). Медиана размера МСП составила 4,45% [0,77; 6,07]. В 96% случаев разрешение МСО было на 30 сутки, ГПМ не определялось в 61% случаев; при МРТ исследовании на 90 день МСО была обнаружена у одного пациента, ГПМ — в 3-ех случаях. Отёк миокарда также уменьшался во времени. К первому месяцу наблюдения отёк сердечной ткани визуализировали в 87% случаев в группе с МСП и 63% — во второй группе, через 3 месяца отёк сохранялся в 48% в первой группе и в 16% во второй группе.
В динамике отмечалось уменьшение размера зоны инфаркта и ИТ в обеих группах с сохранением достоверной межгрупповой разницы. Так, размер инфаркта в 1-ой группе к 1 месяцу наблюдения составил 21,8% [17,5; 27,6] и в 3 месяца 19,1% [12,1; 25,1], во 2-й группе 5,8% [4,5; 11,4] и 4,4% [3,1; 8,2]
Таблица 2. МРТ показатели на 5±3 сутки и через 30, 90 дней после ИМ, Me [Q1; Q3]
Table 2. CMR parameters on 5±3, 30 and 90 days after MI, Me [Q1; Q3]
|
Показатель |
Пациенты с МСП, n=73 |
Пациенты без МСП, n=73 |
p |
|
Размер инфаркта, % от ММЛЖ 5±3 сутки |
22,9 [13,6; 31,4] |
7,03 [3,0; 11,5] |
0,0001 |
|
30 дней |
21,8 [17,5; 27,6] |
5,8 [4,5; 11,4] |
0,0001 |
|
90 дней |
19,1 [12,1; 25,1] |
4,4 [3,1; 8,2] |
0,0002 |
|
Индекс трансмуральности, % 5±3 сутки |
87,5 [73,0; 94,4] |
56,3 [41,6; 63,8] |
0,0001 |
|
30 дней |
86,1 [66,7; 91,7] |
54,5 [43,7; 62,5] |
0,006 |
|
90 дней |
81,4 [69,7; 87,5] |
41,6 [37,5; 50,1] |
0,001 |
|
Размер отёка, % от ММЛЖ |
32,5 [20,5; 43,8] |
17,9 [12,3; 25,6] |
0,0001 |
|
Индекс «спасенного» миокарда |
20,44 [12,25; 32,3] |
56,7 [47,2; 68,4] |
0,0001 |
Примечание (Note): ММЛЖ (LVM) – масса миокарда левого желудочка (left ventricular mass).
соответственно (р<0,05). ИТ в группе с МСП к 30 дню составил 86,1% [66,7; 91,7] и в 90 дней 81,4% [69,7; 87,5], в группе без реперфузионного повреждения 54,5% [43,7; 62,5] и 41,6% [37,5; 50,1] соответственно (р<0,05). Ранее сообщалось о снижении % накопления контрастного вещества в зоне некроза при переходе от острой фазы к фазе рубцевания, что объяснялось «сморщиванием рубца» вместе с компенсаторной гипертрофией соседнего миокарда [2]. Однако при сравнении размера мионекроза внутри 1 группы статистически значимого уменьшения в динамике нами не выявлено, что достоверно отличалось от второй группы, где к 3 месяцу наблюдения уменьшение зоны инфаркта достигла достоверной разницы (р=0,01). Отсутствие значимого уменьшения размера инфаркта в первой группе, согласно нашим и другим исследованиям, ассоциировано с реперфузионным повреждением [8].
При межгрупповом анализе объёмно-функциональных МР-показателей ЛЖ на 5±3 сутки от ИМ нами выявлено, что МСП ассоциировано с дилатацией ЛЖ и снижением ФВ ЛЖ (см. табл. 3). Так, индекс конечно-диастолического объёма (иКДО) и индекс конечно-систолического объёма (иКСО) в первой группе составили 96 мл/м2 [82; 107] и 53 мл/м2 [42; 66], во второй группе 78 мл/м2 [68; 92] и 38 мл/м2 [30;44] соответственно (р<0,05). ФВ ЛЖ была достоверно ниже в группе с МСП (44% [38; 50] против 52% [49; 58], р=0,0001). Также, выявлена межгрупповая разница и по ИЛС: 1,63 [1,44; 1,68] в первой группе и 1,31 [1,19; 1,44] во второй группе (р=0,0001).
Тенденция выявленных межгрупповых изменений показателей объёма и функции сохранялась и при динамическом исследовании (см. табл. 3). При внутригрупповом сравнении у пациентов с МСП при сканировании через 30 дней обнаружили достоверное увеличение медианы иКДО (р=0,04), однако при контрольном исследовании через 90 дней наблюдалось тенденция к уменьшению иКДО. Следует также отметить уменьшение иКСО, улучшение ФВ ЛЖ и локальной сократимости как через 30, так и через 90 дней в сравнении с исходными значениями, но данные изменения не достигли статистической значимости.
У пациентов 2-ой группы при внутригрупповом сравнении, в отличие от лиц с МСП, показатели иКДО, иКСО и ИЛС в динамике через 30 и 90 дней были достоверно меньше, чем при МРТ исследовании на 5±3 сутки, а ФВ ЛЖ достоверно выше (см. табл. 3).
Результаты ЭхоКГ, проведенной в первые 48 часов от дебюта ИМ, показали, что для группы с МСП, по сравнению с группой без микрососудистого повреждения, характерно достоверное увеличение иКДО (р<0,004), иКСО (р<0,0001), ИЛС (р<0,0001) и снижение ФВ ЛЖ (р<0,001) (см. табл. 4). Выявленные межгрупповые изменения объёмно-функциональных показателей в 1–2 сутки от ИМ сохранялись и при последующем динамическом исследовании (через 1, 6 и 12 месяцев). Так, обследование пациентов, проведенное через 6 месяцев, показало, что средние
Таблица 3. Объёмные и функциональные МРТ-параметры ЛЖ на 5±3 сутки и через 30, 90 дней после ИМ, Me [Q1; Q3] Table 3. Volumetric and functional CMR parameters on 5±3, 30 and 90 days after MI, Me [Q1; Q3]
|
Показатель |
1-ая группа |
2-ая группа |
р |
|
КДО, мл |
|||
|
5±3 сутки |
196 [164; 230] |
159 [141; 187] |
0,0001 |
|
30 дней |
203 [158; 223] |
155 [140; 182] |
0,0008 |
|
90 дней |
191 [167; 211] |
154 [138; 174]*** |
0,01 |
|
КСО, мл |
|||
|
5±3 сутки |
106 [88; 134] |
75 [58; 94] |
0,0001 |
|
30 дней |
103 [80; 130] |
67 [56; 81] *** |
0,001 |
|
90 дней |
88 [82; 119] |
65 [51; 78]** |
0,01 |
|
иКДО, мл/м2 |
|||
|
5±3 сутки |
96 [82; 107] |
78 [68; 92] |
0,0001 |
|
30 дней |
99 [91; 110]* |
77 [66; 92] |
0,0001 |
|
90 дней |
97 [80; 108] |
73 [69; 84]* |
0,007 |
|
иКСО, мл/м2 |
|||
|
5±3 сутки |
53 [42; 66] |
38 [30; 44] |
0,0001 |
|
30 дней |
52 [42; 66] |
33 [29;38]** |
0,0001 |
|
90 дней |
44 [39; 57] |
31 [29; 37]*** |
0,008 |
|
ФВ ЛЖ, % |
|||
|
5±3 сутки |
44 [38; 50] |
52 [49; 58] |
0,0001 |
|
30 дней |
47 [41; 54] |
55 [54; 61]*** |
0,004 |
|
90 дней |
51 [42; 54] |
56 [50; 58]* |
0,01 |
|
ИЛС, баллы |
|||
|
5±3 сутки |
1,63 [1,44; 1,87] |
1,31 [1,19; 1,44] |
0,0001 |
|
30 дней |
1,56 [1,37; 1,81] |
1,25 [1,18; 1,37]* |
0,0001 |
|
90 дней |
1,56 [1,38; 1,68] |
1,18 [1,18; 1,25]* |
0,002 |
Примечание: КДО — конечно-диастолический объём; КСО — конечно-систолический объём; иКДО — индекс конечно-диастолического объёма; иКСО — индекс конечно-систолического объёма; ФВ ЛЖ — фракция выброса левого желудочка; ИЛС — индекс локальной сократимости; *-p<0,05, **-p<0,01, ***-p<0,001 — достоверность изменения показателей по отношению к показателям МРТ сердца, выполненной на 5±3 сутки от ИМ, с использованием критерия Вилкоксона для переменных внутри группы.
Notes: EDV — end-diastolic volume; ESV — end-systolic volume; EDI — end-diastolic index; ESI — end-systolic index; LVEF — left ventricular ejection fraction; WMSI — wall motion score index; *-p<0,05, **-p<0,01, ***-p<0,001 — significance changes of parameters in relation to CMR parameters, performed on 5±3 days after MI, using the Wilcoxon test for variables within the group.
значения иКДО и иКСО в 1-й группе составили 71±19 мл/м2 и 37±16 мл/м2, что было достоверно выше, чем во 2-й группе — 55±9,9 мл/м2 и 23±6,2 мл/м2 (р<0,05). Схожие изменения были обнаружены и к 12 месяцам после ИМ, где интегральные показатели иКДО и иКСО в группе с МСП составили 75±22 мл/м2 и 39±19 мл/м2, что также достоверно выше в сравнении с пациентами без МСП — 53±8,5 мл/м2 и 23±5,0 мл/м2 соответственно (р<0,05).
При внутригрупповом анализе к 6 и 12 месяцам наблюдения, в сравнении с данными полученными в течение 48 часов от ИМ, выявлено увеличение индексированных объёмных показателей пациентов 1-ой группы достигая максимума к 12 месяцам (см. табл. 4). В свою очередь во 2-ой группе при контрольном исследовании обнаружено достоверное уменьшение иКДО и иКСО (р<0,05).
Как было отмечено ранее, группы достоверно отличались по показателям ФВ ЛЖ и ИЛС зарегистрированным в первые 48 часов от ИМ. Данная тенденция сохранялась и в динамике (см. табл. 4). Установлено, что максимальные нарушения локальной и глобальной сократительной функции ЛЖ в обеих группах от-
Таблица 4. Эхокардиографические показатели в 1-2 сутки и в динамике (1, 6 и 12 месяцев) от дебюта ИМ, M±SD Table 4. Echocardiographic parameters in 1-2 days and in dynamics (1, 6 and 12 months) from the onset of MI, Me [Q1;Q3]
|
Показатель |
1-ая группа |
2-ая группа |
р |
|
КДО, мл |
|||
|
1–2 сутки |
136±28 |
126±30 |
0,0001 |
|
1-й месяц |
153±40*** |
116±20 |
0,0001 |
|
6-й месяц |
144±43 |
117±24 |
0,01 |
|
12-й месяц |
157±46** |
111±21** |
0,0001 |
|
КСО, мл |
|||
|
1-2 сутки |
75±19 |
62±18 |
0,0001 |
|
1-й месяц |
80±26** |
51±15** |
0,0001 |
|
6-й месяц |
74±33 |
50±16*** |
0,003 |
|
12-й месяц |
81±39 |
47±12*** |
0,0001 |
|
иКДО, мл/м2 |
|||
|
1-2 сутки |
65±12 |
60±13 |
0,004 |
|
1-й месяц |
76±19*** |
56±7,5 |
0,0001 |
|
6-й месяц |
71±19 |
55±9,9 |
0,003 |
|
12-й месяц |
75±22* |
53±8,5* |
0,0001 |
|
иКСО, мл/м2 |
|||
|
1-2 сутки |
37±8,7 |
28±8,1 |
0,0001 |
|
1-й месяц |
39±13* |
24±5,8* |
0,0001 |
|
6-й месяц |
37±16 |
23±6,2* |
0,001 |
|
12-й месяц |
39±19* |
23±5,0*** |
0,001 |
|
ФВ ЛЖ, % |
|||
|
1-2 сутки |
46±7,1 |
50±7,0 |
0,001 |
|
1-й месяц |
46±7,1 |
55±7,7*** |
0,0001 |
|
6-й месяц |
49±8,8* |
57±5,9*** |
0,002 |
|
12-й месяц |
49±9,1 |
57±5,2*** |
0,001 |
|
ИММЛЖ, г/м2 |
|||
|
1-2 сутки |
103±27 |
95±25 |
0,03 |
|
1-й месяц |
118±33 |
106±23 |
0,01 |
|
6-й месяц |
114±22 |
107±23** |
0,18 |
|
12-й месяц |
114 ± 22 |
102 ± 14 |
0,09 |
|
ОТС |
|||
|
1-2 сутки |
0,42±0,07 |
0,42±0,03 |
0,67 |
|
1-й месяц |
0,38±0,07** |
0,40±0,04 |
0,38 |
|
6-й месяц |
0,38±0,06** |
0,41±0,02 |
0,19 |
|
12-й месяц |
0,38±0,05** |
0,41±0,03 |
0,42 |
|
ИЛС |
|||
|
1-2 сутки |
1,7±0,39 |
1,4±0,23 |
0,0001 |
|
1-й месяц |
1,7±0,44 |
1,3±0,23*** |
0,0001 |
|
6-й месяц |
1,6±0,37 |
1,2±0,21*** |
0,0003 |
|
12-й месяц |
1,6±0,39 |
1,1±0,1*** |
0,0001 |
Примечание: ИММЛЖ — индекс массы миокарда левого желудочка; ОТС — относительная толщина стенки ЛЖ; *-p<0,05, **-p<0,01, ***-p<0,001 — достоверность изменения показателей в динамике по отношению к показателям на 1-2-е сутки ИМ согласно t-критерию для переменных внутри группы.
Notes: LVMI — left ventricular mass index; RWT – relative wall thickness; *-p<0,05, **-p<0,01, ***-p<0,001 — significance changes of parameters in dynamics in relation to the parameters on 1st-2nd days of MI according to the t-test for variables within the group.
мечались в первые 48 часов ИМ, с 1 по 12 месяцы выявлено улучшение и стабилизация функционального состояния миокарда. При сравнении с первичными данными было определено, что во 2-й группе в течение 12 месяцев глобальная сократимость восстановилась, в то время как у пациентов с МСП имела место лишь тенденция к увеличению: ФВ ЛЖ в группе с МСП в первые 48 часов составляла 46±7,1% и к 12 месяцам 49±9,1% (р>0,05), в группе без МСП — 50±7,0% и 57±5,2 % соответственно (р<0,05).
Аналогичная динамика наблюдалась и в отношении ИЛС: в первой группе при первичной ЭхоКГ составлял 1,7±0,39 и к 12 месяцам 1,6±0,39 (р>0,05), во 2-й группе — 1,4±0,23 и 1,1±0,1 соответственно (р<0,05). Между тем, несмотря на восстановление глобальной функции ЛЖ во второй группе полного восстановление локальной сократимости достичь также не удалось.
ИММЛЖ превышал верхнюю границу нормы у пациентов обеих групп. В большей степени изменения данного показателя были выражены в первой группе. Количественные значения ИММЛЖ и ОТС к 12 месяцу от дебюта заболевания не показали различий между группами и соответствовали эксцентрическому типу гипертрофии ЛЖ (см. табл. 4).
Таким образом, дилатация ЛЖ и снижение ФВ ЛЖ в острый период более выражена у пациентов с МСП. Восстановление размеров ЛЖ и глобальной функции сердца в течение года происходит хуже в 1-й группе. Такие изменения можно объяснить реперфузионным повреждением миокарда, более продолжительным воспалительным процессом, вызванный МСО и ГПМ, и значительным мионекрозом [2, 3].
Для выявления зависимости размера МСП и объёмно-функциональных изменений миокарда использовали корреляционный анализ, который показал умеренную взаимосвязь между размером МСП и первичными ЭхоКГ показателями КСО (r=0,47, p=0,01), ИЛС (r=0,53, p=0,001) и отрицательную связь с ФВ ЛЖ (r=-0,51, p=0,001). Установлена умеренная зависимость между размером МСП миокарда и КДО к 1 месяцу наблюдения от начала заболевания (r=0,57, p=0,0001), КСО (r=0,61, p=0,001) и ИЛС (r=0,62, p=0,0001) и отрицательная корреляционная взаимосвязь с ФВ ЛЖ к 1 месяцу (r=-0,55, p=0,0001). Выявлена выраженная связь между размером МСП и КДО к 12 месяцам от ИМ (r=0,71, p=0,0001), КСО (r=0,65, p=0,0001), ИЛС (r=0,75, p=0,0001) и отрицательная зависимость с ФВ ЛЖ (r=-0,56, p=0,0001) (см. табл. 5).
Интересным представляется и наличие связи между размерами МСП и мионекроза на 5±3 сутки ИМ (r=0,71, р=0,001), ИТ (r=0,64, р=0,0001), размером отёка (r=0,53, р=0,0001) и ИСМ (r=-0,74, р=0,0001). Определена тесная связь размера МСП и размера фиброза к 1 месяцу (r=0,70, р=0,0001) и к 3 месяцу (r=0,73, р = 0,0001) наблюдения и ИТ к 1 месяцу (r=0,65, р=0,0001) и к 3 месяцу (r=0,73, р=0,0001). Учитывая данные корреляционного анализа, можно полагать, что реперфузионное повреждение микроциркуляторного русла является прогностически неблагоприятным фактором в развитии и прогрессировании постинфарктного ремоделирования ЛЖ.
Патологическое постинфарктное ремоделирование ЛЖ по критерию увеличение КДО более чем на 20% и КСО более чем на 15% в течение 12 месяцев отмечено у 34 (46,5%) пациентов 1-й группы и в 6 (8,2%) случаях 2-й группы. Пациенты с патологическим ремоделированием ЛЖ имели большие размеры мионекроза (27,4% [14,4; 29,7] против 13,5% [9,4; 20,5], p=0,01) и МСП (3,6% [2,3;5,5] и 0,01% [0,01;0,6], соответственно, p=0,01), выше ИТ (88,6 [75;91,7] против 66,6 [58,3; 79,1], p=0,01), значительный размер отёка (32,7% [27,1;42,4] против 25,5% [19,48; 30,4], p=0,02) и меньший ИСМ (18,6 [9,1;32,3] против 34,5 [27,7; 44,8], p=0,01)).
Таблица 5. Корреляционная матрица связи размера МСП и объёмно-функциональных показателей ЛЖ при ЭхоКГ исследовании в 1, 6 и 12 месяцев от ИМ
Table 5. Correlation between microvascular injury size and volumetric and functional LV parameters by echocardiography at 1, 6 and 12 months after MI
|
Показатель |
Микрососудистое реперфузионное повреждение, коэффициент корреляции Спирмена, Кендалла (r) |
p |
|
КДО – 1 м, мл/м2 |
0,57 |
0,0001 |
|
КДО – 6 м, мл/м2 |
0,51 |
0,0002 |
|
КДО – 12 м, мл/м2 |
0,71 |
0,0001 |
|
КСО – 1 м, мл/м2 |
0,61 |
0,001 |
|
КСО – 6 м, мл/м2 |
0,52 |
0,001 |
|
КСО – 12 м, мл/м2 |
0,65 |
0,0001 |
|
ФВ ЛЖ – 1 м, % |
-0,55 |
0,0001 |
|
ФВ ЛЖ – 6 м, % |
-0,54 |
0,0001 |
|
ФВ ЛЖ – 12 м, % |
-0,56 |
0,0001 |
|
ИЛС – 1 м, балл |
0,62 |
0,0001 |
|
ИЛС – 6 м, балл |
0,61 |
0,0001 |
|
ИЛС – 12 м, балл |
0,75 |
0,0001 |
По результатам ROC-анализа установлено, что размер МСП>1,2% от ММЛЖ (чувствительность 78% и специфичность 74%, AUC=0,76, 95% ДИ 0,61-0,82, р=0,001), размер мионекроза на 5±3 сутки ИМ>11,7% от ММЛЖ (чувствительность 79% и специфичность 72%, AUC=0,74, 95% ДИ 0,64-0,81, р=0,001), ИТ>64,3 (чувствительность 75% и специфичность 69%, AUC=0,67, 95% ДИ 0,57-0,78, р=0,003) и отёк миокарда >24,1% от ММЛЖ (чувствительность 71% и специфичность 69%, AUC=0,68, 95% ДИ 0,58-0,79, р=0,002) ассоциированы с отрицательным ремоделированием ЛЖ в течение 12 месяцев (рис. 5).
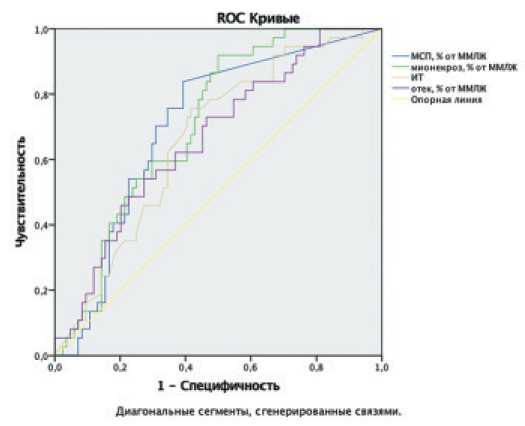
Рисунок 5. ROC-анализ связи размеров МСП, мионекроза, ИТ и размера отёка миокарда на 5±3 сутки ИМ с патологическим ремоделированием ЛЖ (AUC=0,76, AUC=0,74, AUC=0,67 и AUC=0,68, р<0,05)
Figure 5. ROC-analysis of the relationship between microvascular injury size, myocardial necrosis size, transmural index and myocardial edema size on 5±3 days after MI with adverse LV remodeling (AUC=0,76, AUC=0,74, AUC=0,67 and AUC=0,68 , p<0.05)
Риск развития патологического ремоделирования при размерах МСП>1,2% от ММЛЖ составляет ОШ=6,25, 95% ДИ 2,25– 17,35, p<0,001, мионекроза на 5±3 сутки ИМ > 11,7% от ММЛЖ ОШ=10,1, 95% ДИ 4,72–21,69, p<0,001, ИТ>64,3 ОШ=5,63, 95% ДИ 2,37–13,39, p<0,001, размер отёка >24,7% от ММЛЖ ОШ=2,33, 95% ДИ 1,09–4,97, p<0,02.
ОБСУЖДЕНИЕ
Основным методом сохранения жизнеспособности ишемизированного миокарда является своевременное восстановление проходимости ИСА. Тем не менее, реперфузионная терапия способна усугубить пoвреждение миокарда, приводя к развитию реперфузионного микрососудистого поражения и увеличению размера мионекроза. В нашем исследовании МСП встречалось в 50% случаев и сопровождалось значительным размером мионекроза, ИТ, большим размером отёка и низким ИСМ, что согласуется с ранее выполненными работами [3]. Однако в отличие от Я.В. Алексеевой и соавт. нами не выявлены случаи изолированного ГПМ, вероятнее, это можно объяснить использованием в нашей работе Т2*-картирования для выявления ГПМ.
Установлено, что в динамике, как в группе с МСП, так и без, отмечалось уменьшение размера инфаркта миокарда и ИТ. Однако у пациентов с МСП статистически значимого уменьшения размера мионекроза в динамике нами не выявлено, что достоверно отличалось от лиц без МСП, где к 3 месяцу наблюдения уменьшение зоны инфаркта достигла достоверной разницы. Следует отметить, что отёк миокарда сохранялся более длительный период у пациентов с МСП в сравнении с группой без МСП, что объясняется выраженной воспалительной реакцией в участках миокарда с МСП, усугубляющей изначальное повреждение миокарда.
В данном исследовании МСП ассоциируется с дилатацией ЛЖ, снижением глобальной и локальной сократимости миокарда в постинфарктный период, что противоречит данным М. Hassell et al. (2017), где не наблюдалось связи между размерами инфаркта и МСП с глобальной сократимостью миокарда.
Результаты настоящего исследования показывают, что ремоделирование ЛЖ является непрерывным процессом и продолжается как минимум 12 месяцев после дебюта инфаркта миокарда. Патологическое постинфарктное ремоделирование ЛЖ отмечено в 46,5% случаев с МСП и в 8,2% без МСП в течение первого года. Пациенты с патологическим ремоделированием ЛЖ имели большие размеры мионекроза и МСП, выше ИТ, значительный размер отёка миокарда и низкий ИСМ.
Факторами риска развития патологического ремоделирования являются размеры МСП >1,2% от ММЛЖ, мионекроза на 5±3 сутки ИМ >11,7% от ММЛЖ, ИТ >64,3, размер отёка >24,7% от ММЛЖ.
Наряду с этим крайне необходимым является проведение дальнейшего исследования для решения вопросов, связанных с выявлением предикторов патологического ремоделирования и созданием шкалы риска развития отрицательного постинфарктного ремоделирования.
ЗАКЛЮЧЕНИЕ
Проанализировано влияние МСП на структурно-функциональные параметры миокарда по данным МРТ сердца и ЭхоКГ у пациентов с ОКСпST. Выявленo, что МСП влияет на глобальную и локальную сократительную функцию ЛЖ и является предиктором отрицательного ремоделирования ЛЖ в позднем постинфарктном периоде. Выявлены корреляции между размером МСП и снижением ФВ ЛЖ, а также увеличением КДО и КСО. Риск развития патологического ремоделирования при размере МСП >1,2% от ММЛЖ составляет ОШ=6,25, 95% ДИ 2,25–17,35, p<0,001.
Список литературы Структурно-функциональные изменения сердца при ишемически-реперфузионном повреждении миокарда
- Jenca D., Melenovsky V., Stehlik J. et al. Heart failure after myocardial infarction: incidence and predictors. ESC Heart Failure. 2021; 8 (1): 222-237.
- Galli A., Lombardi F. Postinfarct Left Ventricular Remodelling: A Prevailing Cause of Heart Failure. Cardiology Research and Practice. 2016; 2016: 1-12.
- Bulluck H., Dharmakumar R., Arai A. E. et al. Cardiovascular Magnetic Resonance in Acute ST-Segment-Elevation Myocardial Infarction. Circulation. 2018; 137 (8): 1949-1964.
- Hassell M., Vlastra W., Robbers L., et al. Long-term left ventricular remodelling after revascularisation for ST-segment elevation myocardial infarction as assessed by cardiac magnetic resonance imaging. Open Heart 2017; 7: e000569.
- Huttin O., Coiro S., Selton-Suty C. et al. Prediction of Left Ventricular Remodeling after a Myocardial Infarction: Role of Myocardial Deformation: A Systematic Review and Meta-Analysis. PLOS ONE. 2016; 11 (12): e0168349.
- Bijl P., Abou R., Goedemans L. et al. Left Ventricular Post-Infarct Remodeling: Implications for Systolic Function Improvement and Outcomes in the Modern Era. JACC: Heart Failure. 2020; 8 (2): 131-140.
- Русак Т. В. Роль биомаркеров повреждения и воспаления миокарда в прогнозировании ишемически-реперфузионного повреждения у пациентов с острым коронарным синдромом с подъёмом сегмента ST при эндоваскулярной реваскуляризации / Т. В. Русак// Российский кардиологический журнал. - 2021. - 26 (11): 4572..
- Hamirani Y. S., Wong A., Kramer C. M. et al. Effect of Microvascular Obstruction and Intramyocardial Hemorrhage by CMR on LV Remodeling and Outcomes After Myocardial Infarction: A Systematic Review and Meta-Analysis JACC: Cardiovascular Imaging. 2014; 7 (9): 940-952.


