Структурное состояние ксерогелей на основе жидкого стекла, модифицированных никелем, кобальтом и титаном
Автор: Скорикова Ниле Станиславовна, Фофанов Анатолий Дмитриевич, Осауленко Роман Николаевич, Алешина Людмила Александровна, Кудина Елена Федоровна
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Физико-математические науки
Статья в выпуске: 6 (135), 2013 года.
Бесплатный доступ
Представлены результаты рентгенографических исследований атомной структуры ксерогелей на основе жидкого стекла (ЖС), модифицированных никелем, кобальтом и титаном. Исходный образец ксерогеля был получен из водного раствора силиката натрия при дегидратации до постоянного веса при 200 °C. В качестве водного раствора щелочного силиката использовали стандартное натриевое ЖС (ГОСТ 13078, силикатный модуль n = 2,9 ± 0,1 плотность р = 1,45 г/см 3). Композиции ЖС-Me (Ме = Co, Ni и Ti) были получены совмещением модификатора с водным раствором ЖС и последующей дегидратацией до постоянного веса при 200 °C. При изучении структуры использовался метод Уоррена - Финбака: из кривых распределения парных функций D (г) были рассчитаны радиусы координационных сфер и координационные числа для всех исследованных образцов. Полученные характеристики ближнего порядка во взаимном расположении атомов могут быть использованы для формирования компьютерных моделей пространственного расположения атомов в исследованных ксерогелях. Анализ характеристик ближнего порядка показал, что при легировании ЖС Co, Ni и Ti кремний-кислородные тетраэдры сохраняются, при этом в рассматриваемых системах характер возникающего ближнего порядка носит черты расположения атомов в кристаллических фазах близкого состава, однако взаимная ориентация координационных многогранников в пространстве отличается.
Жидкое стекло, ксерогель, рентгенографический анализ, ближний порядок, рентгеноаморфный
Короткий адрес: https://sciup.org/14750491
IDR: 14750491 | УДК: 539.264:661.683
Structural state of xerogels based on water glass modified by cobalt, nickel, and titanium
Results of the X-ray study of the atomic structure of xerogels based on water glass (WG) modified by nickel, cobalt, and titanium are presented. The original xerogel sample was obtained from a standard sodium water glass during dehydration to constant weight at 200 °C. An aqueous solution of alkali silicate was a standard sodium water glass (WG, state standard 13078, silicate modulus n = 2,9 ± 0,1, density p = 1,45 g/cm 3). The WG-Co, WG-Ni and WG-Ti compositions were obtained by the combination of the modifier and the aqueous solution of WG during further dehydration to constant weight at 200 °C. Experimental results were processed with the use of Warren - Finbak method: using pair function curves D(r) radii of coordination spheres and coordination numbers were calculated for all of the investigated samples. The obtained short-range order characteristics can be used to generate computer models of the studied xerogels with spatial arrangement of atoms. Analysis of the short-range order characteristics showed that the silicon-oxygen tetrahedra are saved in WG modified by Co, Ni and Ti. In these systems, the short-range order is similar to the atomic arrangement in crystalline phases of comparable composition, but the mutual orientation of the coordination polyhedra in space is different.
Текст научной статьи Структурное состояние ксерогелей на основе жидкого стекла, модифицированных никелем, кобальтом и титаном
Материалы, находящиеся в аморфном состоянии, являются предметом многих современных теоретических и экспериментальных исследований. Особый интерес представляет высокодисперсный аморфный кремнезем, который обладает целым комплексом свойств, позволяющих широко использовать его как активный наполнитель для полимерных и смазочных материалов, сорбентов в хроматографии, а также в би- отехнологии, медицине, фармации и сельском хозяйстве [9], [14]. На базе высокодисперсных кремнеземных порошков, синтезированных на основе жидкого стекла, создаются новые машиностроительные материалы с повышенными физико-механическими характеристиками [5], [10], [11], [15], [16]. Одним из методов кардинального изменения свойств кремнезема является его химическое модифицирование [4], [6], [17], позволяющее синтезировать порошки с новыми
свойствами. Получение материалов со строго заданными свойствами всегда связано с четким пониманием особенностей их структуры. Таким образом, изучение структурных изменений в высокодисперсных кремнеземных порошках, синтезированных на основе жидкого стекла, при модифицировании их различными добавками является актуальной научно-технической задачей. Целью работы было исследование структурных изменений образцов ксерогелей, полученных из водного раствора щелочного силиката (ВРС) при модифицировании никелем, кобальтом и титаном.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Образец ксерогеля был получен из водного раствора силиката при дегидратации до постоянного веса при 200 °C. В качестве водного раствора щелочного силиката использовали стандартное натриевое жидкое стекло (ЖС, ГОСТ 13078, силикатный модуль n = 2,9 ± 0,1, плотность ρ = 1,45 г/см3). Композиции ЖС-мeталл получали совмещением модификатора, в роли которого выступали соли металлов TiC2O5, NiSO4 и CoSO4, с водным раствором ЖС, после чего смеси дегидратировали, высушивали при 325–330 К, диспергировали и просеивали. Исследования атомной структуры проводили методом рентгеноструктурного анализа. Рентгенограммы получены на дифрактометрах типа ДРОН в Сu- и Mo-Kα-излучениях, монохрома-тизированных кристаллами пиролитического графита в первичных и отраженных лучах. Рентгенографирование образцов проводилось в геометриях на отражение и на просвет в интервале углов рассеяния 2 0 от 2 до 145° с шагом по углам от 0,2 до 0,5° и временем экспозиции в каждой точке 20 с.
Полученные в эксперименте кривые распределения интенсивности рассеяния нормировались на составы: Na2Si3O7, Na2Si3O10.12Co0.78S0.78, Na2Si3O9.88Ni0.72S0.72 и Na2Si3O11Ti0.8C1.6, которые были рассчитаны из данных о композициях ЖС – соли металлов. При анализе результатов эксперимента использовался метод Уоррена – Финбака.
Из нормированных экспериментальных зависимостей интенсивности рассеяния I ( S ) от длины дифракционного вектора S = (4 n sin 0 ) / X рассчитывались функции H ( S ), являющиеся подынтегральными для расчета кривой распределения парных функций D ( r ) и равные:
H ( S ) = S ■ i ( S )exp( - a 2 S 2) g - 2( S ) , (1)
где i(S) – интерференционная функция рассеяния, exp(-a2S2) - множитель затухания. Функция g–2 (S) представляет собой фактор обострения и вводится для повышения контрастности интерференционной картины при больших значениях S. Численным интегрированием функ- ции H(S) рассчитывали кривую распределения парных функций D(r):
max
D ( r ) = 2 n 2 r p e £ Z j + J H ( S )sin( Sr ) dS , (2) j 0
где ρe – средняя электронная плотность, Zj – атомный номер j -го элемента, входящего в состав исследуемого материала.
Экспериментальную функцию D ( r ) можно представить в виде суммы функций парного взаимодействия атомов Pij ( r ), каждая из которых домножена на отношение координационного числа к радиусу соответствующей координационной сферы:
N
D ( r ) = £ £ — ^ -( r ) . (3) ij r ij
Парная функция Pij ( r ) характеризует распределение электронной плотности отдельно взятой пары атомов, находящихся на расстоянии rij друг от друга. Значения парных функций в зависимости от расстояния r рассчитываются из известных данных о функциях атомного рассеяния атомов i , j . Детально методика введения поправок в экспериментальные кривые распределения интенсивности и обоснование расчета H ( S ) и D ( r ) по формулам (2, 3) изложены в работах [2], [19].
Поскольку кривая распределения парных функций D ( r ) линейно связана со значениями координационных чисел Nij , то, задавая значения радиусов rij координационных сфер и их дисперсий σij , координационные числа Nij можно рассчитать методом наименьших квадратов (МНК). Дальнейший анализ структуры проводился в несколько этапов [8]:
-
1. Поиск кристаллических модификаций, химический состав которых соответствует химическому составу исследуемых материалов;
-
2. Расчет для каждой кристаллической фазы наборов радиусов координационных сфер, их дисперсий и координационных чисел;
-
3. Использование рассчитанных для кристаллических модификаций значений радиусов координационных сфер и их дисперсий в качестве исходных данных для расчета координационных чисел МНК из D ( r )эксп;
-
4. Варьирование значений радиусов и их дисперсий с одновременным расчетом (на каждом шаге) координационных чисел МНК до тех пор, пока различие между D ( r )эксп и D ( r )выч не станет меньше или равным погрешности в значениях D ( r ) эксп во всех точках интервала подгонки;
-
5. Сопоставление рассчитанных из эксперимента характеристик ближнего порядка ( rij , σij и Nij ) с соответствующими данными, рассчитанными для кристаллических фаз. Анализ различий между ними, интерпретация полученных результатов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Введение в исходную силикатную матрицу модифицирующих добавок меняет наблюдаемую картину рассеяния рентгеновских лучей: изменяется форма основного диффузного максимума и появляются дополнительные максимумы. Следует отметить, что ход кривых рассеяния, полученных от образцов, модифицированных никелем (Ni) и кобальтом (Co), подобен. На кривой рассеяния образцов с титаном (Ti) присутствуют очень слабые линии кристаллической фазы. На всех кривых появляется интенсивное рассеяние в области малых углов, которое не наблюдалось для исходного ксерогеля. Следовательно, при введении в силикатную матрицу ионов металлов возникают достаточно крупные области неоднородностей электронной плотности.
Рентгенографирование образцов с использованием разного типа излучений позволяет получить картины рассеяния в отличных друг от друга пределах значений длины дифракционного вектора S, что увеличивает информативность дифракционного эксперимента. На рис. 1 срав- ниваются картины рассеяния образцами ЖС с интеркалированными в него ионами кобальта и титана, полученные на излучениях CuKα и MoKα .
На рис. 1а видно, что интенсивное рассеяние в области малых углов (рис. 1б), которое наблюдается при проведении эксперимента на излучении MoK α , выявляется как дополнительный диффузный максимум на излучении CuK α . Аналогичный эффект наблюдается и для системы ЖС-Ni. Данный максимум, по-видимому, обусловлен когерентным рассеянием регулярно расположенными неоднородностями электронной плотности примерно одного и того же размера. Для системы ЖС-Ti на картине рассеяния, полученной на излучении CuK α , наблюдается перегиб при значении S, примерно соответствующем положению первого максимума на рис. 1а, и рост интенсивности рассеяния с уменьшением угла. Более детальную информацию о природе и характере распределения неоднородностей электронной плотности можно получить методом малоуглового рассеяния (МУР) [7].
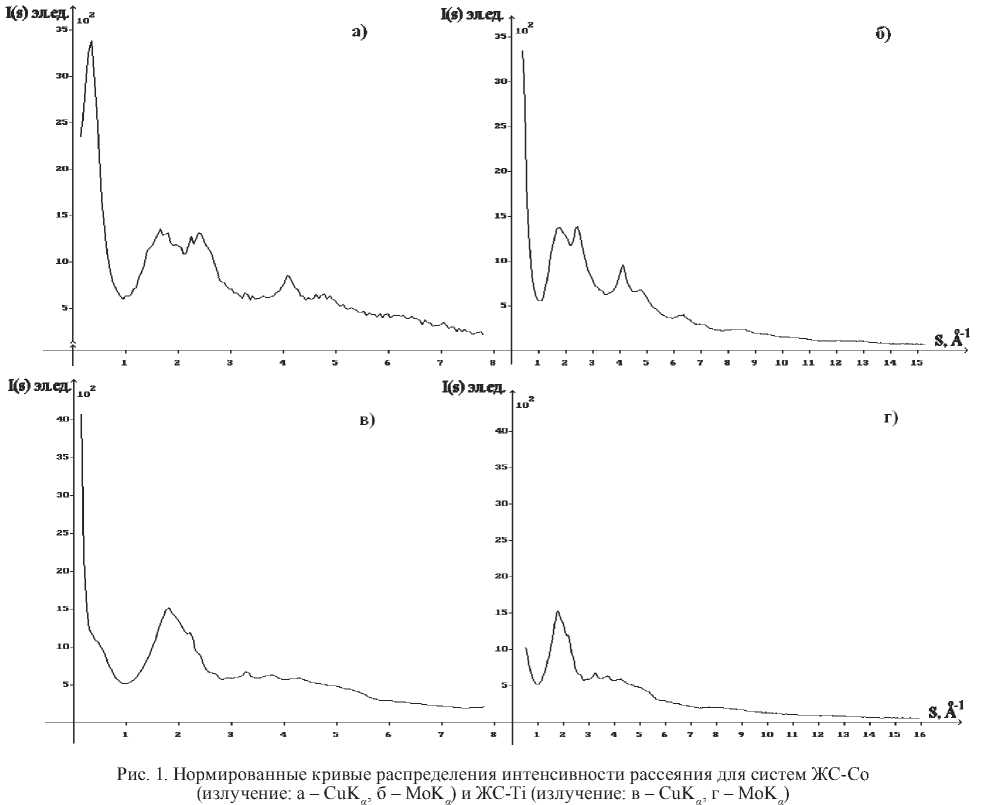
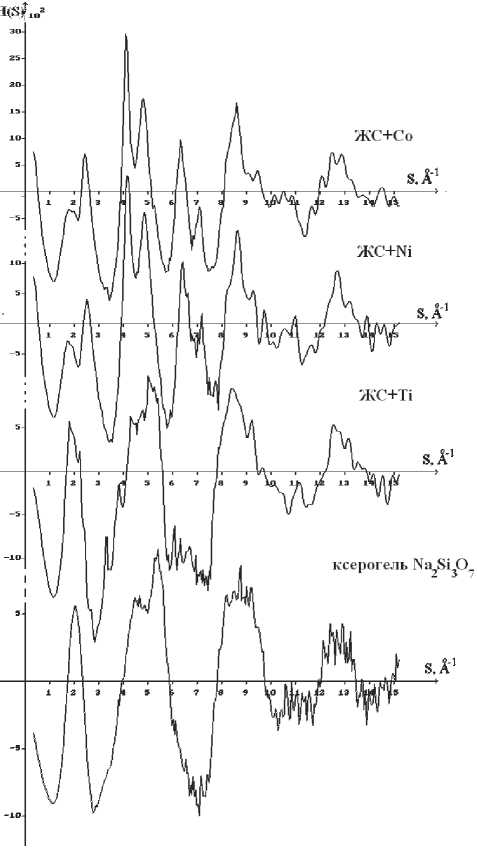
Рис. 2. S-взвешенные интерференционные функции рассе- яния для образцов с интеркалированными в силикатную матрицу ионами Co, Ni, Ti в сравнении с таковыми для образца ксерогеля, полученного дегидратацией при 200 °C
На рис. 2 и 3 представлены функции H ( S ) и D ( r ) для образцов с интеркалированными в силикатную матрицу ионами кобальта, никеля и титана в сравнении с таковыми для образца ксерогеля, полученного дегидратацией при 200 ° C.
На кривых распределения S -взвешенных интерференционных функций H ( S ) (рис. 2) более ярко выражены различия в дифракционной картине, чем на кривых распределения I ( S ). Как следует из рис. 2, интерференционные функции H ( S ), полученные для образцов с Ni и Co, близки друг к другу. Кривая распределения H ( S ) для образца с Ti ближе к таковой для исходного ксерогеля. Следовательно, характер взаимного расположения атомов в системах ЖС-Co и ЖС-Ni подобен, но отличается от упорядочения в исходном (нелегированном) ЖС. Легирование титаном изменяет кривую H ( S ) по сравнению с H ( S ) от
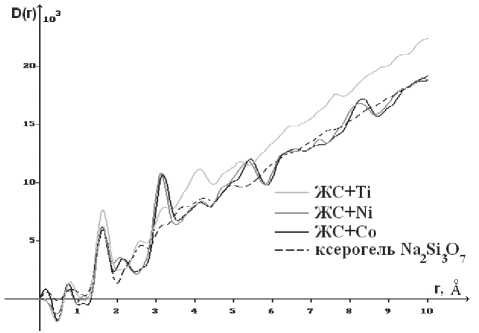
Рис. 3. Кривые распределения парных функций D(r) для образцов с интеркалированными в силикатную матрицу ионами Co, Ni, Ti в сравнении с таковыми для образца ксерогеля, полученного дегидратацией при 200 °C
ЖС не столь значительно. Присутствие на кривой H ( S ) для образца ЖС-Ti небольших узких пиков означает, что он содержит некоторое количество кристаллической фазы, идентифицировать которую из-за малого числа отражений не удалось.
Из анализа кривых распределения парных функций D ( r ), представленных на рис. 3, видно, что первый максимум для всех образцов наблюдается при r = 1,62 Å, что отвечает среднему значению кратчайших расстояний Si-O в тетраэдрах SiO4. Ход зависимостей D ( r ) отличается друг от друга, что свидетельствует о различии ближнего порядка в расположении атомов. Осцилляции на кривых D ( r ) затухают при различных значениях r , следовательно, дальность корелляции ( RD ) в расположении атомов различна: для образцов с Ti и исходного ксерогеля R D ~ 5 А, а для образцов с Ni и Co значение RD почти вдвое выше ( R D ~ 9 А). Таким образом, при интеркалировании в силикатную матрицу ионов Ni и Co размеры области ближнего упорядочения увеличиваются.
Для всех рассматриваемых образцов из кривых распределения парных функций D ( r ) методом последовательных приближений [2] были рассчитаны радиусы rij и размытия σij (дисперсии радиусов) координационных сфер. Координационные числа вычислялись при решении системы условных уравнений (3) методом сингулярного разложения, который оказался более устойчивым по сравнению со стандартным МНК. Результаты расчетов приведены в табл. 1–3. Погрешности в определении радиусов A r ij = ± 0,01 А и дисперсии радиусов Δ σij = 0,02 Å.
Из табл. 1 видно, что в исходном состоянии ЖС характер ближнего упорядочения подобен порядку в кристаллической фазе Na2Si3O7 [13]: различия в значениях радиусов координационных сфер незначительно выходят за пределы погрешности. Число ближайших кислородных
Таблица 1
Результаты расчета характеристик ближнего порядка для исходного ксерогеля в сравнении с данными, рассчитанными для кристаллической фазы Na2Si3O7
При внедрении в ЖС кобальта характер ближнего порядка становится подобен таковому для кристаллической фазы Na2CoSi4O10 (табл. 2). Об этом свидетельствует тот факт, что значения радиусов координационных сфер практически одинаковы. Следует отметить, что в табл. 2 и 3 для координационных сфер разного типа, имеющих одинаковые радиусы, для сравнения с экспериментом были рассчитаны средневесовые значения радиусов
Анализ данных, представленных в табл. 2, показывает, что кобальт, внедряясь в структуру ЖС, стремится окружить себя атомами кислорода, мешая при этом образованию кремний-кислородного каркаса из тетраэдров, подобного таковому в ЖС. Об этом свидетельствует понижение координационного числа на сфере O-Si от NO-Si = 1,7 (табл. 1) для исходного ЖС до NO-Si = 1,1 (табл. 2) для системы ЖС-Со. Кремний-кислородные тетраэдры при этом сохраняются (NSi-O = 3,8 ± 0,2).
Кислородное окружение иона Co несколько отличается от такового в кристаллической фазе Na2CoSi4O10. В последней число атомов кислорода, окружающих кобальт, равно 5 (NCo-O = 5), то есть координационный многогранник – четырехугольная пирамида. В системе ЖС-Со координационное число NCo-O = 4,5, то есть наряду с пирамидами СоО5 имеются тетраэдры СоО4.
Необходимо отметить тот факт, что координационные числа, рассчитанные из эксперимента для системы ЖС-Со вплоть до 6-й сферы, близки к данным для кристалла Na2CoSi4O10, однако на 7-й сфере имеет место резкое возрастание числа атомов. Нет совпадения и на последующих двух сферах. Причина этого – изменение взаимной ориентации координационных многогранников кремния и металлов в пространстве.
Характеристики ближнего порядка, полученные для образца с Ni (табл. 2), коррелируют с данными, приведенными для образца с кобальтом, и с данными, рассчитанными для кристалла Na2NiSi4O10, но, в отличие от системы ЖС-Со, в аморфной фазе ЖС-Ni так же, как и в кристалле, никель в основном окружен 5 атомами: NNi-O = 4,9. Тем не менее все рассмотренные выше для системы ЖС-Со особенности в поведении координационных чисел наблюдаются и в системе ЖС-Ni.
Таким образом, при внедрении в ЖС ионов Ni и Co в аморфных системах возникает ближний порядок, близкий к расположению атомов в изо-структурных кристаллических фазах Na2NiSi4O10 и Na2CoSi4O10 [3] в области ближайшего окружения, но отличающийся по взаимной ориентации координационных многогранников в пространстве.
В случае модифицирования ЖС ионами Ti в системе ЖС-Ti ближний порядок становится подобен таковому для кристаллической фазы Na2TiSi4O10 (табл. 3). Об этом свидетельствуют практически совпадающие значения радиусов координационных сфер.
Однако число кремниевых соседей у атома кислорода уменьшается до NO-Si = 1,2 вместо 1,4 для кристаллической фазы Na2TiSi4O10, то есть мотив взаимного расположения тетраэдров SiO4 различен.
Увеличение числа кислородных соседей у атома кремния до 4,2, возможно, обусловлено замещением части атомов кремния в тетраэдрах атомами титана.
Кроме того, число ближайших соседних атомов кислорода у ионов титана (NTi-O = 3,3) вдвое ниже, чем в кристаллической модификации, в которой титан находится в октаэдрической координации. Координационное число для натрия также занижено: NNa-O = 4,1 в системе ЖС-Ti вместо 5 в кристалле. Таким образом, несоответствие координационных чисел, определенных из эксперимента для системы ЖС-Ti, соответствующим данным для кристалла Na2TiSi4O10 начинается уже с ближайшего окружения. С учетом
Таблица 2
Результаты расчета характеристик ближнего порядка для системы ЖС-M в сравнении с данными, рассчитанными для кристаллической фазы Na2MSi4O10 (M = Co, Ni)
ЗАКЛЮЧЕНИЕ
Из анализа характеристик ближнего порядка, рассчитанных для ксерогелей на основе жидкого стекла, модифицированных никелем, кобальтом и титаном, следует, что при образовании систем ЖС-металл кремний-кислородные тетраэдры сохраняются, однако их взаимная ориентация в пространстве меняется. Изменяется и координационное окружение атомов металлов по сравнению с таковым в кристаллах близкого состава.
Полученные в данной работе характеристики ближнего порядка во взаимном расположении атомов могут быть использованы для формирования компьютерных моделей пространственного расположения атомов в исследованных ксерогелях как в исходном состоянии, так и при легировании атомами различных металлов.
Таблица 3
Результаты расчета характеристик ближнего порядка для системы ЖС-Ti в сравнении с данными, рассчитанными для кристаллической фазы Na2TiSi4O10
|
Na2TiSi4O10 [20] |
ЖС-Ti |
||||||||
|
№ сферы |
Объединяемые сферы |
r ij . Å |
Nij. ат. |
Тип сферы |
|
|
r ij . Å |
σij. Å |
Nij±Δ Nij. ат. |
|
1 |
Si-O [O-Si] |
1,62 |
4,00 [1,45] |
Si-O [O-Si] |
1,62 |
4,00 [1,45] |
1,62 |
0,01 |
4,2 ± 0,2 [1,2 ± 0,1] |
|
2 |
Ti-O |
1,97 |
6,00 |
Ti-O |
1,97 |
6,00 |
1,97 |
0,01 |
3,3 ± 0,1 |
|
3 |
Na-O |
2,46 |
5,00 |
Na-O |
2,46 |
5,00 |
2,38 |
0,01 |
4,1 ± 0,2 |
|
4 |
O-O |
2,66 |
5,82 |
O-O |
2,66 |
5,82 |
2,66 |
0,01 |
5,0 ± 0,2 |
|
5 |
Na-O |
2,72 |
2,00 |
Na-O |
2,72 |
2,00 |
2,76 |
0,02 |
0,6 ± 0,1 |
|
6 |
O-O |
2,89 |
0,73 |
O-O |
2,89 |
0,73 |
2,93 |
0,01 |
0,13 ± 0,01 |
|
7 |
Si-Si |
3,05 |
3,00 |
Si-Si |
3,05 |
3,12 |
3,05 |
0,12 |
7,5 ± 0,2 |
|
O-O |
3,08 |
0,36 |
|||||||
|
8 |
Na-Si |
3,21 |
2,00 |
Na-Ti |
3,22 |
3,37 |
3,20 |
0,01 |
0,6 ± 0,1 |
|
Na-Ti |
3,23 |
2,00 |
|||||||
|
O-O |
3,27 |
0,36 |
|||||||
|
9 |
Si-Ti |
3,33 |
1,00 |
Si-Ti |
3,33 |
1,00 |
3,35 |
0,01 |
1,3 ± 0,1 |
|
10 |
Na-O |
3,46 |
1,00 |
Na-Na |
3,54 |
8,28 |
3,52 |
0,03 |
14,2 ± 0,3 |
|
Na-Na |
3,51 |
2,00 |
|||||||
|
Si-O |
3,56 |
6,00 |
|||||||
|
11 |
Na-Si |
3,61 |
4,00 |
Na-Si |
3,61 |
5,21 |
3,61 |
0,05 |
4,0 ± 0,2 |
|
O-O |
3,64 |
2,91 |
|||||||
* Работа выполнена при поддержке Программы стратегического развития ПетрГУ в рамках реализации комплекса мероприятий по развитию научно-исследовательской деятельности на 2012–2016 гг.
Список литературы Структурное состояние ксерогелей на основе жидкого стекла, модифицированных никелем, кобальтом и титаном
- Алешина Л. А., Ковалев-Троицкий К. Л., Макаров А. М., Никитина Е. А., Фофанов А. Д. Моделирование распределения атомов Alв ГЦК кислородной подрешетке окисла Al2O3. Деп.в ВИНИТИ. 1992. № 2524. В92. 16 с.
- Алешина Л. А., Фофанов А. Д. Рентгеноструктурный анализ аморфныгх материалов. Петрозаводск: Изд-во ПГУ, 1987. 85 с.
- Анфилогов В. Н., Быков В. Н., Осипов А. А. Силикатные расплавы. М., 2005. 357 с.
- Кудина Е. Ф., Злотников И. И., Плескачевский Ю. М. Модифицирование жидкого стекла активными добавками: (обзор)//Материалы. Технологии. Инструменты. 2000. Т. 5. № 2. С. 36-40.
- Кудина Е. Ф., Плескачевский Ю. М., Буря И. А. Органосиликатные нанокомпозиты: получение, структура, свойства//Вестник Фонда фундаментальных исследований. 2008. № 3. С. 16-28.
- Максимов А. И., Мошников В. А., Таиров Ю. М., Шилова О. А. Основы золь-гель-технологии нанокомпозитов. СПб.: Элмор, 2008. 255 с.
- Свергун Д. И., Фейгин Л. А. Рентгеновскоеи нейтронное малоугловое рассеяние. М., 1986. 280 с.
- Фофанов А. Д. Структураи ближний порядокв кислород-и углерод-содержащих системахс особыми свойствами: Автореф. дис.. д-ра физ.-мат. наук. М., 1998. 32 с.
- Шилова О. А., Шилов В. В. Нанокомпозиционные оксидныеи гибридные органо-неорганические материалы, получаемые золь-гель методом. Синтез. Свойства. Применение//Наносистемы, наноматериалы, нанотехнологии: Сб. науч. тр. Т. 1. Киев: Академпериодика, 2003. С. 9-83.
- Chen Yung-Chin, Tsai Chi-Che, Lee Yu-Der. Preparation and properties of silylated PTFE/SiO2 organic-inorganic hybrids via sol-gel process//J. Polym. Sci. A. 2004. Vol. 42. № 7. P. 1789-1807.
- Davis S. R., Brough A. R., Atkinson A. Formation of silica/epoxy hybrid network polymers//J. Non-Crist. Solids. 2003. Vol. 315. № 1/2. P. 197-205.
- Durand G., Vilminot S., Richard-Plouet M., Derory A., Lambour J. P., Drillon M. Magnetic behavior of Na2MSi4O10 (M=Co, Ni) compounds//Journal of Solid State Chemistry. 1997. Vol. 131. № 2. P. 335-340.
- Kahlenberg V, Marler B., Munoz Acevedo J. C., Patarin J. Ab initio crystal structure determination of Na2Si3O7 from conventional powder diffraction data//Solid State Sciences. 2002. Vol. 4. P. 12.
- Kudina E. F. Synthesis and Properties of Dispersed Hybrid Materials Based ona Silicate Matrix//Glass Physics and Chemistry. 2012. Vol. 38. № 1. P. 172-179.
- Kudina E. F., Kushnerov D. N., Tyurina S. I., Chmykhova T. G. Effect of Dispersed Organic Silica on the Tribological Behavior of Greases//Journal of Friction and Wear. 2003. Vol. 24. № 5. P. 71-76.
- Kudina E. F., Pechersky G. G. Nanostructured Organosilicate Composites: Production, Properties, Application//Resin Composites: Properties, Production and Application/Ed. D. B. Song. N. Y.: Nova Science Publishers, 2011. Ch. 3. P. 101-128.
- Kudina E. F., Pleskachevskii Yu. M. Modification of Alkali Silicate Solutions by Organic Reagents and Investigation of the Properties of the Final Products//Glass Physics and Chemistry. 2009. Vol. 35. № 4. P. 442-448.
- Peacor D. R., Buerger M. J. The determination and refenement of the structure of narsarsukite, Na2TiOSi4O//Amer. Mineral. 1962. Vol. 47. № 5, 6. P. 539-556.
- Warren B. E. X-ray diffraction. N. Y.: Mass, 1969. 563 p.


