Структурные характеристики диоксидов (МеO2) d-элементов 4-7 групп таблицы Д.И. Менделеева
Автор: Рябухин Александр Григорьевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия твёрдого тела
Статья в выпуске: 12 (229), 2011 года.
Бесплатный доступ
По уравнениям моделей эффективных ионных радиусов и метаморфозы кристаллических структур из рентгеновских параметров тетрагональных решеток диоксидов МеO2 (Ті, Nb, Та, Cr, Мn) рассчитаны их структурные характеристики (межструктурные расстояния Ме-О, эффективные радиусы О2- в составе диоксидов). Вычисленные радиусы Ме4+ совпадают с полученными ранее из параметров решеток соединений кубической сингонии (галиды, карбиды, силициды).
Диоксиды, d-элементы, структурные характеристики, ионные радиусы
Короткий адрес: https://sciup.org/147160197
IDR: 147160197 | УДК: 548.314.5+669.046
Structural characteristics of d-elements dioxides (MeO2) belonging to 4-7 groups of the periodic table
According to the model equations for effective ionic radii and crystal structure metamorphosis the structural characteristics of MeO2 (Ті, Nb, Та, Cr, Mn) dioxides tetragonal lattices have been calculated (Me-O interstructural distances, O2- effective radii in dioxides), from the X-ray parameters. The calculated Me4+ radii agree with those obtained earlier from the lattice parameters of cubic singony compounds (halides, carbides, suicides).
Текст научной статьи Структурные характеристики диоксидов (МеO2) d-элементов 4-7 групп таблицы Д.И. Менделеева
С кислородом взаимодействуют практически все химические элементы, образуя оксиды. Горные породы и содержащиеся в них минералы в подавляющем большинстве представляют собой именно оксидные системы. Многие оксиды имеют самостоятельное применение, большинство из них - это промежуточные вещества в различных технологиях. Особый интерес представляют оксиды ^/-элементов и среди них диоксиды титана, ниобия, тантала, хрома и марганца. D-элементы - важнейшие легирующие компоненты сталей и разнообразных сплавов, в том числе и собственных. Кристаллохимические свойства оксидов в настоящее время изучены недостаточно.
Результаты расчетов и их обсуждение
Диоксиды (7-элементов (МеО2) кристаллизуются в двух сингониях: моноклинной (структура МоО2, PTJc-T) и тетрагональной (структура TiO2 (SnO2), P^lmnm-T).
Для расчетов структурных характеристик диоксидов используем уравнения математических моделей эффективных ионных радиусов и метаморфозы кристаллических структур в квазикуби-ческую [1,2]. Подробно методика расчетов изложена в работе [3].
Тетрагональная сингония
В этой структуре кристаллизуются диоксиды Ti, Nb, Та, Сг, Мп [4]. Радиусы ионов Ме4+ определены из кубических структур [2].
Порядок расчетов рассмотрим на примере ТЮ2 (рутил), имеющего параметры решетки а = 4,5929; с = 2,9593. Линейные размеры приведены в ангстремах (10-8 см).
Объем элементарной кристаллической ячейки этой сингонии:
V = а1 с = 4,592922,9593 = 62,4256.(1)
Ребро квазикуба:
d = ^V = ^/62,4256 = 3,96693.(2)
Межъядерное расстояние Ме4+-О2” гр:
гр = ad = 0,507306-3,96693 = 2,01245,(3)
где а - структурная постоянная, учитывающая характеристики тетрагональной аТ1 и квазику-бической акк структур:
а = атг а =—-1) = 0,507306.
Дебаевский радиус экранирования rD:
rD=r°D №Дс). (4)
Химия твёрдого тела
Основными фрагментами в структурных группах являются куб, октаэдр, тетраэдр. В качестве Гу в квазикубах выступают Гу (CsCl), Гу (NaCl), ra(ZnF2№), ry (CaF2) и т. д. [1~3]. В рассматриваемом случае Гу = Гу (CaF2) = 15,418081.
Функция заряда /(z):
/(z) = 1 + 7^к za -1 =1 + V4"2-1 = 3,645751.
Функция структуры /(с) содержит постоянные величины, характеризующие исходную /исх и конечную (после преобразования) /кк структуры:
/(с) = /тг/кк
1 + 7з
— = 1,902000. 2
После подстановки полученных величин в ур. (4), получим Гу = 15,418081 -3,645751 -1,902000 = 106,91234.
Радиус катиона г (Ме4+ I:
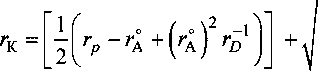
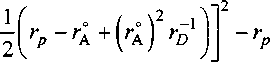
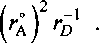
Минимальный радиус иона кислорода согласно [2] составит г°(О2 1 = 1,35806(1), тогда для иона титана в составе ТЮ2:
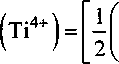
2,01245-1,35806 +
1,844327 \
106,91234 J
+ V 0,1127754-0,0347161 =0,61521.
Постоянство радиуса катиона (минимального радиуса аниона) является подтверждением адекватности расчетов экспериментальным рентгеновским данным. Результаты вычислений радиусов катионов металлов (титана, ниобия, тантала, хрома, марганца) и рентгеноструктурные данные по кристаллическим решеткам их диоксидов приведены в таблице. Полученные значения г(Ме4+ I хорошо согласуются с величинами, рассчитанными ранее [2].
Структурные характеристики диоксидов МеО2
|
МеО2 |
г(Ме4+), [2] |
а, с, [4] |
V, ур.(1) |
d, УР- (2) |
гр’ УР- (3) |
г(ме4+), УР-(5) |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Т1О2(рутил) |
0,61520(d |
4,5929 2,9593 |
62,4256 |
3,96693 |
2,01245 |
0,61521 |
|
P-NbO2 |
0,65886(2) |
4,7060 2,9925 |
66,2732 |
4,04681 |
2,05297 |
0,65836 |
|
ТаО2 |
0,68340(3) |
4,799 3,067 |
68,5887 |
4,09340 |
2,07661 |
0,68338 |
|
СгО2 |
0,65669(з) |
4,420 2,968 |
66,1223 |
4,04373 |
2,05141 |
0,65671 |
|
р-МпО2 |
0,61573(2) |
4,668 2,867 |
62,4726 |
3,96792 |
2,01295 |
0,61574 |
Таким образом, получены величины межструктурных расстояний г , связывающие структурные характеристики веществ и их термодинамические свойства.
Заключение
-
1. Рассчитаны структурные характеристики (межструктурные расстояния Me-О, радиусы О2 в составе МеО2) по рентгеновским параметрам тетрагональных решеток диоксидов ^-элементов (Ti, Nb, Та, Сг, Мп).
Рябухин А.Г.
-
2. Вычисленные радиусы Ме4+ совпадают в пределах доверительных интервалов с полученными ранее из параметров решеток кубических структур галидов, карбидов и силицидов этих металлов.
Структурные характеристики диоксидов (МеОг) d-элементов 4-7 групп таблицы Д.И. Менделеева
Список литературы Структурные характеристики диоксидов (МеO2) d-элементов 4-7 групп таблицы Д.И. Менделеева
- Рябухин, А.Г. Математическая модель метаморфизма кристаллических структур в кубическую/А.Г. Рябухин//Вестник ЮУрГУ. Серия «Металлургия». -Вып. 9. -№ 21(93). -2007. -С. 3-6.
- Рябухин, А.Г. Эффективные ионные радиусы. Энтальпия кристаллической решетки. Энтальпия гидратации ионов: моногр./А.Г. Рябухин. -Челябинск: Изд-во ЮУрГУ, 2000. -115 с.
- Груба, О.Н. Структурные фрагменты силикатов на основе sp-элементов/О.Н. Груба, Н.В. Германюк, А.Г. Рябухин//Вестник ЮУрГУ. Серия «Химия». -Вып. 4. -№ 31(207). -2010. -С. 90-96.
- Химическая энциклопедия. -М.: СЭ -БРЭ. -Т. 3-5. -1992-1998.


