Структурные изменения при моделировании внутрикостных дефектов верхней челюсти
Автор: Киреев Павел Владимирович, Снигур Григорий Леонидович, Фомичев Евгений Валентинович, Ефимова Елена Валерьевна, Ефимов Юрий Владимирович
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 4 (76), 2022 года.
Бесплатный доступ
В статье описаны патогистологические особенности репаративной регенерации костной ткани при моделировании внутрикостных дефектов челюстных костей у белых беспородных крыс
Морфометрия, костны/й дефект, регенерация кости
Короткий адрес: https://sciup.org/142236033
IDR: 142236033 | УДК: 616.314-089
Structural changes in the modeling of intraosseous defects of the upper jaw
The article describes the pathohistological features of reparative regeneration of bone tissue in modeling intraosseous defects of jaw bones in white mongrel rats
Текст научной статьи Структурные изменения при моделировании внутрикостных дефектов верхней челюсти
Совершенствование хирургического лечения пациентов с околокорневыми кистами челюстей возможно не только при применении инновационных методов (тканевая инженерия, регенеративная медицина) но и при оптимизации традиционных методик лечения с применением современных остеопластических материалов [2, 4, 7, 8]. Однако патогистологические изменения костной ткани на разных этапах репаративной регенерации в области дефектов челюстных костей у экспериментальных животных изучены недостаточно, что и послужило поводом к проведению данного исследования.
Цель работы: выявить особенности морфологических изменений при моделировании внутрикостных дефектов верхней челюсти.
Материалы и методы: Экспериментальное исследование выполнено на нелинейных белых крысах. Формирование костного дефекта проводилось в области переднего отдела верхней челюсти. Животные были разделены на две группы: контрольную группу составили интактные крысы (n=8); вторую группу составили животные, у которых восстановление костного дефекта происходило под кровяным сгустком (n=8).
Вывод животных из эксперимента осуществлялся на 7, 14 и 21 сутки. Костно-мышечные фрагменты верхней челюсти фиксировали в 10% растворе нейтрального забуференного формалина (pH=7,4) в течение 24 часов, декальцинировали в растворе этилендиаминтетраацетата натрия. Изготовление и окраску гистологических срезов (гематоксилином и эозином, трихром по Массону) проводили по общепринятым гистоло- гическим методикам [1].
Морфометрически с помощью программного обеспечения (PhotoM 1.21, Россия) определяли удельную площадь костных балок, соединительной и хрящевой ткани (по отношению к общей площади ткани в поле зрения), оценивали интенсивность воспаления и резорбции костной ткани в зоне дефекта. Микрофотосъемку проводили в случайных полях зрения с помощью микроскопа «Axio Scope» (Carl Zeiss, Германия). Статистическую обработку результатов проводили с использованием программы Microsoft office Excel 2007 (Microsoft, США).
Результаты исследования и их обсуждение:
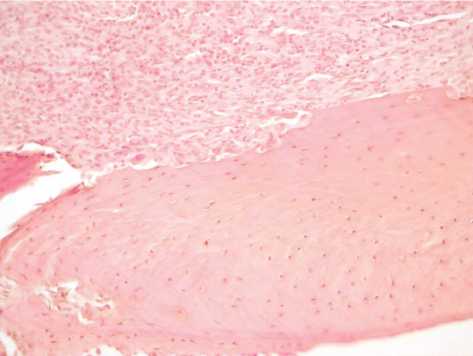
При гистологическом исследовании костной ткани в интактной группе животных во все сроки эксперимента (7, 14 и 21 сутки) отмечалось нормальное строение костной ткани, признаков воспаления не выявлялось, участки остео-кластической или пазушной резорбции костных балок не визуализировались (рис. 1). Удельная площадь костных балок составляла на 7, 14 и 21 сутки эксперимента - 48,3±1,2%, 46,9±2,1% и 43,2±1,8% соответственно, соединительной ткани - 38,4±2,3%, 41,1±1,4% и 36,5±2,7%, хрящевая ткань не определялась (табл. 1).
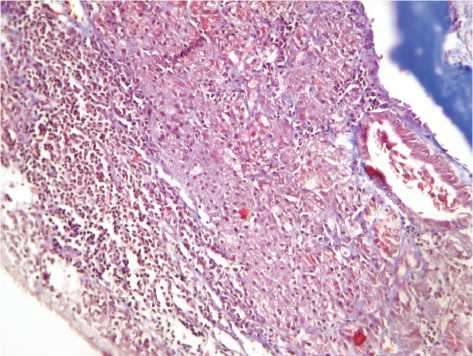
При изучении микропрепаратов во второй группе на 7 сутки в области костного дефекта отмечалась выраженная инфильтрация преимущественно сегментоядерными нейтрофильными гранулоцитами с примесью гистиоцитов, макрофагов и единичных лимфоцитов, неравномерный отёк. Данные изменения являются характерными для ранних сроков деструкции костной ткани [3]. На границе с дефектом в костных балках отмечались единичные гигантские многоядерные остеокласты с формированием лакун остеокластической резорбции, которые составляли 0,2±0,1%, что свидетельствовало о активации ремоделирования костной ткани [7]. Удельная площадь костных балок составляла
33,3±2,8%, соединительной ткани - 44,1±2,9%, хрящевая ткань не определялась (рис. 2. табл. 1). При окраске трихром по Массону на 7 сутки эксперимента определялись единичные тонкие хаотично ориентированные волокна коллагена (рис. 2, табл. 1).
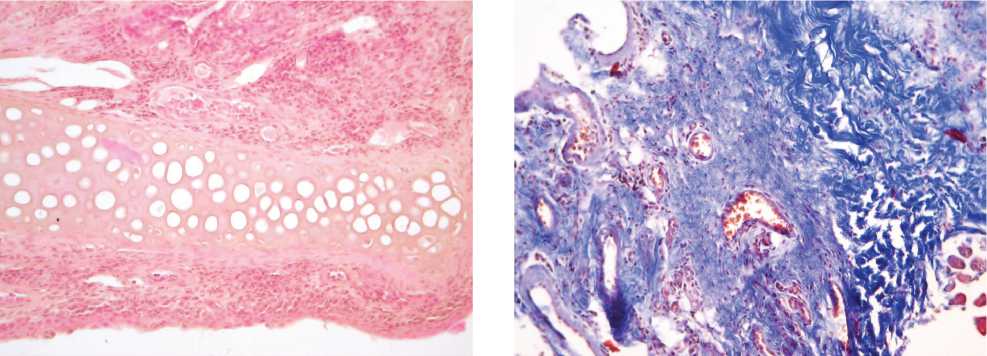
На 14 сутки эксперимента отмечалось уменьшение отека, снижалась интенсивность воспалительной инфильтрации. Количество сегментоядерных нейтрофильных гранулоцитов уменьшалось, в составе экссудате начинали преобладать гистиоциты, макрофаги, лимфоциты и фибробласты. Определялись участки формирования хрящевой ткани. В костных балках признаков формирования остеолиза не визуа-лизирвалось. Удельная площадь костных балок составляла 32,4±3,5%, соединительной ткани -45,8±31%, хрящевой ткани - 32,2±2,7%. В зоне дефекта костной ткани при окраске трихром по Массону на 14 сутки эксперимента определялись структурированные пучки коллагеновых волокон (рис. 2, табл. 1). Данные структурные изменения могут свидетельствовать о недостаточных остеоиндуктивных и остеокондуктивных свойствах кровяного сгустка ввиду отсутствия жесткого каркаса для остеогенных клеток [5, 6].
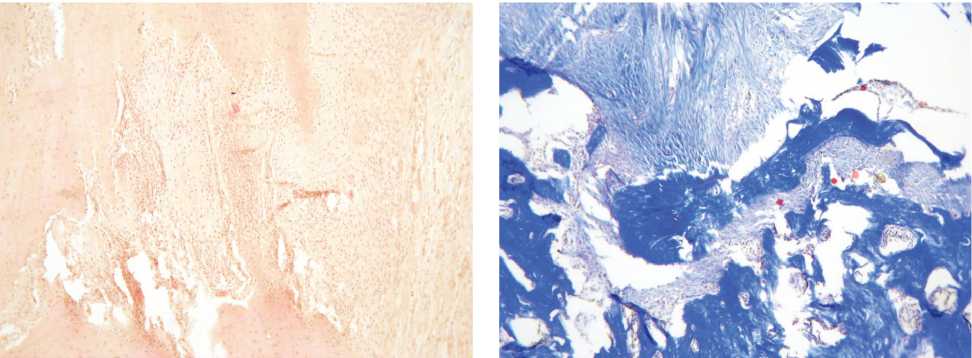
К 21 суткам эксперимента на обзорной окраске сохранялись признаки активной реструктуризации костной ткани в виде незначительной лимфо-гистоицитарной инфильтрации в зоне дефекта, формирования остеоидных и минерализованных костных балок с замещением зоны хрящевой ткани на соединительную ткань (рис. 2). Гистологических признаков остеолиза не выявлялось. Удельная площадь костных балок составляла 28,8±2,4%, соединительной ткани -47,9±5,1%, хрящевой ткани - 9,1±1,3% (табл. 1). При окраске по Массону выявлялась новообразованная костная и соединительная ткани с хаотичным расположением костных балок и разнонаправленными пучками коллагеновых волокон (рис. 2, табл. 1).
Таблица 1.
Морфометрические параметры костного дефекта верхней челюсти (M±m).
|
Морфометрический параметр |
Экспериментальные группы |
Время эксперимента |
||
|
7 сутки |
14 сутки |
21 сутки |
||
|
Удельная площадь костных балок, % |
Интактная |
48,3±1,2 |
46,9±2,1 |
43,2±1,8 |
|
Костный дефект+кровяной сгусток |
33,3±2,8* |
32,4±3,5* |
28,8±2,4* |
|
|
Удельная площадь плотноволокнистой соединительной ткани, % |
Интактная |
38,4±2,3 |
41,1±1,4 |
36,5±2,7 |
|
Костный дефект+кровяной сгусток |
44,1±2,9 |
45,8±31 |
47,9±5,1 |
|
|
Удельная площадь хрящевой ткани, % |
Интактная |
- |
- |
- |
|
Костный дефект+кровяной сгусток |
- |
32,2±2,7 |
9,1±1,3 |
|
* - достоверно по отношению к группе интактного контроля.
Заключение
Результаты гистологического исследования свидетельствуют о развитии острого воспаления в зоне костного дефекта на ранних сроках остеорепарации, которое сменилось признаками репаративной регенерации кости с 14 суток эксперимента. Однако формирование плотноволокнистой соединительной и хрящевой тканей в зоне дефекта не привело к статистически достоверному замещению зоны дефекта полноценной костной тканью даже к 21 суткам исследования. Таким образом, результаты проведенного исследования свидетельствуют о воспроизведении адекватной экспериментальной модели формирования дефектов костной ткани при использовании кровяного сгустка. В силу недостаточных остеоиндуктивных и остеокондуктивных свойств кровяного сгустка во все сроки наблюдения не происходило замещение дефекта новообразованной костной тканью.
АБ
Рис. 1. Костная ткань верхней челюсти интактной группы. А - окраска гематоксилином и эозином, начальное увеличение х400. Б - окраска трихром по Массону, начальное увеличение х100.
А
Б
В
Г
ДЕ
Рис. 2. Костный дефект верхней челюсти, группа сравнения. А - 7 сутки эксперимента. Окраска гематоксилином и эозином, начальное увеличение х400. Б - 7 сутки эксперимента. Окраска трихром по Массону, начальное увеличение х400. В - 14 сутки эксперимента. Окраска гематоксилином и эозином, начальное увеличение х100. Г - 14 сутки эксперимента. Окраска трихром по Массону, начальное увеличение х100. Д - 21 сутки эксперимента. Окраска гематоксилином и эозином, начальное увеличение х100.
Е - 21 сутки эксперимента. Окраска трихром по Массону, начальное увеличение х100.
Список литературы Структурные изменения при моделировании внутрикостных дефектов верхней челюсти
- Основы гистологической техники. Коржевский Д. Э. Гиляров А.В. - Санкт-Петербург, 2010. - 95 c.
- Рахимов З.К., Чиргалиев М.Ж., Пулатова Ш.К. Совершенствование методов лечения радикулярных кист челюстей // Биология и интегративная медицина. - 2019. - № 2. - С. 5-15.
- Bone injury, healing and grafting. In Basic Orthopaedic Sciences. The Stanmore Guide. Bates P., Ramachandran M. Edited by: Ramachandran M. London, 2007. - Р.123-134.
- Chiapasco M., Rossi A., Motta J.J., Crescentini M. Spontaneous bone regeneration after enucleation of large mandibular cysts: a radiographic computed analysis of 27 consecutive cases. - J. Oral Maxillofac Surg. 2000;58(9):942-8.
- Faour O., Dimitriou R., Cousins C.A., Giannoudis P.V. The use of bone graft substitutes in large cancellous voids: any specific needs? - Injury. 2011;42(2):87-90.
- Giannoudis P.V., Dinopoulos H., Tsiridis E. Bone substitutes: an update. - Injury. 2005;36(3):20-7.
- Ho-Shui-Ling A., Bolander J., Rustom L.E., Johnson A.W., Luyten F.P., Picart C. Bone regeneration strategies: Engineered scaffolds, bioactive molecules and stem cells current stage and future perspectives. - Biomaterials. 2018;180:143-162.
- Maumus M., Pers Y.M., Ruiz M., Jorgensen C., Noël D. Cellules souches mesenchymateuses et medecine regeneratrice - Quel avenir pour l'arthrose? [Mesenchymal stem cells and regenerative medicine: future perspectives in osteoarthritis]. - 2018;34(12):1092-1099. French.


