Структурные изменения сосудов микроциркуляторного русла и их окружения в первичной зрительной коре 3- и 18-месячных крыс при фотоповреждении сетчатки, их коррекция
Автор: Бахарева Юлия Олеговна, Варакута Елена Юрьевна, Логвинов Сергей Валентинович, Потапов Алексей Валерьевич, Жданкина Анна Александровна, Плотников Марк Борисович, Солонский Анатолий Владимирович, Герасимов Александр Владимирович, Сагнаева Малика Айтгабуловна
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Физиология
Статья в выпуске: 2, 2020 года.
Бесплатный доступ
Морфофункциональные изменения микроциркуляторного русла играют важную роль в пластичности нервных клеток, их способности менять свое функциональное состояние при воздействии различных факторов. Целью исследования являлось изучение морфологии сосудов микроциркуляторного русла и окружающих их нейронов и глиоцитов в первичной зрительной коре 3- и 18-месячных крыс в норме и при стрессе, вызванном высокоинтенсивным круглосуточным световым воздействием, а также в условиях коррекции. Материалы и методы. Эксперименты выполнены на 60 крысах-самцах линии «Вистар». Возраст -3 и 18 мес. Методами световой и электронной микроскопии, морфометрии оценивали удельную площадь и численную плотность капилляров, удельную площадь измененных (со стазом, сладжем форменных элементов и тромбозом) и неизмененных сосудов, а также морфологию клеток, их окружающих. Для множественных сравнений внутри возрастных групп использовали критерий Крускала-Уоллиса, для парных - Манна-Уитни. Результаты. У 3- и 18-месячных крыс обнаружена различная реакция капилляров на световое воздействие, что выражалось в увеличении численной плотности капилляров у 3-месячных крыс и снижении - у 18-месячных (р
Микроциркуляция, п-тирозол, стресс, первичная зрительная кора
Короткий адрес: https://sciup.org/14117602
IDR: 14117602 | УДК: 611.813.1/.814.4:611.13/.14.08]:616-001.15-08-092.9:599 | DOI: 10.34014/2227-1848-2020-2-123-133
Structural changes in microcirculatory vessels and their surroundings in the primary visual cortex of 3- and 18-month-old rats with retinal photodamage and structural change correction
Morphofunctional changes in microvasculature play an important role in the nerve cell plasticity, the ability to change their functional state under the influence of various factors. The aim of the research was to study the morphology of the microvasculature vessels, surrounding neurons and glia cells in the primary visual cortex of 3- and 18-month-old rats in norm and under stress caused by high-intensity twenty-four-hour light exposure, as well as under correction. Materials and Methods. The experiments were carried out on 60 Wistar male rats, aged 3- and 18-months. The authors used light and electron microscopy, and morphometry to evaluate: capillary surface area and density, surface area of altered vessels (due to stasis, sludge of formed elements and thrombosis) and unchanged ones, as well as the morphology of the surrounding cells. The Kruskal-Wallis test was used for multiple comparisons within age groups, while Mann-Whitney test was used for pair comparison. Results. The authors observed different capillary reactions to light exposure in 3- and 18-month-old rats. It resulted in an increase of capillary density in 3-month-old rats and in a decrease of capillary density in 18-month-old rats (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Структурные изменения сосудов микроциркуляторного русла и их окружения в первичной зрительной коре 3- и 18-месячных крыс при фотоповреждении сетчатки, их коррекция
Введение. Высокоинтенсивное длительное световое воздействие вызывает фотоповреждение нейронов и глиоцитов сетчатки, что приводит к дефициту афферентных импульсов и морфологическим изменениям клеток в центральном отделе зрительного анализатора [1]. Также в условиях круглосуточного светового воздействия наблюдается рассогласование околосуточных биоритмов, которое является мощным стрессирующим фактором для всех систем организма [2]. Известно, что чрезмерные стимулы и различные эндогенные факторы, в т.ч. и старение, могут сопровождаться дезадаптивными реакциями в органах и тканях, что приводит к стрессиндуцированным патологическим состояниям или заболеваниям [3]. На данный момент имеется множество исследований, рассматривающих стрессиндуци-рованные изменения головного мозга, их связь со стрессом, старением и нейродегенератив-ными заболеваниями [4–7]. При этом данных о морфологических изменениях сосудистого русла в зрительной коре при стрессе и повреждении сетчатки недостаточно.
Цель исследования. Изучение морфологии сосудов микроциркуляторного русла и окружающих их нейронов и глиоцитов в первичной зрительной коре 3- и 18-месячных крыс в норме и при стрессе, вызванном высокоинтенсивным круглосуточным световым воздействием, а также в условиях коррекции.
Материалы и методы. Эксперименты выполнены на 3- и 18-месячных крысах-самцах Вистар (n=60). Всех животных содержали на стандартном пищевом рационе с неограниченным доступом к воде. Крыс разделили на 2 группы (табл. 1).
Таблица 1
Table 1
Assignment of animals to experimental groups
|
Возраст Age |
Контрольная группа (n=30) Control group (n=30) |
Экспериментальная группа (n=30) (световое воздействие) Experimental group (n=30) (light exposure) |
||||
|
Интактные Intact |
Коррекция Correction |
Вода Water |
Опыт Test |
Коррекция Correction |
Вода Water |
|
|
3 месяца 3-month-old |
5 |
5 |
5 |
5 |
5 |
5 |
|
18 месяцев 18-month-old |
5 |
5 |
5 |
5 |
5 |
5 |
Разделение животных по экспериментальным группам
Крыс контрольной группы (n=30) содержали в стандартных условиях вивария с дневной освещенностью 25 лк, ночной – 4 лк. Крыс экспериментальной группы (n=30) помещали в специальную установку из пяти прямоугольных рефлекторов с вмонтированными в них люминесцентными лампами, уровень освещенности составил 3500 лк круглосуточно в течение 7 сут.
Для коррекции использовали активный компонент лекарственного растения Rhodiola rosea n-тирозол, обладающий гемореологическими и антиоксидантными свойствами, показавший нейропротективный эффект при тран-зиторной глобальной ишемии головного мозга [8–10]. Дозу 50 мг/кг массы разводили дистиллированной водой и вводили внутри-желудочно через зонд 1 раз в сутки в течение 7 сут. По 5 крыс каждой возрастной и экспериментальной группы получали эквиобъем-ное количество дистиллированной воды 1 раз в сутки в течение недели.
На 8-е сут эксперимента производили декапитацию под легким эфирным наркозом, выделяли затылочную область коры, для све- товой микроскопии фиксировали в 10 % формалине и заливали в парафин. Срезы окрашивали гематоксилин-эозином по стандартной методике, дифференцировали первичную зрительную кору, подсчитывали удельную площадь неизмененных сосудов (венул и артериол), удельную площадь измененных сосудов (венул и артериол со сладжем, стазом и тромбозом), численную плотность и удельную площадь капилляров (расчеты производили на 56 600 мкм2), количество глиоцитов и капилляров на 1 нейрон в срезе (программное обеспечение ImageJ). Для электронной микроскопии (JEN-100 CX, Япония) материал фиксировали в 2,5 % растворе глутаральдегида на какодилатном буфере (рН=7,4), далее производили постфиксацию в 2 % растворе четы-рехоксида осмия и заливали в смесь эпона и аралдита М. Полутонкие срезы окрашивали азуром II. Ультратонкие срезы контрастировали ацетатом уранила и цитратом свинца.
Статистическую обработку проводили в программе SPSS Statistics, использовали непараметрический критерий Крускала–Уоллиса для множественных сравнений внутри воз- растных групп и критерий Манна–Уитни для парного сравнения показателей между 3- и 18-месячными животными. Различия считали статистически значимыми при р≤0,05. На работу получено одобрение регионального этического комитета (№ 4972 от 31.10.2016). Работа выполнена с соблюдением международных принципов Хельсинкской декларации и в соответствии с директивой Европейского сообщества (2010/63/ЕU).
Результаты и обсуждение. При световом воздействии в просвете капилляров 3-месячных крыс встречались явления сладжа и стаза эритроцитов, вокруг гемокапилляров обнаруживались отечные отростки астроцитов (рис. 1).
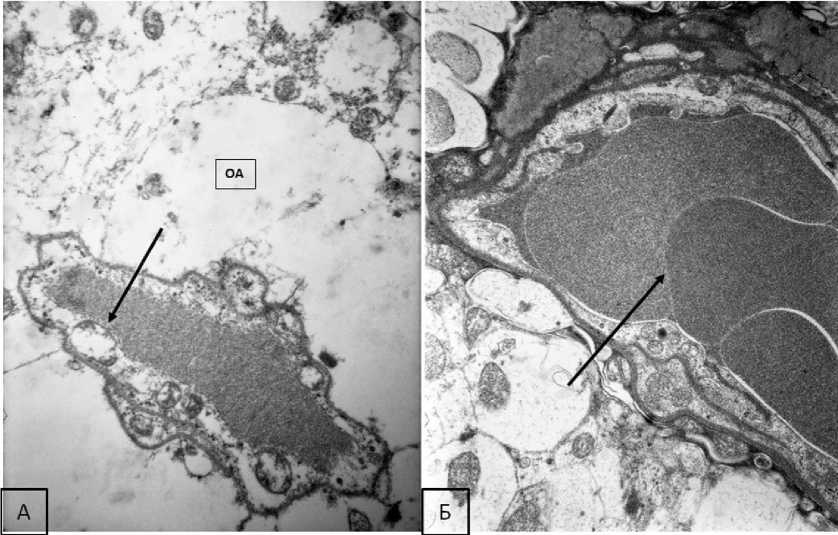
Рис. 1. Электронные микрофотографии первичной зрительной коры 3-месячных крыс со световым воздействием. Контраст ацетатом уранила, цитратом свинца.
А) Разрушение органелл в цитоплазме эндотелиоцита (стрелка), вокруг капилляра отечные отростки астроцитов (ОА). Ув. 5000.
Б) Сладж эритроцитов в просвете капилляра (стрелка). Ув. 6000
Fig. 1. Electron micrographs of the primary visual cortex of 3-month-old rats under light exposure. Contrast with uranyl acetate and lead citrate.
-
A) Destruction of organelles in the cytoplasm of endothelial cells (arrow), edematous astrocyte branching around the capillary, ×5000.
-
B) Erythrocyte sludge in the capillary lumen (arrow), ×6000
На ультраструктурном уровне в цитоплазме эндотелиоцитов и перицитов встречались набухшие митохондрии с частичной или полной деструкцией крист. Нередко цитоплазма эндотелиоцитов выбухала в просвет сосуда, сужая его. Морфологический анализ показал отсутствие значимых различий между подгруппами 3-месячных крыс по показателям удельной площади измененных и неизмененных сосудов. У крыс со световым воздей- ствием выявлено увеличение численной плотности капилляров до 33 (29; 35) по сравнению с показателями интактных 3-месячных крыс – 29 (27; 31), что, вероятно, связано с их открытием, переходом в функционально активное состояние (р=0,04 по критерию Крускала– Уоллиса).
При коррекции n-тирозолом у крыс 3-месячного возраста со световым воздействием обнаружено достоверное увеличение числен- ной плотности капилляров до 40 (38; 43) и удельной площади капиллярного русла до 1,9 (1,4; 2) по сравнению с показателями крыс 3-месячного возраста со световым воздействием без коррекции – 33 (29; 35) и 0,9 (0,75; 0,9) соответственно, что, вероятно, отражало улучшение микроциркуляции в связи с повышением метаболического запроса нервных клеток при стрессе, вызванным световым воздействием (р=0,04; р=0,00 соответственно по критерию Крускала–Уоллиса). По- хожие результаты обнаружены в экспериментах на спонтанно гипертензивных крысах, где n-тирозол также показал достоверное увеличение численной плотности капилляров [9].
При световом воздействии у 18-месячных крыс гемодинамические изменения были более выражены и, наряду с явлением сладжа и стаза форменных элементов в капиллярах, характеризовались появлением периваскулярного отека венул, стазом форменных элементов в их просвете (рис. 2).
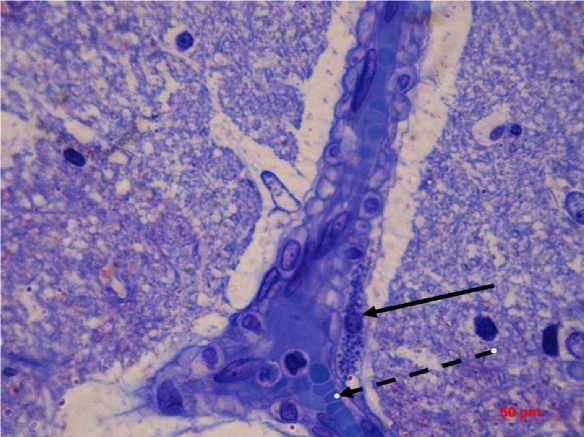
Рис. 2. Микрофотография венулы первичной зрительной коры 18-месячной крысы при световом воздействии с периваскулярным отеком, стазом форменных элементов (пунктирная стрелка). Вдоль стенки сосуда – тучная клетка (стрелка). Полутонкий срез. Окраска азуром II. Ув. 1000
Fig. 2. Microphotograph of a venule in the primary visual cortex of an 18-month-old rat under light exposure with perivascular edema, and stasis of blood elements (dotted arrow). A mast cell (arrow) is along the vessel wall. Azure II staining, ×1000
Морфометрический анализ показал отсутствие различий в группах 18-месячных крыс по показателям удельной площади измененных и неизмененных сосудов. Световое воздействие приводило к значимому снижению удельной площади до 0,6 % (0,5; 0,7) и численной плотности капилляров до 23 (20; 26) у 18-месячных крыс по сравнению с показателями интактных 18-месячных крыс – 0,9 % (0,8; 1,2); 30 (28; 32) соответственно, что могло быть связано с перикапиллярным отеком отростков астроцитов и механической компрессией сосудов извне, а также со спазмом капилляров (р=0,00 по критерию Кру- скала–Уоллиса). При сравнении численной плотности капилляров у молодых (33 (29; 35)) и 18-месячных (23 (20; 26)) крыс при световом воздействии также выявлены значимые различия, что отражает возрастные особенности реактивности микроциркуляторного русла (р=0,00 по критерию Манна–Уитни). В экспериментах показано, что на фоне старения снижается способность сосудов головного мозга адекватно реагировать на изменение метаболической потребности нейронов. В итоге это приводит к их дисфункции и гипоксии [11]. При коррекции у 18-месячных крыс со световым воздействием выявлено достоверное уве- личение численной плотности капилляров до 27 (26; 29) по сравнению с 18-месячными крысами без коррекции – 23 (20; 26), что, вероятно, улучшало микроциркуляцию (р=0,02 по критерию Крускала–Уоллиса).
Люминарная поверхность эндотелия некоторых капилляров у 3- и 18-месячных крыс при световом воздействии на фоне введения n-тирозола образовывала микроворсинки, увеличивающие контактную поверхность эндоте-лиоцитов (рис. 3А). Также в группах со световым воздействием наблюдались множественные пиноцитозные пузырьки, что нетипично для эндотелиоцитов головного мозга (рис. 3Б).
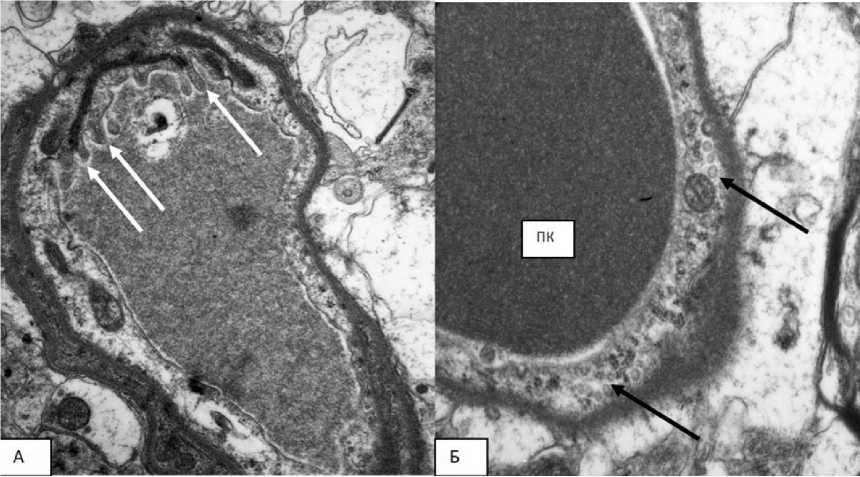
Рис. 3. Электронные микрофотографии капилляров первичной зрительной коры 18-месячных крыс со световым воздействием. Контраст ацетатом уранила, цитратом свинца.
А) Микроворсинки эндотелиоцита капилляра (стрелки). Ув. 6000.
Б) Скопление пиноцитозных пузырьков в цитоплазме эндотелиоцита (стрелки).
ПК – просвет капилляра. Ув. 10 000
Fig. 3. Electron micrographs of the capillaries in the primary visual cortex of 18-month-old rats under light exposure. Contrast with uranyl acetate and lead citrate.
-
A) Microvilli of capillary endothelial cells (arrows), ×6000.
-
B) Accumulation of pinocytotic vesicles in the endothelial cell cytoplasm (arrows).
ПК – capillary lumen, ×10 000
Похожие изменения в эндотелиоцитах головного мозга наблюдали при воздействии микроволнового излучения [12], ишемии головного мозга [13], на модели распространенной деполяризации [14]. Считается, что низкий уровень трансцитоза играет существенную роль в поддержании гомеостаза межклеточной среды головного мозга [15, 16]. Изменение барьерных свойств эндотелия, вероятно, связано с повышением уровня провоспа-лительных цитокинов и хемокинов в центральной нервной системе при стрессе [17], что наряду с окислительным стрессом потенцирует повреждение нервных клеток.
При морфологическом исследовании нейронов 3- и 18-месячных крыс при световом воздействии обнаружены потенциально обратимые изменения в виде очагового хроматолиза и гиперхромных нейронов без сморщивания и деструктивные, необратимые: тотальный хроматолиз и пикноморфные сморщенные клетки. Нейроны с деструктивными изменениями встречались редко, в основном в группе 18-месячных крыс. Ультраструктур-ный анализ показал наличие фрагментов разрушенных органелл, мультивезикулярные, слоистые, миелиноподобные тельца в цитоплазме таких клеток. В нормохромных и обра- тимо измененных нейронах преобладали реактивные изменения: набухание митохондрий и расширение цистерн эндоплазматической сети (ЭПС), свидетельствующие, вероятно, о повышенной метаболической активности клеток (рис. 4А).
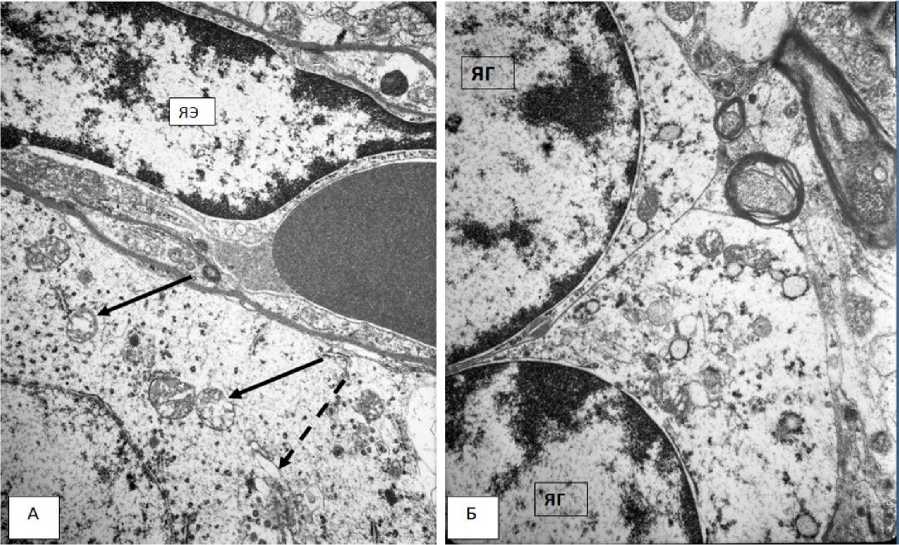
Рис. 4. Электронные микрофотографии первичной зрительной коры 3-месячных крыс со световым воздействием. Контраст ацетатом уранила, цитратом свинца.
А) В цитоплазме нейрона – набухшие митохондрии с частичной деструкцией крист (стрелка), расщирение цистерн эндоплазматической сети (пунктирная стрелка);
ЯЭ – ядро эндотелиоцита. Ув 8000.
Б) Попарно расположенные глиоциты; ЯГ – ядро глиоцита. Ув. 5000
Fig. 4. Electron micrographs of the primary visual cortex of 3-month-old rats under light exposure. Contrast with uranium acetate and lead citrate.
-
A) Swollen mitochondria with partial cristae destruction (arrow), and expansion of cisterns in the endoplasmic reticulum (dotted arrow) are observed in the neuron cytoplasm.
ЯЭ – endothelial cell nucleus, ×8000.
-
B) Paired glia cells, ЯГ – glia cel nucleus, ×5000
Другим важным компонентом нейро-глио-сосудистого ансамбля являются глиоциты, не только обеспечивающие структурную поддержку нейронов, но и регулирующие процессы восстановления нервной ткани после повреждения [18]. Глиоциты 3- и 18-месячных крыс при световом воздействии характеризовались набуханием, увеличением объема цитоплазмы и ядра. В цитоплазме таких глиоцитов обнаруживались реактивные изменения – набухшие митохондрии и цистерны ЭПС. Нередко наблюдались глиоциты, расположенные парами или группами, что, возможно, свидетельствовало об их пролифера- ции и/или миграции (рис. 4Б). В группе 18-месячных крыс при световом воздействии встречались и деструктивно измененные гиперх-ромные сморщенные глиоциты.
Для оценки взаимоотношений между нейронами, глией и капиллярами использовали соотношение количества глии и капилляров на 1 нейрон в срезе. У 3-месячных крыс при световом воздействии на фоне введения n-тирозола значимо повышалось количество глиоцитов на 1 нейрон – до 1,3 (0,9; 1,8) и количество капилляров – до 0,5 (0,4; 0,88), что значимо отличалось от показателей 3-месячных крыс со световым воздействием без кор- рекции (0,8 (0,7; 1) и 0,29 (0,2; 0,46) соответственно) и, вероятно, способствовало лучшей адаптации нервных клеток при высокоинтенсивном световом воздействии (p=0,01; p=0,03 соответственно по критерию Крускала–Уоллиса).
Заключение. Таким образом, изменения сосудов первичной зрительной коры у 3-месячных крыс носили адаптивный характер, что выражалось в увеличении численной плотности капилляров в первичной зритель- ной коре и реактивных изменениях нейронов и глиоцитов. У 18-месячных крыс световое воздействие, вероятно, приводило к срыву адаптации, о чем свидетельствовали снижение числа капилляров и деструктивные изменения нейронов и глиоцитов. N-тирозол был более эффективен у 18-месячных крыс при световом воздействии, препарат способствовал увеличению численной плотности капилляров первичной зрительной коры, что, вероятно, улучшало микроваскуляризацию.
Список литературы Структурные изменения сосудов микроциркуляторного русла и их окружения в первичной зрительной коре 3- и 18-месячных крыс при фотоповреждении сетчатки, их коррекция
- Sverdeva Y.O., Varakuta E.Ju., Zhdankina A.A. Age-related structural changes in the cells of the primary visual cortex of rats under high-intensity light exposure. Advances in gerontology. 2018; 31 (3): 352-355.
- Степанова С.И., Галичий В.А. Космическая биоритмология. Хронобиология и хрономедицина. М.: Триада-Х; 2000. 239.
- McEwen S. Stress, adaptation, and disease: Allostasis and allostatic load. Annals of the New York academy of sciences. 1998; 840 (1): 33-44.
- Смирнов А.В., Григорьева Н.В. Морфофункциональные изменения дорсального и вентрального отделов гиппокампа крыс при моделировании комбинированного стресса с учетом экспрессии CASPASE-3 и GFAP. Вестник Волгоградского государственного медицинского университета. 2018; 1 (65). URL: https://cyberlemnka.ru/article/n/morfofunktsionalnye-izmeneniya-dorsalnogo-i-ventralnogo-otdelov-gippokampa-krys-pri-modelirovami-kom-binirovannogo-stressa-s-uchetom (дата обращения: 24.02.2020).
- Belleau E.L., Treadway M.T., Pizzagalli D.A. The impact of stress and major depressive disorder on hippocampal and medial prefrontal cortex morphology. Biological psychiatry. 2019; 85 (6): 443-453.
- Волобуев А.Н., Романчук П.И. Биофизика кровообращения при сосудистой деменции и болезни Альцгеймера. Бюллетень науки и практики. 2019; 5 (4). URL: https://cyberleninka.ru/article/n/bio-fizika-krovoobrascheniya-pri-sosudistoy-dementsii-i-bolezni-altsgeymera (дата обращения: 24.02.2020).
- Sàntha P. Restraint stress-induced morphological changes at the blood-brain barrier in adult rats. Frontiers in molecular neuroscience. 2016; 8: 88.
- Khanna K., Mishra K.P. Golden root: A wholesome treat of immunity. Biomedicine. Pharmacotherapy. 2017; 87: 496-502.
- Plotnikov M.B., Aliev O.I. Effect of p-tyrosol on hemorheological parameters and cerebral capillary network in young spontaneously hypertensive rats. Microvascular research. 2018; 119: 91-97.
- Khodanovich M.Y. P-Tyrosol Enhances the Production of New Neurons in the Hippocampal CA1 Field after Transient Global Cerebral Ischemia in Rats. Bulletin of experimental biology and medicine. 2019; 168 (2): 224-228.
- Riddle D.R., Sonntag W.E., Lichtenwalner R.J. Microvascular plasticity in aging. Ageing research reviews. 2003; 2 (2): 149-168.
- Логвинов С.В., Зуев В.Г., Ушаков И.Б. Очерки неионизирующей радиобиологии: структурно-функциональный анализ. Томск; 1994. 208.
- Haley M.J., Lawrence C.B. The blood-brain barrier after stroke: structural studies and the role of transcytotic vesicles. Journal of Cerebral Blood Flow & Metabolism. 2017; 37 (2): 456-470.
- Sadeghian H. Spreading depolarizations trigger caveolin 1-dependent endothelial transcytosis. Annals of neurology. 2018; 84 (3): 409-423.
- Ben-Zvi A., Lacoste B., Kur E. Mfsd2a is critical for the formation and function of the blood-brain barrier. Nature. 2014; 509 (7501): 507-511.
- Knowland D. Stepwise recruitment of transcellular and paracellular pathways underlies blood-brain barrier breakdown in stroke. Neuron. 2014; 82 (3): 603-617.
- Marsland A.L., Walsh C. The effects of acute psychological stress on circulating and stimulated inflammatory markers: a systematic review and meta-analysis. Brain, behavior, and immunity. 2017; 64: 208-219.
- Greenhalgh A.D., David S., Bennett F.C. Immune cell regulation of glia during CNS injury and disease. Nature Reviews Neuroscience. 2020; 1-14. URL: https://www.ncbi.nlm.nih.gov/pubmed/32042145 (дата обращения: 10.02.2020).
- DOI: 10.1038/s41583-020-0263-9


