Структурные реакции сердца и печени мышей CD-1 на однократное введение боркаптата натрия
Автор: Каныгин В.В., Колдышева Е.В., Завьялов Е.Л., Разумов И.А., Соловьева О.И., Кичигин А.И., Бутикова Е.А., Капустина В.И.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.31, 2023 года.
Бесплатный доступ
Бор-нейтронозахватная терапия рассматривается как перспективный метод лечения злокачественных опухолей головы и шеи. Считается, что для повышения эффективности этого вида терапии требуется использование больших доз препарата бора, что может повлечь за собой нежелательное воздействие на здоровые ткани. Одним из веществ, применяемых в клинической практике бор-нейтронозахватной терапии, является обогащенный изотопом бора 10В боркаптат натрия Na2B12H11SH (BSH). Цель исследования - изучение структурных реакций миокарда и печени мышей линии CD-1 после введения BSH. Проведено светооптическое и поляризационно-микроскопическое исследование миокарда и печени мышей-самцов линии CD-1 (n=56) после введения борсодержащего вещества в дозах 100 и 1000 мг/кг, однократно, внутрибрюшинно. Оценка структурных изменений в миокарде и печени проводилась через 1, 3 и 7 сутки после введения BSH. Однократное введение BSH в дозе 100 мг/кг не приводило к гибели животных, тогда как через 3 часа после введения BSH в дозе 1000 мг/кг погибло 1 животное. Масса тела животных в течение эксперимента менялась незначительно. Анализ массы сердца показал снижение этого показателя к 3 и 7 суткам по сравнению с показателями в тех же группах на 1 сутки эксперимента. При анализе динамики изменений массы печени достоверные ее изменения на протяжении эксперимента не выявлены. К основным структурным изменениям миокарда относились литические и контрактурные повреждения кардиомиоцитов, гемодинамические нарушения в виде выраженного венозного и капиллярного полнокровия. Повреждения печени проявлялись в дистрофических изменениях гепатоцитов, появлении через 3 суток моноцеллюлярных некрозов гепатоцитов и перицентральных мононуклеарных инфильтратов. Полученные данные свидетельствуют о том, что использованные дозы BSH 100 и 1000 мг/кг при однократном введении вызывают структурные изменения миокарда и печени различной степени выраженности, которые сохраняются в течение 7 суток наблюдения.
Миокард, печень, радиотерапия опухолей, боркаптат натрия, мыши cd-1
Короткий адрес: https://sciup.org/143181183
IDR: 143181183 | DOI: 10.20340/mv-mn.2023.31(3).812
Structural reactions of CD-1 mice heart and liver to a single injection of borocaptate sodium
Boron neutron capture therapy is considered a promising method for the treatment of malignant tumors of the head and neck. It is believed that to increase the effectiveness of this type of therapy, the use of large doses of boron is required, which may entail damaging effects on healthy tissue. One of the substances used in the clinical practice of boron neutron capture therapy is sodium boroncaptate Na2B12H11SH (BSH), enriched with the 10B boron isotope. The purpose of the study was to study the structural reactions of the myocardium and liver of CD-1 mice after administration of BSH. A light-optical and polarization-microscopic study of the myocardium and liver of male CD-1 mice (n=56) was carried out after injection of a boron-containing substance in doses of 100 and 1000 mg/kg, once, intraperitoneally. Assessment of structural changes in the myocardium and liver was carried out 1, 3 and 7 days after BSH administration. A single injection of BSH at a dose of 100 mg/kg did not lead to the death of animals, whereas 3 hours after the injection of BSH at a dose of 1000 mg/kg, 1 animal died. The body weight of the animals changed slightly during the experiment. Analysis of heart weight showed a decrease in this indicator on days 3 and 7 compared with indicators in the same groups on day 1 of the experiment. When analyzing the dynamics of changes in liver mass, no significant changes were revealed during the experiment. The main structural changes in the myocardium included lytic and contractural damage to cardiomyocytes, hemodynamic disturbances in the form of pronounced venous and capillary congestion. Liver damage was manifested in dystrophic changes in hepatocytes, the appearance after 3 days of monocellular necrosis of hepatocytes and pericentral mononuclear infiltrates. The data obtained indicate that the used doses of BSH 100 and 1000 mg/kg with a single injection cause structural changes in the myocardium and liver of varying severity, which persist for 7 days of observation.
Текст научной статьи Структурные реакции сердца и печени мышей CD-1 на однократное введение боркаптата натрия
Kanygin VV, Koldysheva EV, Zav’yalov EL, Razumov IA, Solovyova OI, Kichigin AI, Butikova EA, Kapustina VI. Structural reactions of CD-1 mice heart and liver to a single injection of borocaptate sodium. Morfologicheskie Vedomosti – Morphological newsletter. 2023;31(3):812. (3).812
Введение. Важнейшей медикобиологической задачей остается разработка новых подходов к лечению особо агрессивных злокачественных новообразований, к которым относятся опухоли мозга с высокой пролиферативной активностью, выраженным метастатическим потенциалом, коротким периодом ремиссии и низким уровнем выживаемости пациентов. Одним из таких подходов является бор-нейтронозахватная терапия (далее - БНЗТ), которая относится к разряду лучевой терапии злокачественных опухолей [13]. Считается, что эта технология позволяет объединить принцип органа-мишени, используемый в химиотерапии и принцип анатомической локализации традиционной радиотерапии [4]. Принцип БНЗТ основан на реакции захвата изотопом 10B теплового нейтрона и образованием нестабильного изотопа 11B, который распадается на альфа-частицу и ион лития, что обеспечивает повреждение ДНК и гибель опухолевой клетки, в которой селективно накапливается 10B [5]. Для проведения БНЗТ необходим малотоксичный агент, обогащенный 10B. Одним из таких соединений является боркаптат натрия Na2B12H11SH (BSH). Хотя BSH был впервые использован в клинической практике БНЗТ еще в 1975 году, использование его до сих пор актуально как в экспериментальных исследованиях, так и в клинической практике [6-8]. Однако кардио- и гепатотоксичность этого вещества и его роль в структурных перестройках жизненно важных органов, уровень цитотоксичности для опухолевых и неопухолевых клеток изучена до сих пор недостаточно. Есть данные, свидетельствующие о низкой токсичности BSH применяемом в терапевтической дозе 100 мг/кг [9-11], но, как известно, для подавления опухолевого роста лимитирующим фактором нередко является доза препарата, как, например, это происходит с широко применяемыми антрациклиновыми антибиотиками [12]. В экспериментальных исследованиях использовались дозы препарата до 1000 мг/кг, которые показали LD50 исследуемых лабораторных мышей [13]. Однако такая высокая летальность была связана с недостаточной чистотой синтезированного препарата, а дополнительные морфологические исследования не проводились. В связи с этим актуальность приобретает вопрос дозировки и способа доставки применяемого ве- щества, а также понимание путей взаимодействия борсодержащих препаратов с опухолевой клеткой и организмом в целом. Особое значение имеет исследование возможной структурной реорганизации здоровых тканей в ответ на введение этого вещества [14-15].
Цель исследования: изучение структурных реакций миокарда и печени мышей CD-1 после введения боркаптата натрия, обогащенного изотопом 10В.
Материалы и методы исследования. В эксперименте использованы мыши-самцы линии CD-1 в возрасте 12 недель, массой 38-45 г (n=56), которых содержали в Центре генетических ресурсов лабораторных животных на базе ЦКП «SPF-виварий» Института цитологии и генетики СО РАН в клетках Tecniplast в контролируемых условиях. Животные были разделены на 3 группы. Группа 1 (n=27) получала 0,9% раствор NaCl, который вводили в том же объеме, что и борсодержащее вещество. Группы 2 (n=15) и 3 (n=14) получали боркаптат натрия (BSH) в дозе 100 и 1000 мг/кг, соответственно. Был использован BSH производства Katchem spol. s. r. o. (Чехия) [CAS 12448-24-7], обогащенный изотопом 10В (>99.5%), который растворяли в 0,9% растворе NaCl с учетом максимально допустимого объема для инъекции. Инъекции проводили однократно, внутрибрюшинно. Все манипуляции проводили с соблюдением принципов гуманного отношения к животным (Директивой Европейского сообщества 86/609/ЕЕС).
Из эксперимента животных выводили декапитацией через 1, 3 и 7 суток после введения BSH. После вскрытия животного визуально оценивали состояние внутренних органов, проводили взвешивание внутренних органов. Сердце помещали в холодовую камеру до полной остановки, извлекали печень. Образцы стенки левого желудочка сердца и фрагменты печени фиксировали в 10% растворе нейтрального формалина (Biovitrum, Россия). Проводку осуществляли в аппарате STP120 (Microm GmbH, Walldorf, Germany). Парафиновые срезы толщиной 2-3 мкм получали на ротационном микротоме НМ325 (Thermo Fisher Scientific, Runcorn, UK). После стандартной процедуры депарафинации окрашивали ге- матоксилином и эозином с постановкой реакции Перльса. Светооптическое и поляризационно-микроскопическое исследование препаратов проводили с использованием универсального микроскопа Leica DM 4000B. Для получения снимков с препаратов применяли цифровую фотокамеру Leica DFC230 и компьютерную программу Leica QWin3 (Leica Microsystem, Cambidge, UK). При статистической обработке результатов определяли средние значения параметров, вычисляли дисперсию и стандартную ошибку среднего. Для сравнения нормально распределенных количественных данных использовали непарный t-критерий Стьюдента. Отличия считали статистически значимыми при p<0,05.
Результаты исследования и обсуждение. Однократное введение BSH в дозе 100 мг/кг не приводило к гибели животных, тогда как через 3 часа после вве-
Таблица 1
Масса тела, сердца и печени мышей CD-1 при введении BSH в дозах 100 и 1000 мг/кг, (М±т)
|
Показатель |
1 группа (контроль) |
2 группа |
3 группа |
||||
|
Время после введения BSH |
|||||||
|
1 сутки |
3 сутки |
7 сутки |
1 сутки |
3 сутки |
7 сутки |
||
|
Масса тела, г |
41,30±0,96 |
40,7±0,8 |
39,3±0,5 |
41,1±0,6 |
39,2±2,2 |
38,3±0,9 |
45,0±0,4 |
|
Масса сердца, г |
0,17±0,02 |
0,22±0,0 |
0,12±0,0 # |
0,10±0,0 # |
0,20±0,0 |
0,14±0,0 |
0,16±0,0 |
|
Относительная масса сердца, мг/г |
4,19±0,43 |
5,37±0,4 |
3,06±0,5 |
2,43±0,0 * # |
5,15±0,4 |
3,66±0,7 |
3,55±0,5 |
|
Масса печени, г |
2,08±0,08 |
2,04±0,1 |
1,86±0,0 |
2,10±0,0 |
2,13±0,1 |
2,0±0,1 |
2,4±0,1 |
|
Относительная масса печени, мг/г |
50,18±1,24 |
50,0±1,5 |
47,3±0,8 |
51,1±0,8 |
54,4±1,8 |
52,2±1,9 |
53,3±1,7 |
Примечание: # - p<0,05 по сравнению с показателем той же группы на 1 сутки; * - p<0,05 по сравнению с контрольной группой
Светооптическое исследование печени выявило, что общее строение органа во всех группах было сохранено. У контрольных животных цитоплазма гепатоцитов равномерно окрашивалась эозином. Ядра содержали преимущественно эухро-матин, гетерохроматин располагался некрупными глыбками в околоядрышковой зоне или по периметру кариолеммы. Центральные и портальные вены и синусоидные капилляры иногда были расширены, полнокровны.
Через 1 сутки после введения BSH во 2-й и 3-й группах отмечались сходные изменения строения печени. Одно и двуядерные гепатоциты существенно варьировали по размеру, их цитоплазма окра- дения BSH в дозе 1000 мг/кг погибло 1 животное (7%). Масса тела животных в течение эксперимента менялась незначительно. Анализ массы сердца показал снижение этого показателя к 3 и 7 суткам: у животных 2-й группы на 45 и 55% (p<0,05), а у животных 3 группы на 30 и 20% по сравнению с показателями в тех же группах на 1 сутки. Относительная масса сердца у животных 2 группы к 7 суткам эксперимента снижалась по сравнению с контролем (на 42%; p<0,05) и показателем той же группы на 1 сутки эксперимента (на 55%; p<0,05). В 3 группе к 7 суткам наблюдалась сходная тенденция, снижение составляло 12% по сравнению с контролем и 31% по сравнению с показателями той же группы на 1 сутки эксперимента. При анализе динамики массы печени достоверные изменения не выявлены (табл. 1).
шивалась преимущественно равномерно. В то же время следует отметить, что у животных 3-й группы отмечался выраженный полиморфизм ядер и дистрофические изменения, проявляющиеся в вакуолизации цитоплазмы гепатоцитов (рис. 1-Б). В обеих группах гемодинамические изменения выражались в более выраженном расширении центральных и портальных вен и синусоидных капилляров по сравнению с 1-й группой (рис. 1-А).
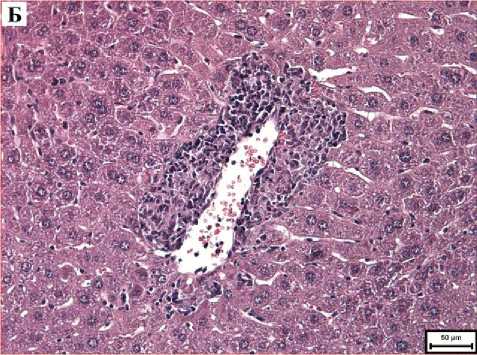
Через 3 суток после введения BSH у животных 2-й группы цитоплазма гепатоцитов окрашивалась в основном равномерно, но одновременно встречались небольшие участки дольки, в которых гепатоциты были более эозинофильными. Такие участ- ки располагались чаще всего перипорталь-но (рис. 1-А). Наблюдались очаги некроза гепатоцитов из 2-3 клеток, инфильтрированные мононуклеарами. У мышей 3-й группы отмечались более выраженные, чем в предыдущий срок, дистрофические изменения гепатоцитов, заключавшиеся в выраженных просветлениях цитоплазмы, ее очаговом лизисе. У мышей этой группы наблюдалось формирование массивных муфтообразных перицентральных моно-нуклеарных инфильтратов (рис. 2-Б). В обеих группах центральные и портальные вены и синусоидные капилляры были расширены, полнокровны; во многих венах наблюдалось эозинофильное пенистое содержимое (плазмостаз, см. рис. 2-А).
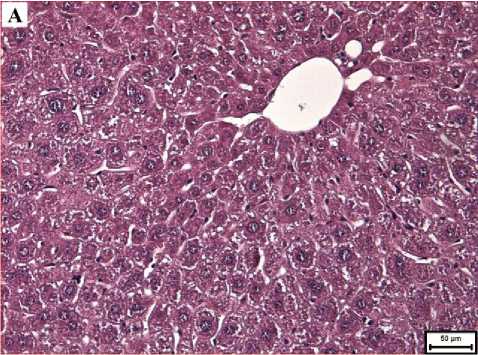
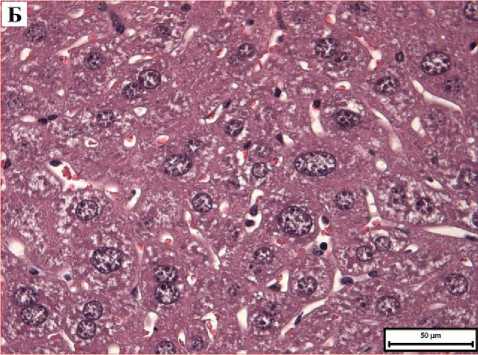
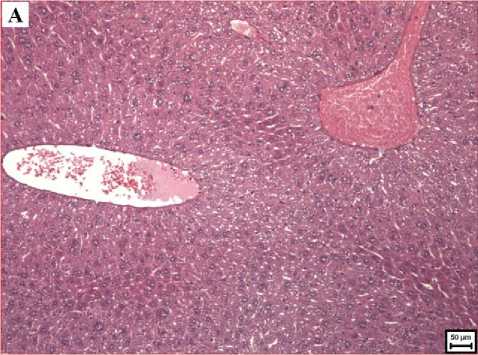
Рис. 2. Микрофото гистологического препарата печени мышей CD-1 через 3 суток после введения BSH. Окр.: гематоксилином и эозином. А - доза препарата 100 мг/кг, ув.: х100. Б -доза препарата 1000 мг/кг, ув.: х200
Рис. 1. Микрофото гистологического препарата печени мышей CD-1 через 1 сутки после введения BSH. Окр.: гематоксилином и эозином. А - доза препарата 100 мг/кг, ув.: х200. Б -доза препарата 1000 мг/кг, ув.: х400
Через 7 суток выраженность структурных изменений печени в каждой группе существенно не менялась по сравнению с предыдущим сроком. Однако следует отметить появление моноцеллюлярных некрозов гепатоцитов (рис. 3-А) в печени мышей обеих групп. У мышей 3-й группы сохранялись более выраженные дистро- фические изменения гепатоцитов по сравнению с мышами 2-й группы (рис. 3, Б). В обеих группах манифестировали выраженные нарушения гемодинамики в виде венозного и синусоидного полнокровия.
Миокард животных контрольной группы не претерпевал заметных изменений. Через сутки после введения BSH в кардиомиоцитах животных 2-й и 3-й групп наблюдались умеренные литические изменения, венозное и капиллярное полнокровие, в остальном миокард этих животных не отличался от контрольного. Следует отметить, что в 3-й группе изменения были более выраженными (рис. 4А-Б).
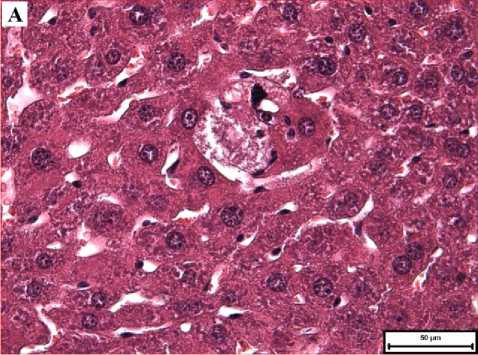
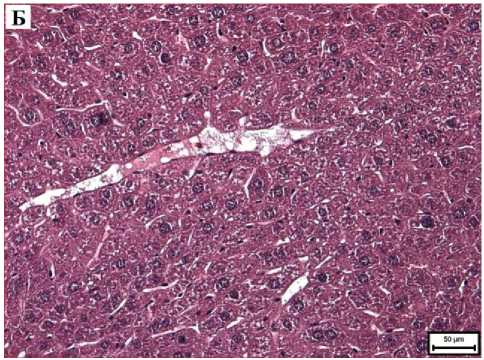
Рис. 3. Микрофото гистологического препарата печени мышей CD-1 через 7 суток после введения BSH. Окр.: гематоксилином и эозином. А - доза препарата 100 мг/кг, ув.: х400. Б -доза препарата 1000 мг/кг, ув.: х200
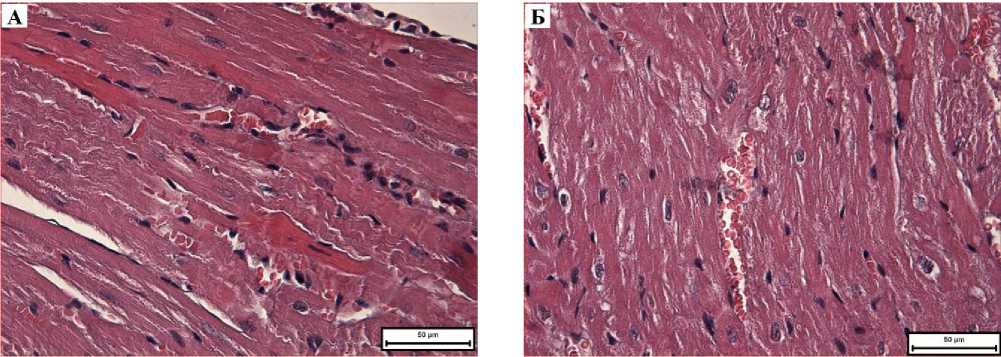
Рис. 4. Микрофото гистологического препарата сердца мышей CD-1 через 1 сутки после введения BSH. Окр.: гематоксилином и эозином. А - доза препарата 100 мг/кг, ув.: х400. Б -доза препарата 1000 мг/кг, ув.: х400
Через 3 суток после введения BSH литические изменения в кардиомиоцитах усиливались по сравнению с 1 сутками, иногда появлялись околоядерные «опустошения». К этому сроку у исследованных мышей были выявлены контрактурные изменения миофибрилл. Гемодинамические нарушения выражались в неравномерном венозном полнокровии. В некоторых сосудах наблюдалось «пенистое» содержимое фибриноидной природы (рис. 5-А). Сосудистая стенка у животных 3-й группы выглядела более рыхлой и утолщенной (рис. 5-Б). Содержимое крупных сосудов часто разделялось на плазму и форменные элементы. При исследовании образцов миокарда с помощью поляризационной микроскопии выяснилось, что в обеих группах появлялись миофибриллы подверженные контрактурным изменениям. Следует отметить, что все вышеуказанные изменения миокарда были более выраженными у животных 3-й группы по сравнению со 2-й.
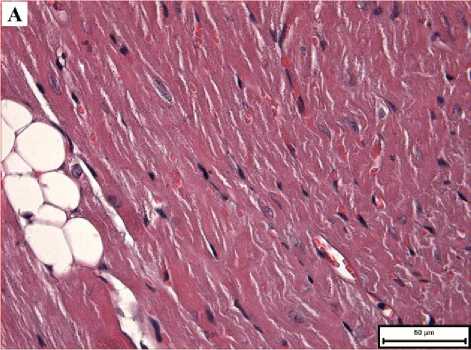
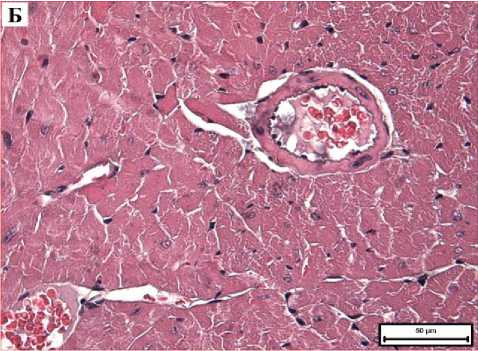
Рис. 5. Микрофото гистологического препарата сердца мышей CD-1 через 3 суток после введения BSH. Окр.: гематоксилином и эозином. А - доза препарата 100 мг/кг, ув.: х200. Б -доза препарата 1000 мг/кг, ув.: х400
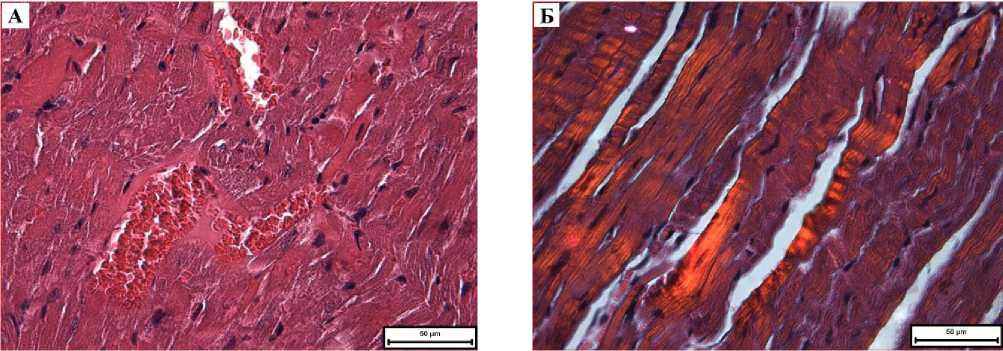
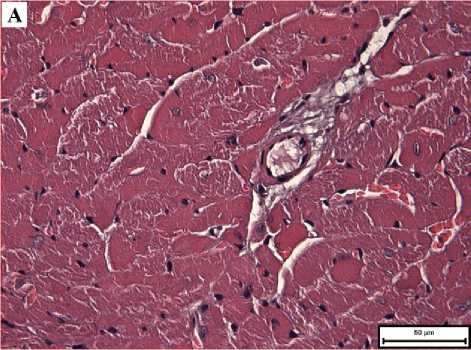
Рис. 7. Микрофото гистологического препарата сердца мышей CD-1 через 7 суток после введения BSH в дозе 1000 мг/кг. А – световая микрсокопия, Б – поляризационная микроскопия. Окр.: гематоксилином и эозином. Ув. х400
Рис. 6. Микрофото гистологического препарата сердца мышей CD-1 через 7 суток после введения BSH в дозе 100 мг/кг. А – световая микрсокопия, Б – поляризационная микроскопия. Окр.: гематоксилином и эозином. Ув. х400

Через 7 суток после инъекции BSH сохранялись литические и контрактурные изменения кардиомиоцитов, при этом миокард животных, получавших различные дозы вещества в этот срок эксперимента, незначительно различался по степени выраженности повреждений. Вне зависимости от дозы полученного вещества манифестировали гемодинамические нарушения в виде венозного и капиллярного полнокровия, нередко со сладжированием эритроцитов и диапедезными явлениями (рис. 6-7).
Результаты проведенного исследования свидетельствуют о сходных структурных реакциях миокарда и печени экспериментальных животных на BSH с реакциями на противоопухолевые препараты таких групп как антрациклиновые антибиотики, алкилирующие агенты, ингибиторы топоизомеразы и некоторые другие. Механизмы, лежащие в основе цитотоксического действия этих агентов, продолжают изучаться, несмотря на длительный период исследования [16-20]. Что касается степени токсичности BSH для неопухолевых клеток этот вопрос остается недостаточно изученным, особенно в аспекте воздействия вещества в виде моно
Список литературы Структурные реакции сердца и печени мышей CD-1 на однократное введение боркаптата натрия
- Hatanaka H. Boron-neutron capture therapy for tumors. Glioma. 1986;1-28. DOI:10.1007/978-3-642-84127-9_18
- Wang S, Zhang Z, Miao L, Li Y. Boron Neutron Capture Therapy: Status and Challenges. Front Oncol. 2022;12:788770. DOI: 10.3389/fonc.2022.788770
- Miyatake SI, Wanibuchi M, Hu N, Ono K. Boron neutron capture therapy for malignant brain tumors. J Neurooncol. 2020;149:1-11. DOI: 10.1007/s11060-020-03586-6
- Farhood B, Samadian H, Ghorbani M, et al. Physical, dosimetric and clinical aspects and delivery systems in neutron capture therapy. Reports of Practical Oncology&Radiotherapy. 2018;23(5):462-473. DOI:10.1016/j.rpor.2018.07.002
- Locher GL. Biological effects and therapeutic possibilities of neutrons. Am J Roentgenol Radium Ther. 1936;36:1-13
- Barth RF, Mi P, Yang W. Boron delivery agents for neutron capture therapy of cancer. Cancer Commun (London). 2018;38(1):35. DOI:10.1186/s40880-018-0299-7
- Fukuda H, Sauerwein W, Masutani M, Hopewell J. Response of Normal Tissues to Boron Neutron Capture Therapy (BNCT) with 10B-Borocaptate Sodium (BSH) and 10B-Paraboronophenylalanine (BPA). Cells. 2021;10(11):2883. DOI:10.3390/cells10112883
- Suzuki M, Masunaga S, Kinashi Y, et al. Intra-arterial administration of sodium borocaptate bsh/lipiodol emulsion delivers B-10 to liver tumors highly selectively for boron neutron capture therapy: experimental studies in the rat liver model. Int J Radiation oncology biol Phys. 2004;59(1):260-266. DOI:10.1016/j.ijrobp.2003.12.018
- Capala J, Stenstam BH, Sköld K, et al. Boron neutron capture therapy for glioblastoma multiforme: clinical studies in Sweden. J Neuro-Oncol. 2003;62:135-144. DOI: 10.1007/BF02699940
- Wittig A, Moss RLM, Sauerwein WAG. Glioblastoma, brain metastases and soft tissue sarcoma of extremities: Candidate tumors for BNCT. Applied Radiation and Isotopes. 2014;88:46-49. DOI:10.1016/j.apradiso.2013.11.038
- Bendel P, Wittig A, Basilico F, et al. Metabolism of bo-rono-phenylalanine-fructose complex (BPA-fr) and borocaptate sodium (BSH) in cancer patients--results from EORTC trial 11001. J Pharm Biomed Anal. 2010;51(1):284-287. DOI:10.1016/j.jpba.2009.08.018
- Wittig A, Stecher-Rasmussen F, Hilger RA, et al. Sodium mercaptoundecahydro-closo-dodecaborate (BSH), a boron carrier that merits more attention. Applied Radiation and Isotopes. 2011;69(12):1760-1764. DOI:10.1016/j.jpba.2009.08.018
- Lushnikova EL, Klinnikova MG, Molodykh OP, Nepomnyashchikh LM. Morfologicheskie proyavleniya remodelirovaniya serdtsa pri di-lyatatsionnoy kardiomiopatii antratsiklinovogo geneza. Byull Eksper Biol. 2004;138(12): 684-689 In Russian
- Larionova VB, Snegovoy AV. Correction possibilities of drug-induced liver toxicity in the treatment of patients with blood system tumors. On-cohematology. 2020;15(4):65-81. DOI:10.17650/1818-8346-2020-15-4-65-81
- Tan W. Cardiotoxicity. Drug Induced Cardiotoxicity: Mechanism, Prevention and Management. 2018:7. DOI:10.5772/intechopen.79611
- Lushnikova EL, Nepomnyashchikh LM, Tolstikova TG. Patomorfologiya myshechnykh kletok serdtsa pri deystvii tsiklofosfamida i triterpenoidov. Moskva: Izd-vo RAMN, 2009.- 272 s. In Russian
- Lushnikova EL, Molodykh OP, Nikityuk DB, et al. Strukturny analiz miokarda pri eksperimental'noy antratsiklinovoy kardiomiopatii i adrenali-novykh vozdeystviyakh. Bull Expr Biol i Med. 2018;166(11)\641-647. In Russian
- Nepomnyashchikh LM, Molodykh OP, Lushnikova EL, Sorokina YUA. Morfogenez i gistostereologichesky analiz gepatopatii, indutsirovannoy tsiklofosfomidom. Bull Exp Biol i Med. 2010;149(1):113-119. In Russian
- Vatutin NT, Sklyannaya EV, El'-Hatib MA i dr. Gepatotoksichnost' protivoopukholevykh preparatov: sovremennoe sostoyanie problemy. Ros-siysky szurnal oncologii. 2016;21(6):325-333. D01:10.18821/1028-9984-2016-21-6-325-333 In Russian
- Hung Y-H, Lin Y-C, Lin Y-T, et al. Therapeutic Efficacy and Radiobiological Effects of Boric Acid-mediated BNCT in a VX2 Multifocal Liver Tumor-bearing Rabbit Model. Anticancer research. 2019;39:5495-5504. D0I:10.21873/anticanres.13742


