Стволовые клетки колоректального рака в первичной опухоли
Автор: Крюкова В.В., Цепелев В.Л., Терешков П.П.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 1 т.25, 2026 года.
Бесплатный доступ
Актуальность. Раковые стволовые клетки (РСК) являются одной из причин прогрессирования и рецидивов колоректального рака (КРР). Детальное изучение фенотипа данных клеток, их иммунобиологических свойств необходимо для разработки методов лечения КРР. Цель исследования – определить содержание РСК, имеющих фенотип EpCAMhighCD44+, в первичной опухоли у больных КРР, а также экспрессию на их поверхности CD133, CD166, CD24 и CD184. Материал и методы. Выполнено одномоментное поперечное исследование клеточного состава опухолевой ткани 123 больных аденокарциномой толстой кишки III cтадии. Контрольную группу составили 87 больных, оперированных по поводу неопухолевых заболеваний толстой кишки. Для получения суспензии клеток опухолевой ткани использовали ферментативный метод. Гейтирование клеток нелимфоидного происхождения (CD45- ) производили в зависимости от экспрессии на их поверхности молекулы адгезии эпителиальных клеток EpCAM и дифференцировочного антигена CD44. Экспрессия EpCAM, CD44, СD133, CD166, СD184 и CD24 на РСК исследована методом проточной цитометрии. Результаты. Относительное содержание РСК с фенотипом CD45- EpCAMhighCD44+ в опухолевой ткани при КРР составило 17,15 [11,76; 26,44] % от пула клеток нелимфоидного происхождения. У больных КРР в структуре РСК обнаружено 42,83 [37,07; 51,77] % клеток, одновременно экспрессирующих СD133 и CD166, и 57,17 [48,23; 62,93] % клеток, экспрессирующих дифференцировочный антиген CD133. Все РСК в первичной опухоли экспрессируют CD184, и 95,18 [88,48; 97,98] % из них одновременно экспрессируют CD24. При высокодифференцированной аденокарциноме количество клеток EpCAMhighCD44+ в первичной опухоли в 1,5 раза ниже по отношению к умеренно дифференцированному КРР (U=326,5, p=0,002) и в 2,1 раза (U=21,0, p<0,001) – по сравнению с низкодифференцированной аденокарциномой. У пациентов c КРР IIIС стадии на 13 % увеличивается количество опухолевых клеток с фенотипом EpCAMhighCD44+CD133+CD166+ по отношению к больным КРР IIIВ стадии (U=1116,0, p=0,007). Заключение. В первичной опухоли при КРР раковые стволовые клетки, высокоэкспрессирующие молекулу адгезии эпителиальных клеток EpCAM и CD44, составляют 17,2 % от пула клеток нелимфоидного происхождения. Количество опухолевых клеток EpCAMhighCD44+ увеличивается при снижении степени дифференцировки аденокарциномы.
Колоректальный рак, раковые стволовые клетки, проточная цитометрия, экспрессия, дифференцировочный антиген, молекула адгезии эпителиальных клеток
Короткий адрес: https://sciup.org/140314349
IDR: 140314349 | УДК: 616.345-006.6:576.385.5 | DOI: 10.21294/1814-4861-2026-25-1-74-84
Cancer stem cells in colorectal cancer
Background. Cancer stem cells (CSCs) are considered to be responsible for progression and recurrence of colorectal cancer (CRC). A detailed study of the phenotype of these cells and their immunobiological properties is necessary for developing CRC treatments. The aim of the study was to assess the percentage of EpCAMhigh/CD44+ cancer stem cells in colorectal cancer and to detect the expression of CD133, CD166, CD24 and CD184 on their surface. Material and Methods. A one-stage cross-sectional study of the cellular composition of tumor tissue was performed in 123 patients with stage III colon adenocarcinoma. The control group consisted of 87 patients who underwent surgery for non-neoplastic diseases of the colon. An enzymatic method was used to obtain a suspension of tumor tissue cells. Gating of non-lymphoid cells (CD45-) was performed depending on the expression of the epithelial cell adhesion molecule EpCAM and the differentiation antigen CD44 on their surface. Expression of EpCAM, CD44, CD133, CD166, CD184 and CD24 on CSCs was studied by fow cytometry. Results. The CD45-EpCAMhighCD44+ colorectal cancer stem cells (CSCs) accounted for 17.15 % [11.76; 26.44] of the non-lymphoid cell population. Within this CSC population, 42.83 % [37.07; 51.77] simultaneously expressed CD133 and CD166, while 57.17 % [48.23; 62.93] expressed the CD133 antigen alone. All CSCs in the primary tumor expressed CD184, and 95.18 % [88.48; 97.98] of them simultaneously expressed CD24. The percentage of EpCAMhighCD44+ cells in well-differentiated tumors was 1.5 times lower than that in moderately-differentiated tumors (U=326.5, p=0.002) and 2.1 times lower than in poorly-differentiated tumors (U=21.0, p<0.001). In addition, the percentage of EpCAMhighCD44+CD133+CD166+ cells in stage IIIC CRC was 13 % higher than that in stage IIIB CRC (U=1116.0, p=0.007). Conclusion. In primary colorectal cancer tumors, cancer stem cells expressing high levels of EpCAM and CD44 accounted for 17.2 % of the non-lymphoid cell pool. The percentage of EpCAMhigh/CD44+ cells in poorly differentiated tumors was higher than that in well-or moderately-differentiated tumors.
Текст научной статьи Стволовые клетки колоректального рака в первичной опухоли
Колоректальный рак (КРР) занимает третье место в мире среди наиболее часто диагностируемых видов рака и второе место в структуре онкологической смертности [1]. В последние годы достигнуты значительные успехи в лечении КРР, прогресс обусловлен внедрением методов иммунотерапии, основанных на использовании моноклональных антител к иммунным контрольным точкам, а также таргетной терапии [2]. Между тем, несмотря на использование этих методов лечения, у многих пациентов отмечается прогрессирование заболевания и позднее метастазирование. Предполагается, что одной из причин этого является наличие раковых стволовых клеток (РСК), резистентных к лекарственной терапии [3, 4].
Существуют две модели формирования и развития злокачественного новообразования толстой кишки. Первая – стохастическая (традиционная), согласно которой в результате мутаций клетки эпителия трансформируются в злокачественные [5]. Стохастическая модель канцерогенеза КРР в последнее время подвергается все большему сомнению в связи с обнаружением роли РСК в прогрессировании заболевания. Вторая гипотеза колоректального канцерогенеза – это модель раковых стволовых клеток (иерархическая модель), согласно которой только субпопуляция недифференцированных стволовых клеток обладает способностью индукции, поддержания и прогрессирования опухоли [6]. Раковые стволовые клетки обладают признаками стволовости, то есть способностью к самообновлению, имеют неограниченный пролиферативный потенциал и демонстрируют эффект мультипотентности [7]. Благодаря наличию механизмов репарации ДНК раковые стволовые клетки устойчивы к противоопухолевой терапии [4]. Способность РСК преодолевать различные методы лечения связывают с пластичностью. Мо- дель обратимой клеточной пластичности указывает на способность к динамическому переходу между несколькими различными клеточными фазами, включая дифференцированные и стволоподобные раковые клетки, асимметрично и симметрично делящиеся, покоящиеся и пролиферирующие, эпителиальные и мезенхимальные, а также фазы лекарственной устойчивости и чувствительности. Клеточная пластичность часто рассматривается как фактор, способствующий агрессивному поведению РСК, что способствует поддержанию и прогрессированию опухоли. Этот процесс запускается внутренними или наследственными факторами, которые действуют посредством активации различных транскрипционных факторов, ответственных как за генетические, так и за эпигенетические механизмы, и внешними или приобретенными факторами, которые инициируются микроокружением опухоли [8].
В настоящее время доказано, что опухолевые клетки с фенотипом EpCAMhighCD44+ демонстрируют все свойства стволовых клеток КРР [9]. Вместе с тем, в литературе недостаточно сведений о коэкспрессии данными клетками CD133, CD166, CD24 и CD184. Данные белковые молекулы во многом определяют функциональное состояние РСК. Особую ценность эти знания имеют в контексте характеристик аденокарцином толстой кишки разных стадий и разной степени злокачественности. На наш взгляд, значительный интерес представляет сравнение экспрессии EpCAM и CD44 у больных КРР и пациентов с неопухолевыми заболеваниями толстой кишки. Данные сведения интересны в контексте феномена эпителиально-мезенхимального перехода (ЭМП), который имеет место при КРР. РСК являются причиной прогрессирования и рецидивов КРР. Детальное изучение фенотипа РСК, их иммунобиологических свойств необходимо для разработки новых методов лечения КРР [10].
Цель исследования – определить содержание РСК, имеющих фенотип EpCAMhighCD44+, в первичной опухоли у больных КРР, а также экспрессию на их поверхности CD133, CD166, CD24 и CD184.
Материал и методы
Выполнено одномоментное поперечное исследование фенотипа РСК у 123 больных аденокарциномой толстой кишки III cтадии, находившихся на лечении в ГУЗ «Краевой онкологический диспансер г. Читы» в период с 2020 по 2025 г. Контрольную группу составили 87 больных, оперированных по поводу неопухолевых заболеваний толстой кишки (пластика колостомы, резекция толстой кишки по поводу дивертикулярной болезни и врожденных аномалий развития) в ГАУЗ «Забайкальская краевая клиническая больница» г. Читы. Основная и контрольная группа сопоставимы по полу и возрасту (p>0,05) (табл. 1).
Забор опухолевой ткани в основной группе и ткани толстой кишки у пациентов контрольной группы производили во время оперативного вмешательства. Исследуемые ткани доставляли в лабораторию в течение 1 ч в термоконтейнере при температуре 5–10 0C, промывали в стерильном фосфатно-солевом буфере (PBS) (Miltenyi BiotecGmbH, Германия) и механически измельчали на мелкие фрагметы (2–4 мм). Для получения клеток использовали ферментативный метод. Из-
Таблица 1/table 1
|
Значимость |
|||
|
Показатель/ |
Основная группа/ |
Контрольная группа/ |
различий/ |
|
Parameter |
Main group (n=123) |
Control group (n=87) |
Significance in differences |
Характеристика больных основной и контрольной групп Characteristics of patients in the main and control groups
Критерии включения/ Inclusion сriteria
Верифицированный колоректальный рак, первичный статус заболевания/ Verified colorectal cancer, primary disease status
Неопухолевые заболевания толстой кишки (коло-стома, неосложненные дивертикулы, долихоколон, травма кишки без перитонита)/ Non-neoplastic diseases of the colon (colostomy, uncomplicated diverticula, dolichocolon, bowel trauma without peritonitis)
|
Злокачественные новообразования любой локали- |
|||
|
Критерии исключения/ Exclusion criteria |
Лучевая терапия или химиотерапия, аутоиммунные и инфекционные заболевания, воспалительные заболевания толстой кишки/ Radiation therapy or chemotherapy, autoimmune and infectious diseases, inflammatory bowel disease |
зации, доброкачественные опухоли толстой кишки, аутоиммунные и инфекционные заболевания, хронические воспалительные заболевания толстой кишки (язвенный колит, болезнь Крона), осложненные формы дивертикулов, долихоколон, перитонит/ Malignant neoplasms of any localization, benign tumors of the colon, autoimmune and infectious diseases, chronic inflammatory diseases of the colon (ulcerative colitis, Crohn's disease), complicated forms of diverticula, dolichocolon, peritonitis |
– |
|
Пол/Gender |
|||
|
Женский/Female |
76 (61,8 %) |
54 (62,1 %) |
χ²=0,002; |
|
Мужской/Male |
47 (38,2 %) |
33 (37,9 %) |
p=0,970 |
|
Возраст, лет/ Age, years, Me(Q1; Q3) |
65,0 (57,0; 70,0) |
63,0 (52,0; 69,0) |
U=4725,5; p=0,145 |
|
Гистологический тип опухоли/Histological type of the tumor, |
|||
|
Аденокарцинома/ Adenocarcinoma |
123 (100 %) |
– |
– |
|
Стадия заболевания/Disease stage |
|||
|
III |
123 (100 %) |
– |
|
|
III А |
6 (4,9 %) |
– |
|
|
III B |
74 (60,1 %) |
– |
– |
|
III С |
43 (35,0 %) |
– |
|
|
Степень злокачественности/Differentiation grade |
|||
|
G1 |
14 (11,4 %) |
– |
|
|
G2 |
94 (76,4 %) |
– |
– |
|
G3 |
15 (12,2 %) |
– |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
мельченные образцы гомогенизировали в течение 60 мин при 37 °C в диссоциаторе GentleMACS Dissociator (Miltenyi BiotecGmbH, Германия) с пробирками С типа и с использованием набора реагентов Tumor Dissociation Kit (Miltenyi BiotecGmbH, Германия) согласно инструкции. Полученную суспензию клеток фильтровали через стерильные клеточные фильтры с размером ячеек 70 мкм, центрифугировали при 400 g в течение 7 мин и ресуспендировали в смеси среды DMEM (Gibco, США) и среды HAM’S F12 (Gibco, США), содержащей 50 МЕ/мл пенициллина–стрептомицина и 4 мМ глутамина в соотношении 2:1. Для оценки жизнеспособности клетки окрашивали красителем 7-AAD (Beckman Coulter, США) и затем подсчитывали с помощью оптического фазово-контрастного микроскопа Nikon Eclipse Ci (Германия).
Суспензию клеток опухолевой ткани в объеме 100 мкл окрашивали следующим коктейлем антител Beckman Coulter, США: CD45-Krome Orange (клон J33), CD44-FITC (клон J.173), CD24-PE (клон ALB9); моноклональными антителами BioLegend, Inc., США: CD166-PE/Cyanine7 (клон 3A6), CD184 (CXCR4)-Brilliant Violet 421™ (клон 12G5), CD326 (EpCAM)-Brilliant Violet 650™ (клон QA20A75), CD133-Brilliant Violet 785™ (клон AC133). Инкубировали при комнатной температуре в течение 15 мин в темноте, затем образцы промывали дважды стерильным PBS с добавлением 2 % фетальной телячьей сыворотки (Sigma-Aldrich Co., США) (330 g в течение 7 мин), ресуспендировали в 300 мкл PBS с 2 % нейтральным формалином (кат. HT5011, Sigma-Aldrich Co., Миссури, США) и анализировали методом проточной цитометрии с использованием цитофлуориметра CytoFLEX LX (Beckman Coulter, США). Для обработки полученных результатов применяли программу CytExpert software v.2.0 и Kaluza™ v.2.1.1 (Beckman Coulter, США). Из каждого образца анализировали не менее 50 000 событий. Стратегия гейтирования опухолевых клеток показана на рис. 1.
Результаты исследования представлены в виде медианы, первого и третьего квартилей (Me [Q1; Q3]). С использованием критерия Колмогорова– Смирнова проводили оценку характера распределения значений в вариационном ряду. Для оценки статистической значимости различий показателей группы больных КРР и контрольной группы использовали непараметрический критерий Манна–Уитни (U). Порогом статистически значимых различий считали р<0,05. При оценке статистической значимости различий в зависимости от степени злокачественности опухоли, в связи с небольшой численностью ряда исследуемых групп (менее 50 наблюдений), проверку нормальности распределения количественных признаков осуществляли с помощью критерия Шапиро–Уилка, обладающего наибольшей статистической мощностью в условиях ограниченных выборок. Первона- чальная оценка различий между тремя группами проведена с помощью непараметрического критерия Краскела–Уоллиса. Попарное сравнение групп проводили с помощью U-критерия Манна–Уитни с учетом поправки Бонферрони, согласно которой критическое значение уровня значимости корректируется по формуле αскорр=α/n, где n – количество проведённых сравнений. При сравнении трёх групп скорректированный порог значимости составляет 0,05/3=0,0167. Таким образом, различия между группами считали статистически значимыми только при условии р<0,0167. Для статистической обработки применяли программу IBM SPSS Statistics Version 25.0 (США).
Результаты
Изучен состав пула клеток нелимфоидного происхождения (CD45-) в зависимости от экспрессии на их поверхности молекулы адгезии эпителиальных клеток EpCAM и дифференцировочного антигена CD44 (табл. 2). При этом не обнаружено значимых различий количества эпителиальных клеток с фенотипом CD45-EpCAM+CD44- в опухолевой ткани у пациентов с КРР и в ткани толстой кишки группы контроля (р=0,072). В первичной опухоли у пациентов с КРР 26,17 [19,35; 31,21] % клеток экспрессируют молекулы EpCAM и CD44. В контрольной группе количество нелимфоидных клеток, имеющих данный фенотип, составило лишь 0,01 [0,0; 0,34] % (р<0,001) (табл. 2). Относительное содержание РСК с фенотипом CD45-EpCAMhighCD44+ в опухолевой ткани при КРР составило 17,15 [11,76; 26,44] % от пула клеток нелимфоидного происхождения. В то же время в контрольной группе не обнаружено клеток, высо-коэкспрессирующих молекулу EpCAM (табл. 2). Установлено, что при КРР в опухолевой ткани в 4,7 раза уменьшается количество клеток стромы, имеющих фенотип CD45-EpCAM-CD44- (р<0,001). Одновременно с этим при КРР значительно увеличивается количество клеток CD45-EpCAM-CD44+ – до 16,28 [9,49; 22,80] %, в контроле – 0,29 [0,02; 1,20] % (р<0,001) (табл. 2).
Наши исследования показали, что у пациентов контрольной группы в ткани толстой кишки не обнаружено РСК с фенотипом EpCAMhighCD44+, экспрессирующих СD133 и CD166. У больных КРР в структуре РСК обнаружено 42,83 [37,07; 51,77] % клеток, одновременно экспрессирующих СD133 и CD166, и 57,17 [48,23; 62,93] % клеток, экспрессирующих дифференцировочный антиген CD133 (табл. 3). Таким образом, показано, что CD133 экспрессируется на всех РСК при КРР.
Кроме того, установлено, что все РСК (EpCAM highCD44+) в первичной опухоли экспрессируют CD184 и 95,18 [88,48; 97,98] % из них одновременно экспрессируют CD24 (табл. 4). Таким образом, истинная частота РСК фенотипа CD44+CD24- при КРР составляет 4,82 %.
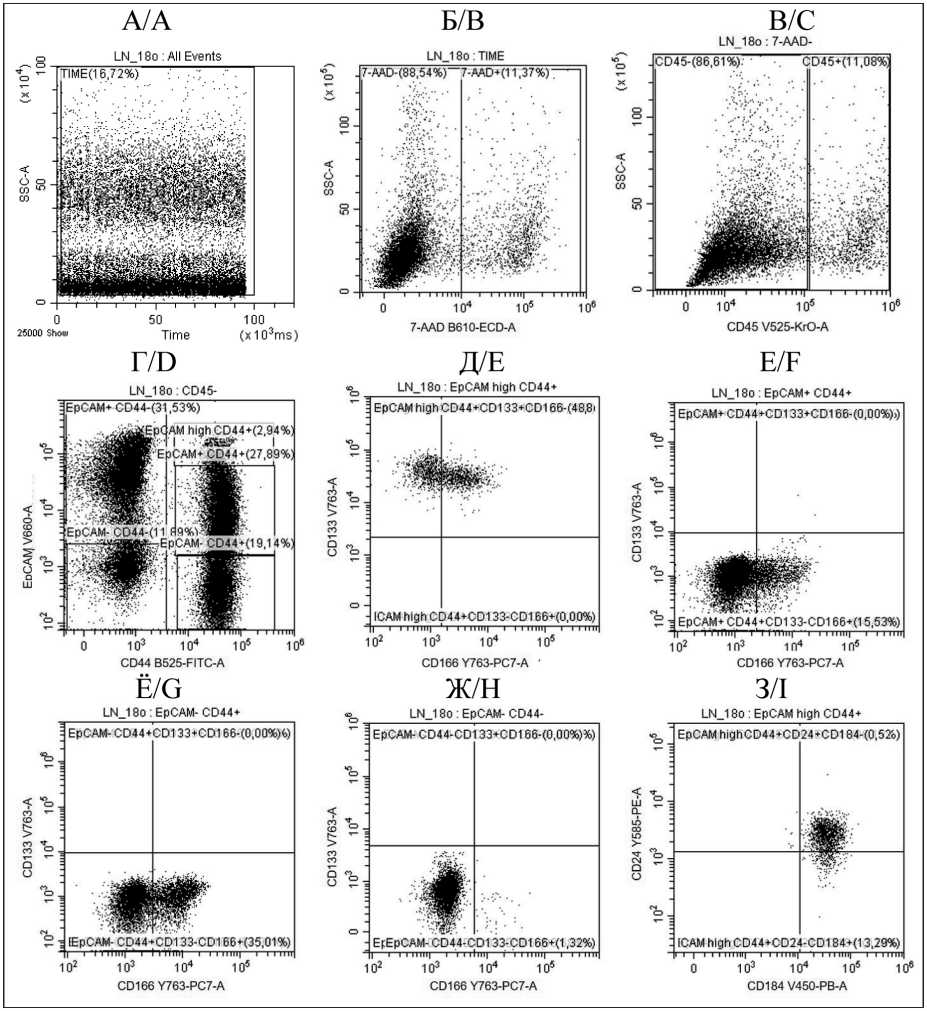
Рис. 1. Алгоритм пошагового выявления (тактика «гейтирования») опухолевых клеток на основании экспрессии поверхностных антигенов: A – исключение артефактов включало временные ограничения; Б – выделение живой популяции клеток отрицательной по 7-аминоактиномицин D (7-AAD); В – выделение CD45-отрицательной популяции живых клеток для дальнейшего анализа опухолевых клеток; Г – профили экспрессии EpCAM/CD44 в первичных опухолях толстой кишки. Определены популяции клеток: EpCAMhighCD44+ – раковые стволовые клетки; EpCAM+CD44+; EpCAM-CD44+; EpCAM+CD44-; EpCAM-CD44;
Д, Е, Ё, Ж – оценка экспрессии CD133 и CD166 на популяциях клеток, идентифицированных по маркерам EpCAM и CD44. Определены популяции стволовых клеток как EpCAMhighCD44+CD133+CD166+ и EpCAMhighCD44+CD133+CD166-. На остальных опухолевых клетках отсутствовала экспрессия CD133, но была экспрессия CD166; З – оценка экспрессии CD24 и CD184 на популяции стволовых клеток. Примечание: рисунок выполнен авторами
Fig. 1. Algorithm for step-by-step detection (gating tactic) of tumor cells based on the expression of surface antigens. A) Artifact exclusion included time restrictions. B) Isolation of a live cell population negative for 7-aminoactinomycin D (7-AAD). C) Isolation of a CD45negative population of live cells for further analysis of tumor cells. D) EpCAM/CD44 expression profiles in primary colon tumors. The following cell populations were identified: EpCAMhighCD44+ – cancer stem cells; EpCAM+CD44+; EpCAM-CD44+; EpCAM+CD44-; EpCAM-CD44-. E, F, G, H) Evaluation of CD133 and CD166 expression on cell populations identified by EpCAM and CD44 markers. Stem cell populations were identified as EpCAMhighCD44+CD133+CD166+ and EpCAMhighCD44+CD133+CD166-. The remaining tumor cells lacked CD133 expression, but did express CD166. I) Evaluation of CD24 and CD184 expression on the stem cell population.
Note: created by the authors
Проведена оценка экспрессии изучаемых белков на поверхности опухолевых клеток в зависимости от степени злокачественности опухоли. У больных с высокодифференцированной аденокарциномой количество клеток EpCAMhighCD44+ в первичной опухоли в 1,5 раза ниже по сравнению с пациентами с умеренно дифференцированной (U=326,5, p=0,002) и в 2,1 раза – по сравнению с низкодифференцированной аденокарциномой (U=21,0, p<0,001). Прочих значимых различий
Таблица 2/table 2
Экспрессия epCaM и Cd44 клетками нелимфоидного происхождения в первичной опухоли у больных колоректальным раком (от Cd45- клеток, %)
expression of epCaM and Cd44 by non-lymphoid cells in the primary colorectal cancer tumor (from Cd45-cells, %)
|
Фенотип клеток/ Cell phenotype |
Группы больных/Patient groups |
Тестовая статистика/Test statistics |
||||||
|
Группа контроля/ Control group |
Колоректальный рак/ Colorectal cancer (n=123) |
Критерий Манна– Уитни/ Criterion Mann–Whitney |
p-value |
|||||
|
Q1 |
(n=87) Me |
Q3 |
||||||
|
Q1 |
Me |
Q3 |
||||||
|
CD45-EpCAM+CD44+ |
0,0 |
0,01 |
0,34 |
19,35 |
26,17 |
31,21 |
0,0 |
<0,001 |
|
CD45-EpCAMhighCD44+ |
0,0 |
0,0 |
0,0 |
11,76 |
17,15 |
26,44 |
0,0 |
<0,001 |
|
CD45-EpCAM+CD44- |
15,86 |
21,99 |
28,66 |
13,60 |
19,03 |
27,16 |
4569,0 |
0,072 |
|
CD45-EpCAM-CD44+ |
0,02 |
0,29 |
1,20 |
9,82 |
16,43 |
21,60 |
172,0 |
<0,001 |
|
CD45-EpCAM-CD44- |
69,13 |
77,12 |
81,85 |
9,49 |
16,28 |
22,80 |
0,0 |
<0,001 |
Примечаниe: таблица составлена авторами.
Notes: created by the authors.
Таблица 3/table 3
Экспрессия Cd133 и Cd166 раковыми стволовыми клетками в первичной опухоли у больных колоректальным раком (от epCaM high Cd44+ клеток, %)
expression of Cd133 and Cd166 by cancer stem cells in the primary tumor of colorectal cancer patients (from epCaMhigh Cd44+ cells, %)
|
Фенотип раковых стволовых клеток/ Phenotype of cancer stem cells |
Группы больных/Patient groups |
Тестовая статистика/Test statistics |
|||||
|
Группа контроля/ Control group |
Колоректальный рак/ Colorectal cancer (n=123) |
||||||
|
Критерий Манна–Уитни/ Criterion Mann–Whitney |
p-value |
||||||
|
Q1 |
(n=87) Me |
Q3 |
|||||
|
Q1 |
Me Q3 |
||||||
|
EpCAM high CD44+ CD133+CD166+ |
0,00 |
0,00 |
0,00 |
37,07 |
42,83 51,77 |
0,0 |
<0,001 |
|
EpCAM high CD44+ |
0,00 |
0,00 |
0,00 |
48,23 |
57,17 62,93 |
0,0 |
<0,001 |
|
CD133+CD166- |
|||||||
Примечаниe: таблица составлена авторами.
Note: created by the authors.
Таблица 4/table 4
Экспрессия дифференцировочных антигенов Cd24 и Cd184 раковыми стволовыми клетками у больных раком толстой кишки (от epCaM high Cd44+ клеток, %)
expression of Cd24 and Cd184 differentiation antigens by cancer stem cells in patients with colon cancer (from epCaMhigh Cd44+ cells, %)
|
Фенотип раковых стволовых клеток/ Phenotype of cancer stem cells |
Группы больных/Patient groups |
Тестовая статистика/Test statistics |
|||||
|
Группа контроля/ Control group (n=87) |
Колоректальный рак/ Colorectal cancer (n=123) |
||||||
|
Критерий Манна–Уитни/ Criterion Mann–Whitney |
p-value |
||||||
|
Q1 |
Me |
Q3 |
Q1 |
Me Q3 |
|||
|
EpCAM highCD44+ CD24+CD184+ |
0,00 |
0,00 |
0,00 |
88,48 |
95,18 97,98 |
0,0 |
<0,001 |
|
EpCAM highCD44+ CD24-CD184+ |
0,00 |
0,00 |
0,00 |
2,02 |
4,82 11,52 |
0,0 |
<0,001 |
Примечание: таблица составлена авторами.
Note: created by the authors.
Таблица 5/table 5
Экспрессия epCaM, Cd44, Cd133, Cd166, Cd24 и Cd184 раковыми стволовыми клетками у больных раком толстой кишки в зависимости от степени злокачественности опухоли, Me [Q1; Q3] expression of epCaM, Cd44, Cd133, Cd166, Cd24, and Cd184 by cancer stem cells in patients with colon cancer depending on the tumor grade, Me [Q1; Q3]
|
Фенотип раковых стволовых клеток/ Phenotype of cancer stem cells |
Больные колоректальным раком/ Patients with colorectal cancer |
Тестовая статистика/ Test statistics |
|||
|
G1 (n=14) 1 |
G2 (n=94) 2 |
G3 (n=15) 3 |
Критерий Краскела Уоллиса/Criterion Kruskal–Wallis |
– Критерий Манна–Уитни/ Criterion Mann–Whitney |
|
|
EpCAMhighCD44+ (от CD45-, %) |
11,7 [9,1; 13,7] |
17,7 [11,9; 25,9] |
24,9 [16,8; 30,2] |
H=15,5 p<0,001 |
U1–2=326,5 p1–2=0,002 U1–3=21,0 p1–3<0,001 U2–3=459,0 p2–3=0,03 |
|
CD133+CD166+ (от EpCAMhigh CD44+, %) |
39,3 [29,4; 44,6] |
43,5 [37,4; 52,1] |
42,8 [37,6; 51,9] |
H=4,0 p=0,13 |
U1–2=439,0 p1–2=0,045 U1–3=72,0 p1–3=0,15 U2–3=704,0 p2–3=0,99 |
|
CD184+CD24+ |
97,1 [93,3; 99,0] |
94,9 [88,3; 98,3] |
95,0 [83,4; 96,4] |
H=3,8 p=0,15 |
U1–2=501,5 p1–2=0,15 |
|
(от EpCAMhigh CD44+, %) |
U1–3=57,0 p1–3=0,036 U2–3=590,0 p2–3=0,31 |
||||


