Свойства электростатического потенциала и электронной плотности в сравнении сорбционной активности хромат- и фосфат-анионов
Автор: Шманина Елена Александровна, Барташевич Екатерина Владимировна, Печенюк София Ивановна, Михайлов Геннадий Георгиевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 4 т.5, 2013 года.
Бесплатный доступ
Проведена сравнительная характеристика распределений функций, получаемых на основе электронной плотности и свойств электростатического потенциала на заданном контуре электронной плотности для фосфати хромат-анионов и их протонированных форм с целью исследования возможности использования данных функций в описании относительной сорбционной активности ионов.
Молекулярный электростатический потенциал, электронная плотность, лапласиан электронной плотности, теория qtaim
Короткий адрес: https://sciup.org/147160276
IDR: 147160276 | УДК: 544.723,
Electrostatic potential properties of electron density regarding to chromate- and phosphate-anions sorption activity
The comparative analysis of functions allocations was performed to describe a sorption activity of PO 43-, CrO 42- and their protonated forms. These functions were obtained on the basis of electron density and electrostatic potential properties of anions at the defined electron density contour to investi gate the possibility of these features in the description of the relative sorption activity of the ions.
Текст научной статьи Свойства электростатического потенциала и электронной плотности в сравнении сорбционной активности хромат- и фосфат-анионов
Решение задач, направленных на ресурсосбережение и снижение рисков техногенных катастроф, требует подходов, основанных на фундаментальных исследованиях структуры и свойств частиц, выступающих загрязнителями окружающей среды. Исследования, ведущиеся в данном направлении, включают как экспериментальные, так и теоретические подходы к изучению сорбционных процессов и действия эффективных сорбентов [1–3]. Отметим важность теоретических подходов, которые позволяют анализировать структурные и электронные особенности строения частиц, поверхностей, адсорбционных комплексов. Подходы, основанные на моделировании структуры и свойств частиц, дают объяснения механизмам невалентных взаимодействий в конденсированных средах, что в свою очередь позволяет прогнозировать условия эффективного извлечения вредных частиц в процессах очистки и разделения. Можно выделить направления, посвящённые либо моделированию свойств сорбента, либо исследованиям строения промежуточного комплекса «сорбат-сорбент», либо свойствам сорбата. Теоретическая оценка сорбционного сродства остается не менее важной задачей, поскольку электронные и пространственные особенности строения частиц содержат необходимую информацию для понимания закономерностей и механизмов протекания сорбции. Такие исследования требуют использования представлений о распределении электронной плотности и формируемых ею особенностей строения, отвечающих за специфику невалентных взаимодействий.
Систематические экспериментальные исследования сорбции анионов на поверхности рентгеноаморфных оксигидроксидов металлов (железа, циркония, алюминия) позволили изучить обширный ряд сорбционных процессов в варьирующихся условиях для ряда анионов, таких как фосфат, карбонат, оксалат, тартрат, цитрат, хромат-анионы [4–8]. Авторы [9] показывают, что положение анионов в относительном ряду их сорбируемости незначительно зависит от природы сорбирующих их оксигидроксидов и ионной среды. В то же время оценка геометрических размеров, формы анионов, их формальных зарядов не позволяет расположить их в ряд симбатно экспериментально наблюдаемому сорбционному сродству. Например, наблюдаемая сравнительно высокая сорбционная активность фосфат-анионов и низкая хромат-анионов никак не может быть объяснена с позиций их сходной геометрической формы и формальных зарядов их гидратированных форм. Экспериментальные данные [9] свидетельствуют, что хромат- и фосфат-анионы обладают контрастно-противоположным адсорбционным сродством по отношению к оксигидроксидам железа или циркония. Известно, что часть исследуемых фосфат и хромат-анионов практически во всей анализируемой в эксперименте области рН существуют в виде гидро- и дигидро-форм: НPO4 2– (при pH 9) или Н 2 PO 4 – (при pH 5), НCrO 4 – (при pH 5).
Соответствующие формы хромат- и фосфат-анионов, обладающие контрастнопротивоположным сорбционным сродством по отношению к оксигидроксидам железа или циркония, выступили объектами нашего исследования. Основной задачей данной работы явилась сравнительная характеристика свойств электронной плотности и распределений молекулярного электростатического потенциала, нанесенного на заданный контур электронной плотности геометрически сходных частиц – фосфат и хромат-анионов, а также их протонированных форм. Мы задались целью оценить возможность интерпретации различной способности к невалентным взаимодействиям исследуемых частиц в терминах полученных данных об их электронной плотности и свойствах электростатического потенциала.
Методы расчетов
Локализация равновесной геометрии ионов PO 4 3– , CrO 4 2– , НPO 4 2– , Н 2 PO 4 – , НCrO 4 – и расчет волновых функций выполнялись методом Кона-Шэма [10] с использованием функционала B3LYP и базисного набора 6-31G** в программе Firefly, version 8.0.0 [11].
В том же приближении, что и оптимизация геометрии, для всех рассматриваемых структур выполнены расчеты волновых функций, которые использовались для вычисления квантовотопологических характеристик электронной плотности на базе теории QTAIM [12]. Поиск критических точек электронной плотности, расчет значений лапласиана электронной плотности и карт электростатического потенциала производились с использованием программы AIMAll 12.06.03 [13].
Мы последовательно обратили внимание на ряд различных величин, полученных на основе электростатического потенциала ( V S ) и его распределении в трехмерном пространстве на поверхности исследуемых анионов. Вычислены величины максимумов ( VS max ) и минимумов ( VS min ) электростатического потенциала, его среднее значение ( V mеan s ). Для анионов среднее значение электростатического потенциала вычислялось следующим образом:
t
V "" = 1 £ V ( r J , t i = 1
где t – общее число точек, задаваемое сеткой на поверхности выбранного контура электронной плотности. Проанализированы закономерности в относительном расположении минимумов и максимумов на поверхности анионов. Наряду с вышеперечисленными величинами была вычислена общая площадь поверхности аниона ( A tot). В качестве внешней сферы частицы мы использовали контур электронной плотности, равный 0,001 ат. ед. [14].
Все процедуры визуализации 2D и 3D карт распределения электростатического потенциала и свойств электронной плотности производились с помощью программных пакетов Multiwfn 2.3 [15], MoleCoolQt [16].
Обсуждение результатов
Ряд современных публикаций [17–28] свидетельствует о том, что молекулярный электростатический потенциал (МЭП) можно рассматривать в качестве фундаментального фактора, определяющего природу и поведение атомов и молекул, их способность к межмолекулярным взаимодействиям. В работах, направленных на поиск взаимосвязи между экспериментально наблюдаемыми сорбционными свойствами и электронными характеристиками частиц, получаемых в результате квантово-химических расчетов, наглядно продемонстрировано успешное использование свойств молекулярного электростатического потенциала (МЭП) [17–19]. Карта электростатического потенциала, как правило, наносится на поверхность частицы, отвечающую контуру электронной плотности, близкой к границам, задаваемым ван-дер-ваальсовыми радиусами. С помощью локальных значений полного электростатического потенциала описываются свойства, включающие в себя потенциальную способность частиц участвовать в межмолекулярных взаимодействиях.
Обратим внимание на то, что пространственное распределение электростатического потенциала зависит от соотношения размеров и зарядов ионов. Для изолированного положительного иона и изолированного нейтрального атома он всюду положителен за пределами ядер и монотонно стремится к нулю с ростом удаления от ядра. В то же время, для изолированных моноядерных отрицательных ионов он монотонно затухает, проходя через ноль и достигая своего единственного отри- цательного минимума на некотором расстоянии от ядра. В дальнейшем, при r→∞, электростатический потенциал стремится к нулю со стороны области отрицательных значений [20, 21].
Д ля ра сс м а тривае м ых нами ф осф а т и хром а т-анионов величина электростатического потенци а ла , на несе нна я н а поверхн ость, задаваемую контуром электронной пл о тнос ти 0, 001 ат. е д. , который близок к границе ван - дер-ваальсового радиуса, везде отрицательна. В силу того, что мы ра с сма три вае м облас ти локализации ег о на и б ол ьш их V s max и наименьших V s min значений, далее в те к с те и спольз у е тс я выражени е «область низких значений потенциала» для б о ль ш и х п о м од у л ю отрицате льн ых ве ли чин п оте нц иа ла.
Ана лиз иру я ве личи ны и положение минимумов и максимумов электро с та т иче ского п отен циа ла на поверхности мо лекул, Поли тцер и соавторы [21, 29] объясняют силу и направленность г а ло г енных с в я зей, пр иб ега я к поня ти ю « σ-hole» (σ-дырка). Она определяется как область повы ш е н ны х (к ак пра вило , по ложи тельных для нейтральных молекул) значений э ле к трос татическо го потенциала на продо лж е н ии ко валентной связи атома галогена. Позднее эти ми ж е а втор а ми б ы ло пре д ло ж е но ис п ольз о ва н ие а налогичной терминологии для концевых атом ов к ис лород а и ли с еры, связанных в молекуле [30 , 3 1]. С точки зрения орбитального подхода [21, 32] такая область хара к т е ри зу е тся истощение м з а с еле нно с ти np z -орбитали атома, если ось z направлена вдоль его ковале нтн ой связ и. Т аким об разом , пон я тие « σ-дырка», описывающее наличие области относи те ль но пов ыше нны х зн аче ний электростатического потенциала, находящейс я на пр од олж ении ковале нтн ой с вя зи а том а, приобре ло у ниверс а льн ый хара к тер.
С у ч ет ом т ого, ч то в и ссле дуемых нами анионах подавляющее число св яз ей – это связи X–O (где Х = С, P, Cr, S ), н ам и бы л о проанализировано распределение областей л о к ализаци и вы со к и х и низких з начен ий э л ектр о ст ат ич еского потенциала на поверхности анионов. Устан о в л ено, ч то в о з можн ы тр и ти п а л о к ал и з аци и о бластей высоких значений потенциала в рассм от р енных анио н ах .
-
1. Лок а лиз а ци я на продо лжении к овале нтн ой с вя з и, та к н а з ы вае м ая σ-дырка [33] – относи те ль ное повыше н ие элект р ос татического потенциала на внешней поверхно сти а том ов кислорода в а нион ах т е траэдрическ ог о ст роения, у которых область истощения электр оста тиче ск ог о п оте н циа ла ф ормируетс я на пр од ол жении связи Х=О. Эти области сосредоточ е ны на ма ксимально д ос ту пн ой вне шней повер хнос ти аниона. Аналогичным образом, для плоских к а р б онат или ок с а-лат- анионов обла с ти в ы соки х значений электростатического потенци а ла , вы д е л е нн ы е на рис. 1, а, б темно-с еры м ц ве том , ра с положены н а а т омах к ислоро д а .
-
2. Концентра ция пов ы шенных значений потенциала на поверхности атомо в водород а . В н а ш е м с л у чае э то анионы кис лых с олей, с о д е ржащие ковалентные О –Н связи, а также С–Н связи в а нион а х ор г аниче ск их с ое д инений.
-
3. Об ла сть наим е нее отр ицатель н ого электро с татич е с к ого поте нциала расположена ортого на ль но плос к ости, в к оторо й рас поло жены s p 2 -гибридизованные орбитали, так называемая «π-дырка» [33 ] . В на ше м слу ча е э та область наблюдается в структурах карбон ат - и оксалат-анионов на д и по д плоск ос тью к арбона тн ой и кар б о к с иль но й групп. Такие области более заметны при ра с смотр е нии ра с преде л ения э лектростатического потенциала на контуре со ответс тву ю щ ем и о н ному рад иу с у к ис лор од а 0, 01 ат. ед . (рис. 1, в, г).
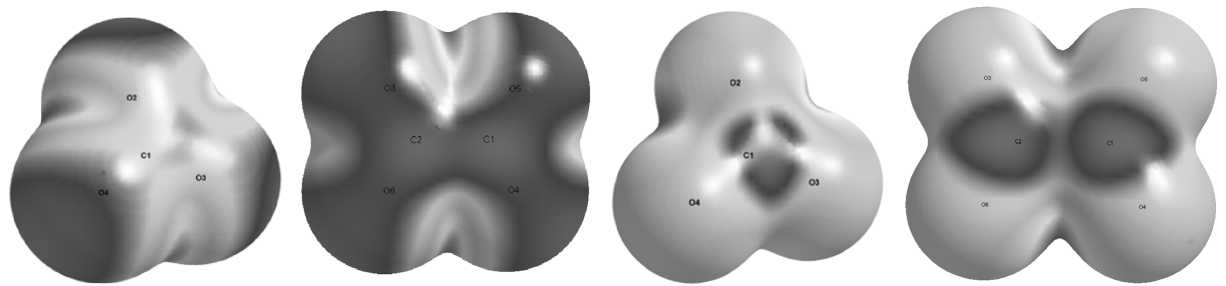
а) б) в) г)
Рис. 1. Локальные значения электростатического потенциала, нанесенные на поверхность, ограниченную контуром электронной плотности 0,001 ат. ед.: а) для CO 3 2– , б) C 2 O 4 2– , и на поверхность, ограниченную контуром электронной плотности 0,01 ат. ед.:в) для CO 3 2– и г) C 2 O 4 2–
Обращение к экстремумам электростатического потенциала обосновано не только традиционным использованием этих величин как дескрипторов межмолекулярных взаимодействий. Как известно, интегрирование свойств по объему, ограниченному выбранной поверхностью, производится с точностью до постоянной интегрирования, которая будет зависеть от размера и индивидуальности сравниваемых частиц. Однако положения экстремальных значений Vsmax и Vsmin определяется однозначно, и может выступать физически обоснованным индикатором при сравнении пространственного расположения областей, отвечающих за способность к невалентным взаимодействиям в разных анионах. Также представляют интерес диапазоны изменений потенциала, вычисление которых произведено на основе разниц его экстремальных значений. Данные о характеристиках электростатического потенциала представлены в табл. 1.
Таблица 1
Значения характеристик электростатического потенциала для фосфат-, гидрофосфат-, дигидрофосфат- и хромат-анионов, рассчитанных на поверхности контура электронной плотности 0,001 ат. ед.
|
Анион |
Vs max, ат. ед. |
Vs min, ат. ед. |
V mеans, ат. ед. |
Ato t , Å2 |
Vs max / Atot , ат. ед./А 2 |
|
H 2 PO 4 – |
–0,083 |
–0,223 |
–0,184 |
373,5 |
–0,00022 |
|
HPO 4 2– |
–0,261 |
–0,409 |
–0,369 |
377,7 |
–0,00069 |
|
PO 4 3– |
–0,516 |
–0,592 |
–0,553 |
377,7 |
–0,00137 |
|
CrО 4 2– |
–0,341 |
–0,389 |
–0,359 |
385,6 |
–0,00088 |
|
HCrО 4 – |
–0,0735 |
–0,207 |
–0,178 |
383,3 |
–0,00092 |
М а кс и м у мы э л е к тро с та тиче с к о го п от е н ц и а ла V s max в непротонированных анионах тетраэдрической конфигурации PO 4 3– , CrO 4 2– , сосредоточены на атомах кислорода на рис. 2, области высо кого э лек трос т а ти че с ког о п оте нциала обозначены более тёмным цветом. Д ля хромат-аниона сре д н и е зн а че н и я э ле к тр ос та ти че ск ого п оте н ц и ал а Vs mean , выделенные белым цветом на рис. 2, о пояс ы в а ю т э к в а т ори а ль н у ю область атома хрома. Минимумы электростати че с к ог о потенциала V s min , в ыд е ле н н ы е н а ри с. 2 с в е тло -серым цветом, сосредоточены по биссектрисам углов О–Cr–O.
М а кс и м альн о е зн а че ни е электростатического потенциала для фосфат-аниона V s max = –0, 516 а т. е д ., э то н и же , че м д ля хром а т-аниона V s max = –0,314 ат. ед. (табл. 1). Следовательно, хромат- а н ион обла д ае т более выраженной способностью к взаимод е й с тв и ям с э лек тр о н одон орны ми и ли форм альн о отри ц а тельн о за ря ж е н н ыми ц е н трами сорбента. Однако если рас сма три ват ь а н и оны в у с л ови ях, близких к экспериментальным [9], то есть уч е с ть, что в ра с тв ор е фосфат- ан ион наход и тс я и с к лю чительно с протонированной форме, следует с ра в н и в а ть с в ой с тв а соответс тв е н н ым об р а зо м протон и ров а н н ых фор м анионов. Известно [9], что дигидрофосфат-анион и гидрохромат-ан ион мо гут совместно сосуществовать в растворе. При с оп о с та в ле н ии р а с че тн ых мак с и му м ов э л е к тро статического потенциала видно, что более вы с ок о е зн а че н и е V s max характерно для дигидрофосфат-аниона. При сравнении минимальных значений потенциала, по л у че н с ле д у ю щ и й ряд , в к отором анионы расположены от большего значени я Vs min к меньшему (ат. ед.): гидрохромат (– 0 , 207) , д и гид ро фосфа т (–0,223), хромат (–0,389), гидрофосфат (–0,409), фосфат (–0,592). То ест ь, в н а б лю да е мы х у с лов и ях ги д ро фосфа т -анион также имеет преимущества перед хромат-ан ион ом. Т ак и м образом, сравнение диапазонов электростат и че с к ог о п оте н ц и а л а , оп ред е ляе м ых ра зн и це й ме жду значениями экстремумов, приводит к выв од у о том, что б ол ьшей потенци альной с п о с об н остью к невалентным взаимодействиям обла д ае т ги д ро фосфа т - ан ион , д ля к оторо го хар а к те рн о на и ме н ьше е зн аче н и е ми н и му ма Vs min и наибольшее значение мак с и м у ма э л е к троста ти чес к о го потенц и ала Vs max .
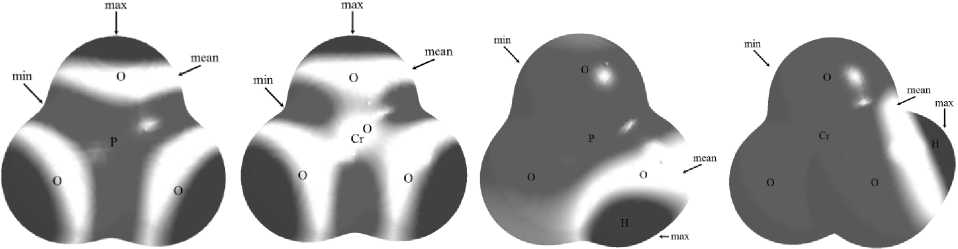
а) б) в) г)
Рис. 2. Локальные значения электростатического потенциала, нанесенные на поверхность, ограниченную контуром электронной плотности 0,001 ат. ед.: а) PO 4 3– , б) CrO 4 2– , в) НPO 4 2– , г) HCrO 4
Для фосфат- аниона средние значения V mеan s расположены в области «экваториального пояса» большого круга атомной поверхности кислородов. В гидрофосфат (НPO 4 2– ), дигидрофосфат (Н 2 PO 4 – ) и гидрохромат-анионах (HCrO 4 – ) минимальные значения электростатического потенциала сосредото чены на атомах кислорода, а максимум электростатического потенциала V s max приходится на атомы водорода ОН групп. Очевидно, что для гидрофосфат и гидрохромат -анионов значения всех представ ленных характеристик электрос татического потенциала (максимальное, минимальное, среднее зна чение электростатического потенциала, среднее отклонение от значений V mеans ) выше, чем для соот ветствующих непротонированных фосфат и хромат -анионов.
Предполагая пространственные аспекты механи зма сорбции, следует ожидать ориентации областей минимумов электрос татического потенциала анионов на области положительного эле к тростатического потенциала со рбента, например, на водороды гидроксильн ых групп или участки поверхностей, формируемые катионами м еталла с ненасыщенной координационной сферой. Од нако данный процесс вероятен в случае непосредственной доступности обл асти минимума эле к тростатического потенциала и в отсутствии других конкурирующих центро в.
При протонировании анионов происходит кардинальное перераспределение электростатиче ского потенциала, которое, вер оятно, будет увеличивать его сорбционное с родство, влияя на п о ведение в процессе сорбции. П ри сопоставлении распределения электроста тического потенциала в области его максимумов, ви дно, что так называемые σ-дырки сосредоточены на каждом из ато мов кислорода. Отметим, что в протонированных формах анионов σ-дырок нет. Области повы шенных значений потенциала наблюдаются только на атомах водорода. Этот факт позволяет предположить, что суще ствую т различные виды связывания с сорбционны ми центрами для пр о тонированной и непротонированной формы анионов.
Наряду с контуром электронной плотности (0,001 ат. ед.), который близок к контуру поверхности, заданной ван-дер- ваальсовым радиусом кислорода (1 ,36 Å) [35], были построены анало гичные изображения для элек тростатического потенциала на контуре (0,0 1 ат. ед.), который по своей величине близок к ионному радиусу кислорода (1,26 Å) [36]. На рис. 3 изображены области максимумов электростатического потенц иала, которые обозначены более тёмным цветом, средние значения – светло- серым, области минимумов электростатического по тенциала – белым на контуре, соответствующему значению электронной плотности 0,01 ат. ед.

а)
б)
в)
г)
Рис. 3. Локальные значения электростатического потенциала, нанесенные на поверхность, ограниченную контуром электронной плотности 0,01 ат. ед.: а) PO 4 3– , б) CrO 4 2– , в) НPO 4 2– , г) HCrO 4 –
М аксимумы электростатич еского потенциала сосредоточены в област и центрального атома (фосфора или хрома), однако в случае фосфат -аниона, средние значения рассматриваемой величины сосредоточены в максимально у даленных от центра областях на поверхности атомов кислорода. Та ким образом, рассмотрение кон тура электронной плотности, более близкого к ядру не приводит к выделению дополнительных раз личий электронной структуре фосфат и хромат-анионов.
На картах распределения лапласиана электронной плотности между атомами фосфор-кислород характерны меньшие значения лапласиана электронной плотности, это означает, что электронная плотность концентрируется вокруг критической точки связи (3, –1) и взаимодействие атомов имеют сравнительно высокую составляющую ковалентного типа. В случае атомов хрома и кислорода межатомные взаимодействия носят характер, определяемый как в большей степени ионный [25] (рис. 4), так как лапласиан электронной плотности локализуется в области близкой к ядрам атомов. Таким образом, при сравнении свойств фосфат- и хромат-анионов пока- зано, что в соответствии с картами лапласиана электронной плотности, большей ковалентной составляющей обладает связь Р–О, по сравнению с Cr–O.
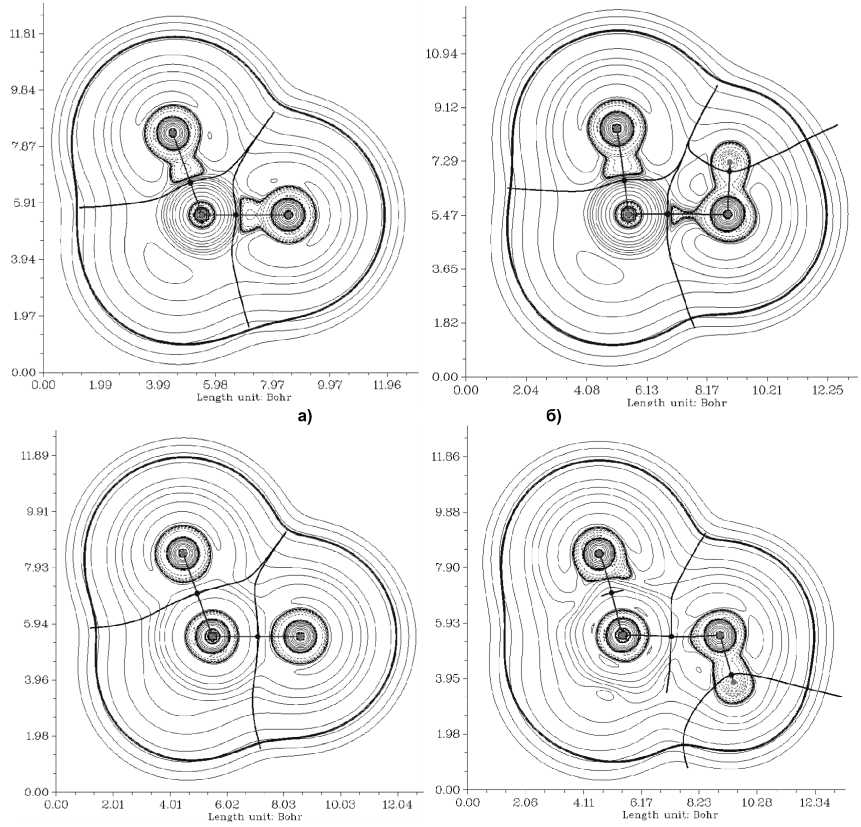
в)
г)
Рис. 4. Карты распределения лапласиана электронной плотности: а) для фосфат-, б) гидрофосфат-, в) хромат-, г) гидрохромат-анионы (сплошными и пунктирными линиями обозначены области положительных и отрицательных значений лапласиана электронной плотности)
Значение электронной плотности в критически х точках связей X–O для протонированных форм выше, чем для непротонир ованных, за исключением связи «центральн ый атом – протони рованный кислород». Также вед ут себя и величины лапласиана электронной плотности в крит ических точках связей (табл. 2).
Таблица 2
Квантово-топологические характеристики в критических точках связей анионов
|
ρ b 1 |
∇ 2ρ b |
ρ b 1 |
∇ 2ρ b |
||
|
Хромат-анион |
Фосфат-анион |
||||
|
Cr – O2 |
0,229 |
0,891 |
P1 – O5 |
0,179 |
0,881 |
|
Гидрохромат- анион |
Гидрофосфат-анион |
||||
|
O2 – H5 |
0,362 |
–1,938 |
O2 – H5 |
0,360 |
–1,933 |
|
Cr1 – O2 |
0,141 |
0,640 |
P1 – O2 |
0,124 |
0,230 |
|
Cr1 – O3 |
0,265 |
0,970 |
P1 – O3 |
0,202 |
1,222 |
|
Cr1 – O4 |
0,262 |
0,965 |
P1 – O4 |
0,197 |
1,125 |
|
Cr1 – O6 |
0,262 |
0,965 |
P1 – O6 |
0,202 |
1,222 |
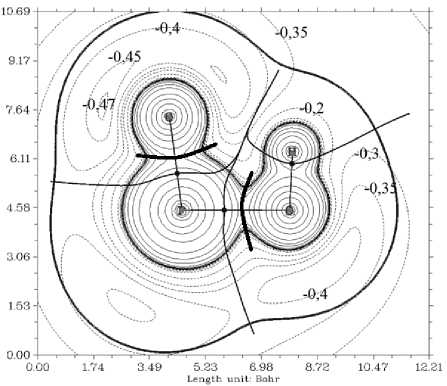
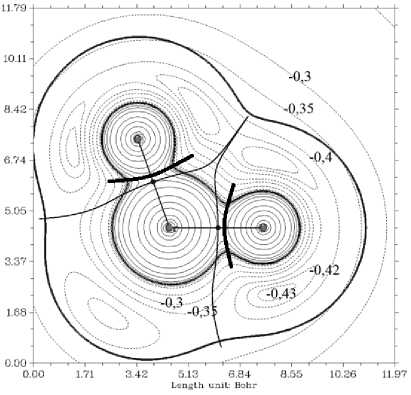
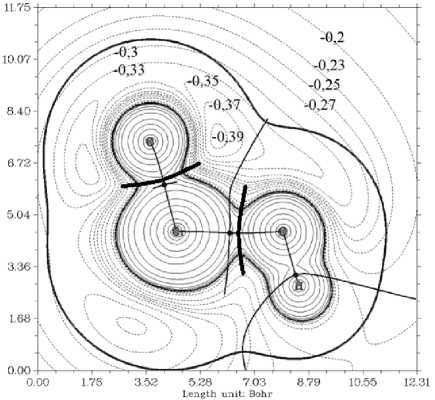
Использование теории QTAIM позволяет выделить границы атомов на основе вектора нулевого потока градиента электронной плотности в сложных частицах [12]. Такие границы формируют атомные бассейны электронной плотности, называемые ρ-бассейнами [26]. С другой стороны, для функции электростатического потенциала можно провести сепаратрисы (обозначены жирной линией на рис. 5), которые будут формировать границы φ-бассейнов электронейтраль-ных атомов [29].
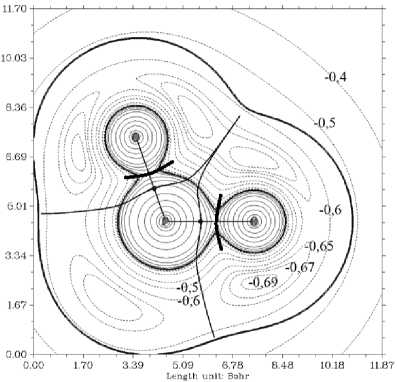
а)
б)
в)
г)
Рис. 5. Контурные карты электростатического потенциала объектов: а) фосфат-, б) гидрофосфат-, в) хромат-, г) гидрохромат-анионы
На рис. 5 представлена суперпозиция атомных бассейнов в хромат- и фосфат-анионах, для чего вычислены градиентные поля [15], на основе чего проведены линии, определяемые как границы атомных бассейнов. Отметим, что φ-бассейн определяет границу электронейтрального атома в ионе для которого вся зарядовая плотность внутри такого бассейна полностью компенсирует заряд ядра данного атома. Интегрирование электронной плотности по объему такого бассейна дает нулевое значение заряда атома.
При сравнении ρ- и φ-атомных бассейнов в хромат- и фосфат-анионах отметим, что для фосфора требуется меньшее количество электронной плотности кислорода для компенсации его заряда. Такая ситуация хорошо согласуется с тем, что концевые атомы кислорода в фосфат-анионе характеризуются более высокой реакционной способностью за счет сил электростатического взаимодействия.
Электроны, принадлежащие атомному бассейну концевого кислорода, в фосфат-анионе в большей степени притягиваются к ядру атома фосфора, чем таковые в хромат-анионе. Кроме того, фосфат имеет более короткое расстояние от ядра центрального иона до контура с плотностью 0,001 ат. ед. Связь Р–О самая короткая (1,60 Å), внешний контур электронной плотности находится на расстоянии 3,31 Å (вдоль линии связи), 2,48 Å (между связями), и контур электронной плотности 0,001 ат. ед. оказывается ближе всего к центральному атому именно в фосфат-анионе. Это хорошо соотносится с тем, что область повышенных значений электростатического потенциала – σ-дырка для фосфат-аниона выражена сильнее. В целом, данные наблюдения за распределением электронной плотности и электростатического потенциала иллюстрируют тот факт, что ядра кислорода в фосфат-анионе оказываются в меньшей степени экранированными вдоль линии их ковалентных связей, а значит, должны проявлять большую способность к невалентным взаимодействиям электростатического характера. Это можно выделить как отдельный фактор, который может оказаться важным при сравнительной оценке сорбционной активности разных анионов сходного строения.
Результаты и выводы
В терминах электростатического потенциала и свойств электронной плотности дано сравнительное описание способности к нековалентным взаимодействиям фосфат и хромат-анионов, а также их протонированных форм.
Электронная плотность, принадлежащая атомным бассейнам кислорода в фосфат-анионе в большей степени притягивается к ядру атома фосфора, чем в хромат-анионе, что наблюдается при анализе суперпозиции атомных бассейнов электронной плотности и электростатического потенциала.
Отсутствие областей истощения электростатического потенциала – σ-дырок на концевых атомах кислорода в гидрофосфат-, дигидрофосфат- и гидрохромат-анионов, позволяет предположить наличие различных видов связывания с потенциальным сорбционным центром для протонированной и непротонированной формы анионов. Показано, что на основе наблюдений за свойствами и распределением электронной плотности и электростатического потенциала можно объяснить экспериментально наблюдаемому факту о том, что большей сорбционной активностью обладает гидрофосфат-анион, для которого характерны наименьшее значение минимума и наибольшее значение максимума электростатического потенциала по сравнению с другими исследованными анионами.
Таким образом, рассмотрение свойств распределения электронной плотности и электростатического потенциала в рассматриваемых близких по форме анионах позволяет объяснить причины различной их способности к нековалентным взаимодействиям электростатического характера. Такая характеризация может оказаться значимой при сравнительной оценке сорбционного сродства и описании механизмов сорбционных процессов.
Список литературы Свойства электростатического потенциала и электронной плотности в сравнении сорбционной активности хромат- и фосфат-анионов
- Особенности необратимой сорбции катионов тяжелых металлов гранулированным сорбентом на основе силикатов и алюмосиликатов кальция/Г.Г. Михайлов, А.Г. Морозова, Т.М. Лонзингер и др.//Вестник ЮУрГУ. -№ 12(229). -2011. -C. 46-53.
- Печенюк, С.И. Сорбция анионов на оксигидроксидах металлов (обзор)/С.И. Печенюк//Сорбционные и хроматографические процессы. -2008. -Т. 8. -Вып. 3. -С. 380-429.
- Шманина, Е.А. Локальные свойства электростатического потенциала в исследовании закономерностей сорбции на поверхности оксигидроксидов/Е.А. Шманина, Е.В. Барташевич, С.И. Печенюк//Сборник тезисов VII Всерос. конф. молодых учёных по химии и наноматериалам «Менделеев-2013». -С. 258-260.
- Печенюк, С.И. Использование значения pH точки нулевого заряда для характеристики свойств оксогидроксидов/С.И. Печенюк//Известия РАН. Серия химическая. -1999. -С. 1029.
- Семушин, В.В. О свойствах поверхности титаногелей/В.В. Семушин, С.И. Печенюк//Сорбционные и хроматографические процессы. -2009. -Т. 9. -№ 3. -С. 448-456.
- Сорбция оксалат-и карбонат-ионов на цирконогелях/С.И. Печенюк, Л.Ф. Кузьмич, Ю.П. Семушина, Г.И. Кадырова//Сорбционные и хроматографические процессы. -2011. -Т. 11.-С. 372-381.
- Печенюк, С.И. Конкурентная сорбция хромат-, оксалат-и карбонат-ионов на цирконогелях/С.И. Печенюк, Л.Ф. Кузьмич, Ю.П. Семушина//Сорбционные и хроматографические процессы. -2012. -Т. 12. -С.189-195.
- Печенюк, С.И. Влияние природы соли-прекурсора оксигидроксидного сорбента на сорбцию оксалат-ионов/С.И. Печенюк, Л.Ф. Кузьмич, Ю.П. Семушина//Журнал физической химии. -2012. -Т. 86. -№ 9. -С. 1584-1587.
- Печенюк, С.И. Адсорбционное сродство анионов к оксигидроксидам металлов/С.И. Печенюк, Л.Ф. Кузьмич, Ю.П. Семушина//Журнал физической химии. -2013. -Т. 87. -№ 3. -С. 505.
- Koch, W. A chemist’s guide to density functional theory/W. Koch, M.C. Holthausen. -Weinheim. Wiley-VCH VerlagGmbH, 2001. -293 p.
- Granovsky, A. -http://classic.chem.msu.su/gran/firefly/index.html
- Бейдер, Р. Атомы в молекулах. Квантовая теория/Р. Бейдер. -М.: Мир, 2001. -532 с.
- Keith, T.A. AIMALL, Version 12.06.03, 2012, Professional. -http://aim.tkgristmill.com.
- Properties of atoms in molecules: atomic volumes/R.F.W. Bader, M.T. Carroll, J.R. Cheeseman, C. Chang//J. Am. Chem. Soc. -1987. -V. 109. -P. 7968.
- Lu, T. Multiwfn: a multifunctional wavefunction analyzer/T. Lu, F. Chen//Journal of Computational Chemistry. -2012. -V. 33. -P. 580-592.
- Hubschle, C.B. MoleCoolQt -a molecule viewer for charge-density research/C.B. Hubschle, B. Dittrich//J. Appl. Cryst. -2011. -V. 44. -P. 238-240.
- Edward, G.M. Calculated surface electrostatic potentials of molecular sieve models containing SiO4, AlO4 and PO4 units/G.M. Edward, J.S. Murray, P. Politzer//J. Mol. Graphics. -1994. -V. 12. -P.169-171.
- Computational study of CO and NO adsorption on magnesium oxide nanotubes/J. Beheshtian, M. Kamfiroozi, Z. Bagheri, A. Ahmadi/Physica E. -V. 44. -2011. -P. 546-549.
- Nature of the NIMOS catalyst edge sites: an atom in molecules theory and electrostatic potential studies/Y. Aray, J. Rodriguez, A.B. Vidal, S. Coll//Journal of Molecular Catalysis A: Chemical. -V. 271. -2007. -P. 105-116.
- Politzer, P. The fundamental nature and role of the electrostatic potential in atoms and molecules/P. Politzer, J.S. Murray//Theor Chem Acc. -2002. -V. 108. -P. 134-142.
- Цирельсон, В.Г. Квантовая химия. Молекулы, молекулярные системы и твердые тела: учебное пособие для вузов/В.Г. Цирельсон. -М.: Бином, 2010. -496 с.
- Murray, J.S. Expansion of the а-hole concept/J.S. Murray, P. Lane, P. Politzer//J. Mol. Mod. -2009. -V. 15.-P. 723.
- Politzer, P. An overview of halogen bonding/P. Politzer, P. Lane, M.C. Concha et al.//J. Mol. Model. -2007. -V. 13. -P. 305.
- Politzer, P. Molecular surface electrostatic potentials in relation to noncovalent interactions in biological systems/P. Politzer, J.S. Murray, Z. Peralta-Inga//International Journal of Quantum Chemistry. -V. 85. -2001. -P. 676-684.
- Shields, Z.P. Directional tendencies of halogen and hydrogen bonds/Z.P. Shields, J.S. Murray, P. Politzer//Int. J. Quantum Chem. -2010. -V. 110. -P. 2823.
- Density functional tight-binding studies of carbon nanotube structures/Z. Peralta-Inga, P. Lane, J. S. Murray et al.//Journal of Structural Chemistry. -2003. -14(5). -P. 431-443.
- Petrova, G.P. Enhanced reactivity of carbonyl compounds on MgO surface: A computational study/G.P. Petrova, G.N. Vayssilov, B. Galabov/Journal of Molecular Catalysis A: Chemical. -V. 342. -2011 -P. 67-73.
- Politzer, P. The electrostatic potential: an overview/P. Politzer, J.S. Murray//Theoretical Chemistry Accounts. -2002. -V. 108. -P. 134.
- Clark, T. σ-Holes/T. Clark//WIREs Computational Molecular Science. -2013. -Vol. 3. -P. 13-20 ( ) DOI: 10.1002/wcms.1113
- Politzer, P. Halogen bonding: an electrostatically-driven highly directional noncovalent interaction/P. Politzer, J.S. Murray, T. Clark//Physical Chemistry Chemical Physics. -2010. -V. 12. -P.7748-7757.
- Piland, G. Halogen bonding of substituted iodobenzenes with potential solvent molecules: A comparison of binding energies/G. Piland, P. Jasien//Computational and Theoretical Chemistry. -Vol. 988. -P. 19-26. - DOI: 10.1016/j.comptc.2012.02.021
- Clark, T. σ-Hole bonding: molecules containing group VI atoms/T. Clark, P. Politzer//Journal Molecular Modeling. -2007. -13. -P. 1033-1038.
- σ-Holes, π-holes and electrostatically-driven interactions/J.S. Murray, P. Lane, T. Clark et al.//Journal Molecular Modeling. -2012. -V. 18. -P. 541-548.
- Китайгородский, А.И. Молекулярные кристаллы/А.И. Китайгородский. -М.: Наука. -1971. -424 с.
- Чупахин, А.П. Общая химия. Химическая связь и строение вещества: учебное пособие/А.П. Чупахин. -Новосибирск: Новосибирский государственный университет, 2003. -168 с.


