Свойства водной дисперсии комплекса хитотозана и хондроитина сульфата, полученных из гидробионтов
Автор: Новиков Виталий Юрьевич, Долгопятова Наталия Владимировна, Коновалова Ирина Никандровна, Кучина Юлия Анатольевна
Журнал: Вестник Мурманского государственного технического университета @vestnik-mstu
Рубрика: Биотехнология пищевых продуктов и биологически активных веществ
Статья в выпуске: 3 т.19, 2016 года.
Бесплатный доступ
Исследование возможности производства хондроитина сульфата и хитозана и полиэлектролитных комплексов на их основе, полученных из местного морского сырья, является актуальным с точки зрения разработки комплексной безотходной технологии переработки природного сырья. Объектами исследования являлись хитозан, полученный из панциря камчатского краба Paralithodescamtschaticus, и хондроитина сульфат, выделенный из хрящевой ткани семги Salmo salar. Для определения поверхностного натяжения растворов полиэлектролитов и дисперсии комплекса использовали метод Вильгельми, эффективный радиус частиц определяли методом дисперсии светорассеяния, измерения эффективной вязкости проводили в условиях сдвиговой деформации. Изучены условия формирования, поверхностные и реологические свойства комплекса хитозана и хондроитина сульфата, выделенных из гидробионтов Баренцева моря. Установлены условия получения и молярные соотношения этих полиэлектролитов, при которых водная дисперсия комплекса сохраняет устойчивость в течение длительного времени. Установлено, что при добавлении раствора хондроитина сульфата к раствору хитозана в молярных соотношениях 1 : 3; 1 : 6 образуется дисперсия полиэлектролитного комплекса, устойчивая в течение 2-3 суток. Дисперсии полиэлектролитного комплекса ведут себя как псевдопластичные неньютоновские жидкости. При молярном соотношении смешиваемых растворов 1 : 1 (независимо от последовательности их смешения) образуется суспензия полиэлектролитного комплекса, затем выпадает осадок. Равновесные значения поверхностного натяжения водной дисперсии полиэлектролитного комплекса выше, чем у растворов хондроитина сульфата и хитозана. Определен эффективный радиус частиц в дисперсии комплекса. Эффективный радиус частиц в дисперсии комплекса зависит от молярного соотношения хондроитина сульфат : хитозан. Предложена качественная схема формирования полиэлектролитного комплекса хитозана и хондроитина сульфата в виде нерастворимого осадка и в виде устойчивой водной дисперсии. Водные дисперсии комплекса на основе хитозана и хондроитина сульфата могут быть использованы для стабилизации суспензий, эмульсий, для создания пищевых продуктов с лечебно-профилактическими свойствами.
Хитозан, хондроитина сульфат, полиэлектролитный комплекс, поверхностное натяжение, вязкость
Короткий адрес: https://sciup.org/14294929
IDR: 14294929 | УДК: 577.114.7 | DOI: 10.21443/1560-9278-2016-3-585-592
Properties of aqueous dispersion of chitosan and chondroitin sulfate complex derived from aquatic organisms
Investigation of production of chondroitin sulfate, chitosan and polyelectrolyte complexes based on them received from the local marine raw materials is relevant from the point of view of developing a comprehensive waste-free technology for natural raw materials processing. The objects of study are chitosan derived from the shell of the Kamchatka crab Paralithodes camtschaticus and chondroitin sulfate derived from cartilage of salmon Salmon salar. To determine the surface tension of polyelectrolyte complex solutions and dispersions the Wilhelmy method has been used, the effective radius of particle dispersion has been calculated by light scattering, measurements of effective viscosity have been carried out under shear deformation. The conditions of formation, surface and rheological properties of the chitosan and chondroitin sulfate complex extracted from aquatic organisms in the Barents Sea have been studied. Obtaining conditions and molar ratios of these polyelectrolytes in which the aqueous dispersion of the complex remains stable for a long time have been established. It has been found that by addition of chondroitin sulfate solution to chitosan solution in molar ratios of 1 : 3; 1 : 6 the dispersion of the polyelectrolyte complex stable for 2 to 3 days has been formed. The polyelectrolyte complex dispersions behave as non-Newtonian pseudoplastic liquid. When the molar ratio of the mixed solution is 1 : 1 (regardless of the sequence of mixing) suspension of the polyelectrolyte complex has been formed, then there is precipitation. Equilibrium surface tension of the aqueous dispersion of the polyelectrolyte complex is higher than that of solutions of chondroitin sulfate and chitosan. The effective radius of particles in the complex dispersion has been determined. The effective radius of the particles in the complex dispersion depends on the molar ratio of chondroitin sulfate : chitosan. A qualitative scheme of formation of polyelectrolyte complex from chitosan and chondroitin sulfate as an insoluble precipitate and as a form of stable aqueous dispersion has been proposed. Aqueous dispersions based on chitosan and chondroitin sulfate complex can be used to stabilize suspensions, emulsions, to create foods with a therapeutic and prophylactic properties.
Текст научной статьи Свойства водной дисперсии комплекса хитотозана и хондроитина сульфата, полученных из гидробионтов
Практическое применение хитозана – линейного полисахарида, состоящего из (1→4)-связанных остатков 2-амино-2-деокси-β-D-глюкопиранозы – постоянно расширяется, что объясняется его биосовместимостью, биодеградируемостью, нетоксичностью для человеческого организма и ярко выраженной антимикробной активностью. Хондроитина сульфат входит в состав многих лекарственных препаратов, применяемых при заболеваниях суставов. Хондроитина сульфат представляет собой сульфатированный гликозаминогликан с молекулярной массой 10 000–100 000 Да. В хондроитина сульфате дисахаридные фрагменты цепи (хондрозины) связаны β-(1-4) гликозидной связью. Дисахарид хондрозин является мономером хондроитина сульфата и состоит из остатков двух моносахаридов: D-глюкуроновой кислоты и D-галактозамина, связанных между собой β-(1→3)-гликозидной связью.
В результате реакции между противоположно заряженными полиэлектролитами в водных растворах образуются полиэлектролитные комплексы (ПЭК) – нерастворимые стехиометрические и растворимые нестехиометрические. Макромолекулы полиэлектролитов в таких комплексах удерживаются ионными, водородными связями, а также дисперсионными силами.
Простейший способ получения полиэлектролитного комплекса (ПЭК) – смешивание водных растворов, один из которых содержит полианионный, а другой – поликатионный компонент. Хитозан (ХТЗ) в растворе при контакте с хондроитина сульфатами образует полиэлектролитные комплексы за счет прочных электростатических связей между - NH 3 + -группами хитозана и -OSO 3 - и –COO – -группами хондроитина сульфата (ХС) [1].
Полиэлектролитные комплексы находят применение в медицине, могут быть использованы в качестве матрицы для создания сорбентов и носителей различного назначения, для использования в процессе адсорбционно-флокуляционной очистки воды, в качестве добавки в ветеринарные препараты, повышающие биологическую ценность мяса, в качестве связующих для почв и грунтов, для создания форм с пролонгированным выделением лекарственных веществ [2–7].
Неиспользуемые источники хиндроитина сульфата и хитозана имеются в Мурманской области. Исследование возможности производства хондроитина сульфата и хитозана и полиэлектролитных комплексов на их основе, полученных из местного морского сырья, является актуальным с точки зрения комплексной безотходной технологии переработки природного сырья. Такое производство позволит повысить рентабельность рыбоперерабатывающей промышленности и получить ценные препараты, имеющие применение в медицине, пищевой и косметической промышленности, сельском хозяйстве и др.
Применение комплексов обусловлено их способностью формировать в объеме раствора локальные гидрофильно-гидрофобные области и поведением на межфазных границах. Водные дисперсии комплекса на основе хитозана и хондроитина сульфата могут быть использованы для стабилизации суспензий, эмульсий, для создания пищевых продуктов с лечебно-профилактическими свойствами. В связи с этим в данной работе изучены условия формирования, поверхностные и реологические свойства устойчивых водных дисперсий комплекса ХТЗ и ХС, предложен качественный механизм его формирования в объеме водной фазы.
Материалы и методы
Хитозан был получен из панциря камчатского краба Paralithodes camtschaticus по известной технологии [5]. Степень деацетилирования хитозана составила 68,8 %, молекулярная масса, определенная вискозиметрическим методом, – 368 кДа.
Хондроитина сульфат был выделен из хрящевой ткани семги Salmo salar по технологии, заимствованной из патента [6]. Молекулярная масса, определенная нефелометрическим методом, составила 60 кДа.
Для определения поверхностного натяжения (на границе с воздухом) водных растворов полисахаридов и дисперсии ПЭК использовали метод Вильгельми [8], размер частиц определяли методом дисперсии светорассеяния (метод "спектра мутности") [9; 10].
Измерение эффективной вязкости растворов проводили в условиях сдвиговой деформации [11] на ротационном вискозиметре Brookfield RVDV–II+Pro с термостатируемой измерительной ячейкой в виде двух коаксиальных цилиндров (R н /R в = 1,14) в области скоростей сдвига γɺ от 0,93 до 186 с –1 при температуре 20 ± 0,1 °С.
Растворы полисахаридов готовили следующим образом: навеску ХТЗ растворяли в 0,5 %-м растворе CH 3 COOH и оставляли раствор на сутки, ХС растворяли в воде. Таким образом получали 1 %-е растворы полисахаридов. Величина pH приготовленных растворов составляла для хитозана 3,7, для хондроитина сульфата – 6,2. pH раствора хитозана доводили до pH 6,2 раствором NaOH (С = 0,1 моль/дм 3 ). Затем растворы смешивали в молярном соотношении 1 : 6, 1 : 3, 1 : 1, 3 : 1.
Соотношение масс ХС и ХТЗ рассчитывалось из условия стехиометрического связывания – -OSO 3 - и –COO – -групп (ХС) и - NH 3 + -групп ХТЗ. При расчете учитывалась степень деацетилирования ХТЗ.
Результаты и обсуждение
При смешивании растворов хитозана и хондроитина сульфата происходит образование полиэлектролитного комплекса, который выделяется в виде новой фазы.
При добавлении раствора хондроитина сульфата к раствору хитозана в молярных соотношениях 1 : 3; 1 : 6 образуется дисперсия полиэлектролитного комплекса, устойчивая в течение всего времени наблюдения (до 3 сут).
При молярном соотношении смешиваемых растворов 1 : 1 (независимо от последовательности их смешения) образуется суспензия полиэлектролитного комплекса, затем выпадает осадок.
Результаты изучения физико-химических свойств устойчивой водной дисперсии полиэлектролитного комплекса хитозана и хондроитина сульфата приведены на рис. 1 и в таблице.
На рис. 1 приведена зависимость поверхностного натяжения водных растворов полисахаридов и дисперсии полиэлектролитного комплекса от времени.
Из данных, приведенных на рис. 1, следует, что равновесные значения поверхностного натяжения для исследованных растворов хитозана и хондроитина сульфата устанавливаются примерно за 8–10 мин, для полиэлектролитного комплекса – за 15 мин.
Равновесные значения поверхностного натяжения для полиэлектролитного комплекса (кривая 3) несколько выше, чем у исходных растворов хитозана и хондроитина сульфата. Анализ кинетических зависимостей поверхностного натяжения показывает, что ПЭК снижает поверхностное натяжение на границе "водный раствор – воздух" по сравнению с чистым растворителем до 53 мН/м, что позволяет использовать его для стабилизации дисперсных систем.
Результаты изучения эффективного радиуса частиц Rэф в дисперсии полиэлектролитного комплекса хитозана и хондроитина сульфата приведены в таблице. Предварительно был определен гидродинамический радиус агрегатов макромолекул в 1 %-м растворе полисахаридов. В условиях эксперимента для хитозана он составил 1 452 нм, для хондроитина сульфата – 310 нм. Такого различия следовало ожидать, поскольку молекулярная масса хитозана примерно в 6 раз больше, чем хондроитина сульфата.
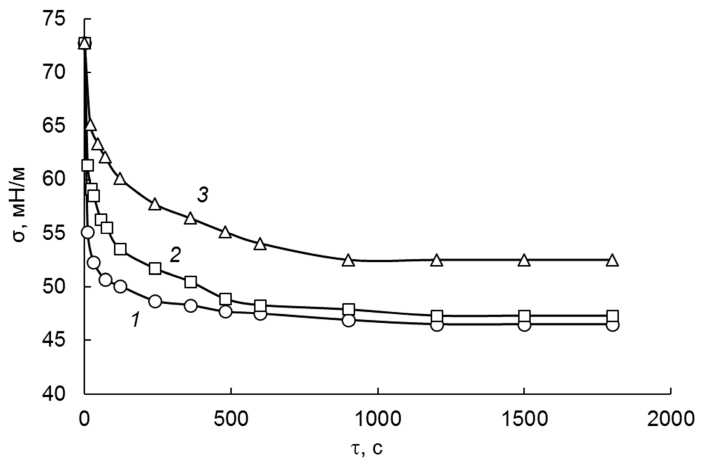
Рис. 1. Зависимость поверхностного натяжения водных растворов полисахаридов и полиэлектролитного комплекса от времени: 1 – ХТЗ; 2 – ХС; 3 – ПЭК. Концентрация растворов – 1 %, t = 22 °С, молярное соотношение в комплексе ХС : ХТЗ = 1 : 3
Таблица
Эффективный радиус частиц R эф в дисперсии полиэлектролитного комплекса хитозана и хондроитина сульфата
|
Мольное отношение хондроитина сульфата и хитозана |
Эффективный радиус (нм) через время формирования ПЭК (мин) |
|||
|
1 |
30 |
60 |
1 440 |
|
|
1 : 3 |
139 |
137 |
138 |
121 |
|
1 : 6 |
176 |
378 |
378 |
279,8 |
Из данных, приведенных в таблице, следует, что R эф комплекса зависит от молярного соотношения ХС : ХТЗ. С увеличением содержания хитозана в исходном растворе R эф увеличивался в 1,2 раза через одну минуту после сливания растворов и в 2,5 раза через 30–60 мин с момента начала формирования комплекса. Это, по всей видимости, можно объяснить различием в молекулярной массе хитозана и хондроитина сульфата: с увеличением содержания более высокомолекулярного компонента R эф увеличивается.
Изучение кинетики комплексообразования показало, что при молярном соотношении ХС : ХТЗ = 1 : 3 комплекс формируется практически сразу. Через сутки наблюдается некоторая компактизация комплекса (R эф уменьшается до 121 нм).
При молярном соотношении ХС : ХТЗ = 1 : 6 время формирования комплекса составляет примерно 30 мин (R эф увеличивается до 378 нм), затем средний эффективный радиус частиц комплекса практически не меняется.
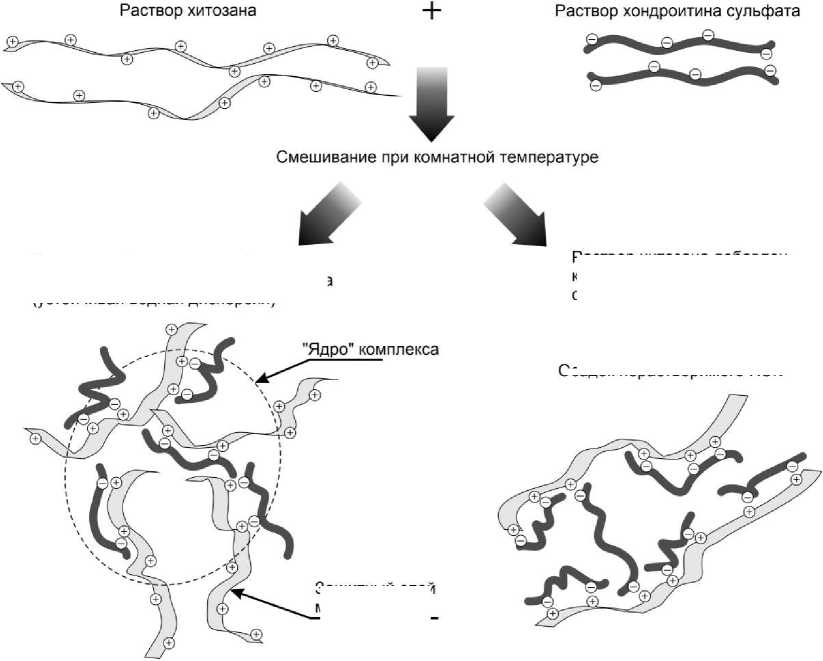
На основании полученных результатов можно предложить качественную схему формирования полиэлектролитного комплекса хитозана с хондроитина сульфатом в водных дисперсиях и образование нерастворимого осадка при смешении хитозана с хондроитина сульфатом (рис. 2).
При образовании нерастворимого осадка (добавление хитозана к хондроитина сульфату) хондроитина сульфат оказывается внутри комплекса, возможно также образование поперечных "сшивок". При образовании устойчивой дисперсии (добавление хондроитина сульфата к избытку хитозана) комплекс состоит из "ядра" и защитного слоя из макромолекул хитозана и хондроитина сульфата, которые обеспечивают устойчивость дисперсии в течение длительного времени.
Результаты реологических измерений для водных растворов хитозана, хондроитина сульфата и дисперсии полиэлектролитного комплекса приведены в виде кривых течения – зависимостей эффективной вязкости η и напряжения сдвига τ от скорости сдвига γɺ (рис. 3, 4). Кривые течения в диапазоне скоростей сдвига от 0,93 до 186 с–1 приведены в логарифмических координатах.
Раствор хондроитина сульфата добавлен к избытку раствора хитозана (устойчивая водная дисперсия)
Раствор хитозана добавлен к раствору хондроитина сульфата (1:1)
Защитный слой макромолекул
Хитозан "снаружи" макромолекул: хондроитина сульфата
Хондроитина сульфат "снаружи1 макромолекулы хитозана
Рис. 2. Качественная схема формирования полиэлектролитного комплекса хитозана с хондроитина сульфатом в водных дисперсиях

Осадок нерастворимого ПЭК
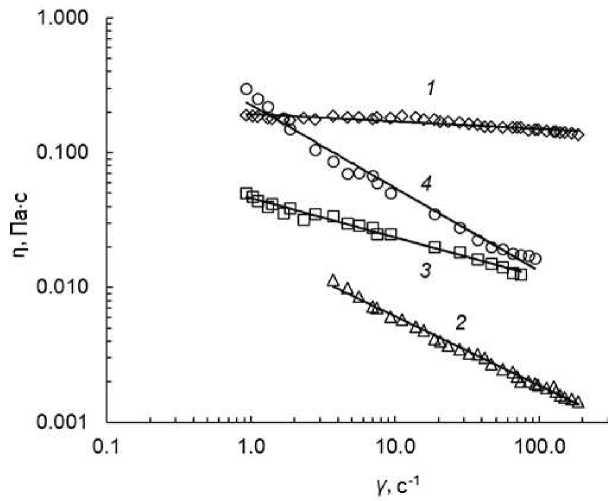
Рис. 3. Кривые течения η = f ( γɺ ) растворов хитозана (С = 1 %), хондроитинсульфата (С = 1 %) и раствора ПЭК в логарифмических координатах, t = 20 °С: 1 – ХТЗ; 2 – ХС; 3 – ПЭК (молярное соотношение ХС : ХТЗ = 1 : 3); 4 – ПЭК (молярное соотношение ХС : ХТЗ = 1 : 6)
Реологическое поведение исследованных 1 %-х растворов хитозана и хондроитина сульфата демонстрируют кривые 1 и 2 на рис. 3 и 4. Эффективная вязкость раствора хитозана примерно в 10 раз превышает вязкость раствора хондроитина сульфата во всем исследованном диапазоне скоростей сдвига. Это, по всей видимости, объясняется значительным различием в молекулярной массе полисахаридов (368 и 60 кДа соответственно).
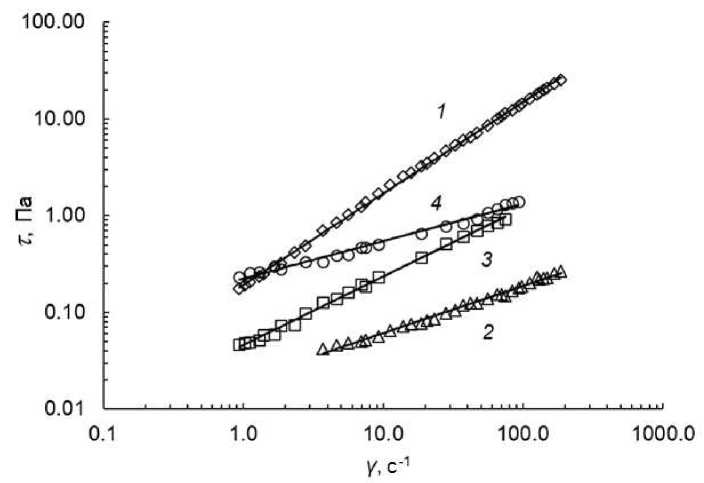
Рис. 4. Кривые течения τ = f ( γɺ ) растворов хитозана (С = 1 %), хондроитинсульфата (С = 1 %) и раствора ПЭК в логарифмических координатах, t = 20 °С. Экспериментальные данные (точки) аппроксимированы моделью Оствальда – де Виля. 1 – ХТЗ; 2 – ХС; 3 – ПЭК
(молярное соотношение ХС : ХТЗ = 1 : 3); 4 – ПЭК (молярное соотношение ХС : ХТЗ = 1 : 6)
Характер реологического поведения также различный. Для раствора хитозана в условиях эксперимента вязкость практически не зависит от скорости сдвига (эффективная вязкость изменяется незначительно от 0,19 до 0,14 Па·с).
Для раствора хондроитина сульфата вязкость уменьшается, достигая минимального значения при γɺ = 186 с –1 . Вероятно, в объеме раствора хондроитина сульфата образуются непрочные коагуляционные структуры из макромолекул полисахарида, которые легко разрушаются при увеличении скорости сдвига.
Реологическое поведение водных 1 %-х дисперсий полиэлектролитного комплекса при различных молярных соотношениях ХС : ХТЗ демонстрируют кривые 3 и 4 (рис. 3, 4). Из этих данных следует, что водные растворы полиэлектролитного комплекса ведут себя как неньютоновские жидкости, для которых вязкость уменьшается во всем исследованном диапазоне скоростей сдвига, достигая минимальных значений при γɺ = 93 с –1 .
При молярном соотношении ХС : ХТЗ = 2,5 : 17 максимальная вязкость раствора полиэлектролитного комплекса практически одинакова с вязкостью исходного 1 %-го раствора хитозана (≈ 0,2 Па·с).
Минимальные значения вязкости водных дисперсий полиэлектролитного комплекса при молярных соотношениях ХС : ХТЗ = 2,5 : 17 и 5 : 17 практически совпадают (0,012 и 0,015Па·с).
Кривые течения растворов хитозана, хондроитина сульфата и водной дисперсии полиэлектролитного комплекса были аппроксимированы с помощью модели Оствальда – де Виля (рис. 2) [12; 13], τ = k · γɺ n , где n – индекс течения; k – коэффициент консистенции.
Коэффициент парной корреляции составил 0,9977 (для молярного соотношения ХС : ХТЗ = 2,5 : 17) и 0,9975 (для молярного соотношения ХС : ХТЗ = 5 : 17). Значение индекса течения n в уравнении Оствальда – де Виля для всех изученных растворов находится в пределах 0 < n < 1 (для раствора хитозана значение n близко к единице 0,9446).
На основании полученных результатов можно сделать вывод о том, что водные дисперсии полиэлектролитного комплекса при изученных молярных соотношениях хондроитина сульфата и хитозана ведут себя как псевдопластичные неньютоновские жидкости.
Заключение
-
1. Впервые изучены коллоидно-химические свойства ПЭК на основе ХС и ХТЗ, полученных из гидробионтов Баренцева моря.
-
2. При взаимодействии хитозана и хондроитина сульфата образуется осадок, в котором молярное соотношение этих полиэлектролитов остается постоянным, приблизительно 1 : 1, что объясняется образованием комплекса, в котором все аминогруппы хитозана соединены со всеми карбоксильными и сульфатными группами хондроитина сульфата; при добавлении раствора хондроитина сульфата к раствору хитозана в молярном соотношении 1 : 3; 1 : 6 образуется дисперсия полиэлектролитного комплекса, сохраняющая устойчивость в течение 2–3 сут.
-
3. Равновесные значения поверхностного натяжения водной дисперсии полиэлектролитного комплекса выше, чем у растворов хондроитина сульфата и хитозана. Эффективный радиус частиц в дисперсии полиэлектролитного комплекса зависит от молярного соотношения хондроитина сульфат : хитозан.
-
4. Предложена качественная схема формирования полиэлектролитного комплекса хитозана с хондроитина сульфатом в виде нерастворимого осадка и в виде устойчивой водной дисперсии.
-
5. Установлено, что водные дисперсии полиэлектролитного комплекса при изученных соотношениях хондроитина сульфата и хитозана ведут себя как псевдопластичные неньютоновские жидкости, реологическое поведение которых может быть описано с помощью модели Оствальда – де Виля.
Работа выполнена при финансовой поддержке Российского научного фонда (Проект № 16-16-00076).
Список литературы Свойства водной дисперсии комплекса хитотозана и хондроитина сульфата, полученных из гидробионтов
- Хитин и хитозан. Получение, свойства и применение/под ред. К. Г. Скрябина, Г. А. Вихорева, В. П. Варламова. М.: Наука, 2002. 365 с.
- Зезин А. Б., Рогачева В. Б. Успехи химии и физики полимеров. М.: Химия, 1973. 360 с.
- Кабанов В. А. Полиэлектролитные комплексы в растворе и в конденсированной фазе//Успехи химии. 2005. Т. 74, № 1. С. 5-23.
- Denuziere A., Ferrier D., Domard A. Chitosan-chondroitin sulfate and chitosan-hyaluronate polyelectrolyte complexes. Physico-chemical aspects//Carbohydrate Polymers. 1996. N 29 (4). P. 317-323.
- Политова Н. К., Бешлей И. В. Интерполиэлектролитные комплексы: получение, строение и перспективы их применения//Вестник Института биологии Коми НЦ УрО РАН. 2002. Вып. 56, № 6. C. 9-12.
- Sui W., Huang L., Wang J., Bo O. Preparation and properties of chitosan chondroitin sulfate complex microcapsules//Colloids and Surfaces B: Biointerfaces. 2008. V. 65, Iss. 1. P. 69-73.
- Huang L., Sui W., Wang Y., Jiao Q. Preparation of chitosan/chondroitin sulfate complex microcapsules and application in controlled release of 5-fluorouracil//Carbohydrate Polymers. 2010. V. 80, Iss. 1. P. 168-173.
- Рабек Я. Экспериментальные методы в химии полимеров. В 2 ч. Ч. 1. М.: Мир, 1983. 384 с.
- Амелина В. А., Долинный А. И., Измайлова В. Н. Методические разработки к спецпрактикуму по коллоидной химии. М.: МГУ, 1981. 59 с.
- Кленин В. И., Щеголев С. Ю., Лаврушин В. И. Характеристические функции светорассеяния дисперсных систем. Саратов: Изд-во Сарат. ун-та, 1977. 177 с.
- Slater S. D., Parsons K. P. Atomic force microscopy//The Imaging Science Journal. 1997. V. 45. P. 269.
- Матвеенко В. Н., Кирсанов Е. А. Вязкость и структура дисперсных систем//Вестник Моск. ун-та. Сер. 2, Химия. 2011. Т. 52, № 4. С. 243-276.
- Шумилина Е. В., Щипунов Ю. А. Гели хитозана с каррагинанами//Коллоидный журнал. 2002. Т. 64, № 3. С. 413-420.


