Тактика хирургического лечения при метастатическом поражении верхнешейного отдела позвоночника
Автор: Бажанов С.П., Гуляев Д.А., Ульянов В.Ю., Островский В.В., Толкачев B.C.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Травматология и ортопедия
Статья в выпуске: 3 т.14, 2018 года.
Бесплатный доступ
Продемонстрирован случай успешного хирургического лечения пациента с метастатическим поражением верхнешейного отдела позвоночника с учетом концепции мульдидисциплинарного подхода. Проведено одномоментное двухэтапное хирургическое вмешательство: первым этапом выполнен окципитоспондилодез полисегментарной конструкцией; вторым — удаление опухоли из расширенного комбинированного доступа. Установлено, что предлагаемая тактика хирургического лечения позволяет осуществить радикальное вмешательство в одну хирургическую сессию без нарастания неврологического дефицита в послеоперационном периоде.
Верхнешейный отдел, метастатическая опухоль, позвоночник, тактика, хирургическое вмешательство
Короткий адрес: https://sciup.org/149135132
IDR: 149135132
The tactics of surgical treatment in metastatic lesions of upper cervical spine
We demonstrated a successful case of surgical treatment of the patient with metastatic lesion of upper cervical spine with respect to multidisciplinary approach. We performed simultaneous two-stage surgical intervention, the first stage being occipitospondylodesis by multi-segment construction; and second —tumor resection from expanded combined access. It has been stated that the proposed surgical tactics allows performing curative resection in one surgical session without neurological deficit buildup in the postoperative period.
Текст научной статьи Тактика хирургического лечения при метастатическом поражении верхнешейного отдела позвоночника
данные свидетельствуют о разнонаправленности и противоречивости методик хирургического лечения пациентов с метастатическим поражением верхнешейного отдела позвоночника, однако большинство авторов склоняются к необходимости осуществления оперативных вмешательств из расширенных комбинированных доступов, соответствующих концепции современной онкологической хирургии [5, 6]. При этом мультидисциплинарный подход, основанный на совместном сотрудничестве нейрохирурга со смежными специалистами при выполнении подобных операций, является наиболее целесообразным [7–9].
Цель: продемонстрировать возможность одномоментного двухэтапного хирургического лечения пациента с метастатическим поражением верхнешейного отдела позвоночника.
Описание клинического случая. Проведен анализ данных медицинской карты стационарного больного, находившегося на лечении в отделении нейрохирургии НИИТОН СГМУ. Пациент К. 55 лет поступил на стационарное лечение в отделение нейрохирургии НИИТОН СГМУ с направительным диагнозом: метастатическое поражение структур 2-го шейного позвонка с синдромом острой атлантоаксиальной нестабильности. Жалобы при поступлении на боль и ограничение движений в шейном отделе позвоночника, невозможность удерживать голову (со слов пациента «голову приходится поддерживать обеими руками»), затруднение при глотании твердой пищи, слабость в верхних и нижних конечностях. Из анамнеза известно, что ранее больному было выполнено хирургическое вмешательство по поводу низкодифференцированного рака мочевого пузыря. Была проведена цистпростатвезикулэктомия с расширенной подвздошно-паховой лимфодиссекцией и формированием илеокондуита по методике Бриккера. Какая-либо адъювантная терапия не осуществлялась. Через 3 месяца с момента хирургического вмешательства стал отмечать перечисленные жалобы, связанные с дисфункцией в шейном отделе позвоночника, позже присоединились признаки дисфагии. Проведено комплексное клинико-интраскопическое обследование на предмет выявления отдаленных метастазов, в том числе позитронно-эмиссионное сканирование в режиме «весь организм», верифицировано интенсивное накопление радиофармпрепарата (2-фтор-2-дезокси-D-глюкоза) в области заглоточного пространства на уровне С1-С2 позвонков. Других патологических очагов накопления радиофармпрепарата выявлено не было.
При объективном осмотре отмечалось ограничение подвижности шейного отдела позвоночника во всех плоскостях. В неврологическом статусе оценка по шкале Karnovsky 70 баллов. Отмечалась гипе-стезия в зоне иннервации корешков спинномозговых нервов, отходящих на уровне С1-С2 позвонков с обеих сторон. Проводниковые расстройства были представлены тетрапарезом до 4 баллов в верхних и нижних конечностях, нарушением чувствительности по спинально-проводниковому типу с уровня С2 сегментов с обеих сторон.
На компьютерных томограммах верхнешейного отдела позвоночника, выполненных в предоперационном периоде, отмечаются значительные остеолитические вторичные изменения в структурах С2 позвонка с формированием обширного мягкотканого компонента, деформирующего заднюю стенку глотки с распространением патологической ткани в просвет позвоночного канала и компрессией твердой мозговой оболочки (рис. 1).
Учитывая массивную зону опухолевой деструкции костно-связочного аппарата верхнешейного отдела позвоночника с вовлечением в неопластический процесс передней дуги атланта, тела и зуба С2 позвонка, а также паравертебральных тканей, было принято решение об одномоментном двухэтапном хирургическом лечении: первым этапом выполнен окципитоспондилодез полисегментарной системой; вторым — удаление опухоли С2 позвонка из расширенного трансмандибулярного циркумглоссально-ре-трофарингеального доступа.
Полисегментарный окципитоспондилодез с трансфасеточной фиксацией полиаксиальными винтами осуществляли в положении пациента на животе в условиях жесткой трехточечной фиксации шейного отдела позвоночника в скобе Mayfield-Kees (рис. 2).
Второй этап хирургического вмешательства проводили с участием челюстно-лицевого хирурга. Предоперационную разметку трансмандибулярного циркумглоссально-ретрофарингеального доступа проводили по методике, предложенной DeMonte F. и соавт. (2001) (рис. 3).
Техника хирургического вмешательства представлена следующим образом: после установки назога-
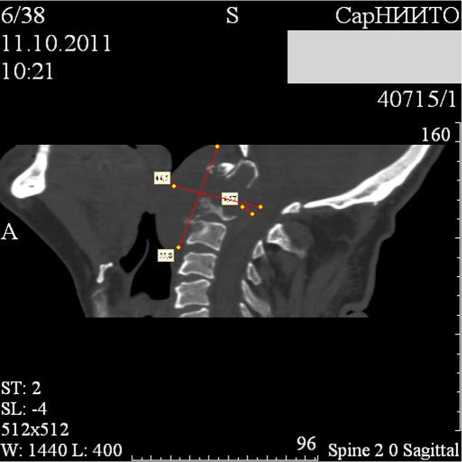
Рис. 1. Остеолитические изменения в структурах С2 позвонка с мягкотканым компонентом, деформирующим заднюю стенку глотки
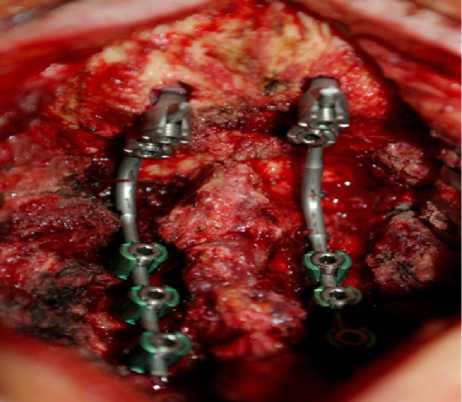
Рис. 2. Окципитоспондилодез полисегментарной конструкцией
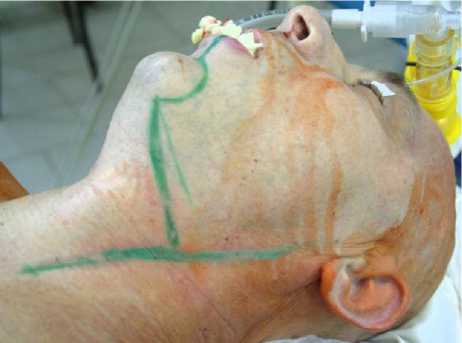
Рис. 3. Предоперационная разметка разреза мягких тканей при осуществлении хирургического доступа по методике DeMonte F. и соавт. (2001)
стрального зонда в положении пациента на спине производили разрез кожи и подкожно-жировой клетчатки по переднему краю грудино-ключично-сосцевидной мышцы от угла нижней челюсти и до уровня перстневидного хряща. Производили мягкотканую диссекцию с обнажением влагалища грудино-ключично-сосцевидной мышцы и пересечением левой лопаточно-подъязычной мышцы, мобилизовывали сосудисто-нервный пучок в сонном и лопаточно-трахеальном треугольниках шеи. Далее разрез продлевали вверх до уровня поднижнечелюстного треугольника, а также вокруг левой полуокружности подбородка на середину нижней губы, осуществляли мобилизацию поднижнечелюстного футляра с поднижнечелюстной железой. По возможности на всем протяжении мобилизовывали ствол левого подъязычного нерва, лигировали общую лицевую вену и лицевую артерию. Для создания более широкого хирургического подхода к срединным образованиям шеи производили диссекцию мышц от подъязычной кости (заднее брюшко двубрюшной мышцы, шило-подъязычную мышцу).
Следующим этапом операции выполняли срединную ступенчатую остеотомию тела нижней челюсти с предварительным наложением титановых мини-пластин для облегчения последующего сопоставления рассеченных фрагментов нижней челюсти. После медианного разъединения фрагментов тела нижней челюсти приступали к внутриротовому этапу вмешательства, а именно препарированию структур дна полости рта. Осуществляли инцизию в месте перехода слизистой оболочки дна рта в слизистую языка, а далее разрез продолжали по внутренней поверхности крыловидно-челюстной складки до бугра верхней челюсти. Выделяли язычный нерв, после чего рассекали мышцы дна полости рта. Отводили единый костно-мягкотканый лоскут нижней трети лица кверху, что позволяло создать оптимальный обзор всей площади хирургического вмешательства с оптимальным углом операционного действия. Срединно расположенные висцеральные структуры шеи смещали от вентральной поверхности шейного отдела позвоночника в медиальную сторону, внутреннюю сонную артерию и внутреннюю яремную вену мобилизовывали вплоть до наружного основания черепа, а именно до входа в наружное отверстие сонного канала и яремное отверстие соответственно. После мобилизации вентральной поверхности шейного отдела позвоночника под оптическим увеличением производили дискэктомию на уровне С2-С3 позвонков до задней продольной связки. Опухоль на уровне С1-С2 позвонков удаляли единым блоком, в том числе с использованием высокотехнологичных моторных систем, предназначенных для резекции костных структур (высокооборотный бор, костный дезинтегратор). С целью повышения абластичности вмешательства производили иссечение задней продольной связки на уровне С1-С2 позвонков вплоть до интактной твердой мозговой оболочки (рис. 4).
Для повышения радикальности вмешательства производили максимальное удаление эпидуральной клетчатки вместе с эпидуральными венами. В случае повреждения твердой мозговой оболочки выполняли ушивание ее дефекта, с дополнительной пластикой медицинским клеем для профилактики ликвореи, а также уменьшения риска развития имплантационных метастазов по ликворной системе. После завершения основного этапа вмешательства выполняли дренирование зоны оперативного вмешательства,
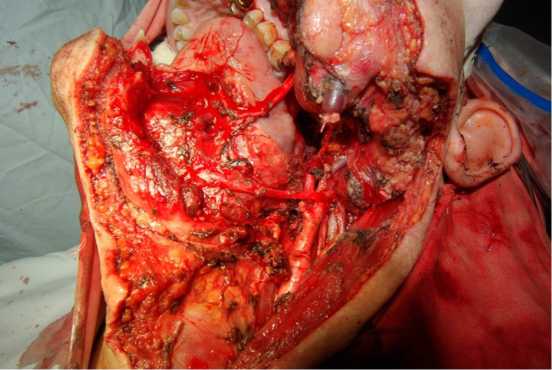
Рис. 4. Трансмандибулярный паралингвальный ретрофарин-геальный доступ к верхнешейному отделу позвоночника по методике DeMonte F. и соавт. (2001)
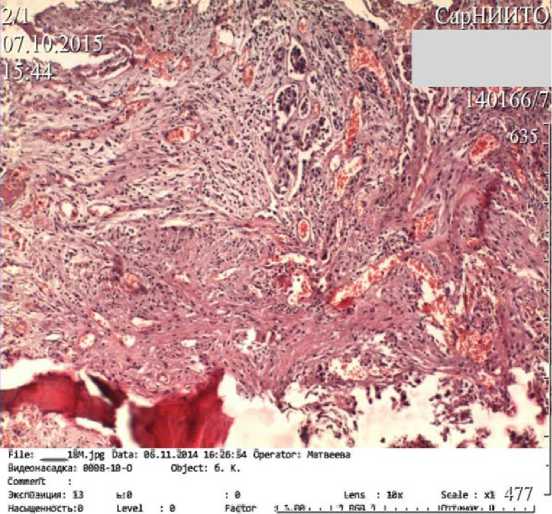
Рис. 5. Гистологическая картина операционного материала остеосинтез нижней челюсти микропластинами, послойное ушивание мягких тканей.
Операционный материал был отправлен на гистологическое исследование: среди фиброзной стромы с большим количеством полнокровных сосудов, воспалением и некрозами отмечены комплексы опухолевых клеток вытянутой формы, напоминающие переходный эпителий с формированием сосочковых структур, что свидетельствовало о метастазе рака мочевого пузыря (рис. 5).
Послеоперационный период протекал без осложнений, оценка по шкале Karnovsky 80 баллов, отмечен полный регресс двигательных и чувствительных расстройств, зона гипестезии по корешковому типу была сохранена на дооперационном уровне. После удаления назогастрального зонда отмечен регресс дисфагии. Швы в зонах дорсального и вентрального доступов были сняты на 14-е сутки, натяжение первичное. В качестве медикаментозной терапии, проводимой в послеоперационном периоде, применяли нестероидные противовоспалительные препараты и антибиотики широкого спектра действия в профилактических дозировках на срок не более 5 дней.
На 15-е сутки после хирургического вмешательства пациент был выписан из нейрохирургического стационара и представлен на онкологический консилиум для решения вопроса о дальнейшем проведении адъювантной терапии.
Обсуждение . Согласно данным [10], тактика одномоментного двухэтапного хирургического лечения позволяет осуществить радикальное хирургическое вмешательство в одну хирургическую сессию с привлечением смежных специалистов. Расширенный трансмандибулярный-циркумглоссальный-ретро-фарингеальный доступ позволил нам осуществить оптимальный обзор верхних отделов пара- и ретро-фарингеального пространств, а также области носоглотки, что создало адекватный угол операционного действия в этих труднодоступных анатомических зонах, необходимый для осуществления полноценной диссекции магистральных сосудов шеи и важных в функциональном отношении нервных стволов. Это дает возможность радикально удалить патологический очаг в структурах С1-С2 позвонков с учетом принципов абластики.
Заключение. Мультидисциплинарный подход в случае хирургического лечения пациентов с вторичными злокачественными опухолями области верхнешейного отдела позвоночника и краниовертебрального перехода позволяет радикально и с наименьшим риском развития неврологического дефицита в послеоперационном периоде удалить опухоль из подобных труднодоступных топографо-анатомических зон.
Список литературы Тактика хирургического лечения при метастатическом поражении верхнешейного отдела позвоночника
- Кушель Ю.В. Анатомо-хирургическое обоснование трансмандибулярного ретрофарингеального и трансцервикального ретрофарингеального доступов к основанию черепа: дис.... канд. мед. наук. М., 1999; 163 с.
- DeMonte F, Diaz Е, Callender D, et al. Transmandibular, circumglossal, retropharyngeal approach far chordomas of the clivus and upper cervical spine. Neurosurg focus 2001; 10 (3), Article 10: 1
- La Corte E., Aldana PR. Endoscopic approach to the upper cervical spine and clivus: an anatomical study of the upperlimits of the transoral corridor. Acta Neurochir (Wien) 2017 Apr; 159(4) 633-9. DOI: 10.1007/S00701-017-3103-6
- Hutchinson IL. The hazard of mandibulotomy in an irradiated field. Oral Dis 1997; 3 (2): 64
- Infante-Cossio P, Torres-Carranza E, Cayuela A, et al. Impact of treatment on quality of life for oral and oropharyngeal carcinoma. Int j oral maxillofac surg 2009; 38: 1052-8
- Infante-Cossio P, Torres-Carranza E, Cayuela A. Quality of life in patients with oral and oropharyngeal cancer. Int j oral maxillofac surg 2009; 38: 250-5
- Jalil MFA, Story RD, Rogers M. Extended maxillotomy for skull base access in contemporary management of chordomas: Rationale and technical aspect. Journal of clinical neuroscience 2017; (39): 212-5. DOI: 10.1016/j.jocn.2017.01.031
- James D, Crockard HA. Surgical access to the base of the skull and upper cervical spine by extended maxillotomy. Neurosurgery 1999; 29: 411-6
- Janecka IP, Sekhar L, Jones N, et al. Treatment of cancer of the skull base. In: Fee W, Goepfert H, Johns M, eds.Head neck cancer. New York: ВС Decker, 1990; p. 382-4
- Valentini V, Cassoni A, Battisti A, Gennaro P, lannetti G. Transmandibular Approaches. In: Cranial, craniofacial and skull base surgery. New York: Springer, 2010; 319-29. DOI: 10.1007/978-88-470-1167-0_24


