Теоретическое исследование адсорбции лития на поверхности BCN-нанотрубки
Автор: Абросимова А.А.
Журнал: Международный журнал гуманитарных и естественных наук @intjournal
Рубрика: Физико-математические науки
Статья в выпуске: 5-2 (104), 2025 года.
Бесплатный доступ
В данной работе представлено теоретическое исследование адсорбции атомов лития на поверхности бор-углерод-нитридных (BCN) нанотрубок с использованием теории функционала плотности (DFT) на уровне теории B3LYP/6-31G. Целью исследования было изучение особенностей адсорбции атома лития на поверхности BCN-нанотрубок, включая определение оптимальных положений адсорбции и энергии адсорбции. Результаты показывают, что адсорбция атома лития наиболее энергетически выгодна в положение над атомом азота, при этом происходит частичный перенос заряда от атомов лития к BCN-нанотрубке. Также наблюдается изменение ширины запрещённой зоны. Полученные данные свидетельствуют о возможности использования BCN-нанотрубок в качестве перспективных материалов для анодов литий-ионных аккумуляторов.
BCN-нанотрубкa, адсорбция атома лития, ширина запрещенной зоны, зарядовое распределение, литий-ионные аккумуляторы
Короткий адрес: https://sciup.org/170209343
IDR: 170209343 | DOI: 10.24412/2500-1000-2025-5-2-79-84
Theoretical study of lithium adsorption on the surface of a bcn nanotube
This paper presents a theoretical study of the adsorption of lithium atoms on the surface of boron-carbon-nitride (BCN) nanotubes using density functional theory (DFT) at the level of theory B3LYP/6-31G. The aim of the study was to study the features of lithium atom adsorption on the surface of BCN nanotubes, including determining the optimal adsorption positions and adsorption energy. The results show that the adsorption of the lithium atom is most energetically advantageous to the position above the nitrogen atom, while a partial charge transfer occurs from the lithium atoms to the BCN nanotube. There is also a change in the band gap width. The data obtained indicate the possibility of using BCN nanotubes as promising materials for lithium-ion battery anodes.
Текст научной статьи Теоретическое исследование адсорбции лития на поверхности BCN-нанотрубки
В настоящее время одной из главных задач в области разработки источников тока является создание анодов литий-ионных аккумуляторов из-за их повсеместного применения в электронике. Основным материалом для анода в таких батареях является графит, однако в данный момент продолжаются поиски новых материалов, позволяющих сократить время зарядки и продлить срок службы батареи [1]. Следует отметить особую важность развития данной области техники для инфокоммуника-ционных технологий, поскольку для работы многих автономных устройств, участвующих в обработке информации, в качестве источника питания используются в именно литий-ионные аккумуляторы.
Уникальные характеристики углеродных нанотрубок (УНТ) открыли новые возможности для их использования в электронных устройствах. На сегодняшний день экспериментально было установлено, что на внешней поверхности нанотрубок могут адсорбироваться атомные и молекулярные системы различной химической природы, начиная от отдельных атомов и заканчивая сложными органическими молекулами и даже простейшими биологическими системами, такими как вирусы. Теоретические оценки также указывают, что даже незначительное количество адсорбируемого вещества на поверхности
УНТ могут значительно изменить свойства создаваемого комплекса [2]. Таким образом, путем функционализации поверхности возможно управление свойствами УНТ.
Свойства УНТ с добавлением лития были предметом интенсивного изучения в последние десять лет. Было установлено, что УНТ способны накапливать в своей внутренней полости больше атомов лития по сравнению с обычным графитом [3-7]. Повышенная концентрация лития, достигаемая в УНТ, потенциально позволяет увеличить ёмкость перезаряжаемых литий-ионных аккумуляторов [8]. Имеет место множество экспериментальных исследований [9-11], в которых были определены характеристики адсорбции лития в нанотрубках. Теоретические исследования сосредоточились на процессе внедрения лития в многостенные углеродные нанотрубки. В нескольких научных работах [12-14] была изучена энергия связи лития с нанотрубками различных диаметров и хиральности, при этом использовались методы ab-initio. Эти исследования выявили некоторые общие закономерности взаимодействия лития и нанотрубок: энергии адсорбции для одного атома лития как внутри, так и снаружи трубки, почти одинаковы. Наблюдается практически полное перемещение заряда от лития к стенкам трубки. Барьер диффузии лития внутри нанотру- бок небольшой, порядка 100 мэВ, что способствует достаточно высокой скорости данного процесса. Рассмотрено множество различных положений атомов Li внутри УНТ. Энергии для разных конфигураций могут прямо зависеть от особенностей взаимодействия как Li-УНТ, так и Li-Li, что существенно зависит от положения лития относительно углеродного каркаса. Детальное исследование демонстрирует, что согласованная диффузия множества ионов Li происходит более эффективно, чем несогласованное движение отдельных ионов.
Целью настоящей работы было исследование адсорбции атома Li на поверхностиBCN-нанотрубки и оценка влияния подобной процедуры на свойства наноматериала.
Квантово-химическое моделирование проводилась методами теории функционала плотности на уровне теории B3LYP/6-31G. Предварительно был построен молекулярный кластер BCN-нанотрубки типа «кресло» с индексами хиральности (6,6) (рис. 1). Оборванные химические связи на границах нанотруб- ки компенсировались путем их насыщения псевдоатомами водорода. Было рассмотрено три положения адсорбции атома лития на поверхности BCN-нанотрубки: 1) над атомом бора, 2) над атомом углерода, 3) над атомом азота. В рассматриваемых положениях адсорбции производилось пошаговое приближение атома лития, причем на каждом шаге приближения фиксировалась потенциальная энергия системы и расстояние между атомом лития и атомом нанотрубки, к которому производилось приближение в конкретном случае. Для оценки изменения зарядового распределения в результате адсорбции атома лития были рассчитаны парциальные атомные заряды по схеме Малликена [15]. Ширина запрещенной зоны определялась как разность между энергией нижней вакантной молекулярной орбитали (НВМО) и энергией верхней заполненной молекулярной орбитали (ВЗМО).Для получения одноэлектронных спектров и плотностей состояний использовалась программа GaussSum [16].
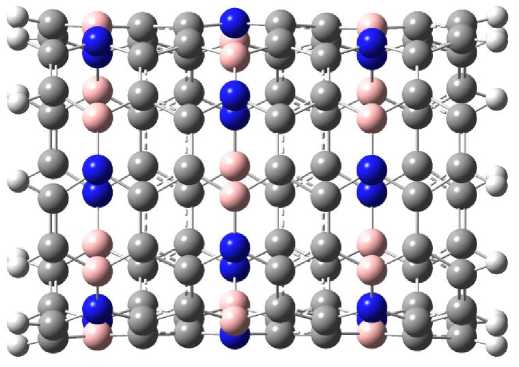
Рис. 1. Молекулярный кластер BCN-нанотрубки с геометрией типа «кресло» с индексами хиральности (6,6).
По полученным профилям поверхности потенциальной энергии (рис. 2) удалось установить, что адсорбция возможна в любое из рассмотренных положений, поскольку в каждом случае наблюдается минимум потенциальной энергии. Для положения адсорбции над атомом азота наблюдается самый глубокий минимум потенциальной энергии, соответственно, в этом случае достигается наиболее энергетически выгодная конфигурации адсорбционного комплекса, расстояние адсорбции при этом составляет 1,9 Å, энергия адсорбции составляет 0,61 эВ. При адсорбции в положение над атомом углерода расстояние адсорбции составляет 2,0 Å, энергия адсорбции составля-ет0,48 эВ. Наименее энергетически выгодна адсорбция в положение над атомом бора: расстояние адсорбции в этом случае составляет 2,1 Å, а энергия адсорбции – 0,47 эВ. С учетом значений расстояния и энергии адсорбции, можно говорить о том, что адсорбция носит химический характер.
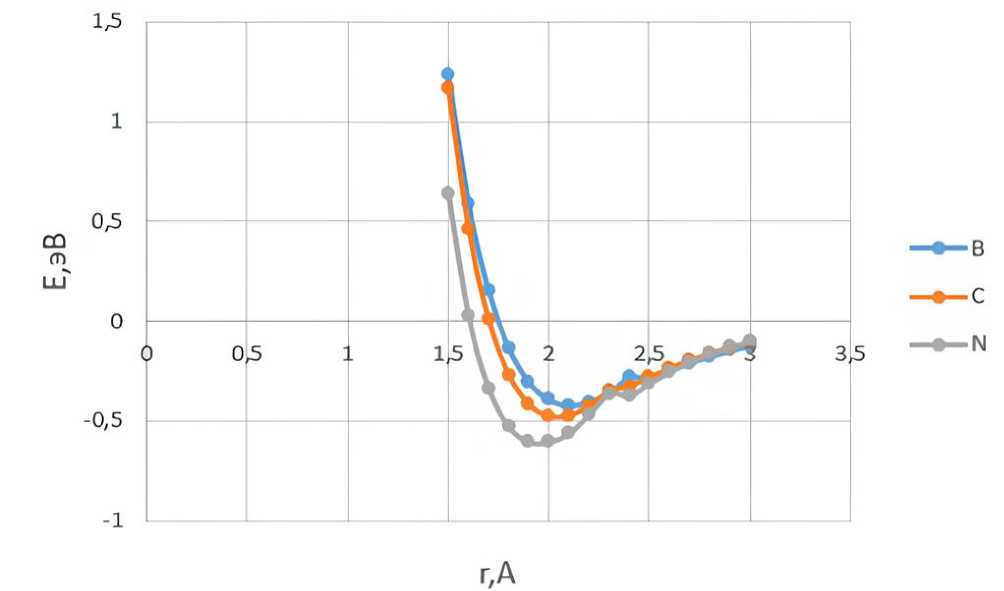
Рис. 2. Профиль поверхности потенциальной энергии процесса присоединения атома лития к поверхности BCN-нанотрубки в положения адсорбции над атомом углерода, бора, азота; пошаговое приближение атома лития производилось перпендикулярно к поверхности нанотрубки
Адсорбция атома лития влияет на электронную структуру BCN-нанотрубки, что проявляется, в частности, в изменении ширины запрещённой зоны. Отметим, что исходная BCN-нанотрубка характеризовалась шириной запрещенной зоны, равной 1,15 эВ. Полученные для адсорбционных комплексов значения данного показателя (табл. 1) свидетельствуют об уменьшении ширины запрещенной зоны в каждом из рассмотренных случаев. Причем наиболее выражена эта тенденция для случая адсорбции над атомом углерода: в этом случае ширина запрещенной зоны уменьшилась на 33% по сравнению с исходной структурой. Таким образом, была установлена возможность управления шириной запрещенной зоны посредством поверхностного модифицирования BCN-нанотрубки атомом лития, что может быть полезно для практических приложений.
Таблица 1. Значения ширины запрещенной зоны ∆Еg для адсорбционных комплексов BCN- нанотрубки с атомом лития
|
Положение адсорбции |
Над атомом бора |
Над атомом углерода |
Над атомом азота |
|
∆Е g , эВ |
0,90 |
0,77 |
0,79 |
Адсорбция атома лития на поверхности BCN-нанотрубки сопровождается выраженным переносом заряда от атома лития к атомам бора, углерода или азота, в зависимости от положения адсорбции, что является еще одним свидетельством образования химической связи. Атом лития выступает в роли донора электронной плотности, а, соответственно, приобретает положительный заряд: значения данной величины составляют 0,63, 0,65 и 0,66 для положений адсорбции над атомом углерода, азота и бора соответственно. Атомы, над которыми произошла адсорбция, приобретают отрицательные заряды. При этом наименьшее значение заряда наблюдается на атоме азота, и значение этой величины составляет -0,93. Наибольшее же значение заряда из рассмотренных случаев имеет атом бора, заряд на нем составляет -0,05. На атоме углерода значение заряда равно -0,20. Подобный разброс значений можно объяснить тем, что в исходной BCN-нанотрубке заряды на атомах бора, углерода и азота различны: атомы изначально имеют достаточно большой положительный заряд, атомы азота – большой по модулю отрицательный заряд, атомы углерода в этом смысле занимают промежуточное положение.
Также в ходе исследования были получены одноэлектронные спектры и плотности состояний (рис. 3). Их анализ позволил определить, что значения энергии как НВМО, так и ВЗМО, увеличиваются для адсорбционных комплексов по сравнению с исходной BCN-нанотрубкой. Большее по абсолютному значению увеличение энергии ВЗМО по сравнению с увеличением энергии НВМО и определяет итоговое уменьшение ширины запрещенной зоны.
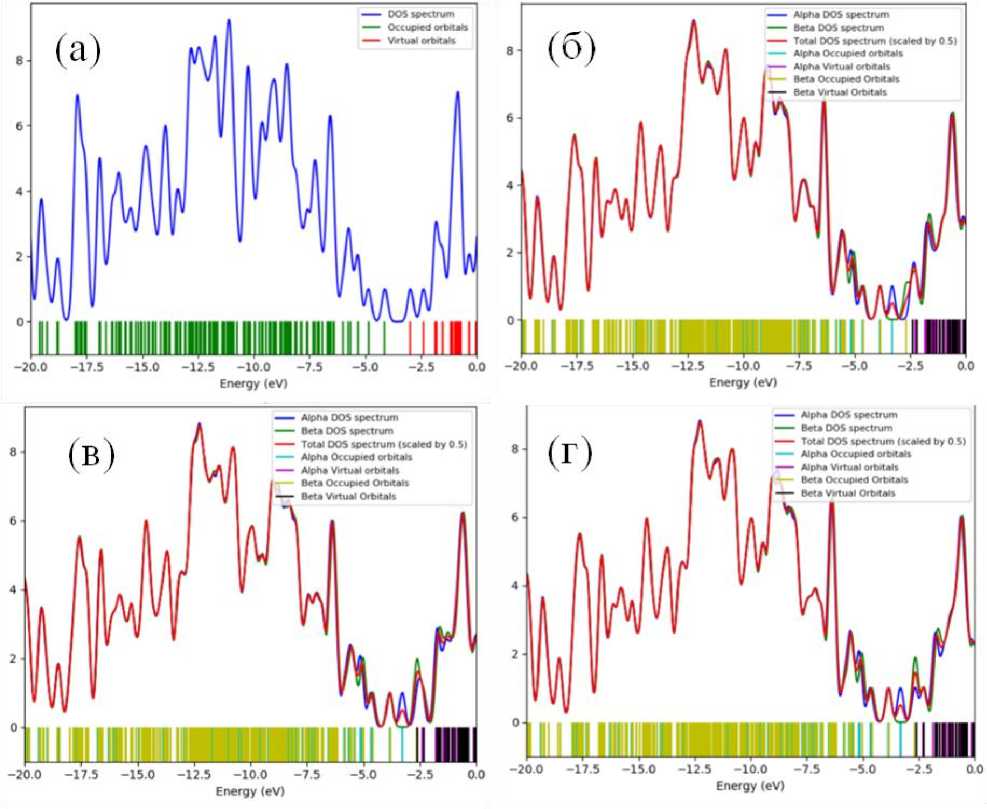
Рис. 3. Одноэлектронные спектры и плотности состояний для исходной BCN-нанотрубки (а) и адсорбционных комплексов при положениях адсорбции над атомом бора (б), углерода (в), азота (г).
Вывод
В ходе настоящей работы было проведено квантово-химическое моделирование адсорбции атома лития на поверхности BCN-нанотрубки для различных положений адсорбции, определены оптимальные геометрии адсорбционных комплексов, оценено влияние подобного модифицирования на электронноэнергетическую структуру и зарядовое распределение. Было установлено, что наиболее энергетически выгодным положением адсорбции является положение над атомом азота, наименее выгодным – над атомом бора. Во всех рассмотренных случаях ширина запрещенной зоны уменьшалась в результате адсорбции. Удалось добиться снижения данного показателя на 33% по сравнению с исходной структурой. Было обнаружено, что вне зависимости от положения адсорбции электронная плотность смещается с атома лития на атомы
BCN-нанотрубки, при этом атом лития приобретает положительный, а атомы нанотрубки, над которыми происходит адсорбция, – отрицательный заряд.
Полученные в работе результаты проливают свет на механизмы формирования компо- зитов на основе BCN-нанотрубок и лития, поэтому они могут быть чрезвычайно полезны для создания новых материалов для электродов Li-ионных аккумуляторов, а также в устройствах наноэлектроники.


