Теоретическое исследование сорбции водорода в интерметаллических соединениях Al 3Ti, Al 3Ni и Al 4Pd
Автор: Куклин А.В., Елисеева Н.С., Кузубов А.А., Краснов П.О., Сержантова М.В.
Журнал: Сибирский аэрокосмический журнал @vestnik-sibsau
Рубрика: Технологические процессы и материалы
Статья в выпуске: 3 (49), 2013 года.
Бесплатный доступ
Представлено теоретическое исследование интерметаллидов Al 3Ti, Al 3Ni и Al 4Pd как потенциальных материалов, которые могут образовываться при синтезе тонких пленок титана, никеля и палладия на поверхности алюминия. При помощи теории функционала плотности изучена возможность образования гидридов данных соединений.
Водородная энергетика, сорбция водорода, теория функционала плотности (dft)
Короткий адрес: https://sciup.org/148177108
IDR: 148177108 | УДК: 544.18
Theoretical study of hydrogen sorption in intermetallic compounds Al 3Ti, Al 3Ni and Al 4Pd
Aluminium is one of the most promising materials for hydrogen storage with high volumetric density. Furthermore, the excellent kinetics of hydrogenation and dehydrogenation can be achieved with surface modification of some transition metals. The possibility of hydrogen usage at the Al 3Ti, Al 3Ni and Al 4Pd phases, which can be obtained by high-temperature synthesis, was investigated by density functional calculations.
Текст научной статьи Теоретическое исследование сорбции водорода в интерметаллических соединениях Al 3Ti, Al 3Ni и Al 4Pd
Водород, как высокоэффективный, возобновляемый и экологически чистый энергоноситель, имеет большие перспективы для широкого использования в энергетике, особенно как топлива для транспортных средств [1; 2].
Наиболее перспективным методом считается хранение водорода в абсорбированном состоянии. Гидриды металлов, такие как MgH2, AlH3, NaAlH4, LiH и другие, с разной степенью эффективности, могут быть использованы в качестве носителя для водорода, часто обратимо. Перспективным металлом для хранения водорода является алюминий ввиду низкой стои- мости, малой молярной массы, доступности и не токсичности.
Одной из проблем использования данного материала в качестве аккумулятора водорода является плохая кинетика реакции сорбции / десорбции. Причина медленной абсорбции водорода связана с высокой окислительной чувствительностью и затрудненностью диссоциации молекул водорода на поверхности, предшествующей диффузии внутрь. Улучшение кинетики реакции может быть достигнуто путем уменьшения размера частиц и модифицированием переходными металлами [3–5].
В обычных условиях гидрид алюминия (алан) имеет полимерную молекулярную структуру (AlH 3 ) n , при этом его кристаллическая форма существует в семи полиморфных модификациях: α-(AlH3)n, α1-(AlH 3 ) n , β-(AlH 3 ) n , δ-(AlH 3 ) n , ε-(AlH 3 ) n , γ-(AlH 3 ) n , ζ-(AlH 3 ) n [6]. Самой устойчивой является модификация α-(AlH3)n, имеющая гексагональную сингонию (пространственная группа R3c, а = 4,449 Å, b = 4,449 Å, c = 11,804 Å) [7; 8].
Авторами работы [9] показано, что размол AlH3 в шаровой мельнице приводит к увеличению скорости десорбции водорода, вероятно, из-за увеличения свободной от оксида поверхности. В работах [10–13] показано, что допирование алюминия переходными металлами, такими как никель и титан, улучшает кинетику реакции и способствует хемосорбции водорода. Замещение алюминия титаном кинетически стабильно при комнатной температуре. В этом случае титан преимущественно располагается в поверхностном и приповерхностном слое. Размещение титана в поверхностном слое располагает к образованию парных комплексов, которые улучшают диссоциацию водорода [13]. Сочетая поверхностную ИК-спектроскопию и теорию функционала плотности, авторами работы [10] показано, что добавление титана приводит к снижению образования больших аланов, за счет уменьшения мобильности водорода и захвата малых аланов. Титан тем самым препятствует олигомеризации. Добавление титана также резко понижает температуру десорбции с 290 до 190 К. Контролируя размещение титана, можно дополнительно снизить барьеры активации распада молекул водорода, а также улучшить диффузию водорода в объем [14].
Однако в данной области исследований остается много открытых вопросов. В частности, неясно какие процессы происходят при более высоких температурах, которые требуются для протекания абсорбции водорода.
Предположительно, при добавлении к алюминию небольшого количества титана, никеля или палладия и их совместном нагревании, будут образовываться соединения вида Al3Ti, Al3Ni и Al4Pd. Исходя из этого, целесообразно изучить поведение водорода в данных системах. Таким образом, целью работы являлось квантово-химическое исследование сорбции водорода в интерметаллических соединениях Al 3 Ti, Al 3 Ni и Al 4 Pd.
Моделирование исследуемых объектов проводили с использованием квантово-химического пакета VASP (Vienna Ab-initio Simulation Package) [15–18] в рамках формализма функционала плотности (DFT) [19, 20], основанного на градиентном приближении (GGA). В расчетах применяли обменно-корреляционный потенциал PBE (Perdew-Burke-Ernzerhof) [21] и метод PAW (projector augmented-wave) [22].
Для изучения сорбции водорода в интерметалли-дах, на начальном этапе работы были смоделированы элементарные ячейки Al 3 Ti, Al 3 Ni и Al 4 Pd с пространственными группами симметрии I4/mmm, Pnma и P3c1 соответственно. Обратное пространство в первой зоне Брюллюэна автоматически разбивалось на сетку по схеме Монхорста-Пака [23]. Количество k -точек вдоль каждого из направлений для Al 3 Ti, Al 3 Ni и Al 4 Pd составляло 8 × 8 × 6, 12 × 12 × 12 и 2 × 2 × 3 соответственно. При моделировании всех исследуемых структур оптимизация геометрии проводилась до значения максимальных сил, действующих на атомы, равных 0,01 эВ/Ǻ.
Получившиеся геометрии элементарных ячеек хорошо согласуются с экспериментальными данными (табл. 1).
Далее суперячейки всех интерметаллидов (3 × 3 × 2 для Al3Ti, 2 × 2 × 2 для Al3Ni и 1 × 1 × 2 для Al4Pd) были получены путем трансляции элементарной ячейки вдоль каждого из направлений.
Для определения наиболее выгодных позиций атома водорода в объеме интерметаллидов были рассчитаны структуры с различным его расположением (рис. 1, 2, 3). При расчете структуры суперячеек количество k -точек вдоль каждого из направлений составляло 3 × 3 × 3 для Al 3 Ti, 2 × 2 × 2 для Al 3 Ni и для Al 4 Pd.
Энергию связи между атомом водорода и супер-ячейкой для всех итерметаллидов рассчитывали по формуле:
, (1) где – полная энергия суперячейки с атомом водорода; – энергия суперячейки; – энергия, приходящаяся на один атом водорода в молекуле водорода.
Во всех интерметаллидах и для всех положений, энергии связи атома водорода со структурой супер-ячейки оказались положительными (табл. 2–4).
Сравнение рассчитанных и экспериментальных параметров решетки
(А)
Таблица 1
|
Параметр |
Al 3 Ti |
Al 3 Ni |
Al 4 Pd |
|||
|
DFT |
X-Ray [24] |
DFT |
X-Ray[25] |
DFT |
X-Ray[26] |
|
|
a |
3,8120 |
3,8537 |
6,5414 |
6,6114 |
13,010 |
13,086 |
|
b |
3,8120 |
3,8537 |
7,3271 |
7,3662 |
13,010 |
13,086 |
|
c |
8,6250 |
8,5839 |
4,7525 |
4,8112 |
9,674 |
9,633 |
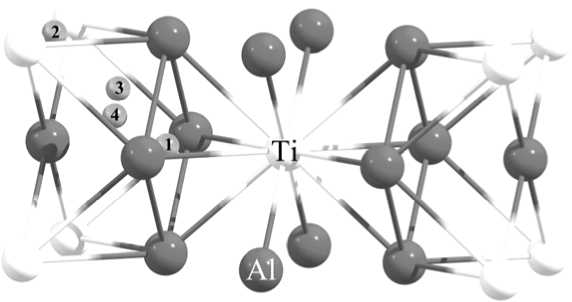
Рис. 1. Расположения атома водорода в структуре Al3Ti
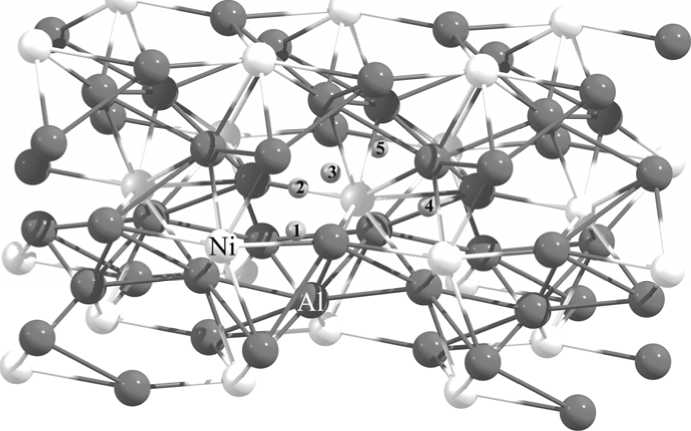
Рис. 2. Расположения атома водорода в структуре Al3Ni
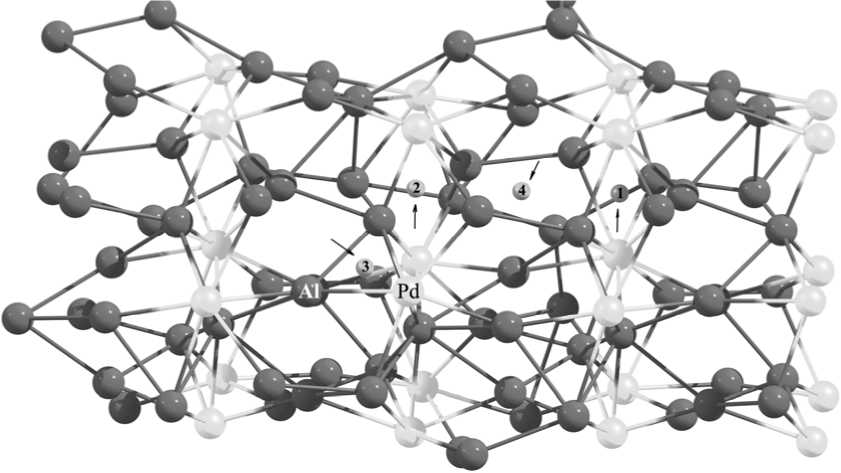
Рис. 3. Расположения атома водорода в структуре Al4Pd
Таблица 2
Энергии образования суперячейки Al3Ti с атомом водорода
|
Расположение атома водорода |
Энергия, eV |
|
1 |
0.0353 |
|
2 |
0.2441 |
|
3 |
0.2986 |
|
4 |
0.2972 |
Таблица 3
Энергии образования суперячейки Al3Ni с атомом водорода
|
Расположение атома водорода |
Энергия, eV |
|
1 |
1.0373 |
|
2 |
1.0380 |
|
3 |
0.1016 |
|
4 |
1.0024 |
|
5 |
1.2352 |
Таблица 4
Энергии образования суперячейки Al4Pd с атомом водорода
|
Расположение атома водорода |
Энергия, eV |
|
1 |
1.4190 |
|
2 |
1.4407 |
|
3 |
1.4310 |
|
4 |
0.8441 |
Исходя из данных таблиц, можно сделать вывод, что при нормальных условиях водороду несвойственно содержаться в данных соединениях. Эти теоретические выводы согласуются с экспериментальными данными работы [27], в которой проводилось исследование сорбции водорода в фазе Al3Ti при высокой температуре и высоком давлении. Авторы отмечают, что при 10 GPa и 898 K формируется гидрид с примерным составом Al 3 TiH x , где x = 0,4. Тем не менее, при понижении давления происходит дегидрирование и данная фаза гидрида не может быть восстановлена в условиях окружающей среды.
Таким образом, при высокотемпературном синтезе тонких пленок титана, никеля или палладия на границах взаимодействия металлов будут образовываться фазы состава Al 3 Ti, Al 3 Ni и Al 4 Pd, которые будут мешать протеканию гидрирования.


