Терапевтическая эффективность модифицированных гидроксикислотами сорбентов при отравлении животных ивермектином в условиях эксперимента
Автор: Дорожкин В.И., Федоров Ю.Н., Герунова Л.К., Пьянова Л.Г., Герунов Т.В., Делягина М.С., Тарасенко А.А.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Ветеринарная медицина
Статья в выпуске: 2 т.55, 2020 года.
Бесплатный доступ
Разработка модифицированных сорбентов, сочетающих адсорбционные свойства исходного пористого материала и биологическую активность используемых модификаторов, актуальна для сорбционной терапии. В частности, продолжаются активные поиски химических модификаторов, не обладающих выраженной токсичностью, совместимых с тканями организма и способных подвергаться биодеструкции. В настоящей работе на модельном объекте нами впервые доказана целесообразность проведения энтеросорбции при остром отравлении ивермектином с использованием нового углеродного сорбента, модифицированного молочной кислотой. Экспериментально обоснованы преимущества предложенного модификатора по сравнению с гликолевой кислотой и сополимером указанных гидроксикислот. Цель исследования - разработать способ модифицирования гидроксикислотами углеродных сорбентов и провести сравнительную оценку их терапевтической эффективности при отравлении животных ивермектином. Матрицей для получения биоспецифических сорбентов служил гранулированный углеродный энтеросорбент с удельной площадью поверхности 300-400 м2/г, модификаторами - гликолевая (50 мас.%, «Merk Schuchardt OHG», Германия), молочная (80 мас.%, «МОСРЕАКТИВ», Россия) кислоты и их сополимер. Для изучения морфологии и рельефа поверхности полученных образцов использовали метод растровой электронной микроскопии (JSM 6460LV, «JEOL Ltd», Япония). Терапевтическую эффективность модифицированных сорбентов оценивали на 5 группах (по 10 особей в каждой) беспородных половозрелых белых крыс с массой тела 180-200 г. Животные разных групп получали в течение 5 сут по одному из модифицированных сорбентов (0,3 г/кг живой массы) на фоне острой интоксикации Баймеком® (1 % раствор ивермектина, производитель ФГБУ Федеральный центр охраны здоровья животных, Россия; разработчик «Bayer Animal Health GmbH», Германия). Контролем служили интактные и интоксицированные животные. По окончании эксперимента у всех животных брали кровь для биохимического исследования, а также проводили гистоисследование органов и тканей. Электронная микроскопия показала, что при модифицировании исходного сорбента размер и форма гранул сохраняются, но рельеф и морфология поверхности изменяются, модификаторы распределяются локально в виде мелких полимерных частиц (олигомер гликолевой кислоты, сополимер) или полимерной пленки (олигомер молочной кислоты). Результаты экспериментов in vivo выявили неодинаковую эффективность энтеросорбции с применением модифицированных сорбентов при острой интоксикации крыс содержащим ивермектин препаратом Баймек® (креатинин - от 40,86±0,66 мкмоль/л, р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Ивермектин, баймек®, модифицированные энтеросорбенты, гидроксикислоты, молочная кислота, гликолевая кислота, клиническая патология, биохимические показатели крови, гистопатология, интоксикация, сорбцинная терапия
Короткий адрес: https://sciup.org/142226304
IDR: 142226304 | УДК: 619:57.084.1:615.9:615.279 | DOI: 10.15389/agrobiology.2020.2.394rus
Therapeutic efficiency of sorbents modified by hydroxic acids during animal experimental poisoning with ivermectin
The development of modified sorbents combining the adsorption properties of the initial porous material and the biological activity of the modifiers is a сurrent issue of sorption therapy. The purpose of the study was to develop a method for modifying carbon sorbents with hydroxyacids and to conduct a comparative assessment of their effectiveness upon poisoning animals with ivermectin. A granular carbon enterosorbent with a specific surface area of 300-400 m2/g was the matrix for the preparation of biospecific sorbents, glycolic acid (50 wt.%, manufactured by Merk Schuchardt OHG, Germany) and lactic acid (80 wt.%, produced by MOSREACTIVE, Russia) and a copolymer thereof were used as modifiers. To study the morphology and surface topography of the obtained samples, scanning electron microscopy (JSM 6460LV, JEOL Ltd, Japan) was used. The therapeutic efficacy of the modified sorbents was measured in 5 groups (10 animals each) of outbred adult white rats weighing 180-200 g. During 5 days animals of different groups received one of the modified sorbents in doses of 0.3 g/kg upon acute intoxication with Baymec® (1 % solution of ivermectin, Bayer Animal Health GmbH, Germany; manufactured by Federal Centre for Animal Health, Russia). The controls were intact and intoxicated animals. At the end of the experiment, blood was taken from all animals for biochemical studies, as well as histological examination of organs and tissues was performed post mortem. Electron microscopic examination showed that upon modification, the size and shape of the granules of the initial sorbent are preserved, but surface topography and morphology change. The results of in vivo experiments showed varying degrees of efficiency of enterosorption in rats when modified sorbents were applied to the animals intoxicated with ivermectin-containing Baymec® preparation. Creatinine varied from 40.86±0.66 μmol/l (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Терапевтическая эффективность модифицированных гидроксикислотами сорбентов при отравлении животных ивермектином в условиях эксперимента
∗ Работа выполнена в рамках государственного задания ЦНХТ ИК СО РАН в соответствии с Программой фундаментальных научных исследований государственных академий наук на 2013-2020 годы по направлению V.45, проект V.45.2.8 (номер госрегистрации в системе ЕГИСУ НИОКТР АААА-А19-119050790074-9).
Сорбционная терапия относится к перспективным направлениям в разработке детоксикационных мероприятий. Отличительная особенность биоспецифических сорбентов — сочетание адсорбционных свойств исходного пористого материала и биологической активности наносимых модификаторов. Химическим модифицированием поверхности сорбентов можно повысить избирательность сорбции. К известным способам химической модификации относятся иммобилизация на поверхности ферментов, по-лиферментных комплексов, клеточных органелл (1-4), введение гетероатомов (Si, N), функциональных групп (–NH2, –COOH, –C=O, остатки фосфоновых кислот) или носителей функциональных групп с последующей обработкой модифицированных сорбентов различными реагентами и растворами белков. В настоящее время растет интерес к полимерным соединениям (5-9). В качестве модификаторов углеродных сорбентов могут быть использованы олиго- и полимеры гидроксикислот (гликолевой и молочной). Они разрешены к применению в медицине, так как не обладают выраженной токсичностью, совместимы с тканями организма и подвержены биодеструкции (10-14). Важное преимущество иммобилизации кислот на углеродной матрице заключается в сохранении антимикробных свойств иммобилизованных соединений и высокой адсорбционной емкости углеродного материала (15-19). При экзогенных отравлениях большое значение имеет изменение pH среды в желудочно-кишечном тракте при десорбции кислот, что существенно влияет на скорость всасывания и элиминации токсикантов.
В настоящей работе на модельном объекте (беспородные белые крысы) впервые доказана целесообразность проведения энтеросорбции при остром отравлении ивермектином с использованием нового углеродного сорбента, модифицированного молочной кислотой. Экспериментально обоснованы преимущества предложенного модификатора по сравнению с гликолевой кислотой и сополимером указанных гидроксикислот.
Цель исследования — разработать способ модифицирования гидроксикислотами углеродных сорбентов и сравнить их терапевтическую эффективность при отравлении животных ивермектином.
Методика. Новые формы углеродных сорбентов получены в Институте проблем переработки углеводородов СО РАН (г. Омск) модификацией гранулированного углеродного энтеросорбента (300-400 м2/г) гликолевой (ГК, 50 мас.%, «Merk Schuchardt OHG», Германия) и молочной (МК, 80 мас.%, «МОСРЕАКТИВ», Россия) кислотами, а также их сополимером по разработанным методикам.
Морфологию и рельеф поверхности полученных образцов сорбента исследовали методом растровой электронной микроскопии (JSM 6460LV, «JEOL Ltd», Япония) с вакуумным напылением золотой пленки толщиной 10-15 нм (напряжение 15-20 кВ, сила тока 10-30 мА для обеспечения контрастности электронных снимков). Микроскопировали по 5-10 гранул сорбентов с разными модификаторами.
Терапевтическую эффективность модифицированного сорбента оценивали на 50 беспородных половозрелых белых крысах с массой тела 180200 г. Животных подбирали по принципу аналогов с учетом возраста, пола и массы тела. Острое отравление ивермектином моделировали препаратом Баймек® (ФГБУ Федеральный центр охраны здоровья животных, г. Владимир), содержащим 1 % ивермектина. До начала опыта крысы в течение 2 нед находились под клиническим наблюдением в условиях карантина с целью исключения инфекционных заболеваний. В тече- ние всего периода животных кормили полнорационной зерновой смесью по общепринятым нормам лабораторного содержания.
Для проведения опыта сформировали пять групп по 10 особей в каждой. В контроле (I группа) интактные крысы никаким манипуляциям не подвергались. Остальным вводили подкожно Баймек® в дозе, превышающей терапевтическую в 10 раз. Во II группе животным лечение не назначали, III группа крыс получала сорбент, модифицированный гликолевой кислотой, IV группа — сорбент, модифицированный молочной кислотой, V группа — модифицированный сополимером гликолевой и молочной кислот. Все энтеросорбенты вводили в форме хлебных болюсов в дозах по 0,3 г/кг массы тела 2 раза в день в течение 5 сут, начиная с 1-х сут после затравки.
Перед началом опыта и по его окончании крыс взвешивали. Поcле завершения эксперимента у всех животных брали кровь для биохимического анализа, затем их подвергали эвтаназии. Для гистологического исследования отбирали фрагменты внутренних органов, брыжеечные лимфатические узлы и головной мозг.
Патологический материал фиксировали в 4 % нейтральном растворе формальдегида и жидкости Карнуа, заливали в парафиновые блоки и готовили срезы (ротационный микротом LaboCut 4055, «Slee», Германия). Для изучения общей гистоморфологической картины срезы окрашивали гематоксилином Ганзена и эозином, а также по Ван Гизону (20). Гликоген и нейтральные гликозаминогликаны (нейтральные ГАГ) выявляли ШИК-реакцией по методу Шабадаша (21). Для изучения образцов применяли световую микроскопию (Альтами Био, «Альтами» Россия, увеличение ½300, ½600).
При работе с лабораторными животными соблюдались принципы, изложенные в Европейской Конвенции о защите позвоночных животных, используемых для экспериментов или в иных научных целях (Страсбург, март 1986 года), и Хельсинкской Декларации о гуманном обращении с объектами исследования (Хельсинки, июнь 1964 года).
Статистическую обработку результатов исследования проводили с использованием программы Statistica 6.0 («StatSoft, Inc.», USA). Экспериментальные данные проверяли на нормальность распределения выборок при помощи W -критерия Шапиро-Уилка, после чего использовали t -критерий Стьюдента для независимых выборок. Различия считали статистически значимыми при p < 0,05. Результаты представляли как среднее арифметическое значение и стандартную ошибку среднего ( M ±SEM).
Результаты. Матрицей для получения биоспецифических сорбентов служил гранулированный углеродный энтеросорбент (УС), характеризующийся мезопористой структурой, высокой химической чистотой, биосовместимостью, удельной площадью поверхности 300-400 м2/г. Выбор модификаторов осуществляли в соответствии с предъявляемыми к ним требованиями по безопасности, растворимости, наличию реакционноспособных групп, возможности закрепления на поверхности сорбента с последующей биодеградацией (22). Гликолевая и молочная кислоты в полной мере обладают указанными свойствами (23), поэтому они были использованы как модификаторы поверхности углеродного сорбента.
Модифицирование матрицы олигомером гликолевой кислоты проводили в две стадии. На первой углеродный сорбент пропитывали водным раствором гликолевой кислоты (50 мас.%) при 20-25 °С на воздухе при соотношении сорбент: раствор модификатора 1:2 в течение 8 ч. На втором этапе сорбент подвергали термообработке на песчаной бане при 105±5 °С и 195±5 °С в течение 1 ч с последующим нагревом при 225±5 °С в течение 5 ч. Полученный модифицированный углеродный сорбент УС-ГК содержит олигомер гликолевой кислоты в количестве 12-15 мас.%, характеризуется удельной площадью поверхности 180-210 м2/г, обеспечивает низкое значение рН физиологического раствора (4,3-4,6) после контакта с образцом в течение 1 сут.
Модифицирование углеродного сорбента олигомером молочной кислоты также включало две стадии. Углеродный сорбент пропитывали водным раствором молочной кислоты (50 мас.%) при 20-25 ° С на воздухе при соотношении сорбент: раствор модификатора 1:2 в течение 24 ч, затем помещали на песчаную баню и обрабатывали при 130±5 ° С в течение 2 ч и при 150±5 ° С в течение 4 ч, после чего нагревали при 170±5 ° С в течение 18 ч в трубчатой печи в токе инертного газа аргона в присутствии осушителя. Модифицированный углеродный сорбент УС-МК содержит олигомер молочной кислоты в количестве 25-30 мас.%, характеризуется удельной площадью поверхностью 30-60 м2/г, обеспечивает низкое значение рН физиологического раствора (2,3-2,6) после контакта с образцом в течение 1 сут.
Процесс модифицирования углеродного сорбента сополимером гликолевой и молочной кислот состоял из трех этапов. Сначала сорбент пропитывали водным раствором гидроксикислот при комнатной температуре в соотношении гликолевая кислота:молочная кислота 70:30 мас.% в течение 24 ч; при этом соотношение по массе сорбент: раствор гидроксикислот 1:2. Далее сорбент высушивали на песчаной бане в течение 1 ч при 103-107 ° С. Затем проводилась продолжительная термообработка сорбента на песчаной бане в присутствии цеолита марки NaА-У формованного (ООО «Ишимбай-ский специализированный химический завод катализаторов», Республика Башкортостан) в качестве осушителя при 160-170 ° С 14 ч с последующим нагревом в трубчатой печи при температуре 170-180 ° С в токе аргона 7 ч (в присутствии цеолита).
В литературе описаны каталитические способы получения полигликолевой, полимолочной кислот и их сополимера при нагревании. При этом в качестве катализаторов представлены соединения на основе сурьмы, цинка, олова и др. (24, 25). Все перечисленные способы синтеза полимеров и сополимеров гидроксикислот небезопасны, при разработке материалов медицинского и ветеринарного назначений, так как предполагают использование токсичных для организма человека и животных органических растворителей и катализаторов на основе тяжелых металлов. Предложенные нами методы получения модифицированных сорбентов исключают применение подобных химических соединений.
Электронная микроскопия показала, что при модифицировании размер и форма гранул исходного сорбента сохраняются. Однако заметно изменяются рельеф и морфология поверхности модифицированных образцов. В отличие от исходного сорбента (рис. 1, А) на углеродной поверхности образцов, модифицированных олигомером гликолевой кислоты, наблюдаются мелкие полимерные частицы различной формы размером менее 1 мкм (см. рис. 1, Б). Они распределены локально, преимущественно в трещинах, порах и иных дефектах поверхности. На образце, модифицированном олигомером молочной кислоты, она распределялась в виде неравномерной полимерной пленки, экранирующей углеродную поверхность (см. рис. 1, В).
А

Б

В

Рис. 1. Гранулы (слева) и сколы (справа) исследуемых сорбентов: А — исходный углеродный сорбент, Б — образец, модифицированный гликолевой кислотой, В — образец, модифицированный молочной кислотой (растровая электронная микроскопия с золотым напылением, JSM 6460LV, «JEOL Ltd», Япония).
Результаты экспериментов in vivo показали разную степень эффективности энтеросорбции с применением модифицированных сорбентов при острой интоксикации крыс ивермектинсодержащим препаратом Баймек®. При моделировании острого отравления клинические симптомы у крыс развивались в течение 2 ч после затравки. На ухудшение состояния указывали взъерошенность волосяного покрова и гиперсаливация. С течением времени обострялась реакция на звуковые и тактильные раздражители. Периоды беспокойства сменялись угнетением, снижением двигательной активности. Отмеченные изменения в клиническом статусе животных обусловлены механизмом действия препарата. Проникая в организм животных из места инъекции, ивермектин взаимодействует с глутаматными ГАМК-
Биохимические показатели сыворотки крови беспородных белых крыс, интоксицированных Баймеком®, при коррекции модифицированными углеродными сорбентами (M±SEM, лабораторный опыт)
|
Общий белок, г/л |
Альбумины, г/л |
Глобулины, г/л |
Мочевина, ммоль/л |
ОБ, мкмоль/л |
Креатинин, мкмоль/л |
Глюкоза, ммоль/л |
ЩФ, ед/л |
АсАТ, ед/л |
АлАТ, ед/л |
Кальций, ммоль/л |
Фосфор, ммоль/л |
Железо, мкмоль/л |
Калий, ммоль/л |
|
К о нт р о л ь ( n = 10) |
|
|
65,3±0,36 27,58±0,69 37,72±0,86 |
3,48±0,13 1,42±0,13 38,22±2,03 5,60±0,28 433,22±46,07 148,88±2,49 79,64±5,23 3,08±0,03 2,82±0,11 40,56±2,88 8,64±0,37 Г р у п п а, и н т о к с и ц и р о в а н н а я Б а й м е к о м® б е з к о р р е к ц и и |
|
73,08±0,96 28,62±0,44 44,46±0,52 p к = 0,0001 p к = 0,2424 p к = 0,0002 |
2,44±0,05 1,80±0,07 87,00±5,52 5,52±0,10 394,56±6,26 155,76±1,70 58,62±0,16 2,84±0,02 2,40±0,20 37,34±0,55 8,82±0,12 p к = 0,0001 p к = 0,0379 p к < 0,0001 p к = 0,7979 p к = 0,4298 p к = 0,0745 p к = 0,0039 p к = 0,0007 p к = 0,1094 p к = 0,3046 p к = 0,6576 Гр у п п ы, и нт о к с и ц и р о в а н н ы е Б а й м е к о м®: с коррекцией сорбентом, модифицированным гликолевой кислотой ( n = 10) |
|
73,32±0,94 29,42±0,47 43,90±0,88 p б = 0,8635 p б = 0,2504 p б = 0,6023 |
3,74±0,10 2,04±0,22 82,32±2,74 7,58±0,37 339,88±23,01 122,84±0,83 49,30±2,52 2,94±0,05 2,28±0,10 52,86±0,86 9,98±0,42 p б < 0,0001 p б = 0,3344 p б = 0,4698 p б = 0,0007 p б = 0,0510 p б < 0,0001 p б = 0,0062 p б = 0,1151 p б = 0,6143 p б < 0,0001 p б = 0,0315 с коррекцией сорбентом, модифицированным молочной кислотой ( n = 10) |
|
78,56±0,63 31,20±0,46 47,36±0,88 p б = 0,0014 p б = 0,0039 p б = 0,0228 |
4,16±0,09 0,89±0,01 40,86±0,66 8,06±0,10 194,88±2,89 120,38±0,76 53,02±1,20 3,16±0,05 2,12±0,03 54,22±0,43 9,06±0,16 p б < 0,0001 p б < 0,0001 p б < 0,0001 p б < 0,0001 p б < 0,0001 p б < 0,0001 p б = 0,0017 p б = 0,0005 p б = 0,2109 p б < 0,0001 p б = 0,2805 с коррекцией сорбентом, модифицированным сополимером гликолевой и молочной кислот ( n = 10) |
|
60,10±0,38 26,48±0,43 33,62±0,32 p б < 0,0001 p б = 0,0085 p б < 0,0001 |
3,76±0,12 0,81±0,01 66,82±2,81 2,80±0,23 466,80±46,51 66,02±17,41 57,60±4,73 2,76±0,04 3,08±0,23 37,68±1,13 10,62±0,46 p б < 0,0001 p б < 0,0001 p б = 0,0116 p б < 0,0001 p б = 0,1624 p б = 0,0008 p б = 0,8350 p б = 0,1265 p б = 0,0599 p б = 0,7941 p б = 0,0058 |
П р и м е ч а н и е. Применен t-критерий для независимых выборок. рк — уровень значимости по отношению к группе контроля, рб — уровень значимости по отношению к группе, обработанной Баймеком®; ОБ — общий билирубин, ЩФ — щелочная фосфатаза, АсАТ — аспартатаминотрансфераза, АлАТ — аланинаминотрансфераза.
эргическими рецепторами хлорных каналов и рецепторами глицин-акти-вируемых каналов. При этом отмечается гиперполяризация постсинаптических мембран и нарушение межнейронной передачи импульсов (26-28).
Через 1 сут после начала эксперимента интоксицированные животные оставались малоподвижными, с тусклым волосяным покровом и легким проявлением гиперсаливации. Аппетит у них был снижен. Крысы опытных (III-V) групп, получавшие сорбенты, стали быстрее проявлять интерес к корму, совершали груминг. Через 48 ч после начала эксперимента и до его окончания существенных различий в поведении и клиническом состоянии животных, подвергавшихся энтеросорбции, не регистрировали
Поведение интактных животных контрольной группы оставалось без изменений на протяжении всего периода наблюдения. Сравнение данных контрольных взвешиваний животных не выявило статистически значимых различий в начале и по завершении эксперимента.
Результаты исследования сыворотки крови представлены в таблице. Полученные данные свидетельствуют о том, что интоксикация Баймеком® вызывает увеличение содержания общего белка в сыворотке крови крыс на 11,9 % (p = 0,0001), причем статистически значимо возрастал показатель по глобулинам (на 17,86 %, p = 0,0002). При этом снижалась концентрация мочевины (на 29,89 %, p = 0,0001), но повышалось содержание общего билирубина (на 26,76 %, p = 0,0379), что служит свидетельством гепатотоксического действия Баймека® (29). Однако более существенным было увеличение концентрации креатинина — в 2,3 раза. Отмеченные изменения указывают на снижение катаболизма белков и нарушение фильтрационной функции почек. При этом активность аланинаминотрансферазы у интоксицированных крыс снижалась. Энтеросорбент с молочной кислотой способствовал повышению концентрации белка на 7,5 % (p = 0,0014) по сравнению с аналогичным показателем в группе крыс, которые подвергались интоксикации без коррекции. Введение сорбентов, модифицированных гидроксикислотами, неоднозначно влияло на содержание общего белка в сыворотке крови крыс.
Сорбент, модифицированный сополимером молочной и гликолевой кислот, напротив, снизил содержание белка на 17,8 % относительно группы крыс, интоксицированных Баймеком®. При этом первый из предлагаемых нами сорбентов (с молочной кислотой) в равной мере повышал концентрацию альбуминов и глобулинов, второй (с гликолевой кислотой) — преимущественно снижал содержание глобулиновых фракций, но не так значительно уменьшал концентрацию креатинина, как сорбент с молочной кислотой. Образец, модифицированный гликолевой кислотой, не вызывал статистически значимых изменений в содержании креатинина по сравнению с показателем в группе интоксицированных животных, не получавших лечения.
Все сорбенты снижали активность аспартат- (АсАТ) и аланинаминотрансфераз (АлАТ). Однако для принятия клинических решений принципиальное значение имеет тот факт, что активность АлАТ у интоксицирован-ных животных была ниже, чем у интактных, хотя чаще о гепатотоксическом действии свидетельствует повышение уровня аланинаминотрансферазы в сыворотке крови (30, 31).
Сорбент с молочной кислотой вызывал максимальное увеличение концентрации железа (на 45,2 % при p < 0,0001) и кальция (на 11,26 % при p = 0,0005) в сыворотке крови крыс, но не оказывал существенного влияния на содержание фосфора. При этом самой низкой была концентрация билирубина и наивысшей — глюкозы.
Анализ посмертных изменений в организме животных, подвергнутых острой интоксикации Баймеком®, указывал на политропный характер действия препарата, отмеченный и другими авторами при изучении системных побочных реакций ивермектина (32).
А
Б
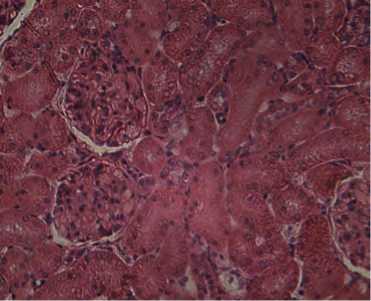
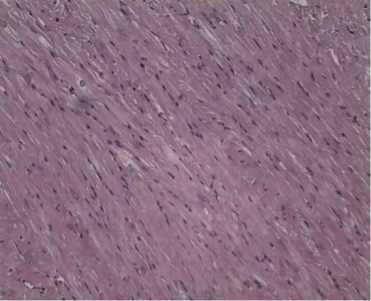
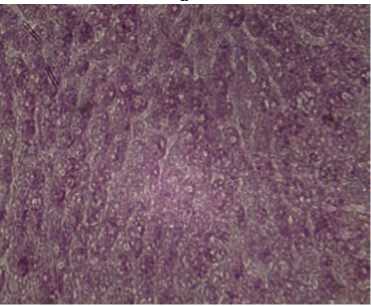
Рис. 2. Патоморфологические изменения в органах беспородных белых крыс, интоксициро-ванных Баймеком®: А — дистрофия миокарда, окрашивание гематоксилином и эозином, увеличение ½300; Б — зернистая дистрофия эпителиоцитов извитых канальцев почек, окрашивание гематоксилином и эозином, увеличение ½600; В — низкое содержание гликогена в гепатоцитах, метод Шабадаша, увеличение ½600 (лабораторный опыт, световая микроскопия, микроскоп Альтами Био, «Альтами», Россия).
У животных была выражена острая застойная гиперемия внут- ренних органов и головного мозга.
Под эпикардом отмечали точечные кровоизлияния. Сердце было расширено, его полости заполнены кровью. Миокард имел сероватый оттенок. При гистологическом исследовании отчетливо проявилось выраженное набухание мышечных волокон с потерей поперечной исчерчен-ности кардиомиоцитов (рис. 2, А). Содержание гликогена в кардиомио- цитах снижалось.
Почки крыс имели красно-коричневый цвет со светло-серыми участками. Их капсула легко снималась. При микроскопическом исследовании наблюдали гиперемию почек, в мозговом веществе — кровоизлияния. Просветы извитых канальцев были сужены и содержали оксифильно окрашенную массу. Цитоплазма эпителиоцитов проксимального отдела нефрона имела зернистую структуру, часть ядер в клетках эпителия находилась в состоянии пикноза или лизиса (см. рис. 2, Б). Печень у животных была неравномерно окрашена. При микроскопическом исследовании отмечалось резкое снижение содержания гликогена в гепатоцитах (см. рис. 2, В), выраженное кровенаполнение сосудов органа с расширением внут- ридольковых синусоидных капилляров, гепатоциты находились в состоянии белково-жировой дистрофии. Ядра многих гепатоцитов были пикно-тичны или лизированы (рис. 3, А).
Легкие крыс были неравномерно окрашены, с участками красного и бледно-розового цвета. Гистоисследование выявило очаговые кровоизлияния, переполнение кровью кровеносных сосудов. В участках эмфиземы наблюдали растяжение альвеол, истончение и разрыв их стенок. У некоторых животных вокруг бронхов отмечали инфильтраты, преимущественно состоящие из клеток лимфоидного ряда. На поверхности клеток бронхиального эпителия имелось значительное количество слизи.
А
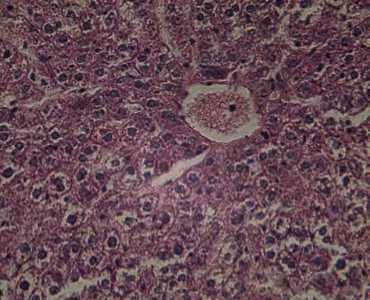
Б
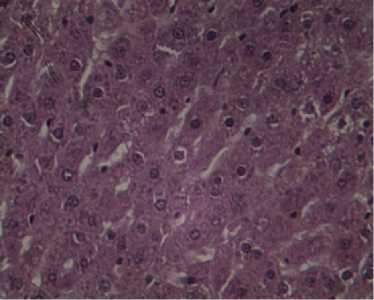
Рис. 3. Гистологическое исследование печени беспородных белых крыс, интоксицированных Баймеком®, при коррекции модифицированными углеродными сорбентами: А — гепатоциты с крупными и мелкими вакуолями в цитоплазме при отравлении Баймеком®; Б — острое отравление Баймеком® и применение сорбента с молочной кислотой; В — острое отравление Баймеком® и применение сорбента с гликолевой кислотой (лабораторный опыт, окрашивание гематоксилином и эозином, световая микроскопия, увеличение ½600, микроскоп Альтами Био, «Альтами», Россия).
В
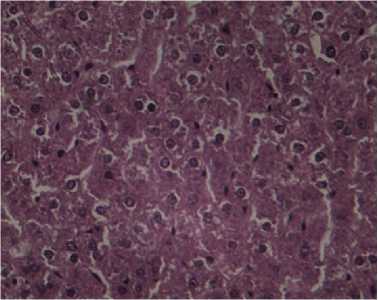
Введение энтеросорбентов, модифицированных гликолевой и молочной кислотами, а также их сополимером, способствовало снижению интенсивности патологических процессов в органах животных. Сравнительное изучение патоморфологических изменений у животных, подвергнутых интоксикации Баймеком® и фармакокоррекции, позволило отметить более выраженное детоксицирующее действие сорбента, модифицированного олигомером молочной кислоты. Гистопрепараты печени при использовании указанного сорбента демонстрируют лишь признаки зернистой дистрофии (см. рис. 3, Б). Энтеросорбенты с гликолевой кислотой и сополимером гидроксикислот не устраняли в полной мере некробиоти-ческие изменения в гепатоцитах (см. рис. 3, В), а также признаки застойной гиперемии органов, что объясняло соответствующие изменения метаболического профиля животных.
Отмеченные различия в действии модифицированных гидроксикислотами сорбентов обусловлены, вероятно, более низким значением pH сорбента с молочной кислотой. Ивермектин подвергается биотрансформации в печени с участием цитохрома P450, главным образом его изофермента CYP3A4, окислительная активность которого значительно возраста- ет в кислой среде (33).
Таким образом, впервые разработаны способы модифицирования поверхности углеродного сорбента олигомерами гликолевой и молочной кислот, а также их сополимером, включающие пропитку сорбента водными растворами гидроксикислот или их смесью и продолжительную термообработку (поликонденсацию) без использования катализаторов и органических растворителей, проявляющих токсичность. Это позволило получить бифункциональные сорбенты, сочетающие адсорбционные свойства матрицы и биологическую активность модификаторов. Результаты исследования подтверждают терапевтическую эффективность сорбентов, модифицированных гидроксикислотами, при интоксикации животных содержащим ивермектин препаратом Баймек ® . Наиболее выражено детоксицирующее действие сорбента, модифицированного молочной кислотой. При его применении максимально повышается уровень глобулинов в сыворотке крови, в два раза снижается содержание общего билирубина, активизируется минеральный обмен. При гистоисследовании отмечаются лишь слабо выраженные дистрофические изменения в паренхиматозных органах после энтеросорбции. Применение модифицированных сорбентов существенно повышает эффективность детоксикационных мероприятий и открывает новые возможности сорбционной терапии.
Список литературы Терапевтическая эффективность модифицированных гидроксикислотами сорбентов при отравлении животных ивермектином в условиях эксперимента
- Клименко Н.А. Влияние различных режимов окисления на изменение структурных характеристик активного угля. Химия и технология воды, 2008, 5(30): 478-489.
- Сидорчук В.В. Некоторые особенности модифицирования активных углей парами воды и пероксида водорода при высоких температурах и давлениях. Журнал прикладной химии, 2006, 9(79): 1444-1447.
- Mykola S. Surface functional groups of carbons and the effects of their chemical character, density and accessibility to ions on electrochemical performance. carbon, 2008, 46: 1475-1488 ( ). DOI: 10.1016/j.carbon.2008.06.027
- Tasis D. Chemistry of carbon nanotubes. Chemical Reviews, 2006, 106: 1105-1136 ( ). DOI: 10.1021/cr050569o
- Bazula P.A. Surface and pore structure modification of ordered mesoporous carbons via a chemical - oxidation approach. Microporous and Mesoporous Materials, 2008, 108: 266-275 ( ). DOI: 10.1016/j.micromeso.2007.04.008
- Hiromi K., Tachimoto K., Anraku Y. Functionalization of single-walled carbon nanotube by the covalent modification with polymer chains. Journal of Colloid and Interface Science, 2007, 306: 28-33 ( ).
- DOI: 10.1016/j.jcis.2006.10.034
- Jianfeng Sh. Thermo-physical properties of epoxy nanocomposites reinforced with amino-functionalized multi-walled carbon nanotubes. Composites: Part A, 2007, 38: 1331-1336 ( ).
- DOI: 10.1016/j.compositesa.2006.10.012
- Niu L., Yanling L., Zhanqing L. A highly selective chemical gas sensor based on functionalization of multi-walled carbon nanotubes with poly(ethylene glycol). Sensors and Actuators B, 2007, 126: 361-367 ( ).
- DOI: 10.1016/j.snb.2007.03.018
- Qiao Ch., Xu R., Yu D. Multiwalled carbon nanotube/polybenzoxazine nanocomposites: preparation, characterization and properties. Polymer, 2006, 47: 7711-7719 ( ).
- DOI: 10.1016/j.polymer.2006.08.058
- Ozdil D., Aydin H.M. Polymers for medical and tissue engineering applications. Journal of Chemical Technology and Biotechnology, 2014, 89: 1793-1810 ( ).
- DOI: 10.1002/jctb.4505
- Botvin V., Pozdniakov M., Filimoshkin A. Intermolecular "zipper" type depolymerization of oligomeric molecules of lactic and glycolic acids prepacked as paired associates. Polymer Degradation and Stability, 2017, 146: 126-131 ( ).
- DOI: 10.1016/j.polymdegradstab.2017.10.004
- Swider E., Koshkina O., Tel J., Cruz L.J., de Vries I.J.M., Srinivas M. Customizing poly(lactic-co-glycolic acid) particles for biomedical applications. Acta Biomaterialia, 2018, 73: 38-51 ( ).
- DOI: 10.1016/j.actbio.2018.04.006
- Kasirajan S., Umapathy D., Chandramohan Ch., Aafrin V., Jenitapeter M., Udhyasooriyan L., Packirisamy A.S.B., Muthusamy S. Preparation of poly(lactic acid) from Prosopis juliflora and incorporation of chitosan for packaging applications. Journal of Bioscience and Bioengineering, 2019, 128(3): 323-331 ( ).
- DOI: 10.1016/j.jbiosc.2019.02.013
- Lee J.C., Choi M.-C., Choi D.-H., Ha C.-S. Toughness enhancement of poly(lactic acid) through hybridisation with epoxide-functionalised silane via reactive extrusion. Polymer Degradation and Stability, 2019, 160: 195-202 ( ).
- DOI: 10.1016/j.polymdegradstab.2018.12.024
- Мещерякова О.В., Чурова М.В., Немова Н.Н. Митохондриальный лактат-окисляющий комплекс и его значение для поддержания энергетического гомеостаза клеток. В сб.: Экологическия физиология и биохимия водных организмов. Петрозаводск, 2010: 163-171.
- Burgos N., Tolaguera D., Jime'nez S.F.A. Synthesis and characterization of lactic acid oligomers: evaluation of performance as poly (lactic acid) plasticizers. Journal of Polymers and the Environment, 2014, 22: 227-235 ( ).
- DOI: 10.1007/s10924-013-0628-5
- Boomsma B., Bikker E., Lansdaal E., Stuut P. L-Lactic acid - a safe antimicrobial for home- and personal care formulations. SOFW Journal, 2015, 141(10): 2-5.
- Wang C., Chang T., Yang H., Cui M. Antibacterial mechanism of lactic acid on physiological and morphological properties of Salmonella enteritidis, Escherichia coli and Listeria monocytogenes. Food Control, 2015, 47: 231-236 ( ).
- DOI: 10.1016/j.foodcont.2014.06.034
- Maharramov A.M., Ramazanov M.A., Hasanova U.A. Nanostructures for antimicrobial therapy - the modern trends in the treatment of bacterial infections. In: Antimicrobial nanoarchitectonics. From synthesis to applications /A.M. Grumezescu (ed.). Elsevier, 2017: 445-473 ( ).
- DOI: 10.1016/B978-0-323-52733-0.00016-1
- Меркулов Г.А. Курс патологической техники. Л., 1979.
- Кононский А.И. Гистохимия. Киев, 1976.
- Алексеев К.В., Аляутдин Р.Н., Блынская Е.В., Квинх Б.Т. Основные направления в технологии получения наноносителей лекарственных веществ. Вестник новых медицинских технологий, 2009, 16(2): 142-145.
- Штильман М.И. Полимеры медико-биологического назначения. М., 2006.
- Кузнецова И.Г., Северин С.Е. Использование сополимера молочной и гликолевой кислот для получения наноразмерных лекарственных форм. Разработка и регистрация лекарственных средств, 2013, 4(5): 30-36.
- Шкарин А.А., Яркова А.В., Похарукова Ю.Е., Новиков В.Т. Выбор условия для получения олигомеров молочной кислоты. Вестник Томского государственного университета, 2014, 385: 224-226.
- Wolstenholme A.J. Glutamate-gated chloride channels. Journal of Biological Chemistry, 2012, 287: 40232-40238 ( ).
- DOI: 10.1074/jbc.R112.406280
- Bai S.H., Ogbourne S. Eco-toxicological effects of the avermectin family with a focus on abamectin and ivermectin. Chemosphere, 2016, 154: 204-214 ( ).
- DOI: 10.1016/j.chemosphere.2016.03.113
- Zhang Y., Luo M., Xu W., Yang M., Wang B., Gao J., Li Y., Tao L. Avermectin confers its cytotoxic effects by inducing DNA damage and mitochondria-associated apoptosis. Journal of Agricultural and Food Chemistry, 2016, 64: 6895-6902 ( ).
- DOI: 10.1021/acs.jafc.6b02812
- Чудов И.В., Исмагилова А.Ф. Коррекция токсического гепатоза у собак, вызванного воздействием макроциклических лактонов. Аграрный вестник Урала, 2012, 5(97): 53-57.
- Сулайманова Г.В., Донкова Н.В. Гепатотоксическое действие лекарственных препаратов у животных. Вестник КрасГАУ, 2015, 10(109): 201-205.
- Сорокин А.В., Машошина Д.О., Драговоз И.С., Молокоедов В.В. Влияние этанола на биохимическую активность гепатоцитов печени при экспериментальном остром деструктивном панкреатите и способы коррекции. Международный студенческий научный вестник, 2018, 4-1: 98-100.
- Sparsa A., Bonnetblanc J.M., Peyrot I., Loustaud-Ratti V., Vidal E., Bédane C. Systemic adverse reactions with ivermectin treatment of scabies. Annales de Dermatologie et de Vénéréologie, 2006, 133(10): 784-787.
- Campbell W.C. History of avermectin and ivermectin, with notes on the history of other macrocyclic lactone antiparasitic agents. Current Pharmaceutical Biotechnology, 2012, 13(6): 853-865 ( ).
- DOI: 10.2174/138920112800399095


