Термодинамическая модель шлакового расплава с произвольным числом сортов катионов и анионов
Автор: Власов В.Н.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 9 (109), 2008 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/147156602
IDR: 147156602 | УДК: 669.1
Текст статьи Термодинамическая модель шлакового расплава с произвольным числом сортов катионов и анионов
Жидкие металлургические шлаки в соответствии с их физико-химическим характеристикам относят к категории ионных расплавов [1, 2]. Известно, что главными исходными составляющими металлургических шлаков являются оксиды. Помимо оксидов исходными компонентами шлаков могут являться также фториды, сульфиды и некоторые другие группы соединений, поставляющие в расплав при плавлении различные сорта катионов и анионов.
Термодинамические свойства шлаковых расплавов определяются их составом и температурой. Поскольку диапазон составов промышленных шлаков широк, экспериментальное исследование их термодинамических характеристик представляет сложную задачу. Изучение даже таких относительно простых объектов, как тройные или четверные системы, является трудоемким и длительным. Исследование свойств пяти-, шестикомпонентных и более сложных систем является еще более сложным, поэтому в литературе содержатся сведения о результатах экспериментального изучения лишь их отдельных фрагментов. В условиях значительного дефицита экспериментальной информации [3-5] основные надежды на получение термодинамических данных о сложных по составу жидких шлаках связываются с модельными методами химической термодинамики, опирающимися на экспериментальные данные о свойствах простых систем, и связывающих на основе теоретических положений свойства простых и многокомпонентных расплавов.
В работе [6] было опубликовано описание термодинамической модели оксидного шлакового расплава, содержащего один сорт анионов - анионы кислорода. В основу этой модели были положены представления об островной структуре ионных расплавов, находящихся в условиях относительно небольшого перегрева над температурой ликвидуса [7]. Теоретические положения термодинамической модели сводились к следующему. Структурными составляющими шлакового расплава являются простейшие по составу ионы, сгруппированные в микрокомплексы (островки), имеющие в пределах нескольких координационных сфер кристаллоподобное упорядочение по типу твердых фаз. Островки неупорядочены во взаимном расположении относительно друг друга, являются неустойчивыми короткоживущими динамическими образованиями, связанными друг с другом непрерывным обменом частиц. Эти образования отражают усредненный состав расплава, разрушаясь в одном месте, они возникают в дру гом и поэтому не могут рассматриваться в качестве микро-фаз. Координационные числа катионов в таких микрокомплексах постоянны и по своим величинам близки к координационным числам соответствующих катионов в жидких простых оксидах. Предложенная термодинамическая модель показала свою хорошую эффективность в термодинамических расчетах [8-12]. Это сделало целесообразным расширение области ее применения на более сложные по составу (полианионные) шлаковые расплавы, что и стало задачей данной работы.
Рассмотрим ионный расплав, содержащий к сортов катионов и I сортов анионов. Допустив при образовании расплава полную электролитическую диссоциацию всех исходных компонентов на простейшие катионы и анионы, выразим общее количество катионов (Акет) и общее количество анионов ( N^ ) в расплаве соотношениями:
^OT=^off^.. (1)
'=1 7=1
N™-NoT?Lvymu ■ (2)
7=17=1
Здесь Nq - число Авогадро; Vy и Vy - количества катионов и анионов (соответственно), образующихся при диссоциации молекулы компонента (у); ту - числа молей исходных молекулярных компонентов (у) в системе.
Ионные доли катиона произвольного сорта (s) и аниона произвольного сорта (7) в расплаве в этом случае будут определяться уравнениями:
^s ^'^j^'sj^sj /^кат ’(^)
7=1/
Vi^W, Jn^.(4)
Будем считать, что зависимость среднего значения координационного числа катиона сорта (s) в полианионном расплаве z* (равного среднему числу анионов в его ближайшей координационной сфере) от анионного состава расплава характеризуется функцией г5=Х4^7> <5)
7=1
в которой величины z* соответствуют значениям координационных чисел катиона сорта (s) в чистых жидких компонентах (s/).
Представим энергию расплава в виде сумы
|
энергий чистых жидких компонентов и избыточной энергии, характеризующей эффект образования расплава к ! 5 = (6) '=1 7=1 Здесь Еу - молярная энергия чистого жидкого компонента (zy). Появление слагаемого Е”6 будем связывать с двумя главными факторами: различиями в структурах жидких компонентов и зависимостью величин энергий связей между катионами и анионами в расплаве от состава расплава. Число связей катионов сорта (z) в расплаве с окружающими их анионами будем определять соотношением = ЦУит>А4 = HVymijNO U^J ) • <7> 7=1 7=1 Зависимость избыточной энергии связи между катионом сорта (z) и анионом сорта (/) в расплаве от состава расплава опишем с помощью ряда '—1 ( йс.. А к (Зе-- А U Е Е -. Хт* m-1 V ^т У m=z+l к ихт У у-1 ( Зе Л l „ ( Зе-у +Д^Уп+^ -^Уп- (8) п=к*1\°Уп ) В суперпозиционном приближении с учетом (7) конфигурационную энергию расплава можно |
Перегруппировав выражение (11) и введя дополнительные обозначения, приведем его к виду к 1 E=hh4mu + i=kj=l ( к 1 А / (к-1 к . .. А + Т^^^У iyj ЕЕ Х,Хт^т + ч ;=1 у=1 у 7=1 к '=1 т=/+1 У (к 1 А * (м i А + EEw Ех- Е Е yjy^v) • <12) к'=17=1 У'=1 к7=1"=7+1 У Здесь Г ( 9бц А . (ЭЕт. А 2V0 5 _ V^m У к ^ /_ = No [zy f + zm ( (14) L 1^7 - функции, характеризующие энергии образования бинарных расплавов из жидких молекулярных компонентов (zy) и (иу) (имеющих одинаковый анион сорта у) и бинарных расплавов из жидких молекулярных компонентов (zy) и (ш) (имеющих одинаковый катион сорта z"), a Zy - координационные числа анионов в жидких компонентах (zy). Допустим, что в расплавах с общими анионом сорта у концентрационные зависимости величин Еу и Emj описываются функциями |
|
представить в виде: к 1 к 1 Е = У^ 4тУ + £ Е ^ ™уИ0У^ Еу = t=l J=1 1=1 7=1 £ / f к I Лк1 + ^EE^- УлУ^ [N^s.j} • (9) '=17=1 k '=17=1 У'=1 7=1 Приняв во внимание, то что EE^4 =ЕЕк2'к 0°) '=1 7=1 ,=1 7=1 выражение (9) с учетом (2) и (8) преобразуем к виду к 1 ( к 1 ' E = TiLEymy+ КоЕ^уМу х '=17=1 V '=17=1 У 1 Г * >-i (ds Л хУ у. У У x.xmNQz*j —У- + ' J 1—11—! 1 т У у 7=1 L'=lm=l \ихт J к '-1 ( 5е ,Л1 ( к 1 Ai ^У.Х>ХтМ02у J + ^Т^У^У Xх'Х /=1 m=l k^myj V /=17=1 у/=1 / j"^ ( Эе х mLyjynN0Zy + 7=1 и=1 Х^Уп ) i 1 (Se\ - ^^УуУАху -У- . (11) 7=1л=7+1 Х^Уп |
Еу=^/хт+ЬУ,х1хт, (15) Emj =<^Рх1*Ь^Х,Хт, (16) а в расплавах с общим катионом сорта z функциями Еу=а'^уп+Ь^УуУ„, (17) £у = а^+Ь(^у»’ (18) в которых параметры а^ , Ь^, а'^, Ь^ являются энергетическими константами. Подставив (15), (16) в (13), а (17), (18) в (14) и проведя дифференцирование, получим ^’ = е^+(4 - 4,)-(^ -».)^’. (I?) “fi-e^-^lk-* (20) Здесь ^=Н^<^*^^, (21) ^^^(z^ + z,;^), (22) ^=N^, (23) qJ^=N< (24) - энергетические параметры модели. Введя в рассмотрение функцию состава расплава |
Власов В.Н.
k I / к I
^=УХу>ч Т3>уту> '=1 7=1 / 7=17=1
совершенного ионного раствора, а 5юб - избы
равную отношению общего числа молей катионов к общему числу молей анионов в расплаве, с учетом записанных выше соотношений получим выражения для энергии расплава и парциальной молярной энергии произвольного компонента (sf) в
точная энтропия смешения жидких компонентов.
Поскольку теплоемкость шлакового расплава
примерно соответствует аддитивно сложенным теплоемкостям чистых жидких компонентов, будем считать слагаемые 8го и 5й36 независящими от температуры и являющимися лишь функциями
расплаве.
состава расплава.
Энтропия образования совершенного ионного
7=1 7=1
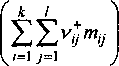
^j=\ /=1 m=i+l
раствора определяется произведением чисел случайных перестановок катионов друг с другом и анионов друг с другом. Ее концентрационная зависимость характеризуется формулой
к-\ к
+ Е Е Х-Хт
z=l m=z+l
+7fE^E Е ъ^б +
*<7=1 7=177=7+1 '
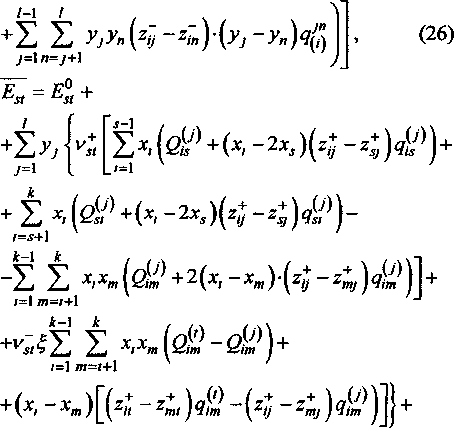
к _ /-1 , ,
+2> N Е^ +(^7 -2Wy -wb)+
+ Е ^ (% Чу к ~2уДу ДД”
j=t+i
~Ё Е У,У»^+Цу,-УпЧ
J=ln=J+i
“(^^^А+уЁ Е уДе^-е(^+
* 7=1 ”=7+1
+(-Ъ ~Уп)^25к-25п)9($)-Чу -z”v)^) |- ^7)
Энтропию расплава выразим соотношением
S^^my+s^+S™6, <28>
7=1 7=1
в котором: Sy - молярная энтропия чистого жид кого компонента (у), 8ВД - энтропия образования
S^-R
к ( 1
Ё 1>уту
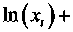
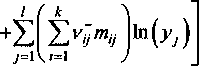
Концентрационную зависимость избыточной
энтропии смешения представим в виде уравнения
к-1 к
+Е Ё Х.Хт
7=1 777 =7+1
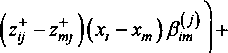
+у(Е^ Ё Е УкУп«^
* <7=1 7=177=7+1
+Е Е УкуД-Дук-уЧ^ - 7=177=7+1 у
в котором а^, р^, а/л , р^ являются посто
янными величинами (энтропийными параметрами модели).
Воспользовавшись зависимостями (29) и (30) проведя дифференцирование уравнения (28) по числу молей произвольного компонента (sZ) получим выражение для парциальной молярной энтропии компонента, ^ = 5° +
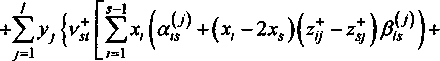
+ Е х< Д+Vх. - 2xJ(4 - 4l^) ” J=S+1 t-i к ,
-Z E X-Xm\«im +2(x,-Xm)x 7=1 777=7+1
AZy ” zmj ^im
)] +
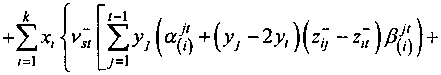
+ Е И) +к ~2У«Х2и -^И))- у=/+1
~Ё Z VjVn («g *4? j z7n^S+ J=\n=j*\ J
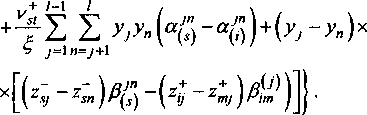
Используя уравнения (27) и (31) несложно перейти к выражению для химического потенциала произвольного компонента (st) в шлаковом расплаве
^^~^> (32)
а также к выражению для его активности
^)=ехр:
трИЗб т сИЗб
RT
Термодинамическая модель шлакового рас плава с произвольным числом сортов катионов и анионов, предложенная в данной работе, сохраняет все основные достоинства опубликованной ранее [6] модели оксидного шлака. Полученные термодинамические зависимости связывают свойства простых и неограниченно сложных по составу систем, обладают хорошими интерполяционными возможностями, разумной гибкостью, изменяющейся в зависимости от структуры и природы исходных компонентов расплава. В силу указанных обстоятельств выведенные соотношения могут найти практическое применение в термодинамических исследованиях, направленных на обобщение и дополнение имеющейся информации о свойствах шлаковых расплавов, моделировании термодинамических характеристик жидких шлаков, а также в расчетах высокотемпературных равновесий в системах с их участием.
Выводы
-
1. С учетом ионной природы жидких шлаков на основе островной модели строения ионных жидкостей разработана термодинамическая модель шлакового расплава, содержащего произвольное число сортов катионов и анионов.
-
2. Выведены уравнения для основных термодинамических характеристик жидких шлаков (энтальпии и энтропии образования расплавов, парциальных молярных свойств компонентов, активности компонентов), выражающие их зависимость от состава и температуры системы.
-
3. Полученные соотношения связывают свойства простых и сложных по составу ионных рас
плавов, обладают хорошими интерполяционными возможностями и могут найти практического применения в термодинамических исследованиях.
Список литературы Термодинамическая модель шлакового расплава с произвольным числом сортов катионов и анионов
- Есин О.А. Физическая химия пирометаллургических процессов/О.А. Есин, П.В. Гельд. М.: Металлургия, 1966. Ч. 2. 704 с.
- Кожеуров В.А. Термодинамика металлургических шлаков/В.А. Кожеуров. Свердловск: Металлургиздат, 1955. 163 с.
- Эллиот Д.Ф. Термохимия сталеплавильных процессов/Д.Ф. Эллиот, М. Глейзер, В. Рамакришна. М.: Металлургия, 1969. 252 с.
- Атлас шлаков: Справ. изд.; пер. с нем. М.: Металлургия, 1985. 208 с.
- Slag Atlas. 2nd Edition. Verlag Stahleisen GmbH. Dusseldorf, 1995. 616 s.
- Власов B.H. К термодинамике жидких металлургических шлаков/B.H. Власов//Вестник ЮУрГУ. Серия «Металлургия». 2004. Вып. 4. № 8(37). С. 3-8.
- Дифракционные исследования строения высокотемпературных расплавов/Э.А. Пастухов, Н.А. Ватолин, В.Л. Лисин, В.М. и др. Екатеринбург: УрО РАН, 2003. 335 с.
- Власов В.Н. Высокотемпературные фазовые равновесия и термодинамические свойства расплавов в системе CaО-SiО2/В.Н. Власов, Е.А. Мамонтова//Вестник ЮУрГУ. Серия «Металлургия». 2005. Вып. 6. № 10(50). С. 21-26.
- Власов В.Н. Комплексное моделирование высокотемпературных фазовых равновесий в системе СаО-А12О3/В.Н. Власов, С.В. Герасимова//Компьютерное моделирование физико-химических свойств стекол и расплавов: труды 8 Российского семинара. Курган: Изд-во Курганского гос. ун-та, 2006. С. 46-48.
- Власов В.Н. Фазовые равновесия и термодинамические свойства расплавов в системе MgО-SiО2/В.Н. Власов, А.А. Беляев//Современные проблемы электрометаллургии стали: материалы XIII Международной конф. Челябинск: Изд-во ЮУрГУ, 2007. Ч. 1. С. 82-88.
- Власов В.Н. Термодинамическое моделирование распределение элементов в процессах выплавки силикомарганца в рудовосстановительных электропечах/В.Н. Власов, Ю.А. Агеев, В.Б. Шмыга//Вестник ЮУрГУ. Серия «Металлургия». 2003. Вып. 3. № 2(18). С. 47-50.
- Власов В. Н Влияние состава шлака выплавки силикомарганца на содержание в нем оксида марганца/В.Н. Власов, Ю.А. Агеев, В.Б. Шмыга//Проблемы и перспективы развития ферросплавного производства ОАО «ТНК Казхром». Актобе, 2003. С. 425-429.


