Термодинамический анализ фазовых равновесий, реализующихся в системах Ni-Al-С-О и Ni-Ca-С-О в условиях существования жидкого металла
Автор: Трофимов Евгений Алексеевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 15 (274), 2012 года.
Бесплатный доступ
Посредством термодинамических расчётов построены поверхности растворимости компонентов в металле (ПРКМ) для систем Ni-Al-C-O и Ni-Ca-C-O. Разработанные ПРКМ могут быть использованы для анализа технологических процессов, связанных с взаимодействием кислорода, углерода, кальция и алюминия в жидком никеле.
Никелевый расплав, углерод, кальций, алюминий, кислород, термодинамические расчёты
Короткий адрес: https://sciup.org/147156724
IDR: 147156724 | УДК: 669.24+541.123
Thermodynamic analysis of phase equilibria in the Ni-Al-C-O and Ni-Ca-C-O systems under the condition of existence of nickel melt
Surfaces of components’ solubility in metal melt for the Ni-Al-С-О and Ni-Ca-С-О systems were plotted using thermodynamic calculations. The diagrams can be used for analyzing technological processes related to interaction of oxygen, carbon, calcium and aluminum in nickel melt.
Текст научной статьи Термодинамический анализ фазовых равновесий, реализующихся в системах Ni-Al-С-О и Ni-Ca-С-О в условиях существования жидкого металла
В рамках систематического исследования фазовых равновесий, реализующихся между металлическим расплавом на никелевой основе и оксидными фазами, образующимися в ходе взаимодействия компонентов никелевых сплавов с кислородом, ранее [1] методом построения поверхностей растворимости компонентов в металле (ПРКМ) проанализированы системы Ni–С–O, Ni–Ca–O и Ni–Al–O в области температур 1500…1800 °С и при содержании никеля в этих системах более 90 %.
Для анализа реальных металлургических систем необходимо, однако, учитывать, что последовательность окисления примесей, температурный режим плавки, раскисленность никелевого расплава во многом определяются соотношением между содержащимся в нём углеродом и другими примесями. С этих позиций важную информацию о фазовых равновесиях, реализующихся в сложном металлическом расплаве на никелевой основе, можно получить, построив ПРКМ систем Ni–Al–С–O и Ni–Ca–С–O, что и стало целью настоящей работы.
При определении координат ПРКМ были совместно проанализированы все возможные реакции между никелем и растворёнными в нём кислородом, углеродом и алюминием или кальцием. В ходе расчётов использованы значения термодинамических параметров, которые ранее применялись для анализа более простых систем (табл. 1–3) [1].
На рис. 1 представлено изотермическое сечение ПРКМ системы Ni–Al–C–O при 1550 °С и суммарном давлении оксидов углерода 1 атм.
Температура сечения выбрана как одна из наиболее типичных для индустрии никелевых сплавов.
На линии a – b заданы составы металла, равновесного с газовой фазой (СО, СO 2 ) и твёрдым оксидом никеля, на линии b – c – с газовой фазой и шпинелью NiAl 2 O 4 , на линии b – e – с NiO и шпинелью, на линии c – d показаны составы металла, находящегося в равновесии с газовой фазой и корундом и, наконец, линия c – f обозначает состав, равновесный как с корундом, так и с NiAl2O4. Тонкие линии – линии равной концентрации кислорода в металлическом расплаве.
Интересно проследить, как меняются границы фазовых равновесий в этой системе при изменении температуры, а также при изменении давления оксидов углерода. Это позволяют сделать сечения диаграммы, представленные на рис. 2 и 3.
На первом из них – сечение ПРКМ системы Ni–Al–C–O при 1650 °С и суммарном давлении оксидов углерода 1 атм. Изменения, произошедшие с системой, сводятся прежде всего к смещению границ b – e и c – f в сторону несколько большего содержания алюминия в металлическом расплаве.
На рис. 3 представлено сечение этой же диаграммы при 1550 °С, но рассчитанное исходя из суммарного давления оксидов углерода, равного 0,1 атм. Сопоставление диаграмм на рис. 1 и 3 демонстрирует, что понижение давления оксидов углерода смещает межфазную границу a – b – c – d в сторону более низких концентраций углерода в жидком металле.
Таблица 1
Температурные зависимости констант равновесия реакций взаимодействия компонентов никелевого расплава
|
№ п/п |
Процесс |
Константа равновесия, K ; a – активность, мас. %; p – давление, атм |
Температурная зависимость lg K |
|
1 |
(NiO) = [Ni] + [O] |
K = a [0]j a ( NiO ) |
–10 318 / T + 5,813 |
|
2 |
|NiO| = [Ni] + [O] |
K = a [O]/ a NiO |
–12 966 / T + 7,000 |
|
3 |
{CO} = [C] + [O] |
K = a [O] a [C]/ p CO |
–5093 / T – 1,878 |
|
4 |
{CO 2 } = [C] + 2[O] |
K = a [O] a [C]/ p CO2 |
–15 433 / T + 2,852 |
|
5 |
(CaO) = [Ca] + [O] |
K = a [O] a [Ca]/ a ( CaO ) |
– 5489 / T + 3,969 |
|
6 |
|CaO| = [Ca] + [O] |
K = a [0] a [Ca] у a |CaO| |
–19 430 / T + 5,350 |
|
7 |
|Al 2 O 3 | = 2[Al] + 3[O] |
K = a 3O] a [Al] |
–63 924 / T + 21,027 |
|
8 |
|NiAl 2 O 4 | = [Ni] + 2[Al] + 4[O] |
42 K = a [O] a [Al] |
–74 480 / T + 25,805 |
Таблица 2
Температурные зависимости параметров взаимодействия в жидком никеле
|
i ej |
Температурная зависимость |
i ej |
Температурная зависимость |
|
e OO |
–41,7 / T |
Al e Al |
337 / Т |
|
e CCaa |
290 / Т |
e CC |
395 / T |
|
Al e OAl |
–82,6 / Т |
e AOl |
–139,4 / T |
|
e OCa |
–69 / T |
e COa |
–172 / Т |
|
e OC |
–160 / T |
e CO |
–120 / T |
Таблица 3
Значения энергетических параметров теории субрегулярных ионных растворов, использованные для описания системы NiO–CaO (Дж/моль)
|
NiO(1)–CaO(2) |
Q 1112 |
Q 1122 |
Q 1222 |
|
Расплав |
3272 |
–30 000 |
–41 596 |
|
Твёрдые растворы |
45 246 |
65 000 |
42 057 |
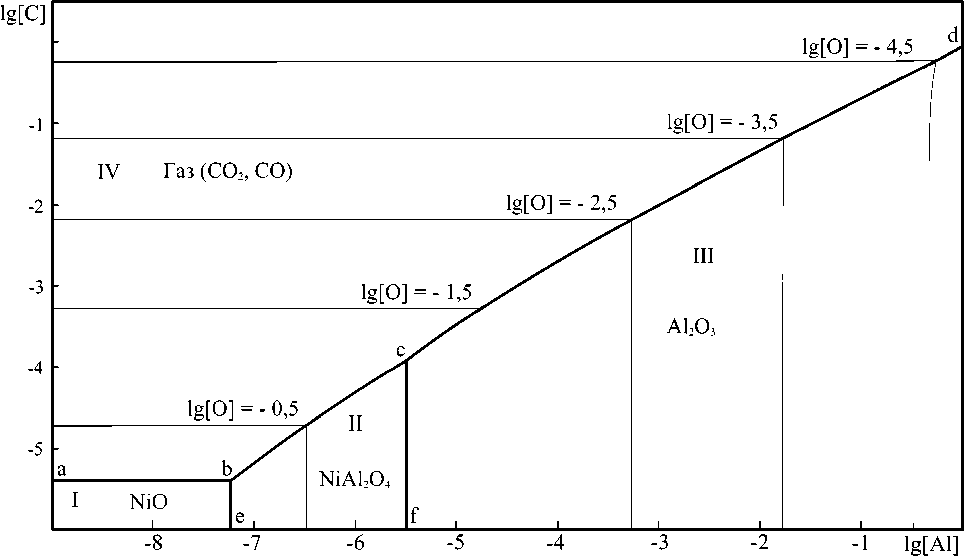
Рис. 1. Изотермический разрез ПРКМ системы Ni–Al–C–O при суммарном давлении оксидов углерода 0,1013 MПа и Т = 1550 °С
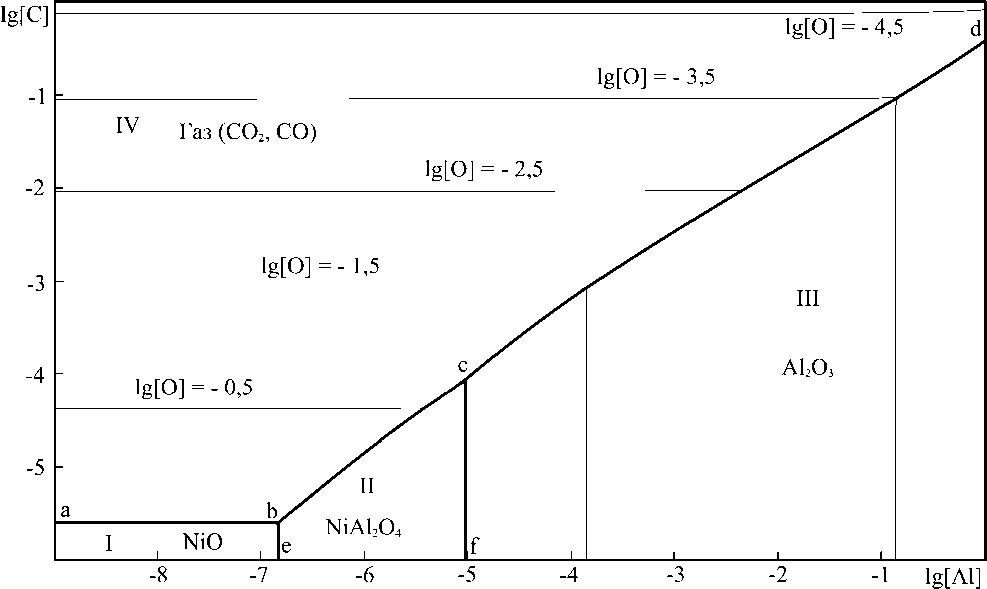
Рис. 2. Изотермический разрез ПРКМ системы Ni–Al–C–O при суммарном давлении оксидов углерода 0,1013 MПа и Т = 1650 °С
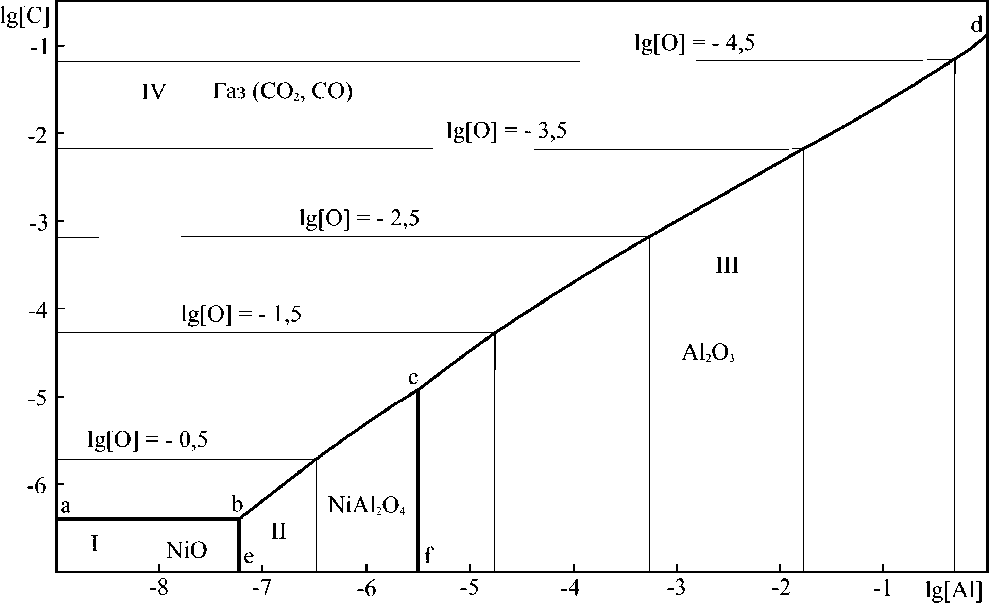
Рис. 3. Изотермический разрез ПРКМ системы Ni–Al–C–O при суммарном давлении оксидов углерода 0,01013 MПа и Т = 1550 °С
Приведённое на рис. 4 изотермическое сечение ПРКМ системы Ni–Сa–C–O при 1550 °С и суммарном давлении оксидов углерода 1 атм характеризуется наличием трёх областей фазовых равновесий. В области I при малых концентрациях углерода и кальция соответствующие составы металла находятся в равновесии с твёрдым раствором CaO в NiO. При более высоком содержании кальция металл, соответствующий составам облас- ти II, находится в равновесии с твёрдым раствором NiO в CaO. Наконец, при достаточном количестве углерода в составе металлического расплава (область III) равновесной с металлом фазой является газовая смесь оксидов углерода.
Представление о том, как меняются границы фазовых равновесий в системе Ni–Сa–C–O при изменении температуры и при изменении давления оксидов углерода, позволяют получить сече- ния диаграммы, представленные на рис. 5 и 6. Увеличение температуры (выше, чем это показано на рис. 5) согласно ПРКМ системы Ni–Ca–O приведёт к тому, что после 1720 °С и в системе Ni–Сa–C–O появится область равновесия жидкого металла с оксидным расплавом.
Построенные диаграммы позволяют объяснить состав неметаллических включений в никеле и его сплавах, проектировать процессы рафиниро- вания металлического расплава на никелевой основе и моделировать технологически необходимые фазовые равновесия.
Выводы
Посредством построения изотермических разрезов поверхностей растворимости компонентов в металле (ПРКМ) для систем Ni–Al–С–O и Ni–Ca–С–O проанализированы фазовые равновесия в этих системах. Рассчитанные координаты
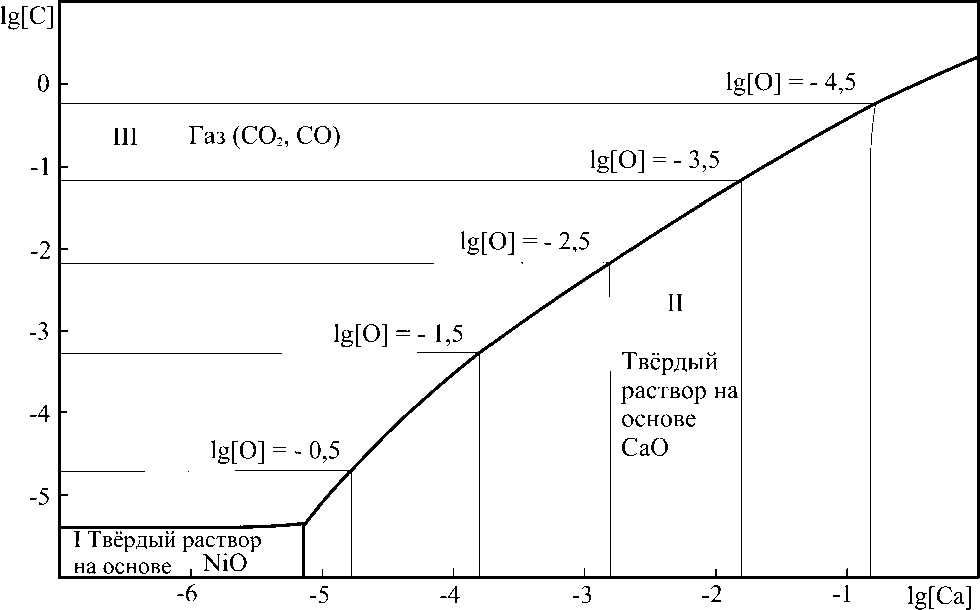
Рис. 4. Изотермический разрез ПРКМ системы Ni–Ca–C–O при суммарном давлении оксидов углерода 0,1013 MПа и Т = 1550 °С
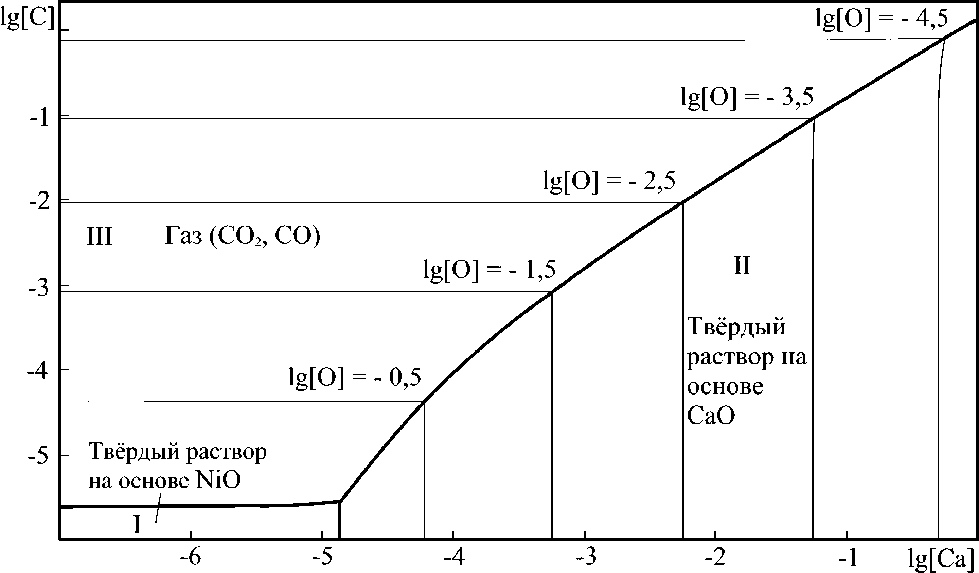
Рис. 5. Изотермический разрез ПРКМ системы Ni–Ca–C–O при суммарном давлении оксидов углерода 0,1013 MПа и Т = 1650 °С
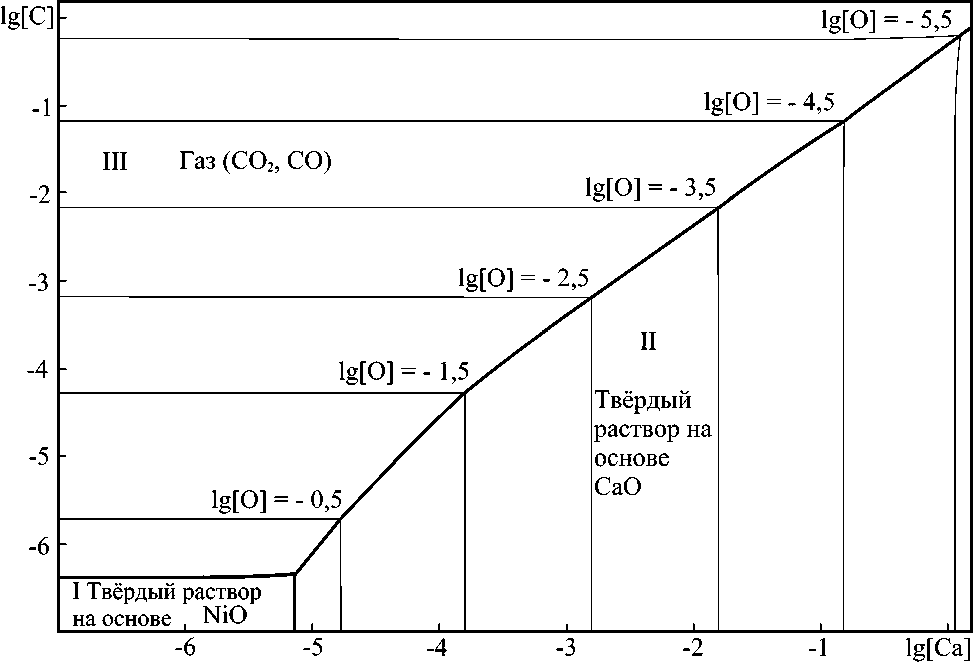
Рис. 6. Изотермический разрез ПРКМ системы Ni–Ca–C–O при суммарном давлении оксидов углерода 0,01013 MПа и Т = 1550 °С
ПРКМ могут быть использованы для анализа технологических процессов, связанных с взаимодействием кислорода, углерода, кальция и алюминия в металлическом расплаве на основе никеля.
Работа осуществлена при финансовой поддержке РФФИ, грант № 11-08-12046-офи-м-2011.
Список литературы Термодинамический анализ фазовых равновесий, реализующихся в системах Ni-Al-С-О и Ni-Ca-С-О в условиях существования жидкого металла
- Трофимов, Е.А. Анализ фазовых равновесий в системах Ni-C-O, Ni-Ca-O и Ni-Al-O в условиях существования жидкого металла/Е.А. Трофимов, Г.Г. Михайлов//Вестник ЮУрГУ. Серия «Металлургия». -2010. -Вып. 14. -№ 13 (189). -С. 4-7.


