Термодинамический анализ и фазовые равновесия в системе железо-хром-углерод
Автор: Леонович Борис Иванович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 36 (169), 2009 года.
Бесплатный доступ
С использованием подрешеточной модели проведен термодинамический анализ трехкомпонентной системы железо-хром-углерод. Результаты расчета фазовых равновесий представлены в виде изотермических сечений и фазовых диаграмм. Приведена схема фазовых превращений в этой системе в сопоставлении с бинарными системами. Рассчитаны и построены политермические разрезы с постоянным значением концентрации хрома в сплаве. Работа выполнена в соответствии с научной программой Федерального агентства по образованию - «Развитие научного потенциала высшей школы (2009-2010 гг.)», код проекта - 713 и при поддержке РФФИ, грант № 08-08-00416.
Термодинамическая модель, фазовая диаграмма, система железо-хром-углерод
Короткий адрес: https://sciup.org/147156632
IDR: 147156632 | УДК: 544.344.013
Thermodynamic analysis and phase equilibria in iron-chromium-carbon system
The thermodynamic analysis of three component system Fe-Cr-C was carried out with the use of sublattice model. The results of calculation of phase equilibria are represented by isothermal sections and phase diagrams. The scheme of phase transmutations in this system is shown with the comparison of binary systems. Polythermic sections with the constant chromium concentration in the alloy are calculated and plotted.
Текст научной статьи Термодинамический анализ и фазовые равновесия в системе железо-хром-углерод
При термодинамическом анализе фазовых равновесий в трехкомпонентной системе Fe-Cr-C, необходимо знать свойства веществ, образующихся в двухкомпонентных системах железо-хром, железо-углерод и хром-углерод.
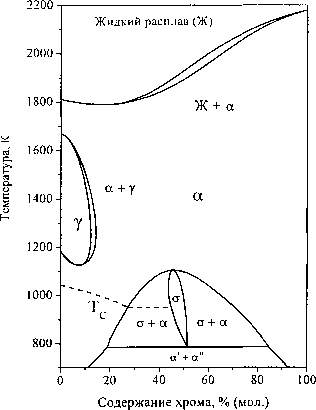
Термодинамический анализ системы железохром проведен в исследованиях [1, 2]. Установлено соответствие расчета и экспериментально определенного минимума линии ликвидуса при концентрации хрома ~17 мол. % и температуре 1516 °C. Хром стабилизирует о.ц.к. модификацию железа и образует с a-железом непрерывный ряд твердых растворов. Область твердых растворов хрома в г.ц.к. модификации железа сравнительно узкая и простирается до концентрации хрома ~14 % (мол.). Хром снижает температуру полиморфного а<^у превращения железа с 910 °C до ~850 °C при содержании хрома ~8,0 % (мол.) (рис. 1, а). При температуре ниже ^1100 К возможно образование упорядоченной сигма-фазы (а).
В системе железо-углерод в зависимости от температуры и концентрации углерода стабильными являются следующие фазы: феррит (а, 5), аустенит (у), жидкий расплав (Ж). Термодинамический расчет диаграммы состояния Fe-C выполнен в ряде исследований [3-5]. Диаграмма состояния этой системы представлена на рис. 1, б.
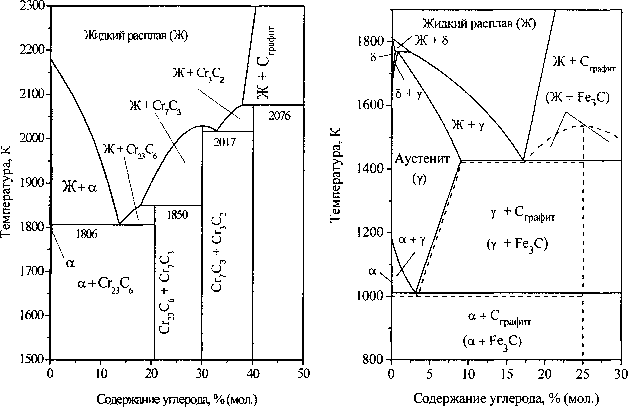
При взаимодействии хрома и углерода воз можно образование карбидов различного состава и структурного типа Сг23С6, Сг7С3 и Сг3С2. Диаграмма состояния системы хром-углерод (рис. 1, в) рассчитана по термодинамическим данным, приведенным в работе [6]. Из вида этой диаграммы следует, что в системе имеют место два эвтектических и два перитектических превращения, приводящих к выделению из жидкого расплава тугоплавких карбидов хрома различного состава.
Система железо-хром-углерод была предметом многочисленных экспериментальных и теоретических исследований [7-9]. Установлено, что в этой системе образуются трехкомпонентный жидкий раствор и тройные твердые растворы внедрения структуры о.ц.к. (феррит) и г.ц.к. (аустенит). Взаимодействие компонентов растворов приводит к образованию карбидов хрома и железа состава М3С, М7С3, М23Сб и Сг3С2, где М = Fe, Сг - компоненты металлической подрешетки.
Жидкий расплав. Молярная энергия Гиббса гомогенного трехкомпонентного сплава задается уравнением
а)
б)
Рис. 1. Диаграммы состояния двухкомпонентных систем: Fe-Cr (а), Сг-С (б), Fe-C (в)
где xt - молярные доли компонентов раствора; Ly - температурно-зависимые параметры модели, значения которых выражаются полиномами Ред-лиха-Кистера:
zv=4+4(x/-x7)+4(x/-x/)2. (2)
Парциальные молярные энергии Гиббса (химические потенциалы) могут быть вычислены по уравнению [10, 11]
из данных, приведенных в таблице. Параметры L вычисляются по формуле (2), а состав твердого раствора определяется мольными долями веществ в каждой подрешетке:
Ж = W(1 ”^с) иуРе + № = 1;
Ус = (я/фс/( 1 - ^с) и Ус + У У = 1 • (7)
В уравнении (5) в подстрочных индексах запятая разделяет компоненты в одной подрешетке, а
G,=H,=Gm + Z(4
7=2
9Gm OX,
Ч
двоеточие означает различие подрешеток.
Парциальные молярные энергии Гиббса гипо
где бу - символ Кронекера (S у = 0 при г ^ j и
тетических компонентов твердого раствора определяются следующим образом [12]:
Ьу= \ при / = у).
Значения параметров модели приведены в таблице.
О.ц.к. и г.ц.к. - твердые растворы внедрения. В таких растворах металлические вещества (железо и хром) образуют подрешетку замещения, а углерод и вакансии (V) - подрешетку внедрения. Тогда такой твердый раствор внедрения можно представить общей формулой (Сг,ГеХ(С,Р)с. В случае г.ц.к.-фазы а = с = 1, для о.ц.к.-фазы а = 1 и с = 3. Образование такого раствора можно также представить смешением гипотетических соединений СтаСс, СгаУС1 БеаСс и ¥еаУс, тогда молярная энергия Гиббса такого «четырехкомпонентного» раствора может быть задана уравнением
^т - УСгУу^СгУ + УСтУс^Сг.С + УреУу^РеУ +
+У?еУсСУ.С + ЯЛа(Ж 111 Ж + Уре 1п Ж ) +
+c(yc\nyc+yv\nyv) + G”6 +G^, (4)
где
^ ' ~ УСтУУе^Ус^СхУе.С + Уу^СхУеУ ) +
+УуУс (УСх^СхУР + У¥е^¥е;У,С )• (^)
Слагаемое G^ определяет магнитную составляющую энергии Гиббса. Её определение следует
Gij =6^+—— + —-- Ук"КГ ^У; дуу к=Сху^еу ^Ук
где i и j - элементы замещения и внедрения соответственно. Парциальные величины реальных компонентов определятся следующим образом:
Gj = GiV; Gc = G,c - С,.у.
Карбидные фазы. В трехкомпонентной системе железо-хром-углерод возможно образование смешанных карбидов стехиометрического состава различного структурного типа. Замещающие металлические элементы (железо и хром) в этих карбидах образуют одну или более подрешеток, в которых все вакантные междоузлия (вакансии) заполняются углеродом. Так что подрешетка внедрения является комплектной, а концентрация элемента внедрения (углерода) равна единице (ус = 1)-
Энергии Гиббса карбидов с одной металлической подрешеткой (хромзамещенный цементит (Сг,Ге)3С, (Сг,Ге)7С3, Сг3С2) определятся выра жением
^т ~ УСх^СхУ + Тге^Ре.С + ^1а(уСт 1п уСг +
+Ж 111 Уре )] + ЖМг,Г=:С - (9) где а - стехиометрический коэффициент элементов металлической подрешетки.
|
Фаза |
Параметр, Дж/моль |
Примеч. |
|
1 |
2 |
3 |
|
Жидкий расплав (Ж) |
С“(ж) - отграфит) =!! 7369 _ 24,637 G^ - G^°yK) = 24335> 93 -11,427 + 2,37615 • 10"2177 G^1 -Я2°98 =-16459 + 335,618-7-5071п7 G^ - G^f' = 12040,17 - 6,558437 - 3,6751551 ■ 10"2177 С°р - ^298 = -10839,7 + 291,3027 - 467 In 7 Z°Y =-90526-25,9117 Z1^ = 80000 Z^r = 80000 £^ж' =-124320 + 28,57 Z^e = 19300 Z^ =49260-197 L°^e =-14550 + 6,657 ^CAFe =-516700 4$,Fe = 75500 Z^Fe = 47310 |
T<2180K 7>2180 T<1811 7>1811 |
|
О.ц.к. -твердый раствор (а, 5); а=15 с=3 |
G^ - Я2°98 = -8851,93 +157,487 - 26,90871n7 -
G^K) - Я298 = -25384,451 + 299,312557 - 467 In 7 +2,2960305 -IO317"9 G^K) -G^ -зс^^афит) = 416000 V-zF.K-z VzF. V V уоСоцк) _GO(OUK) _зсо(графит) = 322050 +75,667 7 1C.V XV. V V/ Z Z® = -1907 Y™Ky =-1907 ^cr+e-v =20500-9,687 ^cr+e-c = -1750000 + 9407 G^ =7?71п(р + 1)/(т) . 1 Г . 79 158 ( 1 ,Y T4 T10 t16 Y тЛ|_ 140/2 497^ 2 45 200 J J 1 Гт"5 t"15 t"25 1 f ( т ) —------- Л|_ 10 315 1500 J , 518 Г 790 ( 1 ^1 1125[_ 497 J J p = 0,4 |
T<2180 7>2180 T<1811 7>1811 T<1 T>1 |
Окончание таблицы
|
1 |
2 |
3 |
|
Тс = -311,5_Усг +1043yFe + уСг>>ре[1650 + 550(jCr - yFe)] Р = -0,008^Сг + 2,22^ре - 0,85yCr_yFe |
||
|
_____ При отрицательных величинах Тс и Р, их значения следует поделить на -1 |
||
|
Г.ц.к. -твердый раствор (у); 0=1, с=\ |
G^ -G^0"^ = 7284 +0,163 Т G^ - G^ = -1462,4 + 8,2827 -1,157 In 7 + 6,4 ■ 10"4 72 G*™' - Я298 = -27098,266 + 300,252567 - 467 In 7 + 2,78854 • 10317"9 G°^ -G^ -б°(графит) = 25000 Gf^k) - С£№ - с^^афит) = 77207 -15,8777 L^.c = -26586-187 Z^v =-29686-187 ^=-34671 L^N =10833-7,4777 ®v = 14Ю |
|
|
(Fe,Cr)3C |
Gp^ - Я298 = -10745 + 706,047 -120,67 In 7 G°(M3C) -з^оС™») „^(графит) = -39744-18 087 Z^c =29260-16.637 |
|
|
(Fe,Cr)7C3 |
С^?Сз1 - Я298 = -209752 + 980,297 -170,57 In 7 - 0,069092172 GO(M7C3) _7(3о(оцк) _зсо(графит) = 113385-78,377 ZCr+e:C =-Ю465 |
|
|
(Fe,Cr)23C6 |
G^c6^-H^s =-521983 + 3622,247-620,9657 In 7-0,12643172 G^!6 1=20/ 23G“(r^3c6} + з / 23Gp^e23c6} Gp^23P6) = 20/23С“^2зСб) +3/23С°^33гСб) re.иг. u re.re.u cr.ur.v Gp^S?61 - 23 / 3Gp^3C) + 5 / зс°(графит) = 66920 - 407 ге.ге.и те.с с Тс™ Fe с = -252350 + 80,47 сг,ге.сг,г с. с ’ |
|
|
Cr3C2 |
°сУсС2) -Я2°98 =-103719+ 496,83477-84,34967In7-0,032709572 |
|
|
Сигма-фаза (о) |
Gv^crc, -22G°(°UK) -8GplruK) =92300-95,967 Л V.X-zI.VzI V-/1 А С GfeCrPe -4GiyuK)-8Gp<™K) + 18Gp•0',к, =117300-95,967 ГС.Сх.ГС JT V JL V |
|
|
С графит |
Отграфит) _ Ho^ = -17369 +170,737 - 24,371n7 - 4,723 • 10"4 72 + + 25626007’1 - 2,643 • 108 7-2 +1,2 ■ 1010 7"3 | |
|
Для карбида состава (Cr,Fe)23C6 установлено наличие двух металлических подрешеток, в которых располагаются совместно атомы хрома и железа. Общей формулой такого карбида является (Cr,Fe)20(Cr,Fe)3C6. Такое разделение металлов по двум подрешеткам (5 и t) позволяет представить энергию Гиббса такой системы уравнением
Gm= У Ст УСт^Сг.Сг.С + УСгУре^СгТе:С +
+УРеУСг^Ре:Сг:С + УРеУРе^РеТе^ +
+^ Л20(Усг In Усг + УРе !п Уре ) + ХУст b Усг + +Уре hl Уре )] + УсгУре (УСг^Сг,Ре:Сг:С +Уре^€г,Ре:Ре:с) + +УСгУре (УСг^Сг:Сг,Ре:С + Уре^Ре:Сг,Ре:С ) +
+УСгУРеУСгУРе^Сг,Ре:Сг,Ре:С • (10)
В этой формуле G£r.Fe.c и GFe:Cr:C определяются через энергии Гиббса подрешеток, содержащих разноименные металлы
23Gcr:Fe:C “ 20^Cr:Cr:C + ^^Fe:Fe:C ’ ^ ^
23GFe:Cr;C = 20GFe;Fe;C + 3GCr:Cr:C.
Парциальные молярные энергии гипотетических «компонентов» можно рассчитать по формуле
Gab.c =Gm Hl-Z^^Va-J^f ^-I Sy А ) V^b )
При использовании значении параметров модели (см. таблицу) будем иметь
^Cr:Fe:C ” ^Cr:Fe:C + ЖЖ (^Cr:Cr:C “ ^Cr:Fe:C “
~^Fe:Cr:C + ^Fe:Fe:C ) + 20 RT Ь yCr + 3RT Ь JFe +
"^УСтУре^УСт + У^е ”^ЖЖ)^Cr,Fe:Cr,Fe:C>
^Fe:Cr:C = ^Fe:Cr:C + ЖЖ (^Cr:Cr:C "^CrFe.C ~
—^Fe:Cr:C + C:Fe:C ) + 20 RT b Ж + 3^ThyCr +
+ЖЖ(Ж + Ж ”^УсхУ^^Сх^е^
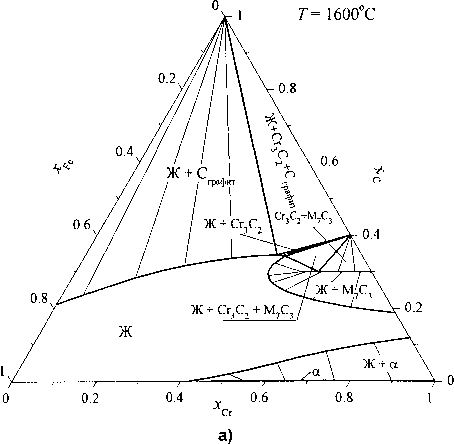
Графическая зависимость результатов расчета по полученным соотношениям представлена на рис. 2 в виде изотермических сечений и фазовых диаграмм металлического сплава в интервале температур 1600... 1000 °C. Из приведенных графических зависимостей следует, что при 1600 °C первично кристаллизующимся металлом является низкоуглеродистый феррит. Расплав, насыщенный углеродом, кристаллизуется с образованием карбида хрома Сг3С2 либо (Ге, Сг)7С3, что приводит к наличию двух трехфазных равновесий Ж + Сг3С2 +СграфИТ и Ж + М7С3 +Сг3С2. При уменьшении температуры до 1597 °C реализуется нонва-риантное равновесие
Ж + Сг3С2<=± МПС3 + С^афщ..
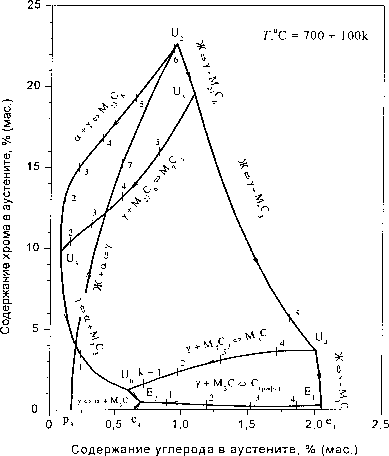
Комплекс фаз, образующихся при кристаллизации жидкого расплава, графически представлен на рис. 3, б линиями трехфазного равновесия с участием
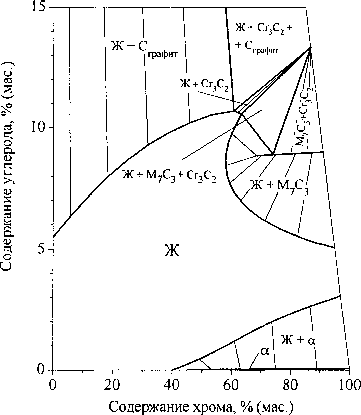
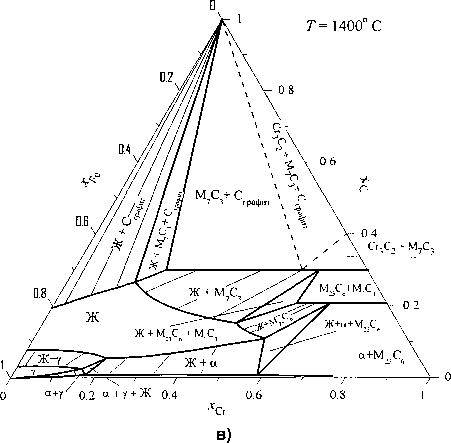
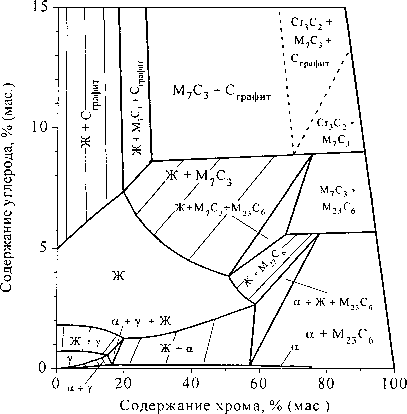
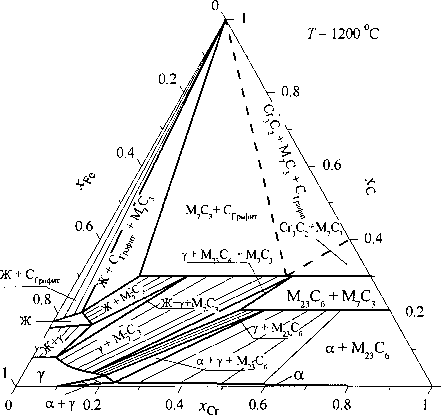
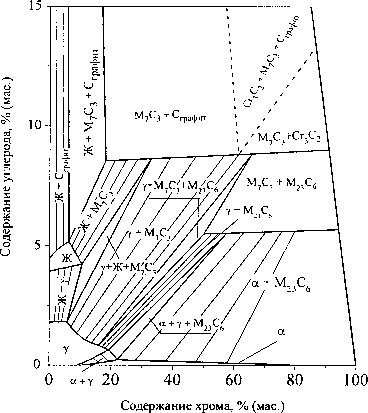
Рис. 2. Изотермические сечения и фазовые диаграммы металлического сплава системы железо-хром-углерод при температуре 1600(а, б), 1400 (в, г), 1200 (д, е), 1000 (ж, з)
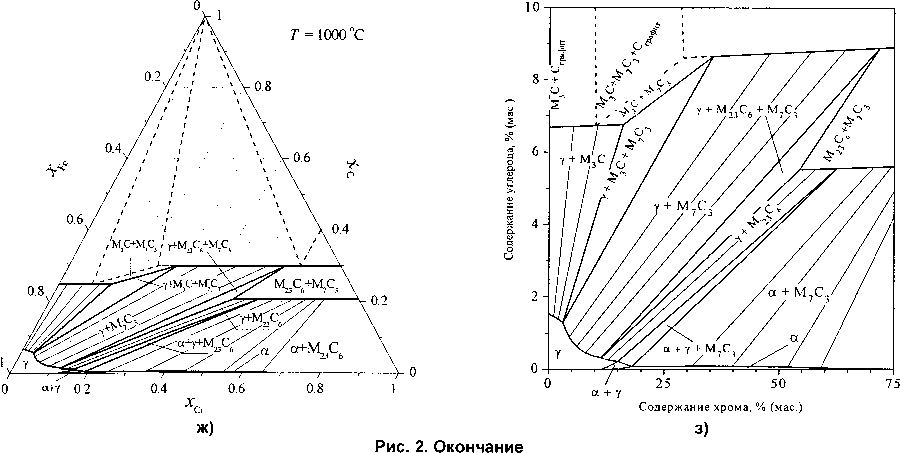
а)
Рис. 3. Диаграммы трехфазных равновесий с участием аустенита (а) и жидкого сплава (б)
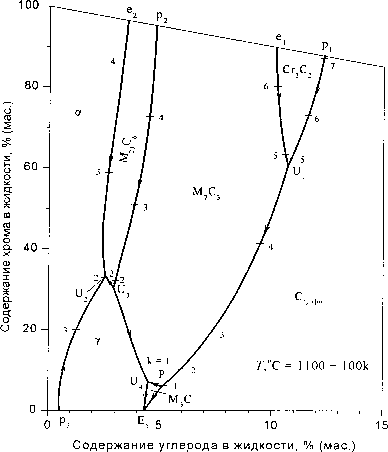
б)
О
С - Сг
С - Cr - Fe
С - Fe
Cr - Fe
|
1803 °C |
Pi |
|
Ж + Сгр |
СгЗС2 |
|
1597 |
Ж + СгЗС2 о М7СЗ + Сгр |
U1 |
|
1744 |
ei |
|
ЖоСг7СЗ + СгЗС2 |
|
Ж <-» Сгр + Сг23С6
Cr3C2 + M7C3 + Сгр
Ж + М7СЗ + Сгр
а + у + М23С6
Ж + у + М7СЗ
" у + М7СЗ + МЗС
у + М23С6 + М7СЗ
у + а + М7СЗ
Ж + а<-»у+М23С6
Ж + М23С6оу+М7СЗ
Ж + М7СЗ + МЗС
Ж+М7СЗоу + МЗС
Ж + у + МЗС
у+М23С6оа + М7СЗ
и2
Ж + у + М23С6
Ж + М7СЗ + Сгр о МЗС

Ж + МЗС + Сгр
Жоу + МЗС + Сгр

и5
а + М23С6 + М7СЗ
у + МЗСоа + М7СЗ
и6
а + ст + М23С6
МЗС + М7СЗ + а
у + а + МЗС
у + МЗС + Сгр
у <-> а + МЗС + Сгр

|
1495 |
е2 |
|
|
Ж + 6<- |
у |
|
|
1154 |
Сз |
|
Ж = у |
+ Сгр |
Вестник ЮУрГУ, № 36, 2009
а + МЗС + Сгр
|
658 |
МЗС о а + М7СЗ + Сгр |
Е3 ' |
а + М7СЗ + Сгр
МЗС + М7СЗ + Сгр
а(Сг)+ ст + М23С6
а(Ре) + ст + М23С6
|
512 |
аГСг) + a(Fe) + ст + М23С6 |
D |
а(Сг) + а(Ре) + ст + М23С6
Рис. 4. Схема фазовых превращений в системе железо-хром-углерод
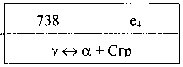
е5
ст <-» а(Сг) + а(Ре)
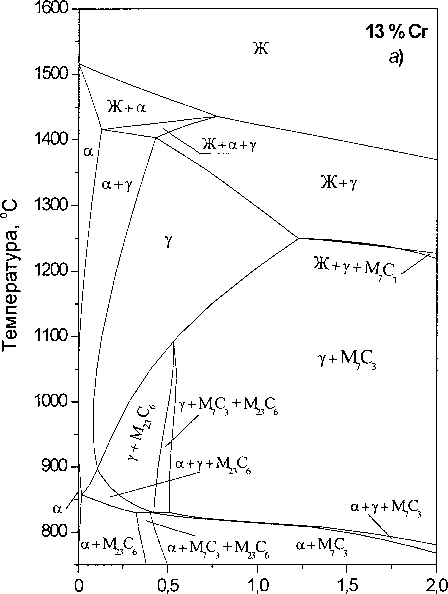
Содержание углерода, % (мае.)
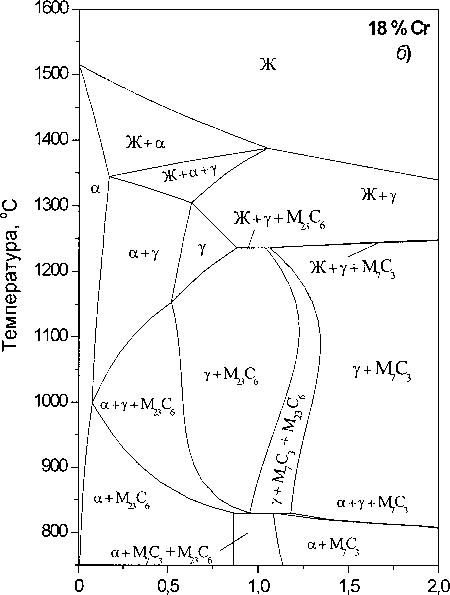
Содержание углерода, % (мае.)
Рис. 5. Политермические разрезы диаграммы состояния системы Fe-Cr-C при содержании хрома в металле 13%(а) и 18 % (6)
жидкости. Области между кривыми определяются как политермические поверхности растворимости компонентов в расплаве, равновесном с одной из кристаллизующихся фаз.
При температуре 1400 °C (рис. 2, в, г) и небольших концентрациях хрома первично кристаллизующимся металлом будет аустенит. Возможно также образование карбида М2зС6 в равновесии с жидким расплавом или ферритом. Дальнейшее снижение температуры приводит к расширению концентрационных пределов устойчивости аустенита и трансформации, равновесных с металлом, карбидов. Фазовые превращения с участием аустенита графически представлены на рис. 3, а. Координаты точек пересечения кривых определяют температуры и концентрации компонентов нонва-риантных превращений с участием г.ц.к.-фазы (аустенита).
Совокупность фазовых превращений в сопоставлении с реакциями в бинарных системах представлена на рис. 4.
На изотермических сечениях при заданной концентрации одного из компонентов можно установить последовательность фазовых превращений и определить количественные соотношения равновесных фаз. Однако наиболее представительными и удобными для анализа являются политермические разрезы при постоянной концентрации одного из компонентов. На рис. 5 приведены такие политермические сечения, соответствующие содер жанию хрома в металлическом сплаве 13 и 18% (по массе) и различной концентрации углерода.
Выводы. Проведен термодинамический анализ и изучены фазовые равновесия в трехкомпонентной системе железо-хром-углерод. Рассчитаны и построены изотермические сечения в интервале температур 1600... 1000 °C. Приведена графическая зависимость проекции поверхности ликвидуса и диаграмма трехфазных равновесий с участием аустенита. Результаты расчета представлены также в виде политермических разрезов с постоянным содержанием хрома в металле.
Работа выполнена в соответствии с научной программой Федерального агентства по образованию - «Развитие научного потенциала высшей школы (2009-2010 гг.)», код проекта - 713 и при поддержке РФФИ, грант № 08-08-00416.
Список литературы Термодинамический анализ и фазовые равновесия в системе железо-хром-углерод
- Andersson J.-O. Thermodynamic Properties of the Cr-Fe System/J.-O. Andersson, B. Sundman//CALPHAD. 1987. V. 11, № 1. P. 83-92.
- Taylor J.R. A Thermodynamic Assessment of the Cr-Fe-O System/J.R. Taylor, A.T. Dinsdale//Z. Metallkd. 1993. V. 84, № 5. P. 335-345.
- Chipman J. Thermodynamics and Phase Diagram of the Fe-C System/J. Chipman//Metallurg. Trans. A. 1972. V. 3, № 1. P. 55-64.
- Chicco B. Experimental Determination of the Austenitic + Liquid Phase Boundaries of the Fe-C System/В. Chicco, W.R. Thorpe//Metallurg. Trans. A. 1982. V. 13A, № 7. P. 1293-1297.
- Agren J. The Thermodynamic Analysis of the Fe-C and Fe-N Phase Diagrams/J. Agren//Metallurg. Trans. A. 1979. V. 10A, № 12. P. 1847-1852.
- Andersson J.-O. Thermodynamic Properties of Cr-C/J.-O. Andersson//CALPHAD. 1987. V. 11, № 2. P. 271-276.
- Carbon -Chromium -Iron/A. Bondar, V. Ivanchenko, A. Kozlow, J.-C. Tedenac//MSIT, London-Bornstein. New Series IV/11D2 -P. 72.
- Hillert M. A Thermodynamic Assessment of the Fe-Cr-Ni-C System/M. Hillert, С. Qiu//Metallurg. Trans. A. 1991. V. 22A, № 10. P. 2187-2196.
- Andersson J.-O. A Thermodynamic Evaluation of the Fe-Cr-C System/J.-O. Andersson//Metallurg. Trans. A. 1988. V. 19A, № 3. P. 627-636.
- Люпис К. Химическая термодинамика материалов/К. Люпис; пер. с англ. под ред. Н.А. Ватолина, А.Я. Стомахина. М.: Металлургия, 1989. 503 с.
- Морачевский А.Г. Термодинамика расплавленных металлических и солевых систем/А.Г. Морачевский. М.: Металлургия, 1987. 240 с.
- Sundman B.J. A Regular Solution Model for Phases with Several Components and Sublattices, Suitable for Computer Applications/B. Sundman, J. Agren//Phys. Chem. Solids. 1981. V. 42. P. 297-301.
- Sundman B. The Sublattice Model/B. Sundman, J. Agren//Mat. Res. Soc. Symp. Proc. 1983. V. 19. P. 115-127.


