Термодинамический анализ процессов взаимодействия в системе Cu-Ni-S-0 в условиях существования медного расплава
Автор: Трофимов Евгений Алексеевич, Михайлов Геннадий Георгиевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 14 (147), 2009 года.
Бесплатный доступ
Посредством термодинамических расчётов построена ПРКМ системы Cu-Ni-S-O, которая может быть использована для анализа имеющихся литературных данных, а также для анализа технологических процессов, связанных с взаимодействием серы и никеля с кислородом в медном расплаве.
Медный расплав, сера, никель, кислород, термодинамические расчёты
Короткий адрес: https://sciup.org/147156612
IDR: 147156612 | УДК: 669.33+541.123
Thermodynamic analysis of the processes of the interaction in the Cu-Ni-S-0 system in the condition of copper melt existence
Using the thermodynamic calculations, the surface of components solubility in metal melt for the Cu-Ni-S-O system was plotted. The plotted surface can be used for analysis of technological processes related to interaction of oxygen with sulphur and nickel in copper melt.
Текст научной статьи Термодинамический анализ процессов взаимодействия в системе Cu-Ni-S-0 в условиях существования медного расплава
Для пирометаллургических процессов, связанных с производством меди, характерны сложные равновесия с участием шлаков, штейнов, расплавленной металлической фазы и газа. Поэтому проведение термодинамического анализа системы Cu-Ni-S-O, в частности, методом построения поверхностей растворимости компонентов в металле, может иметь большое практическое значение.
В ходе работы были построены изотермические разрезы ПРКМ системы Cu-Ni-S-O для температур 1100, 1200 и 1300 °C.
При этих температурах в системе отсутствуют трёх- и четырёхэлементные соединения. Легкоплавкие сульфиды никеля не могут быть основой твёрдой фазы, равновесной с расплавленной медью.
Таким образом, в интервале температур 11001300 °C равновесными с медным расплавом конденсированными фазами могут быть твёрдые NiO, Cu2O, Cu2S, а также оксидно-сульфидный расплав на основе Си2О и сульфидно-оксидный расплав на основе сульфидов меди и никеля. Уравнения, описывающие реакции взаимодействия между этими фазами, а также температурные зависимости констант равновесия этих реакций, приведены в табл. 1. Температурные зависимости параметров взаимодействия первого порядка для растворенных в жидкой меди никеля, серы и кислорода приведены в табл. 2.
Большая часть значений, приведённых в табл. 1 и 2, заимствована из работ [1-5], другие рассчи
таны с использованием данных, приведённых в этих работах.
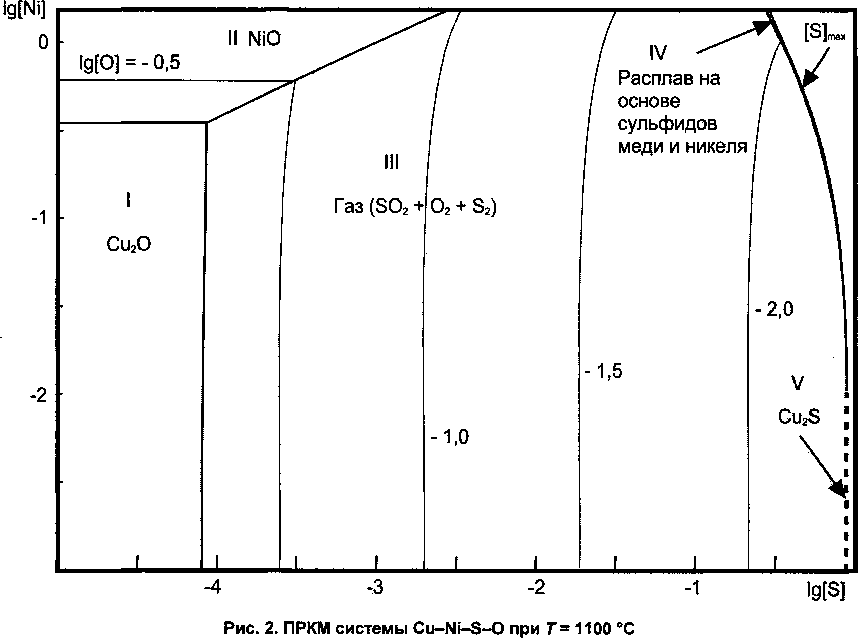
На рис. 1 представлен изотермический концентрационный тетраэдр системы Cu-Ni-S-O для температуры 1100 °C. Поверхность, нарисованная контрастными линиями, - это поверхность растворимости никеля, серы и кислорода в жидкой меди. Здесь она представлена условно. Её точные координаты приведены на рис. 2. Контрастными линиями на этом рисунке показаны границы равновесных с жидким металлом неметаллических фаз. Тонкими - линии равных концентраций кислорода в металле.
В области I определены составы металла, равновесного с твердым купритом, в области II - с твердым оксидом никеля, в области V - с Cu2S, а в области IV - с неметаллическим расплавом на основе сульфидов меди и никеля. Наконец, в области III, при низких концентрациях никеля в металлической меди и, соответственно, при небольшом его содержании в составе неметаллических фаз определены составы металла, находящегося в равновесии с газом, преобладающей составляющей которого является SO2 (кроме него в составе газа присутствуют О2 и S2). Положение границ области III с другими областями зависит от давления компонентов газовой фазы. Представленная на рис. 2 диаграмма (как и диаграммы на рис. 3 и 4) рассчитана исходя из общего давления газа в системе, равного одной атмосфере.
Таблица 1
Температурные зависимости констант равновесия процессов взаимодействия в системе Cu-Ni-S-0
|
№ |
Процесс |
Выражение для константы равновесия |
Температурная зависимость, IgA? (давление - МПа, концентрация - мае. %) |
|
1 |
(Cu2O) = 2Си + [О] |
^ = а[О] * а(Си2О) |
-3140/7+2,250 |
|
2 |
/Си2О/= 2Cu + [О] |
К = а[о] |
-6500 / 7 + 4,468 |
|
3 |
(Cu2S) = 2Cu + [S] |
^ = «[S]/^Cu2S) |
-1924 / 7+1,201 |
|
4 |
/Cu2S/ = 2Cu+[S] |
-2514 / 7+ 1,622 |
|
|
5 |
(NiO) = [Ni] + [О] |
^ = ^[Oj^fNi] ^(NiO) |
-7156/7+5,178 |
|
6 |
/NiO/= [Ni] + [О] |
К = а[°]аМ |
-9803/7+6,365 |
|
7 |
{SO2} = [S] + 2 [О] |
= a[o]a[s]/7(so2) |
-6520 / 7 + 0,996 |
|
8 |
0,5{02} = [0] |
^ = W<) |
4451/7-0,336 |
|
9 |
0,5{S2} = [S] |
^=“1+^) |
6247 / 7- 0,686 |
Таблица 2
Параметры взаимодействия первого порядка в жидкой меди для системы Cu-Ni-S-0
|
Параметры и |
Температурные зависимости (А / Т + В) |
4 |
А/7+В |
4 |
А/7+В |
|
ео |
-630/7+0,327 |
-124/7 |
eNi |
-130/7 |
|
|
es |
-1154/7+0,664 |
-248/7 |
es |
-135/7 |
|
|
е№ |
63/7 |
-38/7 |
eNi |
-249 IT |
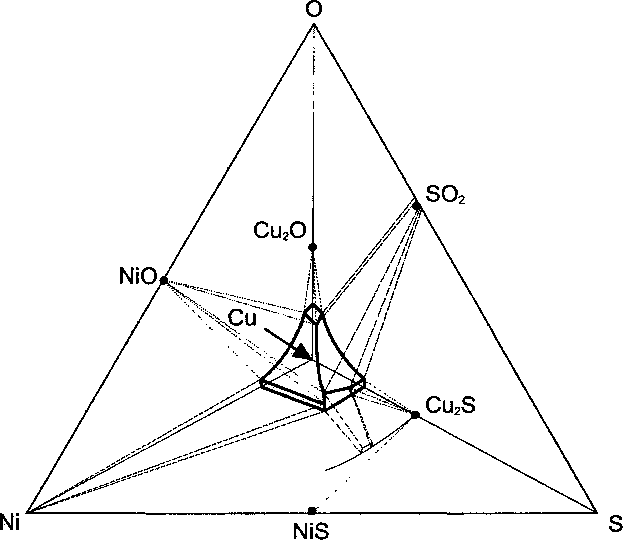
Рис. 1. Схема фазовых равновесий в системе Cu-Ni-S-О при Т= 1100 °C
Трофимов Е.А., Михайлов Г.Г. Термодинамический анализ процессов взаимодействия в системе Cu-Ni-S-O в условиях существования медного расплава
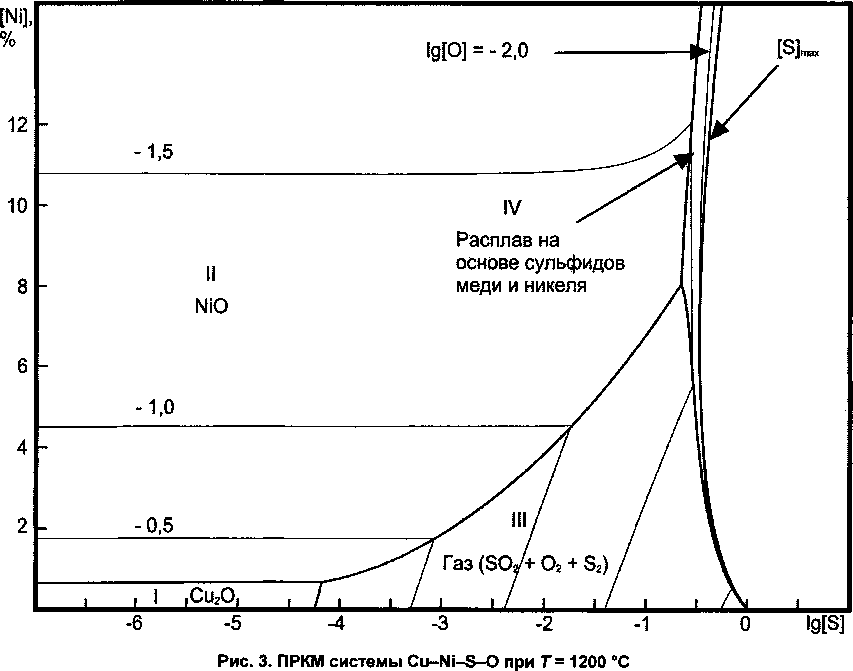
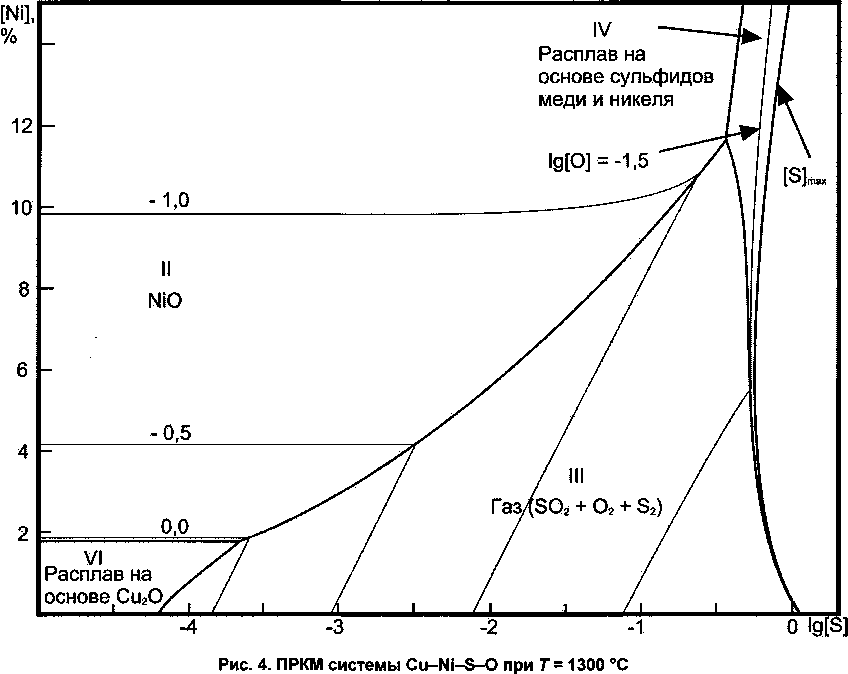
С повышением температуры картина фазовых равновесий в системе меняется. При Т = 1129 °C Cu2S плавится и область V сливается с областью ГУ. На рис. 3 представлен разрез изученной системы для Т = 1200 °C. При высоких концентрациях серы и низких - никеля металл может находиться в равновесии с расплавом сульфидов и оксидов, преобладающим компонентом которого является Cu2S. В ходе дальнейшего повышения температуры исчезает (при Т = 1242 °C) еще одна твердая оксидная фаза - Си2О. ПРКМ системы при Т = 1300 °C представлена на рис. 4. С металлом при этой температуре могут быть сопряжены четыре фазы: в области VI - оксидный (с небольшой примесью сульфидов) расплав, в области II - твердый NiO, в области IV - сульфидный (с примесью оксидов) расплав и в области III - газ.
Заключение
Посредством термодинамических расчётов построены изотермические сечения поверхности растворимости компонентов в металле для системы Cu-Ni-S-O, демонстрирующие, как количественные изменения в составах медного расплава и взаимодействующего с ним газа связаны с качественными изменениями в составе равновесных, сложных, конденсированных фаз. Результаты ра боты могут быть использованы для анализа технологических процессов производства и рафинирования меди, а также сплавов на её основе.
Работа проведена по научной программе Федерального агентства по образованию - «Развитие научного потенциала высшей школы (2009-2010 годы)», код проекта - 375 и при поддержке РФФИ, грант № 07-08-00365.
Список литературы Термодинамический анализ процессов взаимодействия в системе Cu-Ni-S-0 в условиях существования медного расплава
- Пичугин, Б.А. Влияние компонентов на растворимость кислорода в литейных бронзах/Б.А. Пичугин, Л.И. Гофеншефер, В.И. Рыжов//Литейное производство. -1977. -№10.-С. 16.
- Куликов, И.С. Раскисление металлов/И.С. Куликов -М.: Металлургия, 1975. -504 с.
- Козлов, В.А., Рафинирование меди/В.А. Козлов, С.С. Набойченко, Б.H. Смирнов -М.: Металлургия, 1992. -268 с.
- Чурсин, В.М. Плавка медных сплавов (Физико-химические и технологические основы)/В.М. Чурсин -М.: Металлургия, 1982. -152 с.
- Туркдоган, Е.Т. Физическая химия высокотемпературных процессов/Е.Т. Туркдоган; пер. с англ. Ю.И. Уточкина и В.И. Симонова. -М.: Металлургия, 1985. -344 с.


