Термодинамический анализ процессов взаимодействия в системе Cu-Zr-O, реализующихся в условиях существования медного расплава
Автор: Самойлова Ольга Владимировна, Михайлов Геннадий Георгиевич, Макровец Лариса Александровна, Трофимов Евгений Алексеевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 4 т.14, 2014 года.
Бесплатный доступ
Выполнено термодинамическое моделирование процессов взаимодействия циркония и кислорода, растворенных в жидкой меди. Установлено, что компоненты системы Cu 2O-ZrO 2 сопряжены с жидким металлическим расплавом в системе Cu-Zr-O. С использованием данных о температурах и теплотах плавления оксидов Cu 2O и ZrO 2, а также положений субрегулярных ионных растворов и совершенных ионных растворов определены координаты линии ликвидус диаграммы состояния системы Cu 2O-ZrO 2. Расчет активностей оксида меди и оксида циркония показал, что и в области существования оксидного расплава имеют отрицательное отклонение от закона Рауля. Для интервала температур 1100-1300 °С построена поверхность растворимости компонентов в металле (ПРКМ) системы Cu-Zr-O. В ходе моделирования установлена температурная зависимость параметра взаимодействия первого порядка по Вагнеру в медном расплаве. Определены составы металлического расплава, равновесного с чистыми твердыми оксидами Cu 2O и ZrO 2, а также составы металлического расплава, равновесного с оксидным расплавом. Также определены линии трехфазных равновесий («жидкий металл - оксидный расплав - твердый оксид Cu 2O»; «жидкий металл - оксидный расплав - твердый оксид ZrO 2»; «жидкий металл - твердый оксид Cu 2O - твердый оксид ZrO 2») и точка четырехфазного равновесия «жидкий металл - оксидный расплав - твердый оксид Cu 2O - твердый оксид ZrO 2». На ПРКМ нанесены изотермы растворимости кислорода в жидкой меди и определен максимум раскислительной способности циркония. Установлена высокая раскислительная способность циркония в расплавах на основе меди.
Система cu-zr-o, термодинамическое моделирование, поверхность растворимости компонентов в металле, расплавы на основе меди
Короткий адрес: https://sciup.org/147156891
IDR: 147156891 | УДК: 669.33
Thermodynamic analysis of interaction processes in the Cu-Zr-O system realized in liquid copper melt
Thermodynamic modeling of interaction processes of zirconium and oxygen dissolved in liquid copper melt was done. It was found that the components of Cu 2O-ZrO 2 system are conjugated with liquid metal melt in Cu-Zr-O system. The coordinates of a liquidus line of the Cu 2O-ZrO 2 diagram were determined using the mel¬ting temperature data and the heat of fusion data about Cu 2O and ZrO 2 oxides as well as the theory of perfect ionic solutions and subregular ionic solutions. The calculations of activities of Cu 2O and ZrO 2 in the oxide melt showed that and have negative deviation from Raoult’s law in the range of oxide melts existence. The surface of component solubility in metals melts (SCSM) of Cu-Zr-O system was constructed for the temperature range from 1100 to 1300 °С. The temperature dependence of the interaction parameter of liquid copper was determined during SCSM thermodynamic modeling. The compositions of metals melt in equilibrium with pure solid Cu 2O and ZrO 2 oxides and in equilibrium with oxides melt were determined. The lines of three-phase equilibria (“liquid metal - oxide melt - pure solid Cu 2O oxide”; “liquid metal - oxide melt - pure solid ZrO 2 oxide”; “liquid metal - pure solid Cu 2O oxide - pure solid ZrO 2 oxide”) were calculated. The point of the four-phase equilibrium “liquid metal - oxide melt - pure solid Cu 2O oxide - pure solid ZrO 2 oxide” was set. The isotherms of oxygen solubility in liquid copper were plotted in the SCSM. The maximum of the deoxi¬dizing ability of zirconium in liquid copper was defined. High deoxidizing ability of zirconium in liquid copper melt was defined.
Текст научной статьи Термодинамический анализ процессов взаимодействия в системе Cu-Zr-O, реализующихся в условиях существования медного расплава
Цирконий используется при плавке алюминиевых, хромистых бронз как модификатор, улучшающий свойства медных сплавов (например, жаропрочность). Также цирконий рекомендуется использовать при раскислении медноникелевых сплавов [1]. В литературе вопрос о термодинамике процессов взаимодействия, происходящих в системе Cu–Zr–O, практически не освещен. Целью данного исследования является термодинамический анализ системы Cu–Zr–O, выполненный с применением построения поверхности растворимости компонентов в металле (ПРКМ).
Методика термодинамического моделирования подробно изложена в монографии [2] и включает в себя: 1) расчет линий ликвидус оксидных диаграмм состояния с выбором модели, описывающей оксидный шлаковый расплав, находящийся в сопряжении с металлическим; 2) расчёт ПРКМ с использованием данных об оксидном шлаковом расплаве, о константах равновесия взаимодействия элементов в металлическом расплаве и данных о параметрах взаимодействия элементов в металлическом расплаве.
Сведения по диаграмме состояния системы Cu 2 O–ZrO 2 в литературе практически отсутствуют. Только в работе A.M.M. Gadalla и J. White [3] представлен фрагмент этой диаграммы, включающий точку эвтектики, положение которой характеризуется следующими данными: 7,35 мас. % ZrO2 и 1130 °С (рис. 1).
Для термодинамического моделирования оксидной системы в настоящей работе использовались приближения теории совершенных ионных растворов и теории субрегулярных ионных растворов. В качестве исходных данных использовались сведения о температурах и теплотах плавления чистых компонентов системы (табл. 1). Расчет с использованием теории совершенных ионных растворов позволил получить следующее положение точки эвтектики: 5,35 мас. % ZrO2 и 1223 °С (рис. 1, табл. 2). Существенная разница между рассчитанной и экспериментально определённой температурами точки эвтектики продиктовала необходимость использования более сложной модели. В качестве такой модели использовано приближение теории субрегулярных ионных растворов. Наилучший набор энергетических параметров теории Q , а также координаты точки эвтектики, которые эта модель позволила получить, представлены в табл. 2. Результаты расчёта линий ликвидус диаграммы состояния системы Cu2O–ZrO2 в сравнении с литературными данными показаны на рис. 1.
Для оценки адекватности проведенного термодинамического моделирования по теории субрегулярных ионных растворов с использованием полученных значений параметров теории Q были рассчитаны активности компонентов оксидного расплава a (Cu O) и a (ZrO ) . Результаты представлены на рис. 2. Расчет проведён только для концен-
Рис. 1. Результаты моделирования линии ликвидус диаграммы состояния системы Cu 2 O–ZrO 2 : сплошная линия – по теории субрегулярных ионных растворов; пунктир – по теории совершенных ионных растворов. Литературные данные A.M.M. Gadalla и J. White [3] нанесены штрихпунктиром. Римскими цифрами обозначены равновесные составы фаз, используемые при расчете
Таблица 1
Координаты точки эвтектики и энергетические параметры теории субрегулярных ионных растворов
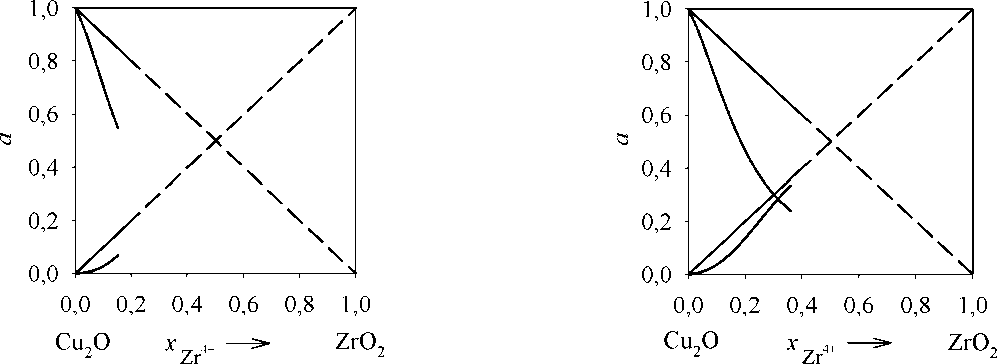
Данные о температурах и теплотах плавления веществ
|
Вещество |
o Tm , С |
Δ mH o o , Дж/моль T m |
Источник |
|
Cu 2 O |
1242 |
64 300 |
[4] |
|
ZrO 2 |
2680 |
86 944 |
[5] |
Таблица 2
|
Методика моделирования |
Резу л ьт ат ы ра счё та к оо рд и н а т т оч ки э вт ек т и ки |
Энергетические параметры теории субрегулярных ионных растворов |
||
|
Q 1112 , Дж/моль |
Q 1122 , Дж/моль |
Q 1222, Дж/моль |
||
|
Теория совершенных ионных растворов |
5, 35 мас . % ZrO 2 ; 1223 °С |
— |
— |
— |
|
Теория субрегулярных ионных растворов |
16 ,0 6 ма с. % ZrO 2 ; 1135 °С |
–39940 |
+18590 |
–29628 |
а) б)
Рис. 2. Зависимость активностей компонентов оксидного расплава (Cu2O, ZrO2) от состава: а) T = 1500 °С; б) T = 2000 °С. Расчёт по теории субрегулярных ионных растворов траций, при которых существует оксидный расплав. В этих интервалах a(Cu O) и a(ZrO ) характе- ризуются отрицательными отклонениями от закона Рауля.
Для построения ПРКМ необходимы сведения о константах равновесия реакций в исследуемой системе. Реакции, протекающие в медном расплаве системы Cu–Zr–O, и константы равновесия этих реакций приведены в табл. 3. Константы равновесия реакций с образованием компонентов шлакового расплава ( K ж ) и с образованием чистых твердых компонентов ( K тв) из компонентов металлического расплава связаны между собой через теплоту плавления A m H О о и температуру плавления T m
Tm чистого твердого компонента
1g K ж = 1g K тв - 1g K пл ;
оо
A m H 70 A m H то
1g K =-- m - +------ m- .
пл 2,3 ■ R ■ T 2,3 ■ R ■ T m
Здесь R – универсальная газовая постоянная; K пл – константа равновесия перехода твердого вещества в жидкое состояние.
Следует отметить, что компоненты шлакового расплава пишутся в круглых скобках, компоненты металлического расплава – в квадратных, а чистые твердые вещества указываются в прямых скобках.
Для моделирования ПРКМ необходимы также и сведения о параметрах взаимодействия компонентов в медном расплаве. Экспериментальные данные о значении параметра взаимодействия eOZr в жидкой меди в литературе не встречаются. В справочнике И.С. Куликова [7] этот параметр оценивается расчетным методом по эмпирической формуле, в результате чего параметр eOZr оказался равен –300 при 1473 К. Однако эмпирическая формула была выведена для разбавленных растворов на основе железа и при расчете разбавленных растворов на основе меди может давать значительную погрешность. В ходе расчета ПРКМ системы Cu–Zr–O в данной работе имелась возможность оценить значение этого параметра, исходя из термодинамики процессов взаимодействия кислорода и циркония, растворенных в медном расплаве. Согласно проведенному термодинамическому моделированию значение параметра eOZr равно –0,17 при 1473 К. Зависимость значений данного параметра от температуры приведена в табл. 4.
Для параметра e ZZrr в литературе данных не имеется. Однако значение этого параметра можно оценить, используя данные по активности циркония в медном расплаве для температуры 1673 К [9]. Для этого использовано соотношение
Zr = 1g a zr - 1g [ Zr, мас.% ]
Zr [ Zr, мас.% ]
.
Согласно расчету по литературным данным параметр e ZZrr равен –0,841 при 1673 К. Зависимость значений данного параметра от температуры приведена в табл. 4.
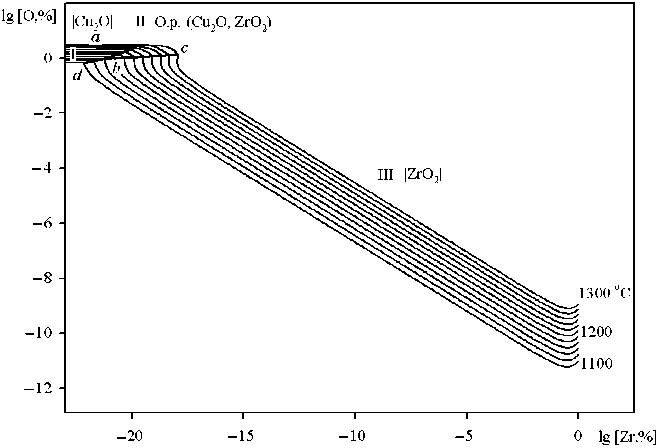
Результаты моделирования ПРКМ для системы Cu–Zr–O приведены на рис. 3. Линия a–b задает составы металлического расплава, равновесного с чистым твёрдым Cu2O и оксидным расплавом (Cu 2 O, ZrO 2 ). Линия b–c задает составы металлического расплава, равновесного с чистым твёрдым ZrO2 и оксидным расплавом (Cu2O, ZrO2). С увеличением температуры эта линия уходит в сторону больших концентраций циркония в металле. Линия b – d задает составы металлического расплава, равновесного с чистым твердым оксидом меди и чистым твердым оксидом циркония. В точке b в равновесии с металлическим расплавом находятся оксидный расплав, чистый твердый оксид меди и чистый твердый оксид циркония. В области I заданы составы металла, равновесного с чистым твер-
Таблица 3
Константы равновесия процессов взаимодействия медного расплава и сопряжённых фаз (lg K = A / T + B )
|
Уравнение реакции |
A |
B |
Источник |
|
(Cu 2 O) = 2 [Cu]+ [O] |
–3141 |
2,251 |
[6] |
|
(ZrO 2 ) = [Zr] + 2 [O] |
–41999 |
8,956 |
Данная работа |
|
|Cu 2 O| = 2 [Cu] + [O] |
–6500 |
4,468 |
[6] |
|
|ZrO 2 | = [Zr] + 2 [O] |
–46540 |
10,494 |
[7] |
Параметры взаимодействия первого порядка в медном расплаве e i j
Таблица 4
|
j i |
O |
Zr |
|
O |
- 630 + 0,327 [8] |
250 (данная работа) |
|
Zr |
1425 —— (данная работа) |
- 14^ [9] |
а)
б)
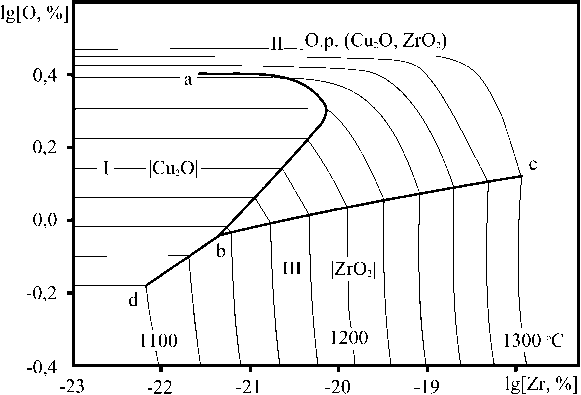
Рис. 3. ПРКМ системы Cu–Zr–O (в логарифмических координатах) для интервала температур 1100–1300 °С: а) общий вид; б) увеличенный фрагмент части с высоким содержанием кислорода
дым Cu2 O; с увеличением концентрации циркония концентрация растворенно го в меди кислорода остается практически неизменной. В области II заданы составы металла, равновесного с оксидным расплавом; концентрация растворенного в меди кислорода незначительно уменьшается с увелич е нием концентрации циркония. В области III зад аны сос тавы металла, равновесного с чистым тве рдым ZrO2 ; концентрация растворенного в меди кислорода резко уменьшается с увеличением с о держания циркония в металле. Таким образом, цирконий является сильным раскислителем для меди, что говорит также и о высокой возм ожно сти угара этого легирующего компонента. В о б ласти III концентрация растворенного в меди к и слорода уменьшается на несколько порядков от [О] ~ 10–1 до 10–11 мас. %. Даже при концентр ации
[Zr] = 10–10 мас. % в равновесии с металлом будет находиться чистый твердый оксид циркония. Максимальной раскислительной способности цирконий достигает при концентрации в 0,33 мас. %. Дальнейшие добавки циркония не приводят к уменьшению содержания кислорода.
Выводы
Впервые построена диаграмма раскислитель-ной способности циркония в жидкой меди. Результаты моделирования (в частности, построенная ПРКМ) демонстрируют высокую раскислительную способность циркония в меди. Даже при очень малых концентрациях циркония в медном расплаве, содержащем кислород, образование оксида меди термодинамически маловероятно. Такое свойство системы Cu–Zr–O необходимо учитывать при легировании медных сплавов цирконием. Для исключения потерь циркония при введении его в металлический медный расплав последний должен быть предельно раскислен.
Работа осуществлена при финансовой поддержке РФФИ, грант № 13-03-00534.
Список литературы Термодинамический анализ процессов взаимодействия в системе Cu-Zr-O, реализующихся в условиях существования медного расплава
- Производство отливок из сплавов цветных металлов: учеб. для вузов/А.В. Курдюмов, М.В. Пикунов, В.М. Чурсин, Е.Л. Бибиков. -М.: Металлургия, 1986. -416 с.
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. -М.: Издат. Дом МИСиС, 2009. -520 с.
- Gadalla, A.M.M. Equilibrium relationships in the system CuO-Cu2O-ZrO2/A.M.M. Gadalla, J. White//Transactions of the British Ceramic Society. -1966. -Vol. 65, no. 7. -P. 383-390.
- Химическая энциклопедия: в 5 т./под ред. И.Л. Кнунянца. -М.: Сов. энцикл. -1990. -Т. 2 -671 с.
- Кубашевский, О. Металлургическая термохимия/О. Кубашевский, С.Б. Олкокк. -М.: Металлургия, 1982. -392 с.
- Трофимов, Е.А. Взаимодействие никеля с кислородом в жидкой меди/Е.А. Трофимов, Г.Г. Михайлов//Известия вузов. Цветная металлургия. -2002. -№ 2. -С. 10-13.
- Куликов, И.С. Раскисление металлов/И.С. Куликов. -М.: Металлургия, 1975. -504 с.
- Линчевский, Б.В. Термодинамика и кинетика взаимодействия газов с жидкими металлами/Б.В. Линчевский. -М.: Металлургия, 1986. -222 с.
- Gierlotka, W. Thermodynamic description of the binary Cu-Zr system/W. Gierlotka, K.-Ch. Zhang, Y.-P. Chang//Journal of Alloys and Compounds. -2011. -Vol. 509. -P. 8313-8318.


