Термодинамический анализ системы хром-никель-азот
Автор: Леонович Б.И., Гусинская К.С.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 13 (189), 2010 года.
Бесплатный доступ
С использованием подрешеточной модели проведен термодинамический анализ трехкомпонентной системы хром-никель-азот. Результаты расчета равновесных состояний системы представлены в виде изотермических сечений и фазовых диаграмм. Рассчитаны и построены политермические разрезы фазовых диаграмм с постоянным значением концентрации хрома и активности азота в сплаве.
Термодинамическая модель, фазовая диаграмма, система хром -никель - азот
Короткий адрес: https://sciup.org/147156640
IDR: 147156640 | УДК: 541.123
Thermodynamic analysis of the chromium-nickel-nitrogen system
Using sublattice model the thermodynamic analysis of the chromium-nickel-nitrogen system was carried out. The results of calculation are represented by isothermal sections and phase diagrams. Polythermic sections of phase diagrams with the constant meaning of chromium concentration in the alloy are calculated and plotted.
Текст научной статьи Термодинамический анализ системы хром-никель-азот
Никельхромовые сплавы являются основой жаростойких и жаропрочных сплавов. Специфические свойства этих сплавов в значительной степени определяются содержанием в них азота. Повышенное содержание азота в расплаве в процессе охлаждения и кристаллизации металла приводит к образованию нитридных и карбонитридных включений, которые могут оказывать значительное влияние на размер зерна, снижать окалиностой-кость, пластичность и живучесть сплавов, а в случае неблагоприятной формы и расположения могут служить причиной хрупкого разрушения металла. Поэтому экспериментальное и теоретическое исследование образования равновесных фаз в этих сплавах, и в частности определение взаимной растворимости компонентов в этих сплавах, имеет первостепенное значение.
При термодинамическом описании металлических сплавов, содержащих азот, использована модель регулярного раствора Хиллерта-Стеффан-сона [1], которая может быть применима к системам Мх-М1-^, содержащим два растворителя Мх и М2 с образованием раствора замещения и одно вещество N, образующее растворы внедрения. Таким образом, вакансии V в подрешетке внедрения рассматриваются как дополнительный компонент системы.
При термодинамическом анализе фазовых равновесий в трехкомпонентной системе Cr-Ni-N необходимо знать свойства веществ, образующихся в двухкомпонентных системах хром-никель, хром-азот и никель-азот. Диаграмма состояния двухкомпонентной системы хром-никель приведена в исследовании [2] (рис. 1, а). Данная система характеризуется наличием в твердом состоянии двухфазной области у + а. В сплавах системы Me-N возможно образование твердых растворов и фаз внедрения е гексагональной структуры на основе химического соединения Me2N (рис. 1, б, в). Система хром-азот характеризуется образованием нестехиометрического нитрида хрома структуры г.ц.к. [2, 3].
Система хром-никель-азот была предметом многочисленных экспериментальных и теоретических исследований [2-4]. Установлено, что в этой системе образуются трехкомпонентный жидкий раствор и тройные твердые растворы внедрения структуры о.ц.к. (а), г.ц.к. (у) и г.п.у. (s). Взаимодействие компонентов растворов приводит к образованию нитрида хрома нестехиометрического состава (Cr, Ni)N.
Жидкий расплав. Молярная энергия Гиббса гомогенного трехкомпонентного сплава задается уравнением
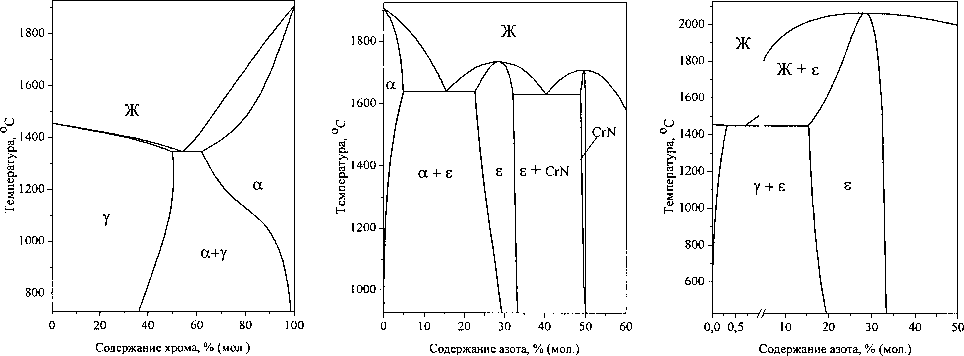
Рис. 1. Диаграммы состояния двухкомпонентных систем Cr-Ni (a), Cr-N (б) и Ni-N (в)
Gm " хСг^Сг + xN^N + xNi^Ni + ^ПхСг lnxCr +
+xN hl XN + XNi In XNi) + XCrXNi 4cr,Ni + хСгхнДзг,Н + +xNxNiZN?Ni +*сгхнХм(хсг^да +xNZ^rjNNi + xNi^Cr,N,Ni)’ (1)
где X, - молярные доли компонентов раствора; Gf - энергия Гиббса чистого компонента; R - универсальная газовая постоянная; Т - абсолютная температура; Ту - температурно-зависимые параметры модели, значения которых выражали полиномами Редлиха-Кистера
Ту^Е^-ХуТ . (2)
и=0
Парциальные молярные энергии Гиббса (химические потенциалы) могут быть вычислены по уравнению [5]:
з
Ц,=Ст + £(бУ
>2
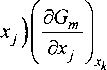
где Ьу - символ Кронекера ( Ьу = 0 при г * j и 5у=1 при г = /).
Твердые растворы внедрения (а, у, s) и CrN. В таких растворах металлические вещества (никель и хром) образуют подрешетку замещения, а азот и вакансии V - подрешетку внедрения. Тогда такой твердый раствор внедрения можно представить общей формулой (Cr,Ni)a(N, Р)с. Образование такого раствора можно представить смешением гипотетических соединений JaNc, AaVc, В^с и BaVc, а молярную энергию Гиббса такого «четырехкомпонентного» раствора - уравнением
Gm = УСтУу^гУ + УСгУм^СгН + ЖТг^№Г +
+У№Ун^№к + ^Wcr In УСг + Ум In УМ) + +c(yN lnyN + Уу ln>) + G®6,(4)
где
Gm = УСгУм (Ун^Сг,№:Н + Уг^Сг,№:К ) +
+Уг Ум (УСг^СгМУ + Ум^М:ИУ )•
Параметры L вычисляются по формуле (2), а состав твердого раствора определяется мольными долями веществ в каждой подрешетке:
Усг = W(1 -^n) И №+Усг= 1;(6)
№ = (a/c>N/(l -xN) и № +ук= 1,(7)
где а и с числа межузельных промежутков в металлической подрешетке. Их значения приведены в таблице.
В уравнении (4) в подстрочных индексах запятая разделяет компоненты в одной подрешетке, а двоеточие означает различие подрешеток.
Парциальные молярные энергии Гиббса гипо тетических компонентов твердого раствора определяются по формуле [7, 8]:
с -с 1 ^Gm । v ^Gm
^Ут ^У) ^=Cr,Ni,N,K ^Ук где i и / - элементы замещения и внедрения соответственно. Парциальные величины реальных компонентов определяются следующим образом:
Gi = Giy » ^N = Gi:M ” Giy • л-фаза. В трехкомпонентной системе хром-никель-азот при температурах менее 1200 °C возможно образование химического соединения стехиометрического состава Cr12j8Ni7j2N4. Молярная энергия Гиббса образования этого химического соединения может быть представлена формулой
Gm = Ум^СгМгК + ^’ 2ЛТ(уСг In уСг + JNi Ь yNj) .
Термохимические данные и температурнозависимые параметры модели, необходимые для расчета, получены при оптимизации экспериментальных данных и приведены в таблице [2, 3].
Графические зависимости результатов расчета по полученным соотношениям представлены на
Параметры модели при расчете системы хром-никель-азот*, Дж/моль
|
Фаза |
Параметр |
Примечание |
|
Жидкая фаза (Ж) |
С^ж) = G^ +16 414,686 -9,39ПТ— 3,82318-10"2177 |
Т< 1455 |
|
С^ж) =Я^98-9549,775 +268,5987-43,1 Лп7 |
Г> 1455 |
|
|
L^ = -1276-5,38737 |
||
|
|
||
|
=14 981 |
||
|
го(ж) --йОДОО bCr,Ni,N |
||
|
Раствор -о.ц.к. (а) (а=1; с=3) |
с^оцк) = G^ + 8715,084-3,5567 |
|
|
G^K) = G^ +3/20^ +200 000+2007 |
||
|
L*^)y =21 310-13,65827 |
||
|
Z^k = 25 800-7,89277 |
||
|
Раствор -г.ц.к. (у), включая CrN ^а=\; с=1) |
G^ruK) =17^98-5179,159+ 117,8547-22,09671n7-0,004840772 |
К 1455 |
|
G“'rllK) = 7/298- 27 098,655 + 279,1357--43,171n7 + 1,12753995-10317-9 |
Т> 1455 |
|
|
G^K> = G^ + 1/20^ + 38 680 + 143,097--10,971n7 + 0,0043872 |
||
|
7^, =8347- 12,10387 |
||
|
=29 895-16,38387 |
||
|
£сда+ =-661 270 + 3057 |
||
|
Раствор -г.п.у. (е) (а=1; с=0,5) |
G^ = G^^ + 1046 + 1,2557 |
|
|
G*^) = G^K) + 1/4G^™^ - 4409 + 72,937- 7,3671n7 + 0,0061472 |
||
|
<",&<-1443 |
||
|
Фазал |
G“^rN = 12,8С^ГОЦК) +7,2G°(™K) +2G^- 651 800 + 3167 |
|
|
Газ |
^ге^ = Я2°98 - 7358,85 + 17,20037- 16,369971n7--6,5Ю7-10^72-3,ОО971О"873 + 563 0707-1 |
* Термохимические данные для системы хром - азот приведены в работе [б].
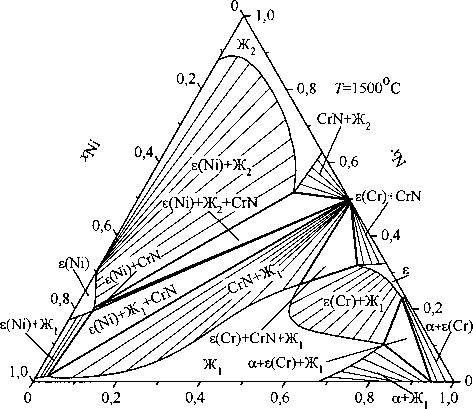
рис. 2 в виде изотермических сечений в интервале температур 1500... 1000 °C. Откуда следует, что при 1500 °C (рис. 2, а) первично кристаллизующими фазами в этой системе будут твердые растворы a, s(Cr), s(Ni) и химическое соединение CrN. При небольших содержаниях хрома металлический сплав может сосуществовать с кристаллической фазой внедрения e(Ni) либо нитридом хрома; средним содержаниям хрома отвечает гомогенный жидкий расплав. В сплавах, обогащенных хромом, первично кристаллизующейся фазой является феррит.
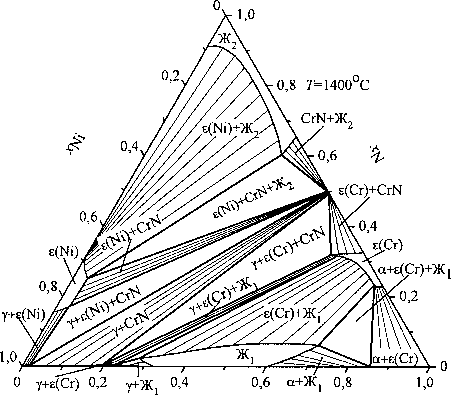
При снижении температуры до 1400 °C (рис. 2, б) область жидкого расплава значительно уменьша ется, а при небольших концентрациях хрома те же фазы равновесны аустениту. При этом изменяется также состав и количество равновесных неметаллических фаз.
Комплекс фаз, образующихся при кристаллизации жидкого расплава, графически представлен на рис. 3 линиями трехфазного равновесия с участием жидкости. Области между кривыми определяются как политермические поверхности растворимости компонентов в расплаве, равновесном с одной из кристаллизующихся фаз. Для данной системы характерно наличие четырех нонвариантных равновесий с участием металлического расплава.
Сг
б)
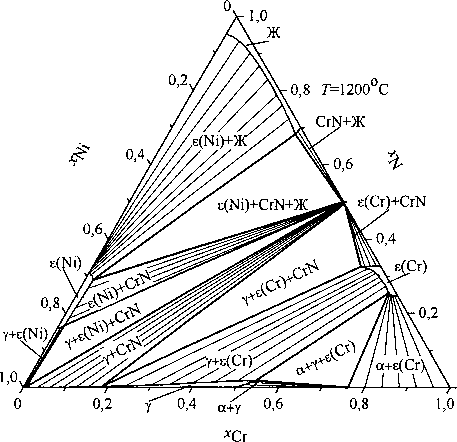
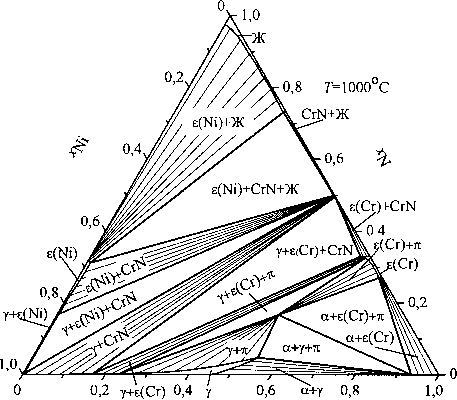
Рис. 2. Изотермические сечения системы хром - никель - азот при температуре, °C: 1500 (а), 1400 (б), 1200 (в), 1000 (г)
*Сг
Изотермическое сечение при 1200 °C (рис. 2, в) характеризуется отсутствием жидкого расплава и значительной протяженностью кривой двухфазного равновесия у + CrN, а снижение температуры приводит к образованию тройного химического соединения тг-фазы (рис. 2, г).
На изотермических сечениях при заданной концентрации одного из компонентов можно установить последовательность фазовых превращений и определить количественные соотношения равновесных фаз. Однако наиболее представительными и удобными для анализа являются политермиче-ские разрезы при постоянной концентрации одного из компонентов. На рис. 4 приведено такое по-литермическое сечение, соответствующее общему содержанию хрома в системе 20% (по массе). Графическая зависимость позволяет установить последовательность образования равновесных фаз в исследованной системе при охлаждении жидкого расплава.
Выводы. Проведен термодинамический анализ и изучены фазовые равновесия в трехкомпонентной системе хром - никель - азот. Рассчитаны и построены изотермические сечения в интервале температур 1000... 1600 °C. Рассчитана проекция поверхности ликвидуса и установлен комплекс первично кристаллизующихся фаз. Результаты расчета представлены также в виде политермиче-ских разрезов с постоянным содержанием хрома и одинаковым значением активности азота в системе.
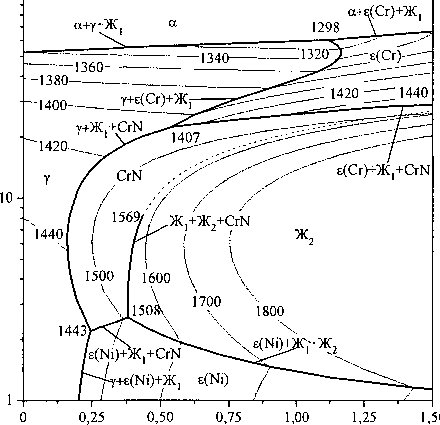
Содержание азота в жидкости, % мае.
Рис. 3. Диаграмма трехфазных равновесий с участием жидкого сплава
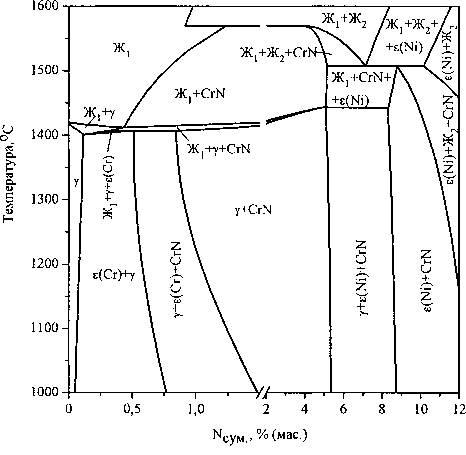
Рис. 4. Политермический разрез диаграммы состояния системы хром - никель - азот при общем содержании хрома в системе 20 % (по массе)
Список литературы Термодинамический анализ системы хром-никель-азот
- Hillert, М. The Regular Solution Model for Stoichiometric Phases and Ionic Melts./M. Hillert, L.I. Staffanson//Acta Chem. Scand. -1970. -Vol. 24, №10.-P. 3618-3626.
- Frisk, K. A Thermodynamic Evaluation of the Cr-Fe-Ni-N System/K. Frisk//Z. Metallkunde. -1991. -Bd. 82, H 2. -S. 108-117.
- Frisk, K. A Thermodynamic Evolution of the Cr-N, Fe-N, Mo-N and Cr-Mo -N System/K. Frisk//CALPHAD. -1991. -V. 15, № 1. -P. 79-106.
- Tschiptschin, A.P. Predicting Microstructure Development During High Temperature Nitriding of Martensitic Stainless Steels Using Thermodynamic Modeling/A.P. Tschiptschin//Materials Research -2002. -Vol. 5, № 3. -P.257-262.
- Люпис, К. Химическая термодинамика материалов: пер. с англ./К. Люпис; под ред. Н.А. Ватолина, А.Я. Стомахина. -М.: Металлургия, 1989. -503 с.
- Леонович, Б.И. Термодинамический анализ системы железо -хром -азот/Б.И. Леонович, Б.В. Ощепков//Вестник ЮУрГУ. Серия «Металлургия». -2009. -Вып. 12. -№14. -С. 21-26
- Sundman, В. A Regular Solution Model for Phases with Several Components and Sublattices, Suitable for Computer Applications/B. Sundman, J. Agren//Phys. Chem. Solids. -1981. -Vol. 42. -P. 297-301.
- Sundman, B. The Sublattice Model/B. Sundman, J.Agren//Mat. Res. Soc. Symp. Proc. -1983. -Vol. 19.-P. 115-127.


