Термодинамический анализ системы железо-хромазот
Автор: Леонович Б.И., Ощепков Борис Владимирович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 14 (147), 2009 года.
Бесплатный доступ
С использованием подрешеточной модели проведен термодинамический анализ трехкомпонентной системы железо-хром-азот. Результаты расчета равновесных состояний системы представлены в виде изотермических сечений и фазовых диаграмм. Рассчитаны и построены политермические разрезы с постоянным значением концентрации хрома и активности азота в сплаве.
Термодинамическая модель, фазовая диаграмма, система железо-хром-азот
Короткий адрес: https://sciup.org/147156613
IDR: 147156613 | УДК: 541
Thermodynamic analysis of the iron-chromiumnitrogen system
The thermodynamic analysis of three component system Fe-Cr-N was carried out with the use of sublattice model. The results of calculation of system equilibrium are represented as isothermal sections and phase diagrams. The scheme of phase transmutations in this system is shown with the comparison of binary systems. Polythermal sections with the constant value of chromium concentration in the alloy are calculated and plotted.
Текст научной статьи Термодинамический анализ системы железо-хромазот
Железохромовые сплавы являются основой жаростойких и жаропрочных сплавов. Специфические свойства этих сплавов в значительной степени определяются содержанием в них азота. Повышенное содержание азота в расплаве в процессе охлаждения и кристаллизации металла приводит к образованию нитридных и карбонитридных включений, которые могут оказывать значительное влияние на размер зерна, снижать окалиностой-кость, пластичность и живучесть сплавов, а в случае неблагоприятной формы и расположения могут служить причиной хрупкого разрушения металла. Поэтому экспериментальное и теоретическое исследования образования равновесных фаз в этих сплавах и, в частности, определение взаимной растворимости компонентов в этих сплавах имеет первостепенное значение.
При термодинамическом описании металлических сплавов, содержащих азот, использована модель регулярного раствора Хиллерта - Стеф-фансона [1], которая может быть применима к системам M1-M2-N, содержащим два растворителя (Mi и М^ с образованием раствора замещения, и одно вещество (N), образующее растворы внедрения. Таким образом, вакансии (Г) в подрешетке внедрения рассматриваются как дополнительный компонент системы.
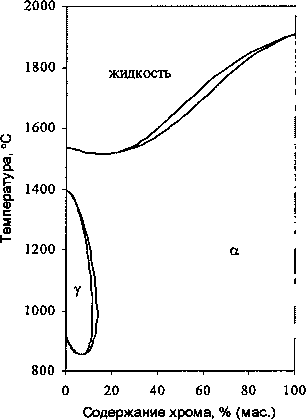
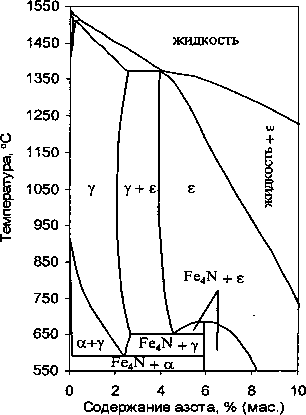
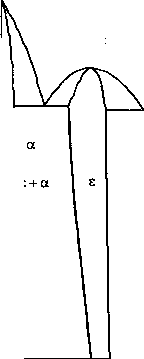
При термодинамическом анализе фазовых равновесий в трехкомпонентной системе Fe-Cr-N, необходимо знать свойства веществ, образующихся в двухкомпонентных системах железо - хром, железо-азот и хром-азот. Термодинамический анализ системы железо-хром проведен в исследовании [2] (рис. 1, а). Данная система характеризуется наличием в твердом состоянии двухфазной области у + а. В сплавах системы Ме-^ возможно образование твердых растворов и фаз внедрения £ гексагональной структуры на основе химического соединения Ме^ (рис. 1,6, в). Система хром -азот характеризуется образованием нестехиометрического нитрида хрома структуры г.ц.к. [3,4].
Система железо-хром-азот была предметом многочисленных экспериментальных и теоретических исследований [5-7]. Установлено, что в этой системе образуются трехкомпонентный жидкий раствор и тройные твердые растворы внедрения структуры о.ц.к. (а), г.ц.к. (у) и г.п.у. (с). Взаимодействие компонентов растворов приводит к образованию нитрида хрома нестехиометрического состава (Сг, Fe)Ni_x.
Жидкий расплав. Молярная энергия Гиббса гомогенного трехкомпонентного сплава задается уравнением
Gm = хСг^Сг + xFe^Fe + xN^N + ^^(хСг ^Х^ +
+xFe lnxFe +xN hxN)+xCrxFeZCr Fe +
+xCrxNZCrN +xFexNZFe>N +xCrxFexN x
x(xCr^Cr,Fe,N + xFe^Cr,Fe,N + xN^Cr,Fe,N). (1)
где x, - молярные доли компонентов раствора; G° - энергия Гиббса чистого компонента; R -
жидкость
1800 -
1600 -
1400 -
1200 -
e + CrN
CrN
0 10 20
Содержание азота, % (мае.)
в)
Рис. 1. Диаграммы состояния двухкомпонентных систем Fe-Cr (a), Fe-N (б) и Cr-N (в)
универсальная газовая постоянная; Т - абсолютная температура; Lij - температурно-зависимые параметры модели, значения которых выражали полиномами Редлиха-Кистера:
Ьу = Т.1^х,-х^ . (2)
77=0
Парциальные молярные энергии Гиббса (химические потенциалы) могут быть вычислены по уравнению [8]:
где 6^ - символ Кронекера (8^ = 0 при i^j и 8,у =1 при i = j\
Значения параметров модели приведены в таблице
Твердые растворы внедрения (а, у, s) и CrN. В таких растворах металлические вещества (железо и хром) образуют подрешетку замещения, а азот и вакансии (Г) - подрешетку внедрения. Тогда твердый раствор внедрения можно представить общей формулой (Cr,Fe)o(N,P)c. Образование такого раствора можно представить смешением гипотетических соединений ЛОКС, АаУс, В^с и ВаУс, а молярную энергию Гиббса такого «четырехкомпонентного» раствора уравнением
Gm= УСгУу^СгУ + УСгУ^Ст:^ + УЕеУу^еУ +
+УреУк^Ре^ + ^ Л а(УСг ^ УСг + Уре I11 УЕе ) +
с(№ lnyN +Уу lnya + G™ 6 +СГ . (3)
где
Gm6 = УСгУРе (yN^Cr,Fe:N + Уу^Сг,Ре:У ) +
+УгУи (УСг ^Cr:P,N + Уре ^e:K,N )• W
Слагаемое G^ определяет магнитную составляющую энергии Гиббса. Её определение следует из данных, приведенных в таблице. Параметры L вычисляются по формуле (2), а состав твердого раствора определяется мольными долями веществ в каждой подрешетке:
yPe = XFe/(l - XN) ИуРе + yCr = U (5)
Ус = HMl - XN) иУы + УК = 1, (6)
где а и с числа межузельных промежутков в металлической подрешетке. Их значения приведены в таблице.
В уравнении (4) в подстрочных индексах запятая разделяет компоненты в одной подрешетке, а двоеточие означает различие подрешеток.
Парциальные молярные энергии Гиббса гипо тетических компонентов твердого раствора определяются по формуле [9]
С -С I 9Gm I ^ V „ ^HL П\
Gi:j Gm+^~ + ~^--L Ук^—Л')
®Vi 9Vj к=Ст,¥е,М,У ^Ук где z иу — элемент замещения и внедрения соответственно. Парциальные величины реальных компонентов определяются следующим образом:
^z = ^1У» ^N = ^/:N ~^г.У-
Термохимические данные и температурнозависимые параметры модели, необходимые для расчета, получены при оптимизации экспериментальных данных и приведены в таблице [5-7].
Графическая зависимость результатов расчета по полученным соотношениям представлена на рис. 2 в виде изотермических сечений в интервале температур 1600... 1000 °C. Из приведенных графических зависимостей следует, что при 1600 °C (рис. 2, а) первично кристаллизующими фазами будут твердые растворы а, е(Сг) и химическое
Термодинамические параметры системы хром-железо-азот
|
Фаза |
Параметр, Дж/моль |
Примеч. |
|
Жидкий расплав (Ж) |
С°(ж) _! / 2G^ = 29950+59,027 б#ж) - G^ = 24335,93 -11,427+2,37615 ■ 10“2177 G^1 -Я2°98 =-16459 + 335,618-7-5071п7 G^"G^ =12040,17-6,558437-3,6751551 10-2177 Gp^ -^298 =-10839,7+291,3027 - 467In 7 £^=-161800-16,117 ^ = 65508 /^ =-19930-12,017 £^е =-14550+6,657 гЖж) _ ^Cr,Fe,N “ |
7<2180K 7>2180K Т<1811К 7>1811 К |
|
О.ц.к. -твердый раствор (а); а=1, с=3 |
со(оцк) _ яод8 = _885 ^93 + J 57,487 _ 26; 90871п7 _ -0,0018943572 -1,47721 •10"673 +1392507’1 G^ - Н298 = -34864+344,187 - 5071п7 - 2,88526 • 1032 7~9 G^ -^298 =+1224,83 + 124,1347-23,514371п7- -0,0043975272 -5,89269 10""873 + 77358,57"1 G^ -^298 = -25384,451+299,312557-4671п7 +2,2960305-10317"9 G”^ - G^ - 3 / 20^ =311870+29,127 g№ - G^ - 3 / 2G^ = 93562+165,077 Z,^^ =-2000007 L^y =20500-9,687 7^n = -799379 + 2937 G“ar=^ln(P+l)/(t) ,. . 1 Г . 79 158 (1 ,Y t4 t10 t16 )1 tA 140p 497^/2 Д2 45 200J 1 Г^-5 ^-’5 ^-25 1 /(t) = -------, где Л[1О 315 1500] , 518 Г 790 (1 Л1 .. 1125|_ 497^р JJ Тс = -31 l,5yCr +1043yFe +yCr7Fe[1650 + 550(yCr -yFe)] Р = -0,008yCr + 2,22yFe - 0,857cryFe |
7<2180К 7>2180К 7<1811К 7>1811К т<1 т>1 |
|
При отрицательных величинах Тс и р, их значения следует поделить на -1 |
||
|
Г.ц.к. -твердый раствор (у) и «CrN»; а=1, с=1 |
G^ -G^) = 7284 + 0,163 7 G^ -G^ = -1462,4 + 8,2827-1,1571n7+6,4-10"472 Gj^ - Я298 = -27098,266+300,252567 - 467In 7+2,78854 • 1031 T9 G^ -G^ -1/20^ =-124460 + 142,167 - 8,571n7 25000 G^ - С°У -1 / 2G*33) = -37460+375,427 - 37,67 In 7 Z^K = 20000 J®v =-26150 Z^v =10833-7,4777 ®:V = 14Ю 7^n = -128930 + 86,497 ^n =24330 ^CrJcN,V =-162516 |
7<1811K 7>1811К |
|
Г.п.у. -твердый раствор (s); а=1, с=0,5 |
G^ "GCr^ =4438 G^ -Я^98 = -2480,955 + 136,72557 - 24,664371n7- -0,0037575272 - 5,89269 • 10"8 73 + 77358,57"1 G^-H^g = -29341,65 + 304,562067 - 4671n7 + 2,78853995-10317"9 G^l -G$°^ -l/4G°(ro) =-65760 + 64,167-3,9371n7 G^ -G^ -IMG*33) = -12015+37,987 Lc^y =21120-10,617 7'сти=-6204 tiy =10345-19,717 7^)^ =-11130 + 11,847 Z,^K =10833 - 7,4777 1^^N =12826-19,487 |
7<1811 7>1811 |
|
N2(ra3) |
1/2G*33) -Я2°98 =-3750,675-9,454257-12,78197 ln7- -0,0017668672 + 2,680735-10-9 73 -323747"1 1/2G*33) -Я298 =-7358,85 + 17,20037-16,369971n7- -0,0006510772 +3,0097-10"873 +5630707”1 |
7<950 7>950 |
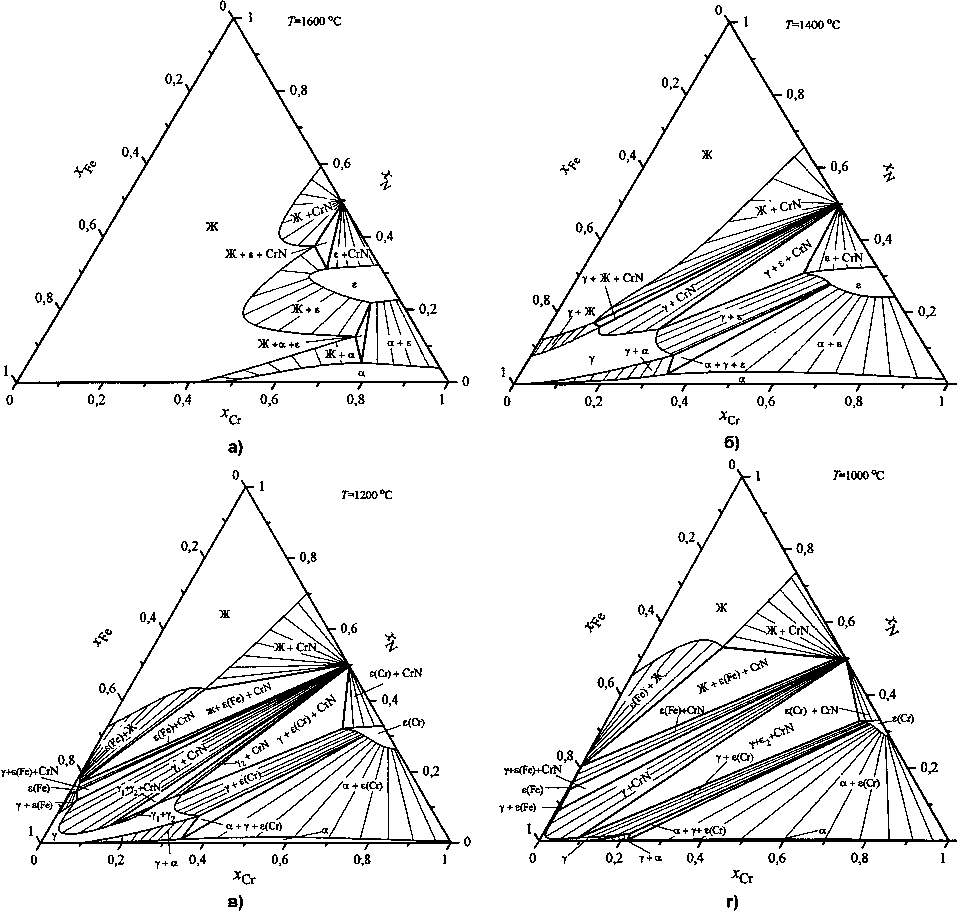
Рис. 2. Изотермические сечения системы железо-хром-азот при температурах (°C): 1600 (а), 1400 (б), 1200 (в) и 1000 (г)
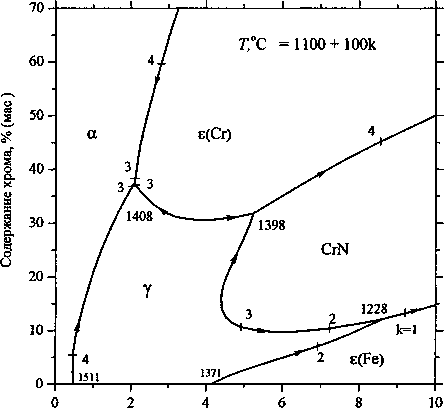
соединение CrN. Комплекс фаз, образующихся при кристаллизации жидкого расплава, графически представлен на рис. 3 линиями трехфазного равновесия с участием жидкости. Области между кривыми определяются как политермические поверхности растворимости компонентов в расплаве, равновесном с одной из кристаллизующихся фаз.
При температуре 1400 °C (рис. 2, б) эти же фазы равновесны аустениту, область гомогенности которого при снижении температуры уменьшается. При этом изменяется также состав и количество равновесных неметаллических фаз.
На изотермических сечениях при заданной концентрации одного из компонентов можно установить последовательность фазовых превращений и определить количественные соотношения равновесных фаз. Однако наиболее представительными и удобными для анализа являются политермические разрезы при постоянной концентрации одного из компонентов. На рис. 4, а приведено такое поли
Содержание азота, % (мае.)
Рис. 3. Диаграмма трехфазных равновесий с участием жидкости
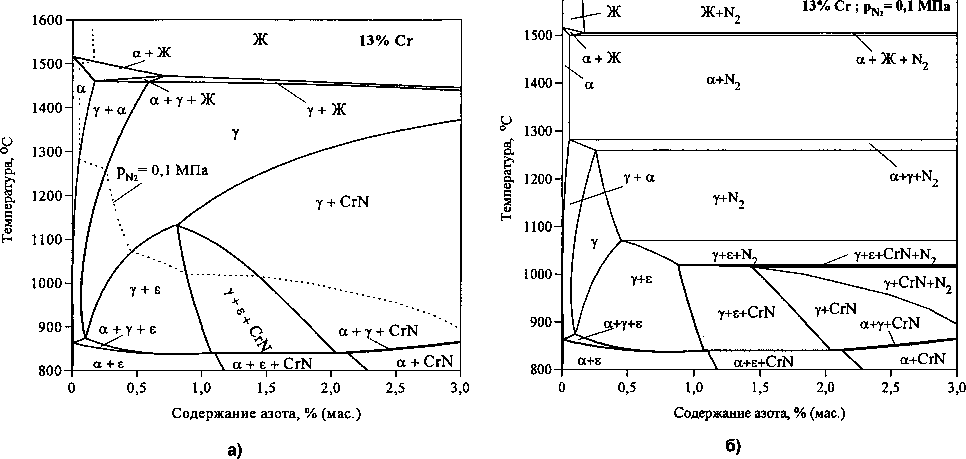
Рис. 4. Политермические разрезы диаграммы состояния системы железо-хром-азот: 13 % Сг (а), 13 % Сг и р(М2) = 0,1 МПа (б)
термическое сечение, соответствующее содержанию хрома в металлическом сплаве 13 % (мае.). Диаграмма на рис. 4, б отвечает тому же политер-мическому разрезу диаграммы Fe-Cr-N, когда давление азота в газовой фазе постоянно и равно 0,1 МПа. При этом реализуются трехфазные равновесия с участием газовой фазы.
Выводы. Проведен термодинамический анализ и изучены фазовые равновесия в трехкомпонентной системе железо-хром-азот. Рассчитаны и построены изотермические сечения в интервале температур 1600... 1000 °C. Рассчитана проекция поверхности ликвидуса и установлен комплекс первично кристаллизующихся фаз. Результаты расчета представлены также в виде политермических разрезов с постоянным содержанием хрома и одинаковым значением активности азота в системе.
Работа выполнена в соответствие с научной программой Федерального агентства по образованию - «Развитие научного потенциала высшей школы (2009-2010 гг.)», код проекта - 713 и при поддержки РФФИ, грант № 08-08-00416.
Список литературы Термодинамический анализ системы железо-хромазот
- Hillert, М. The Regular Solution Model for Stoichiometric Phases and Ionic Melts./M. Hillert, L.I. Staffanson//Acta Chem. Scand. -1970. -V. 24, № 10. -P. 3618-3626.
- Andersson, J.-O. Thermodynamic Properties of the Cr-Fe System/J.-O. Andersson, B. Sundman//CALPHAD. -1987. -V. 11, № 1. -P. 83-92.
- Agren, J. The Thermodynamic Analysis of the Fe-C and Fe-N Phase Diagrams./J. Agren//Metallurg Trans. A. -1979. -V. 10A, № 12. -P. 1847-1852.
- Frisk, K. A Thermodynamic Evаlution of the Cr-N, Fe-N, Mo-N and Cr-Mo-N System/K. Frisk//CALPHAD. -1991. -V. 15, № 1. -P. 79-106.
- Perrot, P. Chromium -Iron -Nitrogen/Pierre Perrot//MSIT, London-Bцrnstein. New Series IV/11D3 -P.23.
- Tschiptschin, A.P. Predicting Microstructure Development During High Temperature Nitriding of Martensitic Stainless Steels Using Thermodynamic Modeling./A.P. Tschiptschin//Materials Research. -2002. -V. 5, № 3. -P. 257-262.
- Frisk, K. A Thermodynamic Evaluation of the Fe-Cr-N System./K. Frisk,//Metallurg. Trans. A. -1990. -V. 21 A, № 9. -P.2477-2488.
- Люпис, К. Химическая термодинамика материалов./К. Люпис; пер. с англ. под ред. H.A. Ватолина, А.Я. Стомахина. -М.: Металлургия, 1989. -503 с.
- Sundman, В.J. A Regular Solution Model for Phases with Several Components and Sublattices, Suitable for Computer Applications./B. Sundman, J. Agren//Phys. Chem. Solids. -1981. -V. 42, P. 297-301.
- Sundman, B. The Sublattice Model./B. Sundman, J. Agren//Mat. Res. Soc. Symp. Proc. -1983. V. 19. -P. 115-127.


