Термодинамический анализ восстановления оксидов железа в газовых смесях (CO-H2) в присутствии углерода
Автор: Кузнецов Юрий Серафимович, Михайлов Геннадий Георгиевич, Качурина Ольга Ивановна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 4 т.17, 2017 года.
Бесплатный доступ
Обсуждены особенности процессов восстановления оксидов железа Fe3O4 до FeO и FeO до Fe в газовых смесях H2 (ao, моль) - CO (co, моль) в контакте с углеродом при нагревании до T = 850…955 К при давлении 1 атм. Общее количество газов в исходной смеси задавалось (ao + co) = 1 моль, а соотношение ao/co варьировалось в пределах от 1/0 до 0/1. Рассчитаны параметры получающихся равновесных систем: Fe3O4 - FeО - Н2 (a) - Н2О (b) - СО (c) - СО2(d) - С, FeO - Feа- Н2 (a) - Н2О (b) - СО (c) - СО2 (d) - С. Определены условия выделения сажистого углерода и его количества. Рассчитаны параметры реакций газификации углерода парами воды Н2О и диоксидом СО2. Вычислены общий и удельный расходы углерода. Рассчитаны количества восстановленных оксидов Fe3O4 и FeO. По результатам этих расчетов определены соотношения восстановительных способностей Н2 и СО γ = b/d. Для восстановления и Fe3O4 до FeO, и FeO до Fe это соотношение изменяется от 0 до 5,76 в зависимости от температуры и величины ao/co. Показано, что восстановление Fe3O4 до FeO при температуре ~ 917 К характеризуется величиной γ = 2,30 и большими количествами восстановленного оксида. Восстановление FeO до Fe при ~ 955 К характеризуется величиной γ = 1,71 и большими количествами восстановленного оксида.
Оксиды железа, восстановление, водяной газ, газификация углерода
Короткий адрес: https://sciup.org/147157114
IDR: 147157114 | УДК: 669.11 | DOI: 10.14529/met170401
Thermodynamic analysis of reduction of ferrous oxide in gaseous mixture (CO-H2) in the presence of carbon
The features of the processes of reduction of iron oxides Fe3O4 to FeO and FeO to Fe in gas mixtures H2 (ao) - CO (co) in contact with carbon are discussed when heated to temperatures of 850-955 K at a pressure of 1 atm. The total amount of gases in the initial mixture was set (ao + co) = 1 mol, and the ratio ao/co varied from 1/0 to 0/1. The parameters of the resulting equilibrium systems: Fe3O4 - FeО - Н2 (a) - Н2О (b) - СО (c) - СО2(d) - С, FeO - Fe - Н2 (a) - Н2О (b) - СО (c) - СО2 (d) - С are calculated. The conditions for the separation of black carbon and its amount are determined. The parameters of gasification reactions of carbon with water vapor H2O and dioxide CO2 are calculated. The total and specific costs of carbon are calculated. The amounts of reduced oxides Fe3O4 and FeO are calculated. Based on the results of these calculations, the reduction ratios of H2 and CO of γ = b/d are determined. For the reduction of Fe3O4 to FeO and FeO to Fe, this ratio varies from 0 to 5.76 depending on the temperature and the value of ao/co. It is shown that the reduction of Fe3O4 to FeO at a temperature of ~ 917 K is characterized by a value of γ = 1.71 and large amounts of the reduced oxide. The reduction of FeO to Fe at ~955 K is characterized by a value of γ = 2.30 and a large amount of the reduced oxide.
Текст научной статьи Термодинамический анализ восстановления оксидов железа в газовых смесях (CO-H2) в присутствии углерода
Фазовые равновесия, реализующиеся при
восстановлении оксидов железа в различных газовых атмосферах в присутствии углерода, обсуждаются в литературе в связи с появлением новых низкотемпературных технологий. В работах [1, 2] обсуждались процессы восстановления оксидов железа в атмосфере водяного газа в присутствии избытка углерода в качестве самостоятельной фазы и особенности графической интерпретации результатов
C+CO2 = 2CO,
A r G T (2) = 172140 - 177,7 ■ T ;
C+H O=CО+H , 2 2
A r G T (3) = 135 560 - 144,235 ■ T ;
Fe O +CO=3FeO+CO , 3 4 2
A GT (4) = - 10 034 - 38,635 ■ T In T + 271,78 ■ T ;
термодинамических расчетов равновесных состояний систем (рис. 1, 2):
Fe 3 O 4 – Fe α – Н 2 – Н 2 О – СО – СО 2 – С; ( а ) Fe 3 O 4 – FeО – Н 2 – Н 2 О – СО – СО 2 – С; ( b ) FeO – Fe α ,γ,ж – Н 2 – Н 2 О – СО – СО 2 – С. ( c )
Равновесные параметры таких систем определялись в работах [1, 2] расчетом совмест-
ных равновесий таких реакций: H2+CO2=H2O+CO,
A r G T (1) = 36 580 - 33,465 ■ T ;
Fe O +H =3FeO+H O, 3 4 2 2
A r G T (5) = 26 546 - 38,635 ■ T In T + 238,315 ■ T ;
FeO+CO=Feα+CO2,
Ar GT (6) = - 21785 + 25 ■ T,
Т < 1185 К;
FeO+H2 =Feα +H2O,
ArGT (7) = 14 799 - 8,465 ■ T,
Т < 1185 К.
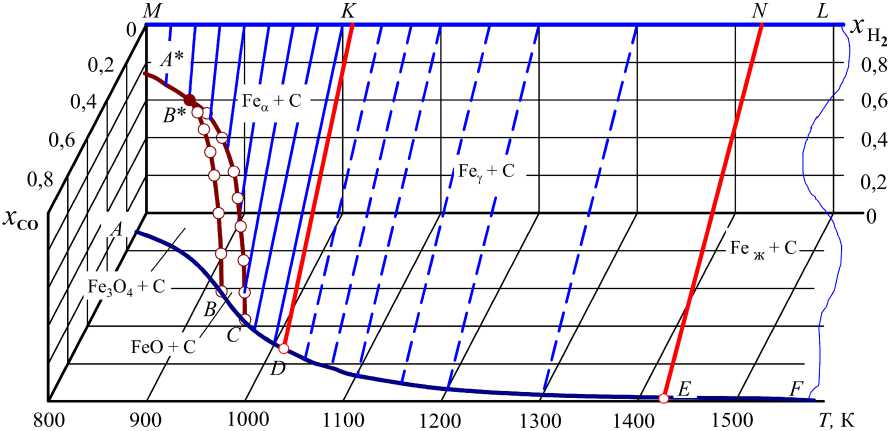
Рис. 1. Области на диаграмме фазовых равновесий в системах «оксиды железа – CO – CO2 – Н2 – Н2O – С »: область ( Fe α + C ) – изотермы от 800 до 1011 К соответствуют концентрациям C в Fe α от ∼ 0 до 0,0195 %; область ( Feγ + C ) – изотермы от 1011 до 1427 К соответствуют концентрациям C в Feγ от ∼ 0,69 до 2,08 %; границы областей: ( Fe α + C ) и ( Fe γ + C ) – 1011 К, Fe α (0,0195 % C ), Fe γ (0,69 % C ), ( x CO Ix γCO ) = 0,7623/0,2377;
( Fe γ + C ) и ( Fe ж + C ) – 1427 К, Fe γ (2,08 % C ), Fe ж (4,26 % C ), ( x CO I x CO ) ≈ 0,999/0,001
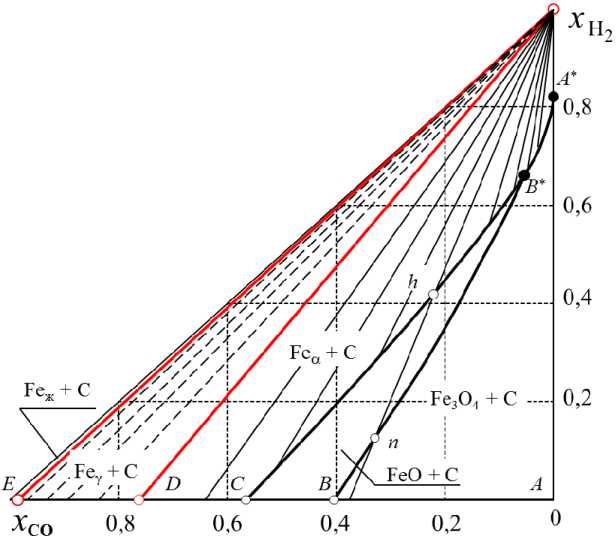
Рис. 2. Проекции линий и изотерм диаграммы фазовых равновесий в системах «оксиды железа – CO – CO2 – Н2 – Н2O – С » [1, 2]
На пространственной диаграмме фазовых равновесий (рис. 1) в системах (а), (b) и (c) линиями представлены три параметра (температура, молярные доли газов-восстановителей Н2 и СО в водяном газе), определяющие возможность восстановления оксидов. Рис. 2 представляет изотермические сечения этой пространственной диаграммы. Являющаяся основой технологических газовых атмосфер, смесь (Н2 – Н2О – СО – СО2) может быть получена разными способами. При выборе оптимального способа в частной технологии переработки железных руд следует учитывать особенности фазовых равновесий систем. В настоящей работе приводится анализ процессов при нагревании исходных систем:
Fe 3 O 4 – H 2 ( a o , моль) – СО ( c o ) – С, FeO – H 2 ( a o , моль)– СО ( c o ) – С.
Для примера детально рассмотрим процессы, протекающие в закрытых системах FeO – H 2 ( a o ) – СО ( c o ) – С при изотермических выдержках выше 850 К при давлении 1 атм. При расчетах параметров перехода исходных систем в равновесия следует определить: количества газов H2, H2O, СО и СО 2 и состав равновесного водяного газа; расход углерода; количество железа, восстановленного H 2 и СО и оценить восстановительные способности водорода и монооксида углерода. Для решения этих задач необходимо определить параметры совместных равновесий пяти возможных в системе реакций (1)–(3), (6) и (7), лишь три из которых независимы. Предлагается такая методика расчета совместного равновесия таких трех независимых реакций:
FeO + H 2 = Fe a + H 2 O FeO + CO = Fe a + CO 2
С + H 2 O = H 2 + CO
– a o c o
(z – y ) ( a o – z + y ) ( c o – x + y )
a o – c o –
( a o – z + y ) (z – y ) ( c o – x + y ) x
Здесь в первой строке после уравнений химических реакций указаны исходные количества H2 и CO, во второй строке – числа молей компонентов водяного газа в состоянии равновесия:
y определяет количество газифицированного углерода, а также количества CO и H 2 , получающиеся по реакции газификации (3);
x определяет число молей оксида СО, затраченного на восстановление, или число молей восстановленного по реакции (6) железа, или число молей полученного при этом СО 2 ;
z определяет число молей водорода, затраченного на восстановление, или число молей восстановленного по реакции (7) железа.
Получаем для общего количества газов в состоянии равновесия:
E « Газ = ( a o - z + y ) + ( z - y ) + ( c o - x + y ) + x = ( a o + c o + y ).
-
(8)
-
(9)
Тогда для констант равновесия выбранных реакций имеем:
( c o - x + y) * ( a o - z + y) n x ( z - y )
K 3 — * P; K 6 — ; K 7 —.
( a o + c o + y ) * ( z - y ) ( c o - x + y ) ( a o - z + y )
Решение системы трех уравнений (9) при 1 атм позволяет определить количественные изменения твердых и газовой фаз:
— K7K3 (1 + K6) (ao + co) - eo y [1-K7 K3 (1 + K6 )]
z — K7 * ao + (1 + K 7) * y ; x — K 6( с o + y)
(1 + K 7 ) ; ( 1 + K 6 ) .
После подстановки выражения (10) в формулу (8) получаем, что общее количество газов в равновесной системе при заданной температуре зависит только от количества водорода в исходной системе:
( a o + c o + y ) =
s —
a o
.
1 - K 7 K 3 (1 + K 6 )
В этом просматривается особая роль водорода, на которую обращали внимание специалисты [3, 4]. Состав равновесного водяного газа определяется уравнениями:
e„ + y - x x z - y a„ + y - z oo xCO — ; xCO2 — ; xH2O — ; xH2 — a o + с o + y 2 ao + с o + y 2 ao + с o + y 2 a o + с o + y
.
Количества восстановленного железа, соотношение восстановительных способностей Н 2 и СО, а
также доля железа, восстановленного водородом, рассчитываются по уравнениям:
E n Fe = x + z ; Y — z/x ; a H 2 = z /( x + z ).
Количества H2 и СО в исходной системе могут быть любыми. Здесь приведены результаты расчетов по уравнениям (8)–(14) для ограниченного количества исходных газов ( a o + c o ) = 1 моль, табл. 1–4 и рис. 3–8.
Таблица 1
Параметры перехода системы FeO – Н2 ( a o = 1 моль) – С в равновесную систему
FeO – Fe α – Н2 ( a o – z + y ) – Н2О ( z – y ) – СО ( y – x ) – СО2 ( x ) – С при изотермических выдержках в интервале температур 850…955 К, P = 1 атм
|
T , К |
850 |
870 |
890 |
910 |
930 |
950 |
955 |
|
[1– K 7 K 3 (1 + K 6 )] |
0,8868 |
0,8219 |
0,7251 |
0,5834 |
0,3792 |
0,0895 |
~ 0 |
|
y |
0,1277 |
0,2167 |
0,3791 |
0,7141 |
1,6370 |
10,169 |
~ 1941 |
|
x |
0,06627 |
0,1086 |
0,1836 |
0,3343 |
0,7412 |
4,4552 |
~ 843 |
|
z |
0,3819 |
0,4802 |
0,6516 |
0,9954 |
1,9269 |
10,467 |
~ 1942 |
|
а = a o – z + y |
0,7458 |
0,7365 |
0,7275 |
0,7187 |
0,7102 |
0,7016 |
0,7 |
|
b = z – y |
0,2542 |
0,2635 |
0,2725 |
0,2813 |
0,2898 |
0,2984 |
0,3 |
|
с = y – x |
0,0614 |
0,1081 |
0,1955 |
0,3798 |
0,8958 |
5,7161 |
~ 1097 |
|
d = x |
0,0663 |
0,1086 |
0,1836 |
0,3343 |
0,7413 |
4,4571 |
~ 843 |
|
∑ ni газ = a + b + c + d |
1,1277 |
1,2167 |
1,3791 |
1,7141 |
2,6371 |
11,173 |
~ 1942 |
|
V , л |
78,6 |
86,8 |
100,6 |
130,4 |
201,1 |
870,4 |
15 ⋅ 104 |
|
x H 2 |
0,6612 |
0,6053 |
0,5275 |
0,4193 |
0,2693 |
0,0628 |
∼ 0,00036 |
|
x H 2 O |
0,2255 |
0,2166 |
0,1976 |
0,1641 |
0,1099 |
0,0267 |
0,00013 |
|
x CO |
0,0545 |
0,0889 |
0,1418 |
0,2216 |
0,3397 |
0,5116 |
0,5652 |
|
x CO 2 |
0,0588 |
0,0893 |
0,1331 |
0,1950 |
0,2811 |
0,3989 |
0,4344 |
|
∑n Fe = x+ z |
0,4482 |
0,5889 |
0,8352 |
1,3297 |
2,6681 |
14,922 |
~ 2785 |
|
γ = z /x |
5,7639 |
4,4208 |
3,5493 |
2,9776 |
2,5997 |
2,3494 |
2,3010 |
|
α H = z /(x + z ) |
0,8522 |
0,8155 |
0,7802 |
0,7486 |
0,7222 |
0,7014 |
0,6971 |
|
∑ n С |
0,128 |
0,217 |
0,379 |
0,714 |
1,637 |
10,18 |
~ 1942 |
|
∑ n С / ∑n Fe |
0,2856 |
0,3685 |
0,4538 |
0,5370 |
0,6135 |
0,6527 |
0,6973 |
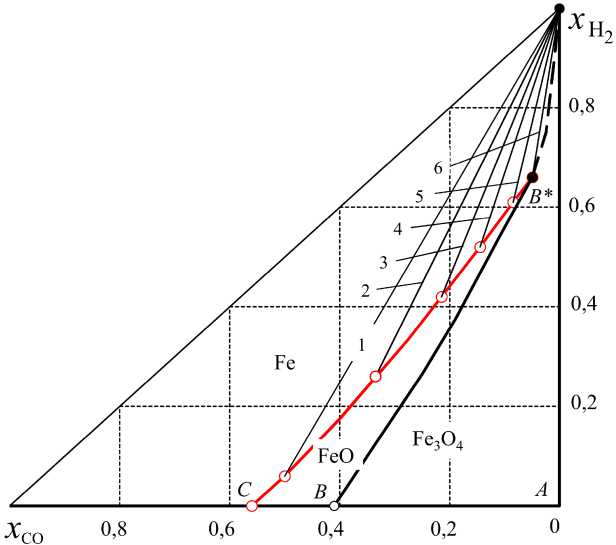
Рис. 3. Восстановление FeO до Fe при изотермических выдержках исходной системы FeO – Н2 – С , давление 1 атм: 1 – Т = 950 К, γ = 2,3494; 2 – 930 К, γ = 2,5997; 3 – 910 К, γ = 2,9776; 4 – 890 К, γ = 3,5493; 5 – 870 К, γ = 4,4208; 6 – 850 К, γ = 5,7639
В табл. 1 и рис. 3 приведены результаты расчетов параметров системы, получающейся при изотермических выдержках смеси FeO – H2 (1 моль) – С для крайнего случая co = 0 – отсутствие в исходной системе CO. На рис. 3 изотермические линии 850…950 К, соединяющие точку xH = 1 с точками линии B*C, условно показывают изменение газовой фазы при переходе исходной системы в равновесные состояния. Вычисленные концентрации компонентов водяного газа, равновесного со смесью FeO – Fe – C, совпадают с концентрациями, полученными в работах [1, 2] расчетами возможных равновесий систем FeO – Feα – Н2 – Н2О – СО – СО2 – С (см. рис. 1 и 2) без задания какого-либо исходного состояния. Введение в систему FeO – С водорода приводит не только к процессу восстановления FeO до Fe по реакции (7), но и активирует реакцию восстановления (6) в результате образования по реакции газификации (3) оксида углерода СО. Этот эффект значительно усиливается с ростом температуры, о чем можно судить по количеству образовавшегося СО2. Кардинальные изменения процессов восстановления водородом в присутствии углерода иллюстрирует рис. 4. На этом рисунке информация о равновесных параметрах системы, получающейся при нагревании исходной системы FeO – Н2(ao) – С (линия 10) сопоставлена с информацией о параметрах восстановления FeO в газовой смеси Н2 (ao) – СО (bo) без углерода – линии 1–9. Этот рисунок без линии 10 впервые привел Н.Л. Гольдштейн [3].
Из результатов расчетов следует, что при изотермической выдержке переход системы FeO – Н 2 – С в равновесное состояние сопровождается увеличением количества газов. При повышенных температурах это увеличение становится весьма значительным: если к моменту достижения равновесия при 850 К количество газов увеличивается на 13 %, то при 955 К в 1942 (!) раза, что объясняется реакциями газификации. При этом количество водорода в состояниях равновесия практически не меняется. Из этого следует, что весь
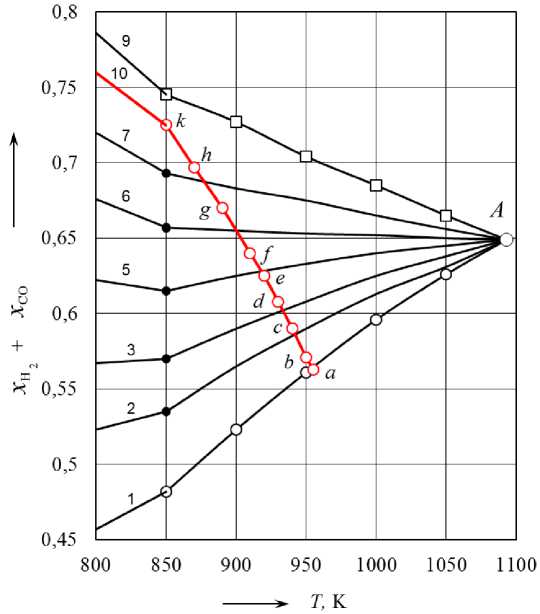
Рис. 4. Суммы равновесных концентраций H 2 и СО при восстановлении оксида FeO в смесях Н2 ( a o ) – СО ( c o ) в отсутствии (линии 1–9) и присутствии (линия 10) углерода: линия 1 – a o / c o = 0; 2 – 0,25; 3 – 0,5; 4 – 0,75; 5 – 1; 6 – 2; 7 – 3; 8 – 4; 9 – ∞ ; точки на линии 10: a – a o/ c o = 0; b – 0,0983; c – 0,3276; d – 0,6109;
e – 0,9624; f – 1,4004; g – 2,6380; h – 4,6138; k – 7,8339
получающийся по реакции газификации (3) водород полностью расходуется на восстановление. Решающее влияние на общее количество газов оказывает реакция газификации углерода диоксидом СО 2 . В предложенной методике расчетов в выбранные три независимые реакции включена реакция газификации (3). Однако из положения изотермических линий на рис. 3 видно, что в любом состоянии до равновесного в газовой фазе отношение ( x CO/ x CO2 ) факт меньше ( x CO/ x CO2 ) равн , характеризующего равновесие реакции (2). Поэтому при изотермических выдержках системы FeO – Н 2 – С протекают обе реакции газификации, а величина y в равновесном состоянии включает общее количество газифицированного углерода. Это подтверждается расчетом материального баланса по количествам СО и Н 2 , получившихся к моменту достижения равновесия.
Баланс по СО – количество СО, получившегося по реакциям (2) и (3), должно быть равным затратам его на восстановление плюс количество его в газовой фазе:
n со (2) + n со (3) = x + Z n™ • x CO .
Например:
850 К, n СО (2) + n СО (3) =
= 0,06627 + 1,1277·0,0545 = 0,1277 = y ;
955 К, n СО (2) + n СО (3) =
= 843 + 1942·0,5652 = 1942 = y .
Баланс по Н 2 – количество Н 2 , получившегося по реакции (3), должно быть равным затратам его на восстановление плюс количество его в газовой фазе минус исходное количество:
n H2 = n H2 (7) + z nT * x H2 - 1 =
= z + z nT • x H 2 • x CO - 1.
Например:
870 К, n = 0,4802 + 1,2167·0,6053 –1 = H 2
= 0,2166 = y ;
950 К, n = 10,467 + 11,173·0,0628 – 1 = H 2
= 10,169 = y .
Таким образом, восстановление FeO до Fe в системе FeO – Н 2 – С по реакции (7) активирует реакцию газификации (3) и реакцию восстановления (6), протекание которой, в свою очередь, активирует реакцию газификации (2).
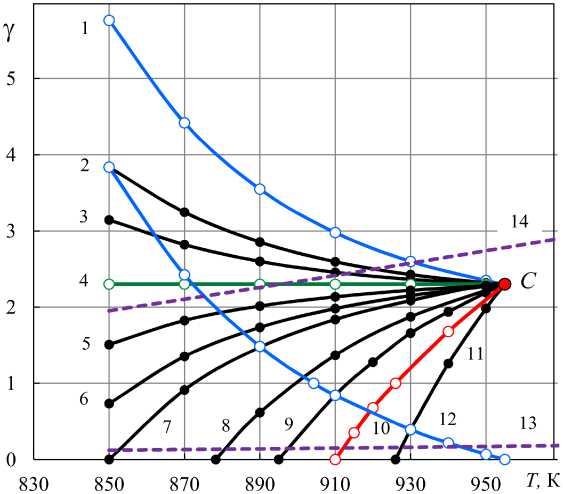
Рис. 5. Соотношение восстановительных способностей Н2 и СО по отношению к FeO при нагревании различных исходных систем: « FeO – Н 2 ( a o ) – С» – линия 1; « FeO – Н 2 ( a o ) – СО ( c o ) – С» с разными количествами Н 2 и СО : 2 – a o / c o = 0,8868/0,1132, 3 – 0,852/0,148, 4 – 0,8133/0,1867 , 5 – 0,78/0,22, 6 – 0,75/0,25, 7 – 0,724/0,276, 8 – 0,65/0,35, 9 – 0,5834/0,4166 (табл. 3), 11– 0,3792/0,6208; « FeO – Fe – Н 2 О ( b o ) – С» – линия 10, не опубликовано; « FeO – Н2 ( a o* ) – СО ( c o* ) – С» – линия 12 при отношениях a o* / c o* , обеспечивающих неизменность количества газа, табл. 1; « FeO – Н2 ( a o ) – СО ( c o )», a o / c o = 1/4 и 4/1 – линии 13 и 14, работа [3]
В результате такого взаимовлияния в закрытой системе при затрате 1 моля (!) водорода восстанавливается при 955 К около 2785 моль (!) оксида FeO.
Поскольку при нагревании системы FeO – Н 2 – С железо восстанавливается и водородом, и оксидом СО можно сравнивать восстановительные способности Н 2 и СО γ = z /x . Видно, линия 1 рис. 5, что величина γ изменяется от 5,76 при 850 К до 2,3 при 955 К. Следовательно, устоявшееся суждение, что при 1093 К (820 °С) восстановительные способности Н 2 и СО одинаковы, а при температурах < 1093 К монооксид СО более сильный восстановитель, нельзя транслировать на все возможные способы организации процессов восстановления.
Если нагревать исходную систему FeO – H 2 ( a o ) – СО ( c o ) – С с любым соотношением С = a o / c o , то параметры равновесного водяного газа получающейся системы FeO – Fe α – Н2 – Н 2 О – СО – СО 2 – С рассчитываются по уравнениям (10)–(14) и определяются той же линией B*C , рис. 1–3, 6, 7 и 8 a . Однако количественные изменения газовой фазы характеризуются некоторыми особенностями. Расчеты количественных изменений фаз при нагревании этих систем до температур 850…955 К выполнялись для произвольных соотношений количеств Н2 и СО при неизменной сумме ( a o + c o ) = 1 моль. Примеры расчетов приведены в табл. 2–4 и на рис. 6–8.
Обнаружены две особенности процессов при нагревании исходной системы. Одна из них состоит в том, что общее количество газов в равновесии зависит от температуры и количества водорода в исходной системе a o , но не зависит от количества монооксида углерода c o , уравнение (12). Вторая особенность следует из того же уравнения (12). Знаменатель [1– K 7 K 3(1 + K 6)] в этом уравнении в интервале температур 850…955 К принимает значения от 0,8868 до 0. Если, например, задать a o = 0,8868 ( c o = 0,1132 моль), то после выдержки исходной системы при 850 К, при этой температуре [1- K 2 - K 4 - (1 + K 1 )] = 0,8868, в результате совокупности процессов общее количество газов остается неизменным – равным единице, табл. 2 и линия GB* на рис. 6. Следовательно, углерод не вовлекается в процессы газификации и восстановления. Если же задать исходные количества a o = 0,5834, c o = 0,4166 моль, то после выдержки исходной системы при 910 К, при этой температуре
[1- K 2 - K 4 - (1 + K 1 )] = 0,5834, суммарное количество газов в системе не изменится, табл. 3 и линия G′ B* на рис. 7. Таким образом, существует такая по составу исходная газовая смесь (H 2 – СО), восстановление оксида FeO в которой при строго определенной температуре не приводит к увеличению общего количества газов, то есть в процессах восстановления оксида углерод не расходуется. В табл. 4 и на рис. 8 представлены некоторые сочетания температуры нагрева и состава исходной газовой смеси, при которых не изменяется общее количество газов. Так как в этом случае углерод не расходуется, то соотношение восстановительных способностей H2 и СО γ равно отношению концентраций x H O и x CO в равновесном газе [1, 2].
В общем случае при нагревании до температур 850…955 К исходных систем FeO – Н 2 ( a o ) – СО ( c o ) – С с разными составами газовой фазы соотношение γ восстановительных способностей Н2 и СО изменяется в пределах от 0 до 5,76. В зависимости от состава смеси (Н 2 – СО) это соотношение может возрастать, уменьшаться или оставаться неизменным с повышением температуры, рис. 5.
Обсудим теперь количественные изменения всех фаз при нагревании до температур 850…955 К систем FeO – Н 2 ( a o ) – СО ( c o ) – С с произвольными количествами Н2 и СО. Сделаем это на примере нагревания до разных температур исходной системы FeO – Н 2 (0,5834 моль) – СО (0,4166 моль) – С.
Результаты расчетов процессов в этой системе приведены в табл. 3. После выдержки этой системы при 910 К в получившемся равновесном состоянии FeO – Fe α – Н 2 ( a ) – Н 2 О ( b ) – СО ( c ) – СО 2 ( d ) – С общее количество газов останется неизменным ( a + b + c + d ) = ( a o + c o) = = 1 моль, см. выделенный жирным курсивом столбец табл. 3. На рис. 5 этому соответствует линия 9, на рис. 7 этому соответствует линия G′h′ , при этом углерод не расходуется , остальные линии условно отражают изменение состава газовой фазы при переходе системы в состояние равновесия при других температурах.
Если эти температуры ниже 910 К , то Σ = ( a + b + c + d ) < ( a o + c o ) = 1 моль, так как при этих температурах интегральная характеристика реакций восстановления и реакции газификации [1– K 2 K 4 (1 + K 1 )] > 0,5834, табл. 3. Это означает, что и в этом случае углерод
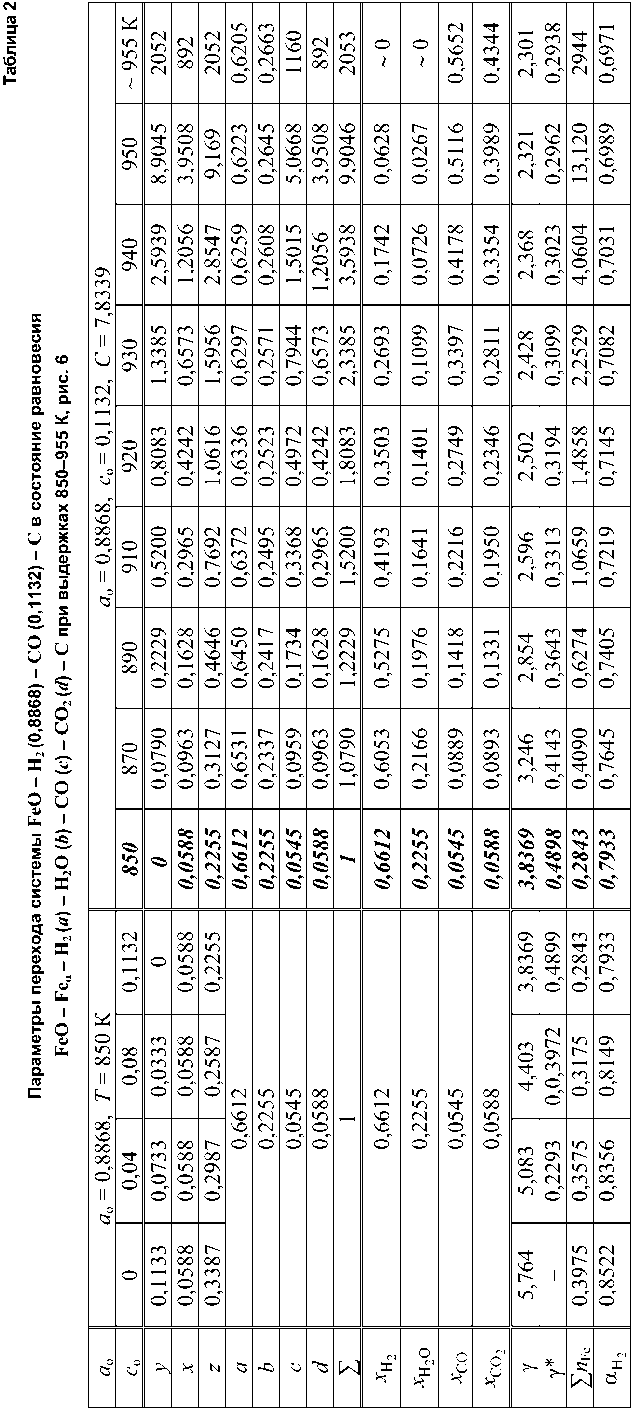
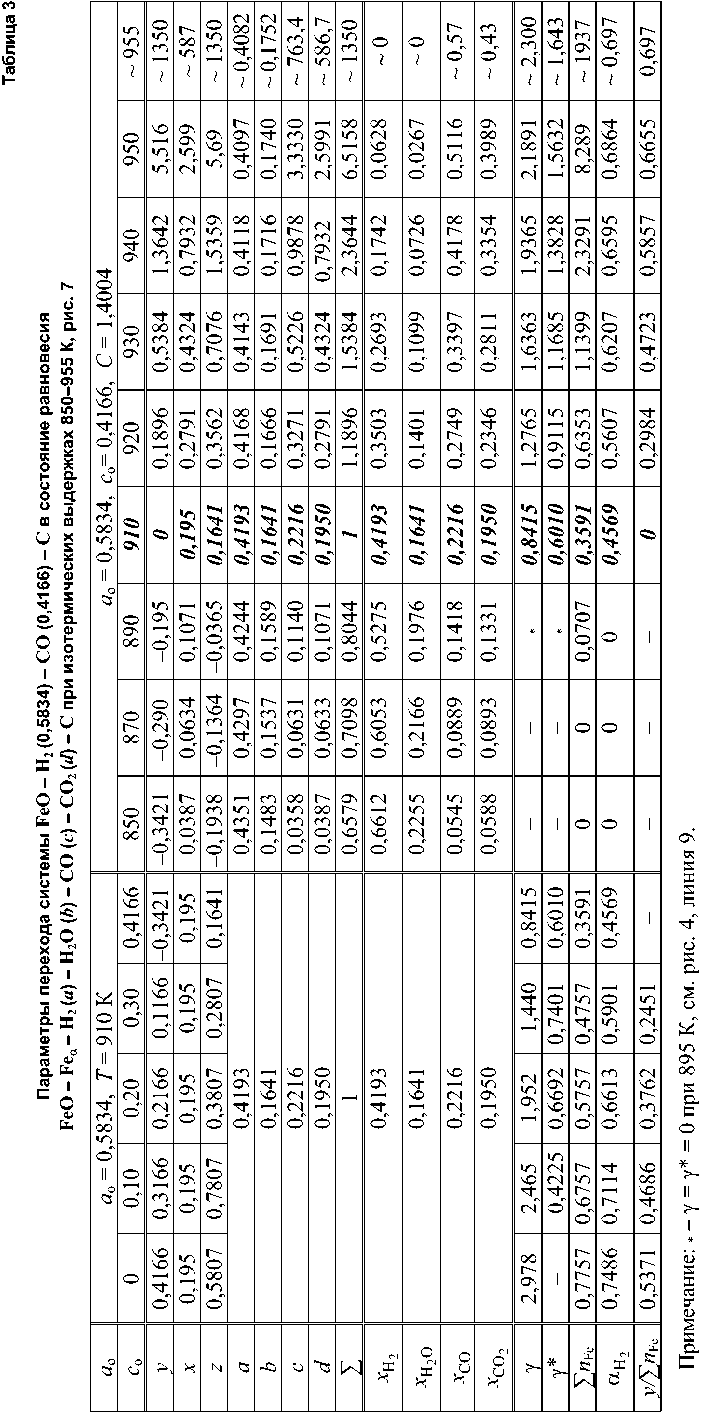
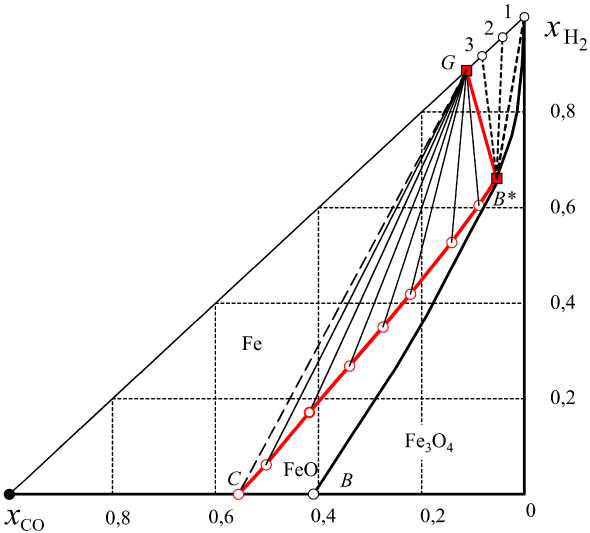
Рис. 6. Параметры перехода системы FeO – Н2 (0,8868) – СО (0,1132) – С в состояние равновесия FeO – Fe α – Н2 ( a ) – Н2О ( b ) – СО ( c ) – СО2 ( d ) – С при изотермических выдержках: 850 К (линии 1, 2, 3 и GB* ) – ∑ = 1 моль, 870, 890, 910, 920, 930, 940, 950 и 955 К (линия GC ) – ∑ > 1 моль пунктирные линии 3, 2, 1 – нагревание систем с неизменным количеством водорода a o = 0,8868 моль и убывающим от 0,1132 до 0 количеством СО
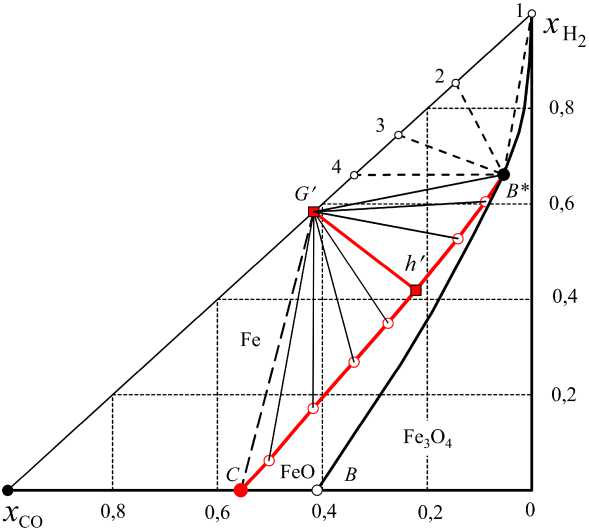
Рис. 7. Параметры перехода системы FeO – Н2 (0,5834) – СО (0,4166) – С в состояния равновесия FeO – Feα – Н2 (a) – Н2О (b) – СО (c) – СО2 (d) – С при изотермических выдержках: 850 (линия G′B*), 870, 890 К – ∑ < 1 моль; 910 К (линия G′h′ ) – ∑ = 1 моль; 920, 930, 940, 950 и 955 К (линия G′C) – ∑ > 1 моль; пунктирные линии 4, 3, 2, 1 – нагревание систем с неизменным количеством водорода ao = 0,5834 моль и убывающим от 0,4164 моль до 0 количеством СО не расходуется на восстановление оксида. Однако углерод не является абсолютно инертной фазой – он выступает катализатором образования сажистого углерода. На это расходуются и Н2 и СО, что снижает эффективность восстановления. Это подтверждает мнения исследователей – выделение сажистого углерода тормозит процесс восстановления оксида, однако это не только кинетическая, но и термодинамическая характеристика системы. Если же температура нагрева системы выше 910 К, то S > (ao + co) = 1 моль, табл. 3, так как при этих температурах интегральная характеристика реакций [1– K2K4(1 + K1)] < 0,5834. Это означает, что углерод расходуется в процессе восстановления оксида – повышается эффективность восстановления из-за многократной регенерации H2 и CO. При этом существенно увеличивается количество газовой фазы. В результате такой «восстановительно-газификационной карусели» при T ^ 955 К концентрации H2 и Н2О становятся весьма малыми, а количество FeO, восстановленного до Fe, весьма значительно. Свидетельством реализации такой «восстановительно-газифи-кационной карусели» являются показанные на рис. 9 результаты расчетов количеств продуктов в газовой и твердых фазах, получающихся при изотермических выдержках.
Тот факт, что за исключением одного единственного сочетания С = a o / c o и температуры в процессах восстановления оксидов либо расходуется углерод, либо получается сажистый углерод, исключает возможность оценки восстановительных способностей H2 и СО величиной x H O / x CO [3]. Для количественной оценки соотношения восстановительных способностей Н2 и СО следует использовать величину у = z]x и долю железа, восстановленного водородом aH2 = z /( x + z ), табл. 3 и рис. 5.
Аналогичные расчеты можно выполнить для восстановления оксида Fe 3 O 4 при нагревании систем Fe 3 O 4 – Н 2 ( a o ) – СО ( c o ) – С. Для этого рассчитываются совместные равновесия реакций (3), (4) и (5). Соотношения между компонентами газовой фазы определяются теми же уравнениям (10)–(14) с заменой констант равновесия K 6 и K 7 на K 4 и K 5 . Количества восстановленного оксида Fe 3 O 4 водородом и оксидом СО определяются величинами z и x , а полученного оксида FeO – величинами 3z и 3 x . Некоторые результаты расчетов приведены на рис. 8 и 10.
Результаты вышеприведенных вычислений позволяют оценить полный и удельный расход углерода на восстановление Fe 3 O 4
Таблица 4
Количество восстановленного железа в отсутствии расхода углерода при переходе исходной системы FeO – Н 2 ( a o ) – СО ( c o ) – С в равновесную FeO – Fe α – Н 2 ( a ) – Н 2 О ( b ) – СО ( c ) – СО 2 ( d ) – С ;
( a + b + c + d ) = ( a o + c o ) = 1 моль , a o = [1 – K 2 K 4 (1 + K 1 )]
|
T , К |
850 |
870 |
890 |
904,3 |
910 |
930 |
940 |
950 |
~ 955 |
|
a o |
0,8868 |
0,8219 |
0,7251 |
0,6290 |
0,5834 |
0,3792 |
0,2468 |
0,0845 |
0,0004 |
|
c o |
0,1132 |
0,1781 |
0,2749 |
0,3710 |
0,4166 |
0,6208 |
0,7532 |
0,9155 |
0,9996 |
|
a o/ c o |
7,8339 |
4,6138 |
2,6380 |
1,6954 |
1,4004 |
0,6109 |
0,3276 |
0,0983 |
0,0004 |
|
y |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
x |
0,0588 |
0,0893 |
0,1331 |
0,1754 |
0,1950 |
0,2811 |
0,3355 |
0,3765 |
0,4023 |
|
z |
0,2255 |
0,2166 |
0,1976 |
0,1754 |
0,1641 |
0,1098 |
0,0728 |
~ 0 |
~ 0 |
|
a |
0,6613 |
0,6053 |
0,5275 |
0,4536 |
0,4193 |
0,2693 |
0,1742 |
0,0628 |
~ 0 |
|
b |
0,2255 |
0,2166 |
0,1976 |
0,1754 |
0,1641 |
0,1099 |
0,0726 |
0,0267 |
~ 0 |
|
c |
0,0545 |
0,0890 |
0,1418 |
0,1956 |
0,2216 |
0,3397 |
0,4179 |
0,5116 |
0,5652 |
|
d |
0,0588 |
0,0893 |
0,1331 |
0,1754 |
0,1950 |
0,2811 |
0,3355 |
0,3989 |
0,4344 |
|
n Fe |
0,2843 |
0,3059 |
0,3307 |
0,3508 |
0,3591 |
0,3909 |
0,4083 |
0,3454 |
0,3284 |
|
γ |
3,8377 |
2,4256 |
1,4845 |
1,000 |
0,8416 |
0,3911 |
0,2163 |
~ 0 |
~ 0 |
|
γ* |
0,4902 |
0,5257 |
0,5627 |
0,5900 |
0,6009 |
0,6403 |
0,6604 |
0,6808 |
0,6911 |
|
a H 2 |
0,7933 |
0,7081 |
0,5974 |
0,5000 |
0,4569 |
0,2811 |
0,1783 |
~ 0 |
~ 0 |
Примечания: a = a o + y – z = x H , b = z – y = x H O , c = c o + y – x = x CO , d = x = x CO , n Fe = x + z ; γ = z / x , γ* = γ/ С , С = a o / c o .
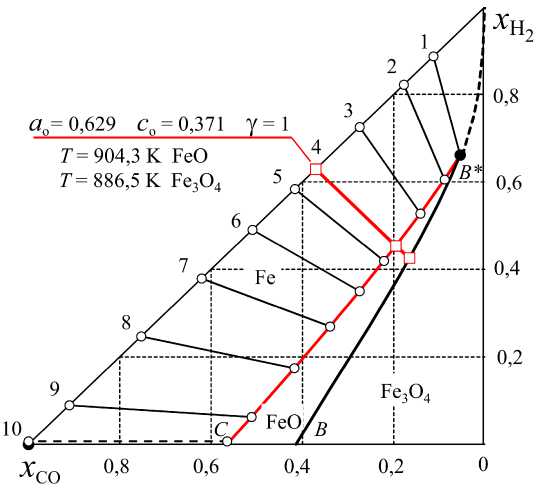
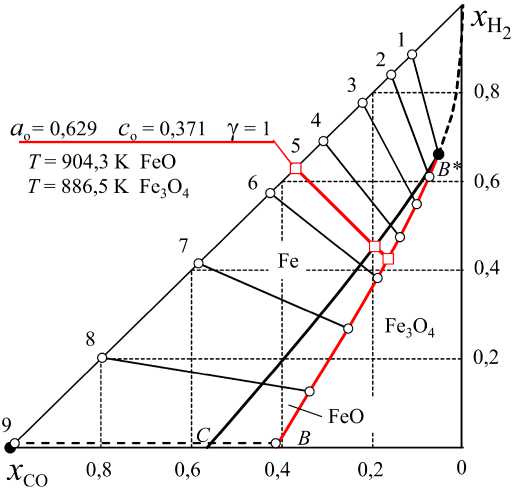
б)
Рис. 8. Концентрации исходных смесей (Н 2 – СО), при которых нагревание оксида не изменяет общее количество газа: а) FeO, координаты точек 1 (850 К)…10 (955 К), см. табл. 1; б) Fe 3 O 4 , координаты точек 1 (850 К) … 9 (917 К)
до FeO и FeO до Fe. Расчет полного расхода углерода y по уравнению (10) может быть проверен на основании очевидного утверждения, что весь газифицированный по двум реакциям (2) и (3) углерод переходит в газовую фазу в виде CO и CO 2 (см. табл. 1, 3, 4):
I nn С = I n^- X co + I n^ x CO 2 = y .
На рис. 9 приведены вычисленные полные расходы углерода для разных систем FeO – Н 2 ( a o ) – СО ( c o ) – С при температурах 850…955 К.
Удельные расходы y* = y L n Fe = y(xx + z ) представлены на рис. 11. Удельные затраты углерода меньше единицы, как это следует
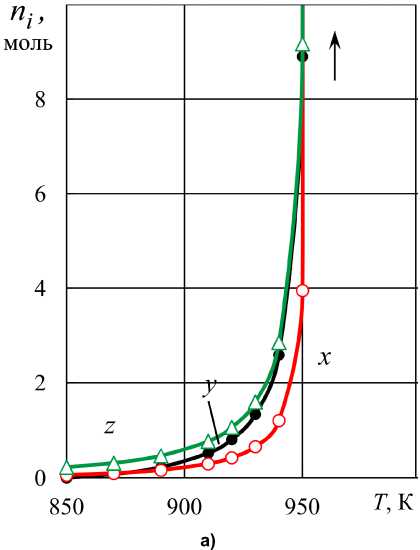
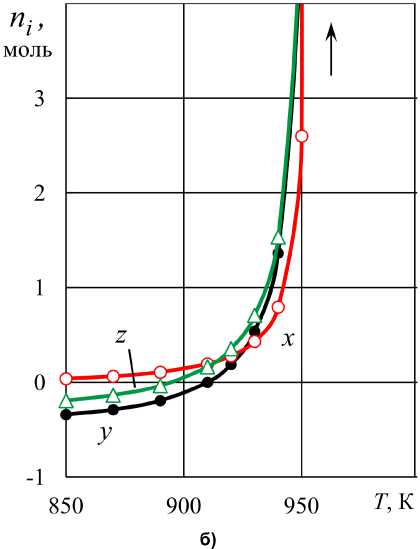
Рис. 9. Количества железа, восстановленного водородом ( z ), монооксидом углерода ( x ) и количества затраченного углерода ( y ) при нагревании исходных систем FeO – Н 2 ( a o ) – СО ( c o ) – С : а) a o = 0,8868, c o = 0,1132 при T → 955 К: y → 2052, x → 892, z → 2052;
б) a o = 0,5834, c o = 0,4166 при T → 955 К: y → 1350, x → 587, z → 1350;
в) a o = 0,3792, c o = 0,6208 при T → 955 К: y → 877, x → 381, z → 877
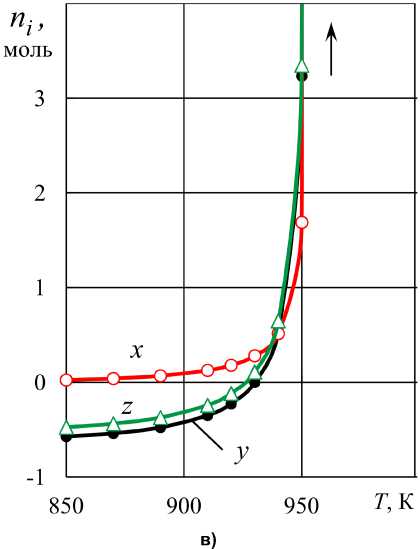
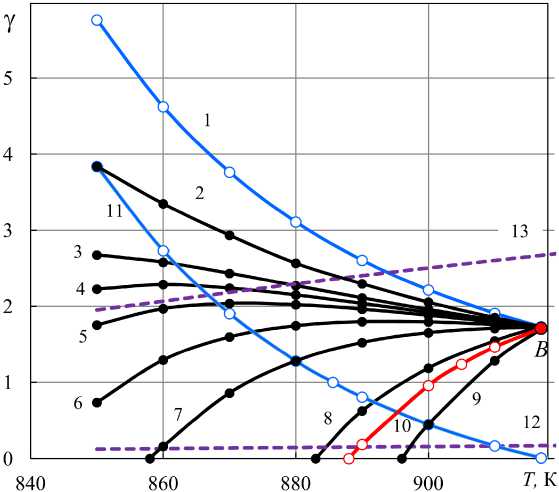
Рис. 10. Соотношение восстановительных способностей Н2 и СО по отношению к Fe3O4 при нагревании различных исходных систем: « Fe3O4 – Н2 ( a o моль) – С» – линия 1, работа [1]; « Fe3O4 – Н2 ( a o моль) – СО ( c o моль) – С» с разными количествами Н 2 и СО : 2 – a o / c o = 0,8868/0,1132, 3 – 0,83/0,17, 4 – 0,81/0,19, 5 – 0,79/0,21, 6 – 0,75/0,25, 7 – 0,6911/0,3089, 8 – 0,55/0,45, 9 – 0,4154/0,5846; « Fe3O4 – Fe – Н2О ( b o моль) – С» – линия 10, не опубликовано; « Fe 3 O 4 – Н 2 ( a o * ) – СО ( c o * ) – С» – линия 11 при отношениях a o * / c o * , обеспечивающих неизменность количества газа; « Fe3O4 – Н2 ( a o моль) –
СО ( c o моль) » , a o / c o = 1/4 и 4/1 – линии 12 и 13, [3]
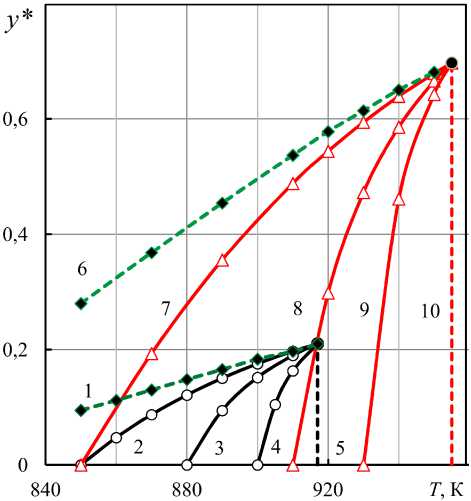
Рис. 11. Удельный расход углерода на восстановление оксидов железа: линия 1 – нагревание системы «Fe 3 O 4 – Н 2 – С», работа [1], 2 – «Fe 3 O 4 – Н 2 (0,8868) – СО (0,1132 моль) – С», 3 – «Fe 3 O 4 – Н 2 (0,6611) – СО (0,3389 моль) – С», 4 – «Fe 3 O 4 – Н 2 (0,4154) – СО (0,5846 моль) – С», 5 – «Fe 3 O 4 – СО – С» работа [4]; линия 6 – нагревание системы «FeO– Н 2 – С», работа [1], 7 – «FeO – Н 2 (0,8868) – СО (0,1132 моль) – С», 8 – «FeO – Н 2 (0,5834) – СО (0,4166 моль) – С», 9 – «FeO – Н 2 (0,37892) – СО (0,6208 моль) – С», 10 – «FeO – СО – С» работа [4]
ожидать из стехиометрии реакций прямого восстановления:
Fe 3 O 4 + C = 3Fe O + CO 2 ;
FeO + C = Fe + CO.
При 917 К удельный расход углерода на восстановление Fe3O4 до FeO составляет не менее 0,21 моль С/моль Fe3O4. При температуре 955 К удельный расход углерода на восстановление FeO до Fe составляет около 0,697 моль С/моль FeO или 0,697 · 12/55,847 = 0,150 г С/г Fe.
Выводы
-
1. Для систем Fe 3 O 4 – Н 2 ( a o ) – СО( c o ) – С и FeO – Н 2 ( a o ) – СО ( c o ) – С существуют такие сочетания температуры T * и С* = ( a o / c o )* (независимо от абсолютных величин a o и c o), при которых после изотермической выдержки в равновесных состояниях сумма чисел молей компонентов образовавшегося водяного газа равна ( a o + c o ). Это означает, что углерод не расходуется на восстановление оксида. При нагревании исходной системы до температур ниже T * происходит выделение сажистого углерода. Это приводит к торможению процессов восстановления, так как и Н 2 и СО расходуются на процессы, обратные реакциям газификации углерода. Следовательно, наблюдаемое в экспериментах отрицательное влияние выделения сажистого углерода на процессы восстановления объясняется не только кинетическими торможениями. При нагревании до температур выше T * существенно повышается интенсивность восстановления, расходуется углерод и имеет место своеобразная «восстановительно-газификацион-ная карусель», приводящая к экспоненциальному возрастанию расхода углерода и количеств продуктов реакций.
-
2. Термодинамическая оценка соотношения восстановительной способности Н2 и СО для оксидов железа в присутствии углерода показала изменение её в пределах от γ = 5,76 до 0 в интервале температур 850…955 К в зависимости от исходного состава смеси (Н 2 – СО). Показано, что величина γ может уменьшаться, увеличиваться или не зависеть от температуры. Это противоречит общепри-
нятому утверждению о равенстве восстановительных способностей H 2 и СО при 1093 К и возрастании восстановительной способности H2 с повышением температуры – информация основана на пересечении кривых наложенных диаграмм фазовых равновесий систем «оксиды – СО – СО 2 » и «оксиды – H 2 – H 2 О».
-
3. В закрытой системе Fe 3 O 4 – Н 2 ( a o ) – СО( c o ) – С полное восстановление Fe 3 O 4 до FeO возможно при температуре ~ 917 К, если в исходной газовой фазе отношения ( a o / c o ) < < 7,83. В закрытой системе FeO – Н 2 ( a o ) – СО( c o ) – С полное восстановление FeO до Fe возможно при температуре ~ 955 К, если в исходной газовой фазе отношения ( a o / c o ) < 7,83. При этом начальное количества водорода и оксида СО могут быть весьма незначительными.
-
4. Удельный расход углерода при восстановлении Fe3O4 до FeO составляет 0,21 моль С/моль Fe3O4, а при восстановлении FeO до Fe составляет 0,697 моль С/моль FeO. Для восстановления Fe3O4 до Fe удельный расход углерода составляет:
0,210 + 3 · 0,697 = 2,3 моль С/3 моль Fe или
-
2, 3 · 12/3 ·55,847 = 0,165 г С/г Fe.
Список литературы Термодинамический анализ восстановления оксидов железа в газовых смесях (CO-H2) в присутствии углерода
- Системный анализ процессов восстановления оксидов железа в атмосфере водяного газа в присутствии углерода/Г.П. Вяткин, Г.Г. Михайлов, Ю.С. Кузнецов и др. -Изв. вузов. Черная металлургия. -2013. -№ 4. -С. 12-17 DOI: 10.3103/S0967091213040153
- Михайлов, Г.Г. Системный анализ процессов восстановления оксидов железа/Г.Г. Михайлов, Ю.С. Кузнецов, О.И. Качурина. -Металлы. -2014. -№ 2. -С. 10-15.
- Гольдштейн Н.Л. Водород в доменном процессе/Н.Л. Гольдштейн. -М.: Металлургия, 1971. -208 с.
- Дигонский, С.В. Роль водорода в восстановлении оксидов металлов твердым углеродом/С.В. Дигонский, В.В. Тен. -Альтернативная энергетика и экология. -2009. -№ 11 (79). -С. 45-55.


