Термодинамический анализ взаимодействия хрома с кислородом в жидком железе
Автор: Самойлова Ольга Владимировна, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 3 т.19, 2019 года.
Бесплатный доступ
Изучение возможности взаимодействия хрома с кислородом при производстве хромсодержащих сталей является одной из практически значимых задач для сталеплавильного производства. В настоящей работе проведено термодинамическое моделирование фазовых равновесий в системе Fe-Cr-O в условиях существования расплава на основе железа (в интервале температур 1600-1800 °С). Термодинамический анализ был выполнен с использованием методики построения поверхности растворимости компонентов в металле, которая представляет собой диаграмму, связывающую изменения в составах жидкого металла с изменениями в составах образующихся продуктов взаимодействия. Для моделирования использовались данные по константам равновесия протекающих в расплаве реакций, а также значения параметров взаимодействия первого порядка (по Вагнеру) компонентов в жидком железе. В ходе работы было установлено, что в интервале температур 1600-1800 °С в качестве продуктов взаимодействия могут образоваться: жидкие оксидные неметаллические включения переменного состава (FeO, CrO, Cr2O3); твердые частицы феррохромита FeCr2O4; чистый твердый оксид хрома Cr2O3; твердые частицы соединения Cr3O4. Также были определены границы термодинамической стабильности данных оксидных фаз, образующихся в расплаве системы Fe-Cr-O. По результатам расчета проведена оценка раскислительной способности хрома в кислородсодержащем расплаве на основе железа. Определено, что максимум раскислительной способности хрома при 1600 °С приходится на область равновесия жидкого металла с твердым оксидом хрома Cr2O3, при этом минимальная концентрация кислорода составляет 0,0204 мас. % для 5,31 мас. % хрома. Полученные в ходе настоящего расчета результаты сопоставлены с имеющимися литературными данными.
Система fe-cr-o, термодинамическое моделирование, фазовые равновесия
Короткий адрес: https://sciup.org/147233925
IDR: 147233925 | УДК: 669.017.3 | DOI: 10.14529/met190301
Thermodynamic analysis of the interaction between chromium and oxygen in the liquid iron
The study of the possibility of the interaction between chromium and oxygen during the production of chromium-containing steels is one of the practically important tasks for the steelmaking. In the present work, thermodynamic modeling of phase equilibria in the temperature range 1600-1800 °C for the Fe-Cr-O system was carried out. Thermodynamic analysis was performed using the method for constructing of the surface solubility of components in a metal, which is a diagram linking changes in the compositions of the liquid metal with changes in the compositions of the resulting interaction products. For the simulation, we used the data on the equilibrium constants of the reactions occurring in the melt, as well as the values of the first-order interaction parameters (according to Wagner) of the components in the liquid iron. In the course of the work, it was found that, in the temperature range 1600-1800 °C, the following products can be formed as interaction products: liquid oxide nonmetallic inclusions of variable composition (FeO, CrO, Cr2O3); solid particles of the ferrochromite FeCr2O4; pure solid chromium oxide Cr2O3; solid particles of the compound Cr3O4. The boundaries of the thermodynamic stability of these oxide phases formed in the melt of the Fe-Cr-O system were also determined. According to the calculation results, the deoxidizing ability of chromium in an oxygen-containing iron-based melt was evaluated. It is determined that the maximum deoxidizing ability of chromium at 1600 °C falls on the equilibrium region of the liquid metal with the solid chromium oxide Cr2O3, while the minimum oxygen concentration is 0.0204 wt. % for 5.31 wt. % chromium. The results obtained in the course of this calculation were compared with the available literature data.
Текст научной статьи Термодинамический анализ взаимодействия хрома с кислородом в жидком железе
Изучение возможности взаимодействия хрома с кислородом при производстве хромсодержащих сталей является одной из практически значимых задач для сталеплавильного производства. Расход хрома на взаимодействие с кислородом влечет за собой как образование оксидных неметаллических хромсодержащих включений, так и понижение концентрации хрома в твердом растворе системы Fe–Cr и, соответственно, понижение качества получаемого металла.
Целью настоящей работы являлось проведение термодинамического анализа процессов взаимодействия в системе Fe–Cr–O в интервале температур 1600–1800 °С.
Термодинамический анализ в данной работе был выполнен с использованием методики построения поверхности растворимости компонентов в металле (ПРКМ) [1, 2], которая позволяет связать изменения в составе металлического расплава с изменениями в составе образующихся продуктов взаимодействия и определить области термодинамической стабильности оксидных фаз, находящихся в равновесии с металлическим кислородсодержащим расплавом. Также данная методика позволяет рассчитывать кривые раскислитель-ной способности элементов в выбранном интервале температур в условиях существования жидкого железа.
Для определения оксидных фаз, которые могут образоваться при взаимодействии в системе Fe–Cr–O, необходимо рассмотреть как простые двойные Fe–O и Cr–O системы, так и оксидную систему FeO–CrO–Cr 2 O 3 .
При анализе сталеплавильных процессов для кислородсодержащего жидкого железа принимается во внимание в основном возможность образования монооксида железа (вюсти-та) FeO [1, 3], температура плавления которого составляет 1378 °С [4]. В системе Cr–O возможно образование оксидов Cr2O3 и CrO, а также соединения Cr3O4 [5]. Температура плавления оксида Cr2O3 составляет 2300 °С [6]. Существование оксида CrO в виде отдельной конденсированной фазы принято только гипотетически в условиях равновесия с металлическим хромом; присутствие иона Cr2+ в литературе рассматривается только либо в составе соединений (например, силикатов), либо в составе оксидных хромсодержащих расплавов
[5, 7–9]. Литературные данные по температуре плавления соединения Cr3O4 различаются между собой. Так, согласно работе [5] температура плавления Cr 3 O 4 составляет 1705 °С. В справочнике [7] указано, что соединение Cr 3 O 4 плавится инконгруэнтно при температуре порядка 2100 °С. А в диссертации [10] равновесие жидкого железа с Cr 3 O 4 рассматривается вплоть до температуры 1900 °С.
В оксидной системе FeO–CrO–Cr 2 O 3 помимо наличия соединения Cr 3 O 4 также имеется соединение FeCr 2 O 4 с температурой плавления порядка 2100 °С [11].
Таким образом, в интервале температур 1600–1800 °С в качестве продуктов взаимо-
Таблица 1
Температурные зависимости констант равновесия химических реакций*, протекающих в расплаве системы Fe–Cr–O
|
lg K |
Значение lg K при 1600 °С (1873 К) |
Источник |
|
(FeO) = [Fe] + [O] |
||
|
–6320/ T + 4,734 \ |
+1,360 \ |
[1] |
|
(CrO) = [Cr] + [O] |
||
|
–8200/ T + 4,510 |
+0,132 |
[12] |
|
–12516/ T + 6,495 |
–0,187 |
[настоящая работа] |
|
(Cr 2 O 3 ) = 2[Cr] + 3[O] |
||
|
–33460/ T + 14,850 |
–3,014 |
[12] |
|
–55600/ T + 26,010 |
–3,675 |
[13] |
|
–36332/ T + 15,675 |
–3,723 |
[настоящая работа] |
|
|FeCr 2 O 4 | = [Fe] + 2[Cr] + 4[O] |
||
|
–51870/ T + 24,480 |
–3,214 |
[12] |
|
–51806/ T + 21,832 |
–5,827 |
[14] |
|
–53420/ T + 22,920 |
–5,601 |
[15] |
|
–45796/ T + 18,830 |
–5,621 |
[16] |
|
–50755/ T + 21,660 |
–5,438 |
[17] |
|
–50873/ T + 22,744 |
–4,417 |
[настоящая работа] |
|
|Cr 2 O 3 | = 2[Cr] + 3[O] |
||
|
–40010/ T + 17,370 |
–3,992 |
[12] |
|
–43140/ T + 18,634 |
–4,399 |
[14] |
|
–44040/ T + 19,420 |
–4,093 |
[15] |
|
–45531/ T + 20,250 |
–4,059 |
[16] |
|
–36200/ T + 16,100 |
–3,227 |
[18] |
|
–41800/ T + 17,800 |
–4,517 |
[настоящая работа] |
|
|Cr 3 O 4 | = 3[Cr] + 4[O] |
||
|
–53350/ T + 23,510 |
–4,974 |
[12] |
|
–48850/ T + 21,430 |
–4,651 |
[16] |
|
–53510/ T + 23,960 |
–4,609 |
[17] |
|
–53521/ T + 23,960 |
–4,615 |
[19] |
|
–56170/ T + 24,300 |
–5,689 |
[настоящая работа] |
* В уравнениях реакций в квадратных скобках приведены компоненты металлического расплава, в круглых – оксидного расплава, в прямых скобках – твердые вещества.
действия могут образоваться: жидкие оксидные неметаллические включения переменного состава (FeO, CrO, Cr 2 O 3 ); частицы ферро-хромита FeCr2O4; чистый твердый оксид хрома Cr 2 O 3 ; частицы соединения Cr 3 O 4 .
Непосредственно расчет ПРКМ основан на законе действующих масс, связывающем константы равновесия высокотемпературных химических реакций с активностями компонентов металлического и оксидного расплавов, а также конденсированных фаз.
Для расчета координат ПРКМ необходимы сведения о температурных зависимостях констант равновесия реакций, протекающих в металлическом расплаве исследуемой системы. В табл. 1 приведены данные по константам равновесия из разных литературных источников в сравнении как между собой, так и с используемыми в ходе настоящей работы значениями.
Расчет активностей оксидного расплава для системы FeO–Cr 2 O 3 проводили с использованием приближения теории субрегулярных ионных растворов [1], энергетические параметры которой оказались равными [20]:
Q 1112 = 0 Дж/моль;
Q 1122 = +12115 Дж/моль;
Q 1222 = –60565 Дж/моль.
Моделирование оксидного расплава систем FeO–CrO, CrO–Cr 2 O 3 , FeO–CrO–Cr 2 O 3 проводили с использованием теории совершенных ионных растворов [1].
Активности металлического расплава рассчитывались с использованием параметров взаимодействия первого порядка по Вагнеру (табл. 2).
Активности чистых твердых веществ (в данном случае оксида Cr 2 O 3 , а также соединений FeCr 2 O 4 и Cr 3 O 4 ) принимались равными единице.
Результаты расчета ПРКМ системы Fe–Cr–O представлены на рис. 1. В области I приведены составы жидкого металла, находящегося в равновесии с оксидным расплавом переменного состава (FeO, CrO, Cr 2 O 3 ); в области II – c твердыми частицами соединения FeCr 2 O 4 ; в области III – с твердыми частицами оксида хрома Cr 2 O 3 ; в области IV – с твердыми частицами соединения Cr 3 O 4 . Также на рис. 1 приведены границы стабильности фаз: линия a – b определяет трехфазное равновесие «жидкий металл – оксидный расплав – FeCr2O4»; линия c – d – «жидкий металл – FeCr 2 O 4 – Cr 2 O 3 »; линия e – f – «жидкий металл – Cr 2 O 3 – Cr 3 O 4 ». Максимум раскислительной способности хрома приходится на область III, соответст-
Таблица 2
Параметры взаимодействия первого порядка в жидком железе e i j (1600 °С)
|
j i |
O |
Cr |
|
O |
–0,2 [21] |
–0,055 [15] |
|
Cr |
–0,179 [настоящая работа] |
–0,0003 [22] |
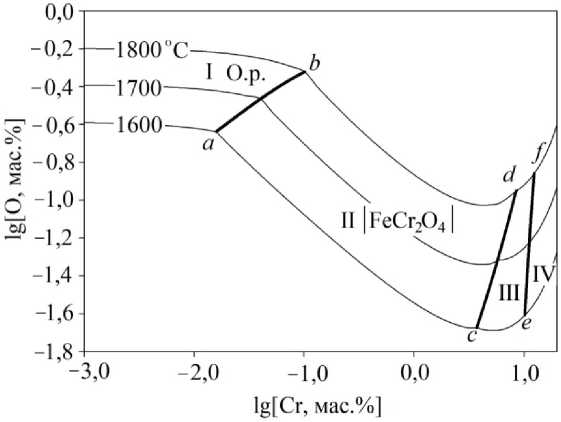
Рис. 1. Поверхность растворимости компонентов в металле системы Fe–Cr–O для интервала температур 1600–1800 °С
вующую равновесию жидкого металла с твердым оксидом хрома Cr2O3. При этом минимальная концентрация кислорода составляет 0,0204 мас. % для 5,31 мас. % хрома при 1600 °С.
Полученные в ходе настоящего расчета результаты по раскислительной способности хрома в системе Fe–Cr–O при 1600 °С были сравнены с имеющимися в литературе данными (рис. 2 и табл. 3).
Согласно рис. 2 угол наклона полученной в ходе настоящего расчета изотермы растворимости кислорода в системе Fe–Cr–O при 1600 °С (для области с концентрациями хрома менее чем 3 мас. %) согласуется с результатами работ [16, 26], однако расчетная изотерма проходит при более низких концентрациях кислорода по сравнению с литературными значениями. В области же с концентрациями хрома более чем 10 мас. %, угол наклона расчетной изотермы имеет хорошую сходимость с данными, опубликованными в работах [14, 18, 26].
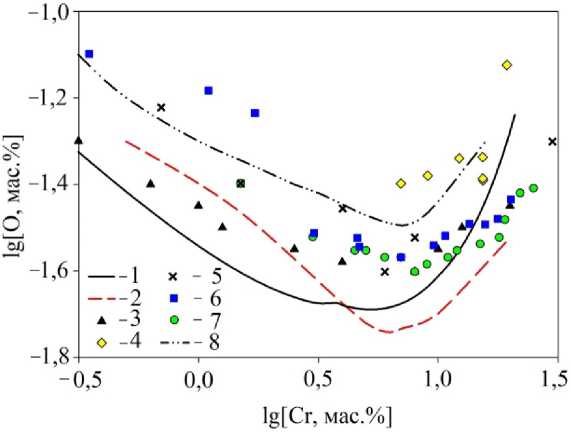
Рис. 2. Раскислительная способность хрома при 1600 °С в системе Fe–Cr–O: 1 – настоящая работа; 2 – данные И.С. Куликова [14];
3 – результаты расчета A. Ghosh и G.V.R. Murthy [16]; 4 – экспериментальные данные T. Itoh et al. [18]; 5 – экспериментальные данные D.C. Hilty et al. [23]; 6 – экспериментальные данные R.J. Frue-han [24]; 7 – экспериментальные данные D. Janke и W.A. Fischer [25];
8 – расчет I.-H. Jung et al. [26]
Таблица 3
Границы стабильности фаз и максимум раскислительной способности хрома при 1600 °С в системе Fe–Cr–O
|
Границы стабильности фаз по концентрации [Cr], мас. % |
Максимум раскислительной способности хрома |
Источник |
|||
|
FeCr 2 O 4 |
Cr 2 O 3 |
Cr 3 O 4 |
[Cr], мас. % |
[O] min , мас. % |
|
|
< 1,78 |
1,78–11,00 |
> 11,00 |
~ 11,20 |
~ 0,0200 |
[10] |
|
< 0,95 |
> 0,95 |
– |
7,10 |
0,0185 |
[14] |
|
< 3,00 |
3,00–8,00 |
> 8,00 |
~ 8,00 |
0,0250 |
[16] |
|
< 2,00 |
2,00–8,00 |
> 8,00 |
5,00 |
~ 0,0250 |
[17] |
|
– |
– |
– |
7,00 |
0,0400 |
[18] |
|
< 3,00 |
3,00–8,00 |
> 8,00 |
6,00 |
0,0250 |
[23] |
|
– |
– |
– |
7,00 |
0,0270 |
[24] |
|
< 1,50 |
1,50–8,00 |
> 8,00 |
8,00 |
0,0250 |
[25] |
|
< 4,47 |
> 4,47 |
– |
7,08 |
0,0320 |
[26] |
|
< 3,73 |
3,73–10,19 |
> 10,19 |
5,31 |
0,0204 |
[настоящая работа] |
Положение максимума раскислительной способности хрома практически совпадает с данными работы J. Chipman [17] по концентрации хрома и с расчетами Г.Г. Михайлова [10] по концентрации кислорода. Результаты расчета минимальной концентрации кислорода при 1600 °С превышают данные И.С. Куликова [14], но несколько ниже значений, приведенных в работах [18, 26].
Таким образом, полученные в ходе настоящей работы результаты показывают хорошую сходимость с литературными данными.
На основании проведенного исследования можно заключить, что хром не является сильным раскислителем для жидкого кислородсодержащего железа и должен рассматриваться в первую очередь как легирующий компонент. Потери хрома все же возможны при выплавке хромсодержащих сталей, в частности, при использовании недостаточного количества раскисляющих лигатур.
Выводы
Проведен термодинамический анализ взаимодействия хрома с кислородом в жидком железе. Для этого был выполнен расчет координат поверхности растворимости компонентов в металле в системе Fe–Cr–O для интервала температур 1600–1800 °С. В результате чего были определены границы термодинамической стабильности оксидных фаз, образующихся в процессе взаимодействия компонентов исследуемой системы. Так, для температуры 1600 °С жидкие неметаллические включения будут образовываться в качестве продуктов раскисления при концентрациях хрома в железе менее чем 0,016 мас. %; частицы феррохромита – при концентрациях хрома в железе от 0,016 до 3,73 мас. %; частицы оксида хрома Cr 2 O 3 – от 3,73 до 10,19 мас. % хрома; а образование в качестве продукта раскисления Cr 3 O 4 возможно лишь при концентрациях хрома в железе более чем 10,19 мас. %. В ходе моделирования также были построены изотермы раскислительной способности хрома в исследуемой системе. Минимальная концентрация кислорода, которую можно достичь в системе, составляет величину 0,0204 мас. % при 1600 °С. Таким образом, хром не является сильным раскислителем для жидкого кислородсодержащего железа и должен рассматриваться в первую очередь как легирующий компонент.
Список литературы Термодинамический анализ взаимодействия хрома с кислородом в жидком железе
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем / Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. - М.: Издат. Дом МИСиС, 2009. - 520 с.
- Самойлова, О.В. Фазовые равновесия в жидком металле системы Cu-Al-Cr-O / О.В. Самойлова, Л.А. Макровец, Г.Г. Михайлов // Известия вузов. Цветная металлургия. - 2017. - № 5. - С. 19-27. DOI: 10.17073/0021-3438-2017-5-19-27
- Thermodynamic reevaluation of the Fe-O system / T. Hidayat, D. Shishin, E. Jak, S.A. Decterov // Calphad. - 2015. - Vol. 48. - P. 131-144. DOI: 10.1016/j.calphad.2014.12.005
- Кубашевский, О. Металлургическая термохимия / О. Кубашевский, К.Б. Олкокк. - М.: Металлургия, 1982. - 392 с.
- Degterov, S. Critical evaluation and optimization of the thermodynamic properties and phase diagrams of the CrO-Cr2O3, CrO-Cr2O3-A12O3, and CrO-Cr2O3-CaO systems / S. Degterov, A.D. Pelton // Journal of Phase Equilibria. - 1996. - Vol. 17, no. 6. - P. 476-487. DOI: 10.1007/BF02665994


