Термодинамическое моделирование диаграммы состояния системы FeO-BaO-Al2O3
Автор: Самойлова Ольга Владимировна, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 3 т.21, 2021 года.
Бесплатный доступ
Щелочноземельные металлы (ЩЗМ) в последнее время становятся все более востребованными при производстве сталей и сплавов и являются частью большинства композиций для рафинирования и модифицирования. В связи с этим возрастает необходимость построения диаграмм состояния оксидных (шлаковых) систем, включающих в качестве компонентов оксиды ЩЗМ, в частности BaO. Эти сведения необходимы как для анализа состава образующихся неметаллических включений, так и для понимания влияния концентрации оксидов ЩЗМ на температуру плавления шлака. Как известно, термодинамическое моделирование является ключевым инструментом для выбора оптимального направления проводимых исследований в области металлургических технологий, поэтому расчет фазовых диаграмм оксидных систем как части многокомпонентного шлакового расплава является важной задачей для исследователей. Особенно это актуально для систем, содержащих BaO в качестве компонента, так как имеющиеся в литературе данные ограничиваются практически только диаграммами состояния двойных систем. В настоящей работе была построена поверхность ликвидус фазовой диаграммы системы FeO-BaO-Al2O3. Для термодинамического моделирования использовали теорию субрегулярных ионных растворов, энергетические параметры которой были подобраны в ходе настоящего расчета. Также нами были оценены температуры, энтальпии и энтропии образования алюминатов бария Ba3Al2O6, BaAl2O4, BaAl12O19 из компонентов оксидного расплава. Эти значения для Ba3Al2O6 оказались равны 1604 °С, 159 410 Дж/моль, 16,215 Дж/(моль∙К); для BaAl2O4 - 1814 °С, 101 424 Дж/моль, 7,332 Дж/(моль∙К); для BaAl12O19 - 1911 °С, 613 406 Дж/моль, 201,201 Дж/(моль∙К) соответственно. Полученные сведения были сравнены с имеющимися немногочисленными литературными данными.
Термодинамическое моделирование, фазовые равновесия, теория субрегулярных ионных растворов, система feo-bao-al2o3, оксид бария
Короткий адрес: https://sciup.org/147235285
IDR: 147235285 | УДК: 669.18 | DOI: 10.14529/met210302
Thermodynamic modeling of the FeO-BaO-Al2O3 phase diagram
Alkaline earth metals have recently become more and more in demand in the production of steels and alloys and are part of most compositions for refining and modification. In this connection, the need to construct the phase diagrams of the oxide (slag) systems, including alkali-earth metals oxides as components, in particular BaO, increases. This information is necessary both for analyzing the composition of the formed non-metallic inclusions and for understanding the effect of the concentration of alkali-earth metals oxides on the melting point of the slag. As is known, thermodynamic modeling is a key tool for choosing the optimal direction of research in the field of metallurgical technologies, therefore, the calculation of phase diagrams of oxide systems as part of a multicomponent slag melt is an important task for researchers. This is especially true for systems containing BaO as a component, since the data available in the literature are limited only to phase diagrams of binary systems. In this work, the surface of the liquidus of the FeO-BaO-Al2O3 phase diagram was plotted. The theory of subregular ionic solutions was used, the energy parameters of which were obtained in the course of this calculation. We also estimated the temperatures, enthalpies and entropies of formation of barium aluminates Ba3Al2O6, BaAl2O4, BaAl12O19 from the components of the oxide melt. These values for Ba3Al2O6 turned out to be 1604 °C, 159 410 J/mol, 16.215 J/(mol∙K); for BaAl2O4 - 1814 °C, 101 424 J/mol, 7.332 J/(mol∙K); for BaAl12O19 - 1911 °C, 613 406 J/mol, 201.201 J/(mol∙K), respectively. The information obtained was compared with the few available literature data.
Текст научной статьи Термодинамическое моделирование диаграммы состояния системы FeO-BaO-Al2O3
В связи с все более широким применением щелочноземельных металлов (в частности бария) для рафинирования и модифицирования сталей и сплавов [1–5] возрастает актуальность исследований оксидных (шлаковых) систем, включающих в качестве компонента оксид бария BaO.
Влияние концентрации оксида бария на технологические параметры металлургических шлаков и флюсов можно найти в работах [6–9]. Однако для анализа технологических аспектов металлургического производства также важно и знание диаграмм состояния оксидных (шлаковых) систем. В атласе шлаков [10] представлена некоторая информация о диаграммах состояния оксидных систем с BaO, но данных для большинства практически значимых систем не приводится. Нет сведений и по диаграмме FeO–BaO–Al 2 O 3 , в то время как она является ключевой для дальнейшей оценки влияния оксида бария на фазовый состав и температуру плавления барийсодержащих многокомпонентных оксидных систем.
Следует отметить, что для оценки фазовых равновесий как в металлических, так и в оксидных системах на настоящий момент широко используются методики термодинамического моделирования [11]. Применимость методик расчета из монографии Г.Г. Михайлова и др. [11] для некоторых систем с барием и оксидом бария рассматривалась нами ранее в работе [5].
Целью же настоящей работы является термодинамическое моделирование диаграммы состояния системы FeO–BaO–Al2O3. Для выполнения указанной цели было необходимо в первую очередь провести моделирование диаграмм состояния двойных оксидных систем FeO–BaO, FeO–Al 2 O 3 и BaO–Al 2 O 3 , а уже затем на основании полученных данных построить поверхность ликвидус для системы FeO–BaO–Al 2 O 3 .
Термодинамическое моделирование двойных и тройной оксидных систем проводили с использованием теории субрегулярных ионных растворов [11]. Значения параметров мо-
Физическая химия и физика металлургических систем
дели определяли в процессе решения систем нелинейных уравнений, для чего применялся метод Ньютона. Используя сведения о координатах ряда опорных точек (точек фазовых переходов, эвтектических или перитектических превращений и т. п.) на выбранной фазовой диаграмме, составлялись выражения, связывающие данные о равновесных составах при данной температуре с параметрами модели. С использованием этих данных подбирались энергетические параметры теории, а уже затем моделировалась вся линия или поверхность ликвидус исследуемой системы.
Системы FeO–BaO и FeO–Al 2 O 3 были рассчитаны по указанному алгоритму нами ранее [12, 13]. Согласно полученным в ходе расчета данным система FeO–BaO представляет собой диаграмму с простой эвтектикой с координатами 31,58 мол. % BaO и 1066 °С [12]. Диаграмма состояния системы FeO–Al 2 O 3 характеризуется двумя эвтектическими равновесиями (координаты точек эвтектики: 5 мас. % и 1335 °С; 65 мас. % и 1765 °С) и наличием соединения FeAl 2 O 4 , которое плавится конгруэнтно при температуре 1770 °С [13].
Для расчета систем Al 2 O 3 –BaO и FeO– BaO–Al 2 O 3 в настоящей работе согласно указанному алгоритму использовались данные по температурам, энтальпиям и энтропиям плавления чистых оксидов и их соединений
(табл. 1). Термодинамические данные о плавлении герцинита были оценены нами ранее в работе [13], а сведения по алюминатам бария были получены в ходе настоящего исследования.
Энергетические параметры теории субрегулярных ионных растворов для расчета исследуемых систем приведены в табл. 2. Следует отметить, что в системе Al2O3–BaO для использования выражений для расчета активностей компонентов оксидного расплава оксиду алюминия был присвоен индекс «1», а оксиду бария – индекс «2». В системе FeO–BaO–Al 2 O 3 оксиду железа был присвоен индекс «1», оксиду бария – «2», оксиду алюминия – «3». При изменении порядка и индексирования компонентов систем энергетические параметры необходимо менять местами, так как они описывают взаимодействие ионов в расплаве относительно первого компонента.
Результаты моделирования диаграммы состояния системы Al2O3–BaO приведены на рис. 1 и в табл. 3 в сравнении с литературными данными [17, 18]. Как видно из сравнения, мы при моделировании опирались прежде всего на экспериментальные данные, полученные G. Purt [17]. Данные из работы Н.А. Торопова и Ф.Я. Галахова [18] характеризуются значительно более высокими температурами большинства нонвариантных равновесий.
Таблица 1
Температуры, энтальпии и энтропии плавления чистых оксидов и их соединений
|
Вещество |
Температура плавления, °С |
Энтальпия плавления, Дж/моль |
Энтропия плавления, Дж/(моль∙К) |
|
FeO |
1378 [14] |
33 470 [15] |
20,273 |
|
BaO |
1925 [14] |
57 768 [16] |
26,282 |
|
Al2O3 |
2051 [14] |
107 530 [14] |
46,269 |
|
FeAl 2 O 4 |
1770 [13] |
217 584 [13] |
87,454 [13] |
|
Ba 3 Al 2 O 6 |
1604 |
159 410 |
16,215 |
|
BaAl 2 O 4 |
1814 |
101 424 |
7,332 |
|
BaAl 12 O 19 |
1911 |
613 406 |
201,201 |
Таблица 2
Энергетические параметры теории субрегулярных ионных растворов для расчета диаграммы состояния системы FeO–BaO–Al 2 O 3
|
Система |
Энергетические параметры Q ijkl , Дж/моль |
||
|
FeO–BaO [12] |
–22 505 |
–35 041 |
–27 933 |
|
FeO–Al 2 O 3 [13] |
+212 |
–21 502 |
–11 091 |
|
BaO–Al 2 O 3* |
–88 680 |
–42 147 |
–135 547 |
|
FeO–BaO–Al 2 O 3 |
–117 158 |
–163 302 |
–199 832 |
* Примечание. Для расчета диаграммы состояния системы Al2O3–BaO первый и последний параметры необходимо поменять местами
Таблица 3
Координаты точек нонвариантных равновесий в системе Al 2 O 3 –BaO
|
Равновесие |
Координаты |
Источник |
||
|
мас. % BaO |
x Ba2 + |
t , °C |
||
|
Ж ↔ Al 2 O 3 + BaAl 12 O 19 |
16,00 |
0,060 |
1875 |
[17] |
|
17,00 |
0,063 |
1890 |
[18] |
|
|
19,97 |
0,077 |
1910 |
[Настоящая работа] |
|
|
Ж ↔ BaAl 12 O 19 + BaAl 2 O 4 |
38,00 |
0,169 |
1620 |
[17] |
|
45,00 |
0,214 |
1790 |
[18] |
|
|
47,33 |
0,230 |
1600 |
[Настоящая работа] |
|
|
Ж ↔ BaAl 2 O 4 + Ba 3 Al 2 O 6 |
76,50 |
0,520 |
1485 |
[17] |
|
77,50 |
0,534 |
1710 |
[18] |
|
|
75,77 |
0,510 |
1569 |
[Настоящая работа] |
|
|
Ж ↔ Ba 3 Al 2 O 6 + BaO |
90,00 |
0,749 |
1425 |
[17] |
|
85,00 |
0,653 |
1660 |
[18] |
|
|
88,80 |
0,725 |
1485 |
[Настоящая работа] |
|
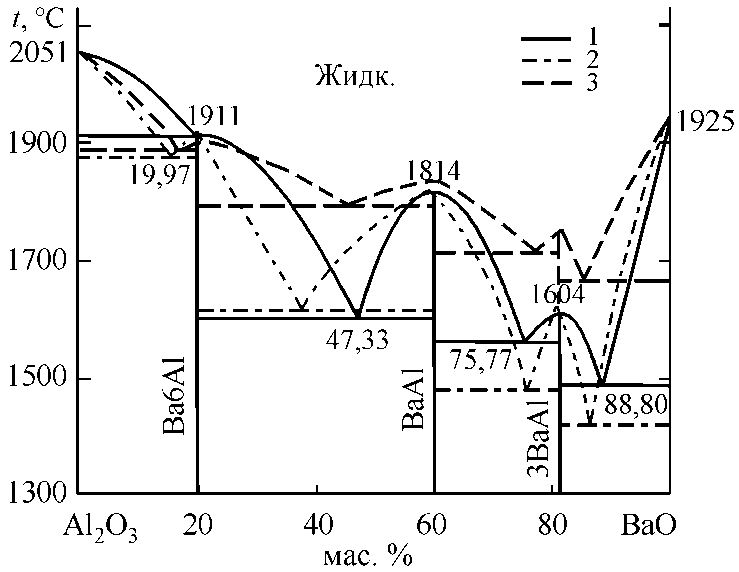
Рис. 1. Диаграмма состояния системы Al 2 O 3 –BaO: 1 – результаты проведенного нами моделирования; 2 – экспериментальные данные G. Purt [17]; 3 – экспериментальные данные Н.А. Торопова и Ф.Я. Галахова [18]. Ba6Al – BaAl 12 O 19 ; BaAl – BaAl 2 O 4 ; 3BaAl – Ba 3 Al 2 O 6
В ц е л о м ра с сч и тан н а я н а м и л и н и я л и кв идус ди аг ра мм ы с о сто я ния с и стемы Al 2 O 3 –BaO за н и ма ет п р о м е жут очное положен и е между данными [17] и [18].
П олуче н ные те м пе ра туры пл авле ни я а люм ин а т о в б ар и я с р а в н и м ы с л итера т ур н ыми данными [17–1 9]. Т ак , д л я г е кса а л юм и ната бария было получено значение t расч = 1911 °C, ч то сопостав и м о с 1 9 15 [1 7 ], 1 90 0 [ 1 8] и
1860 °C [19]. Для моноалюмината бария t расч = 1814 °C, в то же время это значение 1815 [17], 1830 [18] и 2000 °C [19]. А для Ba 3 Al 2 O 6 согласно моделированию t расч = 1604 °C, что сопоставимо с 1620 °C по данным G. Purt [17], но значительно ниже, чем 1750 °C по данным Н.А. Торопова и Ф.Я. Галахова [18].
Расчет поверхности ликвидус в системе FeO–BaO–Al 2 O 3 опирался на оценочные дан-
Физическая химия и физика металлургических систем
А12О3
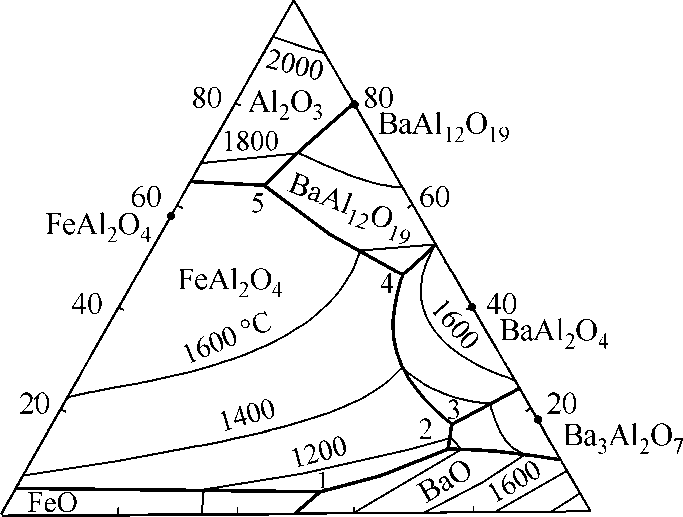
FeO 20 40 60 80 BaO
мае. %
Рис. 2. Результаты расчета поверхности ликвидус диаграммы состояния системы FeO–BaO–Al 2 O 3 . Координаты точек 1–5 приведены в табл. 4
ные ра б от ы [5], на р асчет дво йных окс ид ны х с ис тем в ра б ота х [12 , 1 3 ] и на ре з уль та ты, п о луче нные в ход е нас тоя щег о и сследован ия .
Пове рхно сть лик ви дус д иа г р а ммы с остояния системы FeO–BaO–A l 2O3 приведена на ри с. 2, в та бл. 4 п р е д ставл е ны координаты точе к но нва риа нтн ых р а внове с ий. На д и а г ра мм у на не с ены из отермич е ские сече н ия от 1200 до 2000 °С с шаг ом в д ве сти гр адусо в.
Сог ла с но рис . 2 д ля бол ь шин с тва с ос тавов системы FeO–BaO–Al2O3 в равновесии с окси д ны м рас плавом б уде т на ход и т ь с я ге рцинит FeAl2O4. Алю ми наты б ар ия б удут вы х о д ить на по верхн ос ть ли к вид у с п ри д ос та точно больших концентрациях о к с ида ба р ия (б олее 40 м а с. % ). Р а внове с ие о кс ид ного ра с плава с на иб ол ее тугопл а вк им веще с твом в с ис т е м е (кору н дом ) на чин а ет р е ализ о вы ва ть с я пр и е го конце нтр аци и бо лее че м 60 ма с . %.
Выводы
Проведено термодинамическое моделирование диаграмм состояния систем Al2O3–BaO и FeO–BaO–Al 2 O 3 . Определены энергетические параметры теории субрегулярных ионных растворов для расчета активностей компонентов оксидного расплава исследуемых систем. Получены термодинамические данные (температуры, энтальпии и энтропии) образования алюминатов бария из компонентов оксидного расплава. Результаты настоящего исследования позволяют перейти к решению проблем рафинирования и модифицирования сталей барийсодержащими лигатурами, а также оценить влияние образующегося в ходе технологического процесса оксида бария на параметры шлакового расплава. В частности, можно заключить, что для большинства составов систе-
Таблица 4
Координаты точек нонвариантных равновесий в системе FeO–BaO–Al 2 O 3
Список литературы Термодинамическое моделирование диаграммы состояния системы FeO-BaO-Al2O3
- Breitzmann, M. Refining of steel melts using alkaline earth metals / M. Breitzmann, H.-J. Engell, D. Janke // Steel Research. – 1988. – Vol. 59, no. 7. – P. 289–294. DOI: 10.1002/srin.198801505
- Перспективы применения барийсодержащих лигатур для раскисления и модифицирования транспортного металла / К.В. Григорович, К.Ю. Демин, А.М. Арсенкин, А.К. Гарбер // Металлы. – 2011. – № 5. – С. 146–156.
- Критерии оценки качества раскислителей и модификаторов для стали / И.В. Рябчиков, В.Г. Мизин, Р.Г. Усманов и др. // Сталь. – 2015. – № 2. – С. 24–27.
- Экспериментальное исследование рафинирования и модифицирования стали сплавами Si–Ca, Si–Sr и Si–Ba / И.В. Бакин, Н.А. Шабурова, И.В. Рябчиков и др. // Сталь. – 2019. – № 8. – С. 14–18.
- Михайлов, Г.Г. Барий как раскислитель и модификатор жидкой стали / Г.Г. Михайлов, Л.А. Макровец, Д.А. Выдрин // Вестник ЮУрГУ. Серия «Металлургия». – 2013. – Т. 13, № 1. – С. 45–50.
- Gao, E. Effect of alkaline earth metal oxides on the viscosity and structure of the CaO–Al2O3 based mold flux for casting high-Al steels / E. Gao, W. Wang, L. Zhang // Journal of Non-Crystalline Solids. – 2017. – Vol. 473. – P. 79–86. DOI: 10.1016/j.jnoncrysol.2017.07.029
- Viscosities of CaO–SiO2–Al2O3–(R2O or RO) melts / S. Sukenaga, N. Saito, K. Kawakami, K. Nakashima // ISIJ International. – 2006. – Vol. 46, no. 3. – P. 352–358. DOI: 10.2355/isijinternational.46.352
- Wang, Z. Effect of substituting CaO with BaO on the viscosity and structure of CaO–BaO–SiO2–MgO–Al2O3 slags / Z. Wang, I. Sohn // Journal of the American Ceramic Society. – 2018. – Vol. 101. – P. 4285–4296. DOI: 10.1111/jace.15559
- Effect of substituting CaO with BaO and CaO/Al2O3 ratio on the viscosity of CaO–BaO–Al2O3–CaF2–Li2O mold flux system / Z. Li, X. You, M. Li et al. // Metals. – 2019. – Vol. 9. – P. 142. DOI: 10.3390/met9020142
- Slag Atlas. 2nd Edition. Edited by Verein Deutscher Eisenhüttenleute (VDEh). – Düsseldorf: Verlag Stahleisen GmbH, 1995. – 616 p.
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем / Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. – М.: Издат. Дом МИСиС, 2009. – 520 с.
- Самойлова, О.В. Фазовая диаграмма системы FeO–SrO–BaO / О.В. Самойлова, Л.А. Макровец, И.В. Бакин // Вестник ЮУрГУ. Серия «Металлургия». – 2020. – Т. 20, № 3. – С. 5–11. DOI: 10.14529/met200301
- Samoilova, O.V. Thermodynamic modeling of phase equilibria in the FeO–MgO–Al2O3 system / O.V. Samoilova, L.A. Makrovets // Materials Science Forum. – 2020. – Vol. 989. – P. 3–9. DOI: 10.4028/www.scientific.net/MSF.989.3
- Кубашевский, О. Металлургическая термохимия / О. Кубашевский, С.Б. Олкокк. – М.: Металлургия, 1982. – 392 с.
- Darken, L.S. The system iron–oxygen. II. Equilibrium and thermodynamics of liquid oxide and other phases / L.S. Darken, R.W. Gurry // Journal of American Chemical Society. – 1946. – Vol. 68. – P. 798–816.
- Физико-химические свойства окислов. Справочник / под ред. Г.В. Самсонова. – М.: Металлургия, 1969. – 456 с.
- Purt, G. Binary system BaO–Al2O3 / G. Purt // Radex Rundschau. – 1960. – Vol. 4. – P. 198–202.
- Торопов, Н.А. Диаграмма состояния системы BaO–Al2O3 / Н.А. Торопов, Ф.Я. Галахов // Доклады АН СССР. – 1962. – Т. 82, № 1. – С. 69–70.
- Critical Melting Points and Reference Data for Vacuum Heat Treating / Ed. by V. Osterman, H. Antes Jr. – Solar Atmospheres Inc., 2010. – 42 p.


