Термодинамическое моделирование фазовой диаграммы системы Cu2O-BaO-Fe2O3
Автор: Самойлова Ольга Владимировна, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 2 т.18, 2018 года.
Бесплатный доступ
Выполнено термодинамическое моделирование диаграмм состояния двойных систем Cu2O-BaO, Cu2O-Fe2O3, BaO-Fe2O3, а также тройной системы Cu2O-BaO-Fe2O3. В ходе работы определены термодинамические модели и их параметры, необходимые для термодинамического описания активностей компонентов оксидного расплава в данных системах. Для расчета использовались приближения теории совершенных ионных растворов (для системы Cu2O-Fe2O3) и теории субрегулярных ионных растворов (для систем Cu2O-BaO, BaO-Fe2O3, Cu2O-BaO-Fe2O3). По результатам проведенного моделирования определены координаты точек нонвариантных превращений на фазовых диаграммах исследуемых двойных и тройной систем. Полученные результаты по термодинамическому моделированию координат линий ликвидуса фазовых диаграмм двойных систем Cu2O-BaO, Cu2O-Fe2O3, BaO-Fe2O3 были сопоставлены с разрозненными малочисленными литературными данными для исследуемых систем. В ходе работы впервые были определены области существования ферритов бария в тройной оксидной системе Cu2O-BaO-Fe2O3, а также построены изотермы на полной проекции поверхности ликвидуса диаграммы состояния системы Cu2O-BaO-Fe2O3. Используемая в работе методика моделирования позволила оценить энтальпии, температуры и энтропии плавления соединений оксида бария BaO с оксидом меди (I) (BaCu2O2); с оксидом железа (III) (Ba3Fe2O6, Ba2Fe2O5, BaFe2O4, BaFe12O19). Результаты моделирования, полученные в ходе выполнения настоящей работы, могут быть использованы для разработки технологических условий синтеза из оксидного расплава монокристаллов гексаферрита бария, в кристаллической решетке которого часть катионов железа замещена ионами меди.
Система cu2o-bao-fe2o3, термодинамическое моделирование, фазовые равновесия
Короткий адрес: https://sciup.org/147157135
IDR: 147157135 | УДК: 669.35 | DOI: 10.14529/met180201
Thermodynamic modeling of the phase diagram of the system Cu2O-BaO-Fe2O3
The thermodynamic modeling of the phase diagrams of the double systems Cu2O-BaO, Cu2O-Fe2O3, BaO-Fe2O3, and also the ternary system Cu2O-BaO-Fe2O3 was carried out. Thermodynamic models and their parameters, necessary for the thermodynamic description of the activity of the oxide melt components in these systems, are determined. For the calculation, the approximations of the theories of ideal ionic solutions (for the system Cu2O-Fe2O3) and subregular ionic solutions (for the systems Cu2O-BaO, BaO-Fe2O3, Cu2O-BaO-Fe2O3) were used. Based on the results of the simulation, the coordinates of the points of nonvariant transformations in the systems under study are defined. The obtained results on the thermodynamic modeling of the coordinates of the liquidus lines of the phase diagrams of the binary systems Cu2O-BaO, Cu2O-Fe2O3, BaO-Fe2O3 were compared with disparate small literary data for the systems under study. In the course of the work, the areas of existence of barium ferrites in the ternary oxide system Cu2O-BaO-Fe2O3 were determined for the first time. Also isotherms are constructed on the full projection of the liquidus surface of the phase diagram of the Cu2O-BaO-Fe2O3 system. The modeling method allowed to estimate the enthalpy, temperature and entropy of melting of compounds BaO with copper (I) oxide (BaCu2O2); with iron (III) oxide ((Ba3Fe2O6, Ba2Fe2O5, BaFe2O4, BaFe12O19)). The data obtained during the work will be necessary for the development of technological conditions for the synthesis of the barium hexaferrite monocrystals, in the crystal lattice of which part of the iron cations is replaced by copper ions.
Текст научной статьи Термодинамическое моделирование фазовой диаграммы системы Cu2O-BaO-Fe2O3
Гексаферрит бария представляет интерес как материал с ферромагнитными свойствами с возможностью использования в СВЧ устройствах [1–4]. Известно, что ионы железа в кристаллической решетке BaFe 12 O 19 могут быть частично заменены ионами других металлов, что может значительно повлиять на свойства гексаферрита [5–10]. В частности, возможно частичное замещение ионов железа ионами меди [10], что значительно повышает интерес к системе Cu 2 O–BaO–Fe 2 O 3 . Следует отметить, что в литературе отсутствуют сведения по фазовой диаграмме данной системы.
Целью настоящей работы является термодинамическое моделирование поверхности ликвидуса диаграммы состояния системы Cu 2 O–BaO–Fe 2 O 3 .
Подробно методика моделирования диаграмм состояния оксидных систем приведена в работах [11–15]. Для расчета координат поверхности ликвидуса фазовой диаграммы тройной системы необходимо провести расчет координат линий ликвидуса диаграмм состояния двойных систем, входящих в состав исследуемой системы. Следовательно, в рамках настоящей работы в первую очередь необходимо провести термодинамическое моделирование линий ликвидуса диаграмм состояния систем Cu 2 O–BaO, Cu 2 O–Fe 2 O 3 , BaO–Fe 2 O 3 , а затем, опираясь на полученные данные, рассчитать координаты поверхности ликвидуса фазовой диаграммы тройной системы Cu 2 O–BaO–Fe 2 O 3 .
Методика применяемого в данной работе расчета опирается на координаты (состав и температура) наиболее надежно определенных характерных точек на диаграммах: точек эвтектических, перитектических, фазовых переходов (например, плавления веществ в исследуемой системе) и т. п. Таким образом, для моделирования диаграмм состояния необходимы сведения о температурах и энтальпиях плавления веществ исследуемой системы. В табл. 1 приведены данные для веществ, входящих в систему Cu2O–BaO–Fe2O3.
Для моделирования линии ликвидуса диаграммы состояния системы Cu2O–Fe2O3 использовалось приближение теории совершенных ионных растворов [11]. Расчет координат линий ликвидуса систем Cu2O–BaO, BaO–Fe 2 O 3 , а также координат поверхности ликвидуса системы Cu 2 O–BaO–Fe 2 O 3 проводился с использованием приближения теории субрегулярных ионных растворов [11]. При проведении моделирования оксиду меди Cu 2 O был присвоен индекс «1», оксиду бария BaO – индекс «2», а оксиду железа Fe 2 O 3 – индекс «3». Все расчеты производились для парциального давления кислорода, равного 10 Па (10–4 атм) в каждой из исследуемых систем.
Значения энергетических параметров модели субрегулярных ионных растворов для двойных оксидных систем определялись в процессе решения систем нелинейных уравнений, для чего использовался метод Ньютона. Для составления уравнений использова- лись данные о составах ряда опорных точек, выбранных на линии ликвидуса фазовых диаграмм. Для каждого набора данных составлялось выражение, связывающее данные о равновесных составах при данной температуре с параметрами модели.
Для моделирования тройной оксидной системы необходимы также сведения о перекрестных энергетических параметрах взаимодействия теории субрегулярных ионных растворов, формула для расчета которых приведена в работе [13].
Энергетические параметры теории субрегулярных ионных растворов, использованные в данной работе при проведении термодинамического моделирования, приведены в табл. 2.
Сведений о виде диаграммы состояния системы Cu 2 O–BaO в литературе не имеется, однако есть данные о наличии соединения BaCu 2 O 2 , а также о том, что характер плавления этого соединения – конгруэнтный, а его температура плавления равняется 1015 °С [20]. Также согласно экспериментальным данным авторов работы [20] в системе имеются две точки эвтектики: при температуре 940 °С оксидный расплав находится в равновесии с Cu 2 O и BaCu 2 O 2 ; при температуре 890 °С оксидный расплав находится в равновесии с BaO и BaCu 2 O 2 . Результаты проведенного в ходе выполнения данной работы термодинамического моделирования линии ликвидуса
Таблица 1
Данные о температурах и энтальпиях плавления веществ, входящих в систему Cu 2 O–BaO–Fe 2 O 3
|
Вещество |
Т 0 ОГ Tm , С |
A m H 0 , Дж/моль T m |
|
Cu 2 O |
1242 [16] |
64 300 [16] |
|
BaO |
1925 [17] |
57 768 [18] |
|
Fe 2 O 3 |
1539 [19] |
87 000 [19] |
|
BaCu 2 O 2 |
1015 [20] |
97 310 [настоящая работа] |
|
CuFeO 2 |
1197 [17] |
64 350 [17] |
|
Ba 3 Fe 2 O 6 |
1318 [настоящая работа] |
240 300 [настоящая работа] |
|
Ba 2 Fe 2 O 5 |
1358 [настоящая работа] |
119 300 [настоящая работа] |
|
BaFe 2 O 4 |
1358 [настоящая работа] |
207 175 [настоящая работа] |
|
BaFe12O19 |
1457 [настоящая работа] |
424 265 [настоящая работа] |
Таблица 2
Энергетические параметры ( Q ijkl ) теории субрегулярных ионных растворов, Дж/моль
Литературных экспериментальных данных о диаграмме состояния системы Cu2O– Fe2O3 в литературе также не приводится. Имеются сведения о наличии соединения CuFeO2 [17]. Несмотря на то, что приводятся данные о температуре плавления CuFeO2 (1197 °С), сведений о характере плавления соединения (конгруэнтный или инконгруэнт-ный) не имеется. Результаты термодинамического моделирования линии ликвидуса фа- зовой диаграммы системы Cu2O–Fe2O3 приведены на рис. 2. Согласно проведенному расчету наиболее термодинамически вероятен конгруэнтный характер плавления соединения CuFeO2.
Сведения о диаграмме состояния системы BaO–Fe 2 O 3 достаточно противоречивы [21–23]. Согласно экспериментальным данным Y. Goto и T. Takada [21] в системе присутствуют три соединения: Ba 2 Fe 2 O 5 , BaFe 2 O 4 , BaFe 12 O 19 , которые имеют конгруэнтный характер плавления. По экспериментальным данным H. Sato [22]
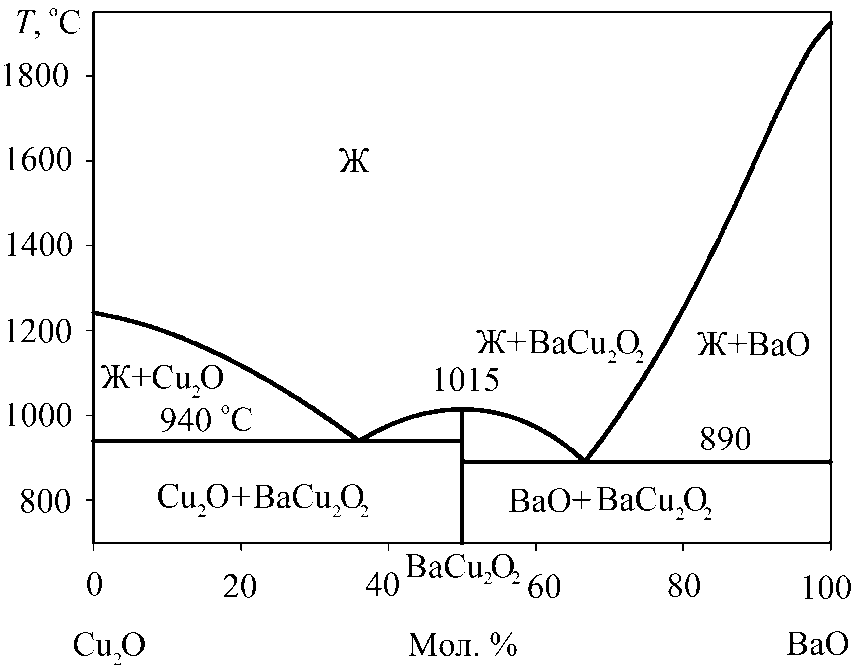
Рис. 1. Результаты расчета фазовой диаграммы системы Cu 2 O–BaO
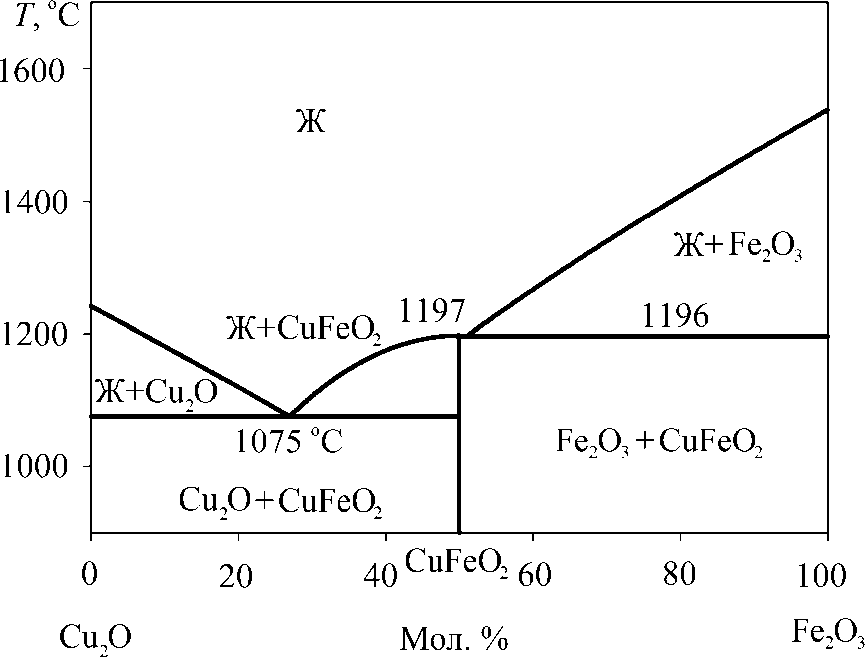
Рис. 2. Результаты расчета фазовой диаграммы системы Cu 2 O–Fe 2 O 3
в системе BaO–Fe2O3 имеются четыре соединения. Помимо ферритов бария, указанных в работе [21], в работе [22] приводится еще и соединение Ba3Fe2O6. Причем согласно [22] только Ba2Fe2O5 и BaFe2O4 имеют конгруэнтный характер плавления, соединения Ba3Fe2O6 и BaFe12O19 плавятся инконгруэнтно (по перитектическим реакциям). Д.А. Винник и др. в работе [23] приводят расчетную диаграмму состояния системы BaO–Fe2O3. Помимо четырех вышеуказанных ферритов бария, согласно [23] в системе имеется соединение Ba2Fe6O11, которое претерпевает твердофазный распад при температуре 1145 °С. Данные о положении линии ликвидуса исследуемой диаграммы состояния согласно литературным источникам [21–23] приведены на рис. 3 и в табл. 3.
Результаты проведенного в ходе выполнения данной работы термодинамического моделирования линии ликвидуса фазовой диаграммы системы BaO–Fe 2 O 3 также приведены на рис. 3 и в табл. 3.
Как следует из табл. 3 и рис. 3, в целом расчет, проведенный в ходе выполнения настоящей работы, достаточно хорошо совпадает с литературными данными. Наибольшее расхождение наблюдается для температуры плавления феррита бария BaFe 2 O 4 как между литературными источниками, так и между нашим расчетом и литературными данными.
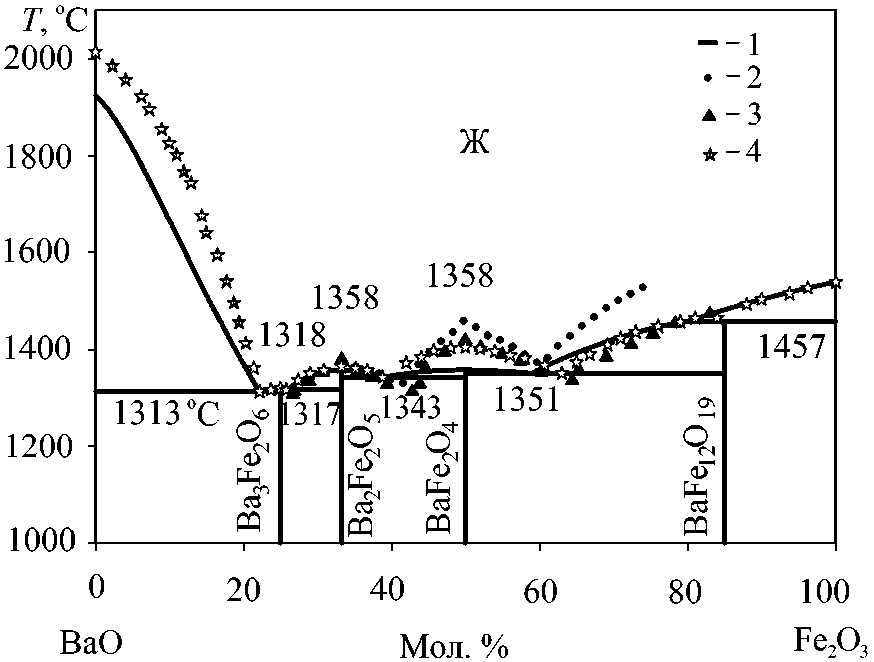
Рис. 3. Фазовая диаграмма системы BaO–Fe 2 O 3 : 1 – настоящая работа; 2 – экспериментальные данные [21]; 3 – экспериментальные данные [22];
4 – расчетные данные [23]
Таблица 3
Координаты характерных точек на диаграмме состояния системы BaO–Fe2O3
|
Вид фазового превращения |
Состав, мол. % |
Температура, °С |
||||||
|
[21] |
[22] |
[23] |
Настоящая работа |
[21] |
[22] |
[23] |
Настоящая работа |
|
|
Ж↔BaO+Ba 3 Fe 2 O 6 |
– |
– |
22,2 |
22,2 |
– |
– |
1313 |
1313 |
|
Ж↔Ba 3 Fe 2 O 6 |
– |
– |
25,0 |
25,0 |
– |
– |
1320 |
1318 |
|
Ж ↔ Ba 3 Fe 2 O 6 + Ba 2 Fe 2 O 5 |
– |
26,7 |
25,8 |
25,9 |
– |
1307 |
1317 |
1317 |
|
Ж↔Ba 2 Fe 2 O 5 |
33,3 |
33,3 |
33,3 |
33,3 |
1370 |
1380 |
1365 |
1358 |
|
Ж↔Ba 2 Fe 2 O 5 +BaFe 2 O 4 |
42,0 |
42,8 |
38,8 |
38,8 |
1330 |
1313 |
1343 |
1343 |
|
Ж↔BaFe 2 O 4 |
50,0 |
50,0 |
50,0 |
50,0 |
1460 |
1420 |
1405 |
1358 |
|
Ж↔BaFe 2 O 4 +BaFe 12 O 19 |
60,2 |
64,4 |
63,0 |
58,9 |
1370 |
1336 |
1351 |
1351 |
|
Ж+Fe 2 O 3 ↔BaFe 12 O 19 |
– |
83,0 |
84,0 |
79,9 |
– |
1474 |
1465 |
1457 |
Однак о в е ли чи н а рас хо жд е н и я н а хо д и тс я в п ред е л а х д оп у с ти мой п о гре ш н о с ти . Т ак, относительная погрешность δ д ля оп ре д е л е н н ой терм оди намическ им м о де л и ровани ем в на стоя ще й ра боте те мпе ра ту ры п ла в ле н и я BaFe2O4 п о отн ош ен ию к э к с п е ри ме н та л ьн ым данным [21] составляет 6,99 %; по отнош е н и ю к э к с п е ри ме н та л ьным д а н н ым [ 22 ] равняется 4,37 %; а п о от н о ш ени ю к рас че тным да н н ым [23] и м е е т в е ли ч и н у в 3, 35 %.
В ходе моделировани я ди а грамм с о с тоя н и я д в ой н ых сис те м бы ли оц е н е ны э н та л ь п и и , те мп е рат у ры и э нтроп и и п лавл е н и я со ед и н е н и й , об р а зующ и хся в э ти х с и с те ма х. Да н н ые п о те мпе ра ту ра м и э н та льп и ям п л ав л е н и я с ое д и не н и й п ри в ед е н ы в та бл. 1. Э н троп и и п лавл е н и я с ое ди н е н и й с лед у ю щ и е, Дж /( мо ль· К) : 26,12 (д ля сое д и н е н и я BaCu 2 O 2 );
20,76 (для соединения CuFeO 2 ); 90,12 (для соединения Ba 3 Fe 2 O 6 ); 25,91 (для соединения Ba 2 Fe 2 O 5 ); 97,25 (для соединения BaFe 2 O 4 ); 199,25 (для соединения BaFe 12 O 19 ).
В литературе отсутствуют сведения по фазовой диаграмме системы Cu 2 O–BaO– Fe2O3. Результаты выполненного в ходе настоящей работы расчета координат поверхности ликвидуса данной тройной оксидной системы приведены на рис. 4. На диаграмму нанесены изотермы с шагом в 100 °С в интервале температур от 900 до 1900 °С. Координаты точек нонвариантных превращений, реализующихся в системе, приведены в табл. 4. Следует отметить, что в тройной системе, согласно результатам моделирования, реализуется ряд равновесий, которых нет на двойных диаграммах состояния исследуемых систем.
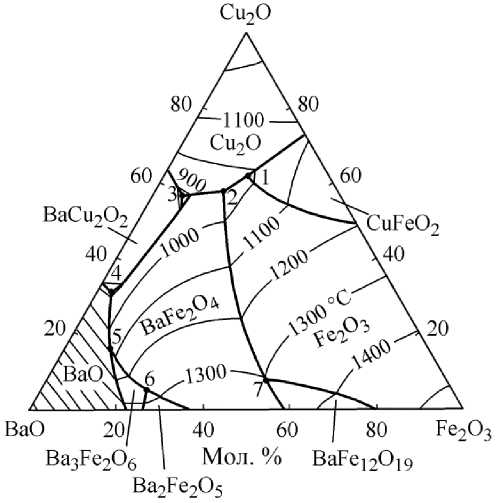
Рис. 4. Результаты моделирования полной проекции поверхности ликвидуса системы Cu 2 O–BaO–Fe 2 O 3 . Точки 1–7 – см. табл. 4
Таблица 4
Координаты точек нонвариантных превращений на диаграмме состояния системы Cu2O–BaO–Fe2O3
|
№ точки |
Состав, мол. % |
Температура, °С |
||
|
Cu 2 O |
BaO |
Fe 2 O 3 |
||
|
1 |
61,7 |
18,9 |
19,4 |
974 |
|
2 |
58,1 |
26,7 |
15,2 |
929 |
|
3 |
56,9 |
35,9 |
7,2 |
888 |
|
4 |
31,0 |
65,5 |
3,5 |
860 |
|
5 |
13,8 |
73,6 |
12,6 |
1108 |
|
6 |
4,1 |
70,9 |
25,0 |
1268 |
|
7 |
7,8 |
40,5 |
51,7 |
1306 |
Так, в частности, имеется равновесие оксидного расплава с моноферритом бария и с оксидом железа Fe 2 O 3 (линия «2–7»), которого нет в двойной системе BaO–Fe 2 O 3 .
Выводы
Проведено термодинамическое описание фазовых равновесий в системе Cu 2 O–BaO– Fe 2 O 3 . Определены термодинамические модели и их параметры, необходимые для описания фазовых диаграмм двойных систем Cu 2 O–BaO, Cu 2 O–Fe 2 O 3 , BaO–Fe 2 O 3 , а также поверхности ликвидуса тройной системы Cu 2 O–BaO–Fe 2 O 3 . В ходе моделирования оценены энтальпии, энтропии и температуры плавления соединений BaCu 2 O 2 , CuFeO 2 , Ba 3 Fe 2 O 6 , Ba 2 Fe 2 O 5 , BaFe 2 O 4 , BaFe 12 O 19 . Впервые определены координаты точек нонвариантных превращений в системе Cu 2 O–BaO–Fe 2 O 3 . Определены условия образования монокристаллов гексаферрита бария из оксидного расплава исследуемой тройной системы. При добавлении третьего компонента (оксида меди Cu 2 O) в систему BaO–Fe 2 O 3 температуры точек нонвариантных превращений с участием гексаферрита бария снижаются практически на 100 градусов до 1306 °С.
Работа осуществлена при финансовой поддержке РФФИ, грант № 16-08-00133 а.
Список литературы Термодинамическое моделирование фазовой диаграммы системы Cu2O-BaO-Fe2O3
- Gambino, R.J. Growth of Barium Ferrite Single Crystals/R.J. Gambino, F. Leonhard//J. Am. Ceram. Soc. -1961. -Vol. 44, no. 5. -P. 221-224 DOI: 10.1111/j.1151-2916.1961.tb15364.x
- Barium Hexaferrite Nanoparticles: Synthesis and Magnetic Properties/K.S. Martirosyan, E. Galstyan, S.M. Hossain et al.//Mater. Sci. Eng. B. -2011. -Vol. 176, no. 1. -P. 8-13 DOI: 10.1016/j.mseb.2010.08.005
- Pullar, R.C. Hexagonal Ferrites: A Review of the Synthesis, Properties and Applications of Hexaferrite Ceramics/Pullar R.C.//Prog. Mater. Sci. -2012. -Vol. 57, no. 7. -P. 1191-1334 DOI: 10.1016/j.pmatsci.2012.04.001
- Development of Z-type Hexaferrites for High Frequency EMI Shielding Applications/S.B.S. Magham, M. Sharma, S.R. Shannigrahi et al.//J. Magn. Magn. Mater. -2017. -Vol. 441. -P. 303-309 DOI: 10.1016/j.jmmm.2017.05.066
- Growth, Structural and Magnetic Characterization of Co-and Ni-substituted Barium Hexaferrite Single Crystals/D.A. Vinnik, D.A. Zherebtsov, L.S. Mashkovtseva et al.//J. Alloys Compd. -2015. -Vol. 628. -P. 480-484 DOI: 10.1016/j.jallcom.2014.12.124
- Jamalian, M. Magnetic and Microwave Properties of Barium Hexaferrite Ceramics Doped with Gd and Nd/M. Jamalian, A. Ghasemi, Asl M.J. Pourhosseini//J. Electron. Mater. -2015. -Vol. 44, no. 8. -P. 2856-2861 DOI: 10.1007/s11664-015-3720-x
- Cheng, Y. Enhanced Microwave Absorbing Properties of La3+ Substituting Barium Hexaferrite/Y. Cheng, X. Ren//J. Supercond. Nov. Magn. -2016. -Vol. 29, no. 3. -P. 803-808 DOI: 10.1007/s10948-015-3355-4
- Structural, Magnetic and Microwave Absorption Properties of Ce-doped Barium Hexaferrite/Z. Mosleh, P. Kameli, A. Poorbaferani et al.//J. Magn. Magn. Mater. -2016. -Vol. 397. -P. 101-107 DOI: 10.1016/j.jmmm.2015.08.078
- Kumar, S. Complex Permittivity, Permeability, Magnetic and Microwave Absorbing Properties of Bi3+ Substituted U-type Hexaferrite/S. Kumar, R. Chatterjee//J. Magn. Magn. Mater. -2018. -Vol. 448. -P. 88-93 DOI: 10.1016/j.jmmm.2017.06.123
- Cu-substituted Barium Hexaferrite Crystal Growth and Characterization/D.A. Vinnik, A.Yu. Tarasova, D.A. Zherebtsov et al.//Ceram. Int. -2015. -Vol. 41, no. 7. -P. 9172-9176 DOI: 10.1016/j.ceramint.2015.03.051
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. -М.: Издат. Дом МИСиС, 2009. -520 с.
- Михайлов, Г.Г. Фазовые равновесия в многокомпонентных системах с жидкими цветными металлами/Г.Г. Михайлов, Е.А. Трофимов, А.Ю. Сидоренко. -М.: Издат. Дом МИСиС, 2014. -158 с.
- Термодинамическое моделирование поверхности ликвидус диаграммы состояния системы Cu2O-Al2O3-ZrO2/О.В. Самойлова, Г.Г. Михайлов, Л.А. Макровец и др.//Вестник ЮУрГУ. Серия «Металлургия», 2015. -Т. 15, № 4. -С. 15-21 DOI: 10.14529/met150402
- Самойлова, О.В. Термодинамическое описание фазовых равновесий в системе Cu2O-CeO2-Ce2O3-La2O3/О.В. Самойлова, Г.Г. Михайлов, Л.А. Макровец//Вестник ЮУрГУ. Серия «Металлургия». -2017. -Т. 17, № 1. -С. 16-23 DOI: 10.14529/met170102
- Самойлова, О.В. Фазовые равновесия в жидком металле системы Cu-Al-Cr-O/О.В. Самойлова, Л.А. Макровец, Г.Г. Михайлов//Известия вузов. Цветная металлургия. -2017. -№ 5. -С. 19-27 DOI: 10.17073/0021-3438-2017-5-19-27
- Химическая энциклопедия: в 5 т./под ред. И.Л. Кнунянца. -М.: Сов. энцикл., 1990. -Т. 2. -671 с.
- Kubaschewski, O. Metallurgical Thermochemistry/O. Kubaschewski, C.B. Alcock. -Pergamon Press Ltd Publ., Oxford, 1979. -392 p.
- Физико-химические свойства окислов. Справочник/под ред. Г.В. Самсонова. -М.: Металлургия, 1969. -456 с.
- FactSage Thermochemical Software and Databases/C.W. Bale, P. Chartrand, S.A. Degterov et al.//Calphad. -2002. -Vol. 26, no. 2. -P. 189-228 DOI: 10.1016/S0364-5916(02)00035-4
- Lindemer, T.B. The BaO-Cu-CuO System. Solid-Liquid Equilibria and Thermodynamics of BaCuO2 and BaCu2O2/T.B. Lindemer, E.D. Specht//Physica C. -1995. -Vol. 255, no. 1-2. -P. 81-94 DOI: 10.1016/0921-4534(95)00460-2
- Goto, Y. Phase Diagram of the System BaO-Fe2O3/Y. Goto, T. Takada//J. Am. Ceram. Soc. -1960. -Vol. 43, no. 3. -P. 150-153 DOI: 10.1111/j.1151-2916.1960.tb14330.x
- Sato, H. Liquidus Surface and Isothermal Section Diagram at 973 K in BaO-Fe2O3-(0-50 mol%) B2O3 Pseudo-ternary System/H. Sato//Mater. Trans., JIM. -1997. -Vol. 38, no. 10. -P. 858-864. https://doi.org/10.2320/Matertrans1989.38.858
- Термодинамический анализ возможности использования расплавов системы BaO-Na2O-Fe2O3 для выращивания кристаллов гексаферрита бария/Д.А. Винник, Е.А. Трофимов, Д.П. Галкина и др.//Вестник ЮУрГУ. Серия «Металлургия». -2017. -Т. 17, № 3. -С. 34-45 DOI: 10.14529/met170305


