Термодинамическое моделирование фазовых равновесий с оксидными системами, содержащими РЗМ. Сообщение 2. Диаграммы состояния оксидных систем с Y 2O 3
Автор: Михайлов Геннадий Георгиевич, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 4 т.14, 2014 года.
Бесплатный доступ
Изучены оксидные системы, содержащие в качестве независимого компонента Y 2O 3. Установлены квазибинарные и тройные оксидные системы, сопряженные с областью существования жидких расплавов стали, содержащей иттрий и раскисленной высокоактивными элементами - кальцием, магнием, алюминием. Сведений о диаграмме состояний FeO-Y 2O 3, определяющей состав оксидных равновесных фаз с жидким железом, в научной литературе не имеется. По аналогии с диаграммой с La 2O 3 оксидная система FeO-Y 2O 3 может быть описана в приближении теории совершенных ионных расплавов. Используя данные о температурах и теплотах плавления FeO и Y 2O 3, установлена температура эвтектического превращения, состав двойной эвтектики и координаты линий ликвидус. Для двойных диаграмм состояний Y 2O 3-MgO, Y 2O 3-СaO, Y 2O 3-Al 2O 3 определены термодинамические параметры образования алюминатов иттрия (2Y 2O 3•Al 2O 3, Y 2O 3•Al 2O 3, 3Y 2O 3•5Al 2O 3) и соединений Y 2O 3 с оксидом кальция (CaO•2Y 2O 3, CaO•Y 2O 3, 3CaO•Y 2O 3). На основании данных о свойствах кристаллических составляющих рассмотренных двойных и тройных систем и сведений об энергетических параметрах теории субрегулярных растворов построены тройные диаграммы состояний систем FeO-Y 2O 3-CaO, FeO-Y 2O 3-MgO, FeO-Y 2O 3-Al 2O 3. Информация о координатах поверхности ликвидус для этих систем получена впервые. На основании выполненных расчетов построена поверхность растворимости кислорода и иттрия в жидком железе.
Термодинамика, фазовые равновесия, диаграммы состояния, оксид иттрия
Короткий адрес: https://sciup.org/147156897
IDR: 147156897 | УДК: 669.017
Thermodynamic simulation of phase equilibria with oxide systems containing rare-earth metals. Report 2. Phase diagrams of oxide systems with Y 2O 3
The oxide systems containing Y 2O 3 were studied. The quasibinary and ternary oxide systems conjugated with the area of existence of steel liquid melts containing yttrium and deoxidated by highly active elements i.e. calcium, magnesium, aluminum were defined. In literature there is no data on the FeO-Y 2O 3 phase diagram defining the composition of the oxide phases in equilibrium with liquid iron. By analogy with the La2O3 diagram the oxide system FeO-Y 2O 3 can be described using the theory of perfect ionic melts. With the data on temperatures and melting heats of FeO and Y 2O 3 the temperature of the eutectic transformation, the composition of binary eutectic and the coordinates of liquids lines are determined. For the binary phase diagrams of Y 2O 3-MgO, Y 2O 3-CaO, Y 2O 3-Al 2O 3 the thermodynamic parameters of formation of aluminates of yttrium (2Y 2O 3•Al 2O 3, Y 2O 3•Al 2O 3, 3Y 2O 3•5Al 2O 3) and Y 2O 3 with calcium oxide were defined (CaO•2Y 2O 3, CaO•Y 2O 3, 3CaO•Y 2O 3). Based on the data of the crystalline component properties of the binary and ternary systems considered and on the data of the energetic parameters of the theory of the subregular solutions the ternary phase diagrams of systems FeO-Y 2O 3-CaO, FeO-Y 2O 3-MgO, FeO-Y 2O 3-Al 2O 3 were constructed. The novelty of the research is the data obtained on the liquids surface coordinates for these systems. Calculations made allowed to create the surface of oxygen and yttrium solubility in liquid iron.
Текст научной статьи Термодинамическое моделирование фазовых равновесий с оксидными системами, содержащими РЗМ. Сообщение 2. Диаграммы состояния оксидных систем с Y 2O 3
Значительная часть исследований рафинирующей и модифицируещей способности РЗМ сводится к изучению свойств некоторого обобщенного металла, в котором в основном находятся церий, неодим, празеодим, лантан и некоторое количество иттрия [1]. Можно отметить лишь несколько работ, в которых освещается раскисли-тельная способность иттрия [2, 3]. Сплав (силико-иттрий) используется для некоторых специальных целей и выпускается в крайне незначительных количествах. В современной металлургии иттрий нашел применение при выплавке жаропрочных сплавов на хромовой основе для газовых турбин как антикоррозионная добавка или жаростойкое покрытие [4, 5]. Иттрий высокоактивный металл, обладающий высоким сродством к кислороду и сере [5]. Для того чтобы определить концентрационные пределы рафинирующего и модифицирующего действия иттрия, необходимо установить строение поверхности растворимости компонентов в жидком железе, содержащем иттрий, в которое может быть введены и другие высокоактивные элементы, такие как алюминий, кальций, магний. Для получения достоверных термодинамических данных о раскислительной способности вышеуказанных композиций высокоактивных металлов необходимо иметь сведения о строении оксидных диаграмм состояний, сопряженных с областью существования жидких металлических расплавов. Поэтому в настоящей работе было необходимо
установить вид двойных диаграмм состояний FeO–Y 2 O 3 , Y 2 O 3 –CaO, Y 2 O 3 –MgO и Y 2 O 3 –Al 2 O 3 , а также тройных диаграмм состояний FeO–Y2O3–CaO, FeO–Y 2 O 3 –MgO, FeO–Y 2 O 3 –Al 2 O 3 . Данные по системе FeO–Y 2 O 3 и всем тройным оксидным системам в литературе отсутствуют. Для систем Y 2 O 3 –CaO, Y 2 O 3 –MgO и Y 2 O 3 –Al 2 O 3 имеются сведения об образовании химических соединений, а также температурах и составах двойных эвтектик. С использованием теории субрегулярных ионных оксидных расплавов была реализована возможность построения диаграмм состояний Y2O3–CaO, Y2O3–MgO и Y2O3–Al2O3 по методике, изложенной в монографии [6]. В связи с полным отсутствием данных по диаграмме FeO–Y 2 O 3 допустили, что оксидные расплавы в системе FeO–Y 2 O 3 есть совершенные ионные растворы. Результаты таких расчетов приведены на рис. 1. На рис. 2 представлены результаты термодинамических расчетов координат линий ликвидус для систем Y 2 O 3 –MgO, Y 2 O 3 –CaO, Y2O3–Al2O3. В табл. 1 представлены данные по процессам плавления оксидов, а также реакциям раскисления железа с образованием оксидов соответствующих компонентов. В табл. 2 указаны зависимости констант равновесия реакций образования соединений из соответствующих простых оксидов для диаграмм состояний от температуры Y 2 O 3 –CaO и Y 2 O 3 –Al 2 O 3 . Также в табл. 2 приведены подобранные в данной работе теплоты плавления соединений иттрия с оксидами кальция и
Рис. 1. Расчетная диаграмма состояния системы FeO–Y 2 O 3
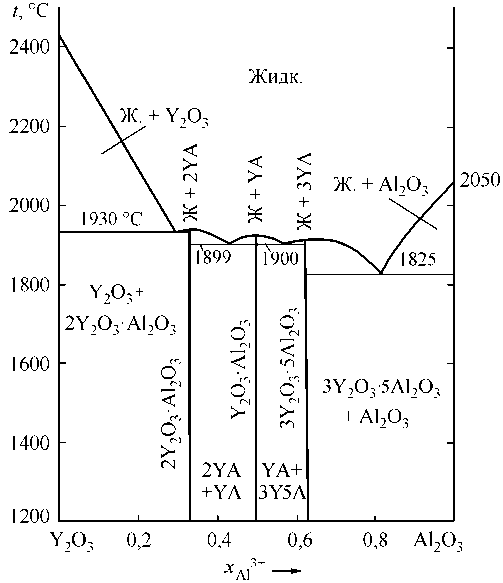
в)
Рис. 2. Расчетные диаграммы состояния систем: а) MgO–Y 2 O 3 ; б) CaO–Y 2 O 3 ; в) Al 2 O 3 –Y 2 O 3
Таблица 1
Зависимости констант равновесия от температуры для оксидов
|
Оксид |
lg K пл |
lg K ж |
lg K тв |
|
FeO |
–1749/ Т + 1,062 |
–6320/ Т + 2,734 |
–8069/ Т + 5,8 |
|
Y 2 O 3 |
–4372/ T +1,617 |
–67 028/ Т + 20,19 |
–71 400/ Т + 21,81 |
|
MgO |
–3016/ Т + 1,37 |
–22 457/ Т + 6,54 |
–26 500/ T + 7,85 |
|
CaO |
–2623/ Т + 0,913 |
–31 480/ Т +12,55 |
–34 103/ Т + 13,46 |
|
Al 2 O 3 |
–5683/ Т + 2,447 |
–58 320/ Т + 18,02 |
–64 000/ Т + 20,48 |
Таблица 2
Теплоты плавления и зависимости констант равновесия от температуры для соединений
|
Соединение |
Δ H пл , кал/моль |
lg K пл |
lg K тв |
|
|
Расчет |
[7] |
|||
|
CaO·2Y 2 O 3 (C2Y) |
58 400 |
58 800 |
–12 769/ Т + 2,25 |
–178 305/ Т + 55,181 |
|
CaO·Y 2 O 3 (CY) |
37 800 |
33 500 |
–8261/ Т + 1,326 |
–106 769/ Т + 34,066 |
|
3CaO·Y 2 O 3 (3CY) |
54 500 |
54 800 |
–11 916/ Т + 0,975 |
–173 384/ Т + 58,815 |
|
2Y 2 O 3 ·Al 2 O 3 (2YA) |
35 840 |
–7833/ Т + 1,482 |
–200 210/ Т + 59,882 |
|
|
Y 2 O 3 ·Al 2 O 3 (YA) |
23 850 |
–5212/ Т + 0,847 |
–130 560/ Т + 39,057 |
|
|
3Y 2 O 3 ·5Al 2 O 3 (3Y5A) |
310 250 |
–67 815/ Т + 25,115 |
–560 500/ Т + 175,785 |
|
Таблица 3
Значения параметров теории субрегулярных ионных растворов Q ijkl
|
Система |
Параметры теории Qijkl , кал/моль |
||
|
FeO–Y 2 O 3 |
0 |
0 |
0 |
|
Y 2 O 3 –Al 2 O 3 |
–4186 |
–1835 |
–7105 |
|
Y 2 O 3 –CaO |
–26 845 |
–42 106 |
–21 622 |
|
Y 2 O 3 –MgO |
5304 |
953 |
2479 |
|
FeO–Y 2 O 3 –Al 2 O 3 |
–50 000 |
20 000 |
–50 000 |
|
FeO–Y 2 O 3 –CaO |
–33 438 |
–54 795 |
–56 469 |
|
FeO–Y 2 O 3 –MgO |
0 |
0 |
0 |
Таблица 4
Инвариантные точки системы Y 2 O 3 –CaO
|
Фаза |
Процесс |
Состав, x Ca 2 + |
Т , °С |
||
|
Расчет |
[7] |
Расчет |
[7] |
||
|
Y2O3 + CaO·2Y2O3 + жидкость |
Эвтектика |
0,117 |
0,111 |
2140 |
2140 |
|
CaO·2Y2O3 + жидкость |
Плавление |
0,200 |
0,200 |
2254 |
2280 |
|
CaO·2Y2O3 + CaO·Y2O3 + жидкость |
Перитектика |
0,360 |
0,440 |
1950 |
– |
|
CaO·Y2O3 + жидкость |
Инконгр. плавление |
0,333 |
0,333 |
||
|
CaO·Y2O3+3CaO·Y2O3 + жидкость |
Эвтектика |
0,434 |
0,400 |
1860 |
1860 |
|
3CaO·Y2O3 + жидкость |
Плавление |
0,600 |
0,600 |
2230 |
2230 |
|
3CaO·Y2O3 +CaO+ жидкость |
Эвтектика |
0,740 |
0,670 |
1960 |
1960 |
Таблица 5
Инвариантные точки системы Y 2 O 3 –Al 2 O 3
|
Фаза |
Процесс |
Состав, x Al 3 + |
Т , °С |
||
|
Расчет |
[8] |
Расчет |
[8] |
||
|
Y 2 O 3 + 2Y 2 O 3 ·Al 2 O 3 + жидкость |
Эвтектика |
0,294 |
0,295 |
1930 |
1930 |
|
2Y 2 O 3 ·Al 2 O 3 + жидкость |
Плавление |
0,333 |
0,333 |
1937 |
1990 |
|
2Y 2 O 3 ·Al 2 O 3 + Y 2 O 3 ·Al 2 O 3 + жидкость |
Эвтектика |
0,431 |
0,440 |
1899 |
1900 |
|
Y 2 O 3 ·Al 2 O 3 + жидкость |
Плавление |
0,5 |
0,5 |
1918 |
1925 |
|
Y2O3·Al2O3 + 3Y2O3·5Al2O3 + жидкость |
Эвтектика |
0,565 |
0,560 |
1900 |
1900 |
|
3Y2O3·5Al2O3 + жидкость |
Плавление |
0,625 |
0,625 |
1905 |
1950 |
|
3Y2O3·5Al2O3 + Al2O3 + жидкость |
Эвтектика |
0,817 |
0,810 |
1825 |
1825 |
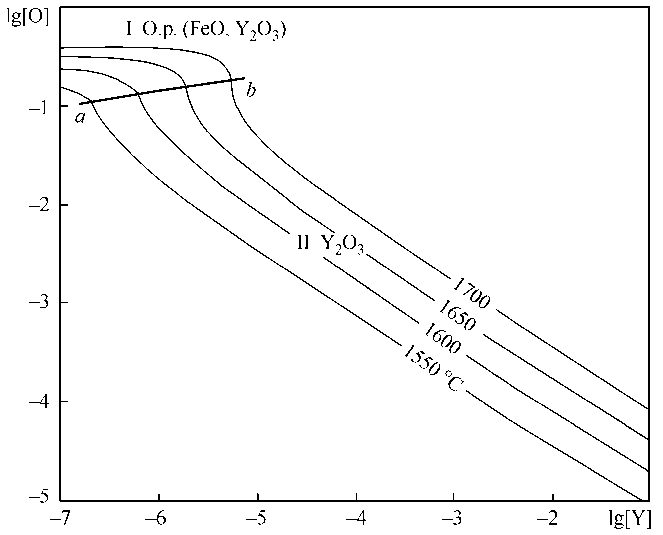
Рис. 4. ПРКМ системы Fe–Y–O
Выводы
-
1. Диаграмма состояний FeO–Y 2 O 3 относится к простейшим диаграммам с простой эвтектикой.
-
2. Определены термодинамические характеристики оксидных расплавов и соединений в двойных диаграммах состояний Y2O3–CaO, Y2O3–MgO и Y2O3–Al2O3 и сформирована база термодинамических данных для учета влияния кальция, магния и алюминия на раскислительную способность иттрия.
-
3. Выполнено термодинамическое моделирование диаграмм состояний FeO–Y2O3–CaO, FeO– Y 2 O 3 –MgO, FeO–Y 2 O 3 –Al 2 O 3 . Установлено отсутствие тройных оксидных соединений. Определены энергетические параметры теории субрегулярных растворов для трехкомпонентных оксидных расплавов. Сформулирована база данных для построения сложных 4-компонентных поверхностей растворимости компонентов в жидком металле.
-
4. Построена политермическая поверхность растворимости иттрия в жидком железе. Раскисли-тельная способность иттрия в жидком железе несколько ниже, нежели раскислительная способность лантана.
-
2. Сенин, А.В. Термодинамика процессов взаимодействия иттрия с кислородом и серой в жидком железе / А.В. Сенин, Г.Г. Михайлов // Изв. вузов. Черная металлургия. – 1987. – № 9. – С. 59–63.
-
3. Тарасюк, Л.И. Термодинамика раскисления железа иттрием / Л.И. Тарасюк, В.В. Морнева, Е.А. Казачков // Вест. Приазов. гос. техн. ун-та. Сер. «Технические науки». – 2011. – № 2 (23). – С. 33–38.
-
4. Симс, Ч. Жаропрочные сплавы / Ч. Симс, В. Хагель. – М.: Металлургия, 1976. – 567 с.
-
5. Фабер, Г.Х. Влияние хрома на сопротивление коррозии и сопротивление сплавов и покрытий / Г.Х. Фабер //Жаропрочные сплавы для газовых турбин: материалы междунар. конф. – М.: Металлургия, 1981. – С. 125–141.
-
6. Михайлов, Г.Г. Термодинамика металлургических процессов и систем / Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов – М.: Издат. Дом МИСИС. – 2009. – 519 с.
-
7. Удалов, Ю.П. Диаграмма плавкости системы CaO–Y2O3–А12О3 / Ю.П. Удалов, З.С. Аппен, В.В. Паршина // Журн. неорган. химии. – 1979. – Т. 24, № 10. – С. 2786–2792.
-
8. Lakiza, S.M. Phase diagram of the Al2O3– HfO2–Y2O3 system / S.M. Lakiza, Ya.S. Tishchenko, L.M. Lopato // Journal of the European Ceramic Society. – 2011. – No. 31 (7). – P. 1285–1291.
Работа поддержана грантом РФФИ № 13-08-12167.
Список литературы Термодинамическое моделирование фазовых равновесий с оксидными системами, содержащими РЗМ. Сообщение 2. Диаграммы состояния оксидных систем с Y 2O 3
- Ферросплавы с редкоземельными и щелочноземельными металлами/И.В. Рябчиков, В.Г. Мизин, Н.П. Лякишев и др. -М.: Металлургия. 1983. -272 с.
- Сенин, А.В. Термодинамика процессов взаимодействия иттрия с кислородом и серой в жидком железе/А.В. Сенин, Г.Г. Михайлов//Изв. вузов. Черная металлургия. -1987. -№ 9. -С. 59-63.
- Тарасюк, Л.И. Термодинамика раскисления железа иттрием/Л.И. Тарасюк, В.В. Морнева, Е.А. Казачков//Вест. Приазов. гос. техн. ун-та. Сер. «Технические науки». -2011. -№ 2 (23). -С. 33-38.
- Симс, Ч. Жаропрочные сплавы/Ч. Симс, В. Хагель. -М.: Металлургия, 1976. -567 с.
- Фабер, Г.Х. Влияние хрома на сопротивление коррозии и сопротивление сплавов и покрытий/Г.Х. Фабер//Жаропрочные сплавы для газовых турбин: материалы междунар. конф. -М.: Металлургия, 1981. -С. 125-141.
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов -М.: Издат. Дом МИСИС. -2009. -519 с.
- Удалов, Ю.П. Диаграмма плавкости системы CaO-Y2O3-А12О3/Ю.П. Удалов, З.С. Аппен, В.В. Паршина//Журн. неорган. химии. -1979. -Т. 24, № 10. -С. 2786-2792.
- Lakiza, S.M. Phase diagram of the Al2O3-HfO2-Y2O3 system/S.M. Lakiza, Ya.S. Tishchenko, L.M. Lopato//Journal of the European Ceramic Society. -2011. -No. 31 (7). -P. 1285-1291.


