Термодинамическое моделирование линии ликвидус системы Ni-Si
Автор: Самойлова Ольга Владимировна, Макровец Лариса Александровна, Михайлов Геннадий Георгиевич, Трофимов Евгений Алексеевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 24 (283), 2012 года.
Бесплатный доступ
Используя модели регулярных и субрегулярных растворов, рассчитана линия ликвидус диаграммы состояния Ni-Si. Показано, что модель регулярных растворов неудовлетворительно описывает данную систему. Результаты расчета по теории субрегулярных растворов хорошо согласуются с литературными данными. Полученные значения энергетических параметров теории могут быть использованы для термодинамического моделирования более сложных систем.
Теория регулярных растворов, теория субрегулярных растворов, диаграмма состояния системы ni-si
Короткий адрес: https://sciup.org/147160236
IDR: 147160236 | УДК: 544.3.01+544.32
Thermodynamic modeling of liquidus line of Ni-Si system
Liquidus line of Ni-Si system has been calculated, using theories of regular and subregular solutions. Theory of regular solutions does not describe the diagram satisfactorily. Results of calculations using theory of subregular solutions are in good agreement with literature data. Energy parameters of the theory of subregular solutions have been defined. These data may be used for thermodynamic modeling of more complicated systems.
Текст научной статьи Термодинамическое моделирование линии ликвидус системы Ni-Si
Интерес к системе Ni–Si обусловлен большим количеством образующихся в ней силицидов. Известно, что силициды никеля в сплавах системы Cu–Si–Ni существенно упрочняют их [1]. С другой стороны, одной из рекомендуемых [2] методик повышения эффективности удаления никеля из меди при окислительном рафинировании является использование кремния при раскислении меди (так называемое «силицирование»). В работе [3] содержатся данные о возможности отделения силицидов никеля при электрохимическом растворении медного анода. Указывается, что скорость растворения основного материала анода на 2,5–3 порядка больше скорости растворения силицидных фаз.
Ключевой для понимания процессов, реализующихся в системе Cu–Si–Ni, является система Ni–Si, адекватная термодинамическая модель которой откроет путь к моделированию более сложных систем.
Методика исследования
Для моделирования фазовых равновесий, реализующихся в системе Ni–Si, опробовано два подхода: посредством модели регулярных растворов и с помощью модели субрегулярных растворов.
Активность компонентов бинарной системы в приближении теории регулярных растворов описывается выражением [4]:
(1-Ni )2 Q ai = Nie RT . (1)
В соответствии с приближением теории субрегулярных растворов [5] активность компонентов для бинарной системы будет равна
Nj 2( NiQj + NjQji )
a i = N i e RT . (2)
В этих формулах N – атомные доли компонентов раствора; Q – энергии смешения его компонентов; Т – температура; R – универсальная газовая постоянная.
Методика моделирования состоит в следующем. На первом этапе расчета определяются значения энергий смешения Q . Для этого используются данные по температурам и теплотам плавления чистых простых веществ, а также литературные данные о положении некоторых (реперных) точек на линии ликвидус диаграммы состояния. Далее, зная параметры Q и задаваясь значением атомной доли компонентов раствора, рассчитывается вся линия ликвидус для выбранной системы. Следует отметить, что для систем с интерметаллидами, силицидами и т. п. на стадии определения Q требуются данные по константам плавления соединений. Если литературных данных нет, то методика расчета позволяет их оценить.
Согласно диаграмме состояния системы Ni–Si [6] в ходе взаимодействия никеля с кремнием могут образовываться следующие соединения: Ni 3 Si, Ni 5 Si 2 , Ni 2 Si, Ni 3 Si 2 , NiSi и NiSi 2 . В некоторых источниках указывается на существование еще и фаз Ni 31 Si 12 и Ni 25 Si 9 [7, 8] (рис. 1).
Физическая химия
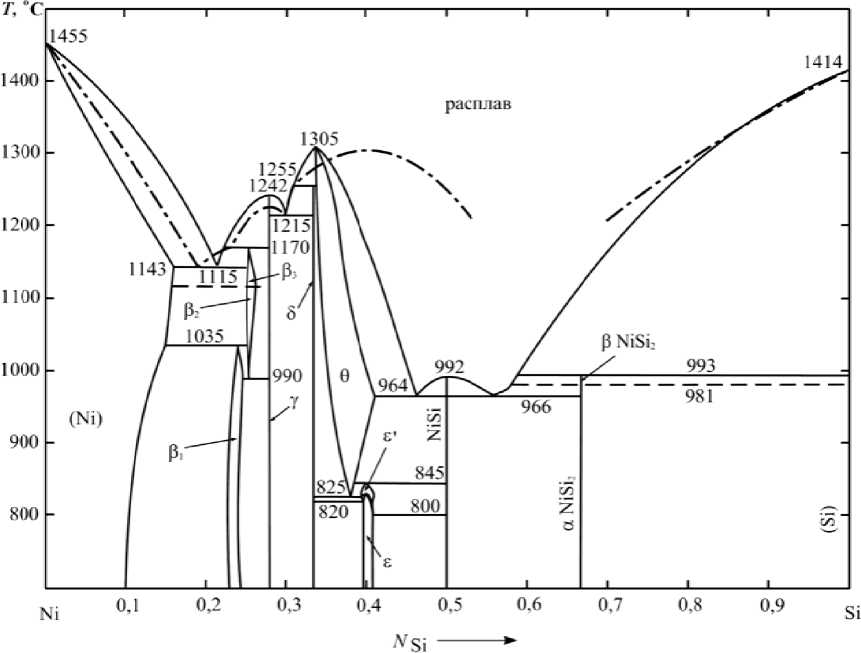
Рис. 1. Диаграмма состояния системы Ni–Si: сплошные линии – литературная диаграмма [8]; пунктир – результат расчета по теории регулярных растворов
Данная диаграмма состояния характеризуется большим количеством двойных соед и нений.
Процесс перехода соединения в жидкое состояние будем описывать сле д ующей реакцией:
|MmNn| = m[M] + n[N].(3)
Здесь |M m N n | – чистое твердое соединение; [М] и [N] – компоненты металли ч еского расплава.
Для реакции (3) закон действующих масс (актив н ость соединения равна 1)
K = «[M]«[N].
Если температурную зависимость константы рав н овесия реакции (3) записать в виде
1g K = -T + B,(5)
то с учетом соотношений (4), (5) можно получить
A m lg «[M] + n lg «[N] + T " B = 0.
Используя выбранные опорные точки диаграммы, а также значения т еплот плавления для никеля и кремния, можно определить значения энергий смешения компон е нтов расплава системы Ni–Si, а также величины A и B для реакций образования из компонентов расплава с илицидов этой системы.
Термодинамические характеристики плавления чистых веществ приведены в табл. 1.
Таблица 1
Температуры и теплоты плавления веществ по данным справочника [9]
|
Вещество |
o T m , С |
A m H O0 , Дж/моль Tm |
|
Si |
1414 |
49789 |
|
Ni |
1455 |
17489 |
Обсуждение результатов
Помимо литературных данных, обобщенных в с п равочнике [8], на ри с . 1 приведена диаграмма состояния, рассчитанная по теории регулярных растворов. Значение энергетического параметра, использованное в ходе расчета, Q = –18741 Дж/моль. Расчет по теории регуляр н ых растворов недостаточно корректно описывает линию ли к видус, а для некоторого интервала значений атомной доли кремния полученные данные не имеют физического смысла и на рис. 1 этот участок линии ликвидус не представлен.
На рис. 2 представлены результаты расчета по теории субрегулярных рас т воров. Полученные результаты вполне согласуются с литературной диаграммой состояния. Однако есть и ряд отличий расчетной диаграммы состояния от литературной. Прежде всего, в избранном нами приближении не учитывалась нестехиометричность состава некоторых силицидов. Допустимос т ь такого упрощения связана с тем, что нас, прежде всего, интересовало положение линии ликви д ус. Фаза Ni 2 Si на расчетной диаграмме конгруэнтно плавится п ри 1305 °С, в то время как по литературным данным это соединение распадается по перитектической реакции. Также пришлось сделать некоторые допущения при описании равновесия распл а ва с силицидом NiSi2. При расчете учитывалась только одна из его кристаллографических модификаций. Полученны е в работе з начения энергетических параметров для теории субрегулярны х растворов приведены в табл. 2, 3. Константы, характеризующие процесс перехода вещества в жидкое состояние, приведены в табл. 4.
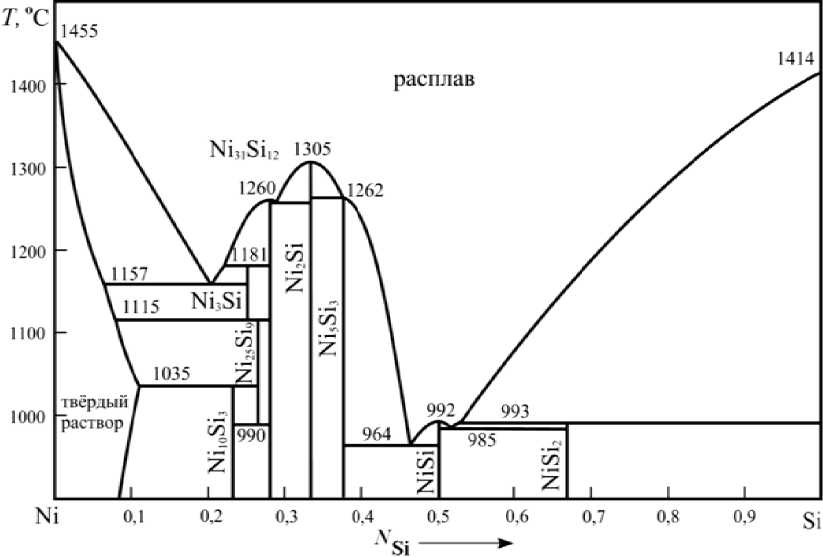
Рис. 2. Диаграмма состояния системы Ni–Si, рассчитанная в приближении теории субрегулярных растворов
Таблица 2
Параметры модели субрегулярного раствора для расплава (Дж/моль)
|
1 2 |
Si |
Ni |
|
Si |
0 |
–26269 |
|
Ni |
–25970 |
0 |
Таблица 3
Параметры модели субрегулярного раствора для твёрдого раствора (Дж/моль)
|
1 2 |
Si |
Ni |
|
Si |
0 |
0 |
|
Ni |
6000 |
0 |
Список литературы Термодинамическое моделирование линии ликвидус системы Ni-Si
- Dynamics of phase transformation of Cu-Ni-Si alloy with super-high strength and high conductivity during aging/L. Qian, L. Zhou, P. Zhi-yong et al.//Trans. Nonferrous Met. Soc. China. -2010. -Vol. 20 -P. 1006-1011.
- Вольхин, А.И. Анодная и катодная медь/А.И. Вольхин, Е.И. Елисеев, В.П. Жуков. -Челябинск: ЮУКИ, 2001. -431 с.
- Киткина, М.Г. Физико-химический фазовый анализ литых и термически обработанных сплавов системы Cu-Ni-Si/М.Г. Киткина, Р.В. Седлецкий, Н.П. Капитонова//Заводская лаборатория. -1980. -Т. 46, № 11. -С. 995-998.
- Бурылев, Б.П. О применении теории регулярных растворов к жидким сплавам кремния с элементами II-V периодов/Б.П. Бурылев//Известия вузов. Черная металлургия. -1963. -№ 8. -С. 35-40.
- Hardy, H.K. A «sub-regular» solution model and its application to some binary alloy systems/H.K. Hardy//Acta metallurgica. -1953. -Vol. 1. -P. 202-209.
- Хансен, М. Структуры двойных сплавов/М. Хансен, К. Андерко. -М.: Металлургиздат, 1962. -Т. 2. -880 с.
- Binary Alloy Phase Diagrams, Second Edition/Ed. T.B. Massalski. -ASM International, Materials Park, Ohio. -1990. -Vol. 3. -P. 2859-2861.
- Диаграммы состояния двойных металлических систем: справ.: в 3 т./под общ. ред. Н.П. Лякишева. -М.: Машиностроение, 1999. -Т. 3, кн. I. -880 с.
- Глушко, В.П. Термические константы веществ. База данных/В.П. Глушко. -http://www.chem.msu.su/


