Термодинамическое моделирование процессов взаимодействия кальция, магния, алюминия и бора с кислородом в металлических расплавах
Автор: Михайлов Геннадий Георгиевич, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 1 т.19, 2019 года.
Бесплатный доступ
Разработана методика расчета диаграмм раскисления и модифицирования стали кальцием, магнием, алюминием и бором. Установлены координаты поверхностей ликвидус оксидных систем B2O3-Al2O3-MgO, B2O3-Al2O3-CaO, B2O3-MgO-CaO при 1600 °С. Определены энергетические параметры теории субрегулярных ионных растворов для изученных оксидных систем. Рассчитаны координаты поверхностей растворимости для систем Fe-Mg-Al-B-O, Fe-Ca-Al-B-O, Fe-Mg-Ca-Al-B-O. Изучено влияние общего давления на растворимость магния и кальция в жидком железе. Активности компонентов металлического расплава рассчитаны с применением параметров взаимодействия первого порядка (теория Вагнера). Активности компонентов твердых растворов (оксидов и шпинелей) приравнивали их мольным долям. Показано, что при глубоком рафинировании металла от кислорода лишь незначительная часть бора будет окисляться и эти оксиды войдут в состав оксидных расплавов. Основными неметаллическими оксидными включениями будут магнезиальная шпинель, биалюминат кальция и жидкие оксидные образования. Так называемый свободный бор может быть растворен в жидком металле в количествах, отвечающих равновесию с оксидными фазами.
Моделирование, термодинамика, бор, магний, алюминий, кальций, раскисление, фазовые равновесия
Короткий адрес: https://sciup.org/147232525
IDR: 147232525 | УДК: 669.017.3 | DOI: 10.14529/met190104
Thermodynamic modeling of the processes of interaction of calcium, magnesium, aluminum and boron with oxygen in metallic melts
A method for calculation of the diagrams of steel deoxidation and modification by calcium, magnesium, aluminum and boron was developed. The coordinates of the liquidus surfaces of the oxide systems B2O3-Al2O3-MgO, B2O3-Al2O3-CaO, B2O3-MgO-CaO were found at 1873 K. The energy parameters were determined for the theory of subregular ionic solutions of the studied oxide systems. The coordinates of the solubility surfaces for the systems Fe-Mg-Al-B-O, Fe-Ca-Al-B-O, Fe-Mg-Ca-Al-B-O were calculated. The effect of the total pressure on solubility of magnesium and calcium in liquid iron was studied. The activity of the components of the metallic melt was calculated using the first-order interaction parameters (Wagner's theory). The activities of the components of solid solutions (oxides and spinels) were equated with their molar fractions. It was shown that during extensive refining of metal from the oxygen, only a small fraction of boron oxidizes and these oxides form fraction of the oxide melts. The major non-metallic oxide inclusions were magnesia spinel, calcium bialuminate and liquid oxide formations. The “free” boron was dissolved in liquid metal in amounts which were in equilibrium with oxide phases.
Текст научной статьи Термодинамическое моделирование процессов взаимодействия кальция, магния, алюминия и бора с кислородом в металлических расплавах
Все более широкое применения бора в металлургии, особенно при выплавке малоуглеродистых сталей, связано с уникальной способностью бора повышать механические и эксплуатационные свойства стали при микродобавках бора в сталь, не превышающих 0,002–0,008 % по массе. При этом необходимо учитывать, что бор активно взаимодействует с серой, азотом и кислородом в стали, способен образовывать интерметаллиды с компонентами жидкого металла [1]. Сейчас путем лабораторных и промышленных экспериментов доказано, что положительное влияние на прочность, прокаливаемость, пластичность, снижение показателей анизотропии удается реализовать в технологии выплавки борсодержащей стали при наличии в металле так называемого свободного бора, бора, растворенного в металле, а не связанного в неметаллические включения [2–3]. Использование микролегирования стали бором, вводимым в пределах 0,001–0,025 % по массе, позволяет заменить в ряде случаев до 1,3 % никеля, 0,3 % хрома, 0,04 % молибдена на 0,001 % бора [4]. Прокаливаемость стали увеличивается с увеличением содержания углерода до 0,6 % [3, 5]. По мере работы над оптимизацией процесса микролегирования бором открываются все новые возможности использования бора. Бористые стали с содержанием бора 1–2 % являются эффективными поглотителями нейтронов и применяются в атомной энергетике [6, 7]. Использование далеко не полного перечня положительных свойств бора в металлургии требует дальнейшего изучения этих свойств. Для этого необходимо расширить круг изучаемых металлургических систем. Предварительно в работе [8] изучены и построены отдельные диаграммы состояний оксидных систем FeO–B2O3, B2O3–Al2O3, MnO–B2O3, SiO2–B2O3, MgO–B2O3, CaO–B2O3 с указанием сложных оксидных соединений, образующихся в этих системах. Также были построены поверхности растворимости компонентов в металлических системах (ПРКМ) для систем Fe–B–O, Fe–B–Si–O, Fe–B–Mg–O, Fe–B–Ca–O, Fe–B–Mn–O, Fe–B–Al–O [9]. Термодинамическая проработка литератур- ных и экспериментальных данных позволила установить зависимости констант равновесия, необходимых для расчетов, от температуры и параметры теории субрегулярных ионных растворов для оксидных систем. На основе этих расчетов установлено, что при современном уровне металлургических технологий можно добиться рафинирования стали по кислороду до 0,0001 %, по сере – до 0,002 % при реализации технологии печь-ковш. Для снижения концентрации азота в металле необходимо использовать присадки титана [10]. Это позволит снизить потери «эффективного» бора.
Для выяснения строения ПРКМ для бор- содержащих систем, раскисленных кальцием, алюминием и магнием, необходимо построить диаграммы состояния MgO–Al2O3–B2O3, CaO–Al2O3–B2O3, CaO–MgO–B2O3, т. е. существенным образом усложнить термодинамические расчеты. С использованием данных изученных ранее диаграмм состояний можно построить ПРКМ систем Fe–Mg–Al–B–O, Fe–Ca– Al–B–O и Fe–Ca–Mg–Al–B–O при фиксированном содержании бора ([B] = 0,001 мас. %), давления (1 и 1,5 атм) и температуры (1600 °С).
На рис. 1 представлены полученные расчетом координаты поверхностей ликвидус для систем MgO–Al 2 O 3 –B 2 O 3 , CaO–Al 2 O 3 –B 2 O 3 ,
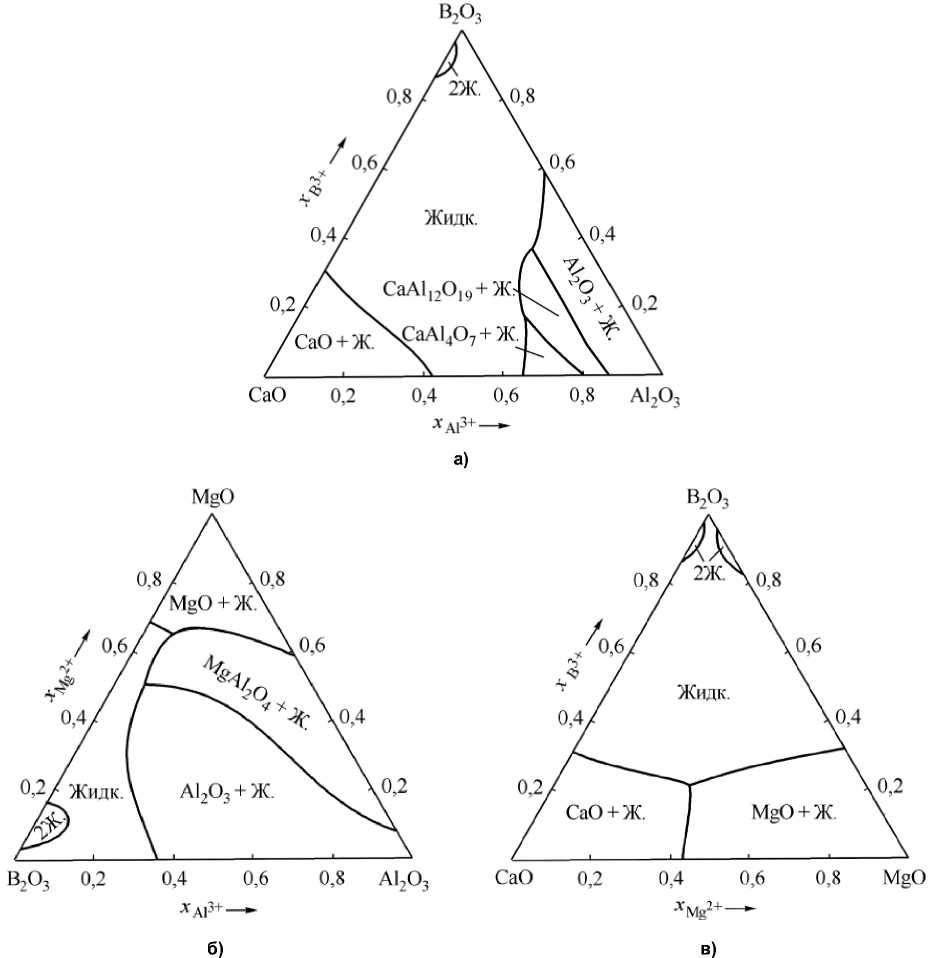
Рис. 1. Расчетные диаграммы состояний систем при 1600 °С: а) B 2 O 3 –Al 2 O 3 –CaO; б) B 2 O 3 –Al 2 O 3 –MgO; в) B 2 O 3 –MgO–CaO
CaO–MgO–B 2 O 3 при температуре 1600 °С, сведения о которых практически отсутствуют в научной литературе.
Диаграмма CaO–Al 2 O 3 –B 2 O 3 изучена Шефером и Куцелем только при 900–1500 °С [11]. В работе установлено существование двух тройных соединений: CaO·Al 2 O 3 ·B 2 O 3 и 2CaO·Al 2 O 3 ·B 2 O 3 . Температура плавления 2CaO·Al 2 O 3 ·B 2 O 3 по данным [11] на 9Al 2 O 3 ·2B 2 O 3 и расплав составляет 1015 °С. Соединение 9Al 2 O 3 ·2B 2 O 3 может существовать до температуры 1440 °С. Соединение 2CaO·Al2O3·B2O3 плавится инконгруэнтно при 1098 °С. Следовательно, в тройной диаграмме CaO–Al 2 O 3 –B 2 O 3 при 1600 °С возможно образование только алюминатов кальция, оксидов кальция и алюминия и наблюдалось расслоение расплава при высоком содержании В 2 О 3 в жидкости. В данной работе на основании двойных оксидных систем смоделирована тройная диаграмма состояний CaO–Al 2 O 3 –B 2 O 3 . Ранее тройные оксидные системы с B2O3 и FeO рассчитывали при 1600 °С, так как в литературе присутствует только одна диаграмма с FeO и B 2 O 3 – диаграмма FeO–B 2 O 3 –CaO, которая приводится именно при этой температуре, поэтому и наши расчетные тройные диаграммы состояний с B 2 O 3 приведены в [8] при 1600 °С. Энергетические параметры, подобранные в данной работе для системы CaO–Al 2 O 3 –B 2 O 3 , имеют следующие значения: Q 1123 = –110 000; Q 1223 = –72 000; Q 1233 = = –70 000 кал/моль.
На полях диаграмм (см. рис. 1) указаны химические оксидные соединения, которые могут быть в равновесии с оксидным расплавом (жидкостью). Так, на рис. 1а указаны поля изотермических фазовых равновесий
(CaO + Ж.), (CaAl 4 O 7 + Ж.), CaAl 12 O 19 + Ж.), (Al 2 O 3 + Ж.). Расслоение оксидного расплава обозначено символом (2 Ж.). Символом Ж. обозначены оксидные расплавы (CaO–Al 2 O 3 –B 2 O 3 ) для рис. 1а, (MgO–Al 2 O 3 –B 2 O 3 ) – для рис. 1б, (CaO–MgO–B 2 O 3 ) – для рис. 1в.
Диаграмма состояний B 2 O 3 –MgO–Al 2 O 3 (см. рис. 1 б) изучалась при более низких температурах [12–15], но полная диаграмма состояний системы B 2 O 3 –MgO–Al 2 O 3 не построена. В настоящей работе была построена эта диаграмма при 1600 °С. Подобранные в данной работе параметры теории субрегулярных ионных растворов для данной системы: Q 1123 = –50 000; Q 1223 = –100 000; Q 1233 = = –30 000 кал/моль.
Также были рассчитаны координаты поверхности ликвидус для диаграммы состояний системы B 2 O 3 –MgO–CaO (рис. 1в). Данная диаграмма была изучена в работе [16] только при 900 °С. Энергетические параметры, подобранные для этой системы в данной работе, имеют следующие значения: Q 1123 = –116 000; Q 1223 = –120 000; Q 1233 = –110 000 кал/моль.
В табл. 1 представлены необходимые для построения тройных диаграмм состояний значения зависимостей констант равновесия (плавления) от температуры. Круглые скобки обозначают жидкое состояние фазы, прямые – чистая твердая фаза.
В работе используется теория субрегулярных растворов с допущениями о квадратичной зависимости координационного числа раствора от химического состава взаимодействующих фаз. Основы теории и ее использование при определении термодинамических параметров взаимодействующих неметаллических фаз достаточно подробно изложены
Таблица 1
Термодинамические данные для реакций фазовых превращений, K – константа плавления оксидов и их соединений
В табл. 2 приведены реакции, константы равновесия и их температурные зависимости, используемые для описания процесса раскисления стали кальцием, магнием, алюминием и бором. у - коэффициент активности иона металла в оксидном расплаве с использованием теории субрегулярных ионных растворов. Активности компонентов твердого раствора оксидов | FeO, CaO | приравнивали их ионным долям ( ^F^ = xFe2+|, ас^ = xСа2+| ), твердого раствора оксидов | FeO, MgO | также приравнивали их ионным долям а|FeO| = xF 2+|, aMgO| = xMg2+ . Твердые растворы | FeO, CaO | и | FeO, MgO | не смешиваются между собой в случае присутствия в системе и магния, и кальция. Активности компонентов твердого раствора шпинелей | FeAl2O4, MgAl2O4 | приравнивали их мольным долям ( а|FeAl2O4 = xFeAl2O4| , a|MgAl2O4| = xMgAl2O4|).
Опыт расчетов и анализов показывает, что при построении диаграмм рафинирования
Таблица 2
Зависимости констант равновесия реакций раскисления от температуры
Имеющиеся в справочных и научных изданиях сведения о высокотемпературных реакциях зачастую либо отрывочны, либо неизвестны, либо получены методом косвенных термодинамических расчетов. Для целей выполнения представленной работы необходимо получить сведения по химическим реакциям, представленным в табл. 1 и 2.
Особенности термодинамических расчетов, методы построения систем уравнений и их решения достаточно подробно изложены в монографии [17]. Активности компонентов металлического расплава рассчитывали с использованием параметров взаимодействия первого порядка (по теории Вагнера) [18–22]. Активности компонентов оксидных расплавов рассчитывали с использованием теории субрегулярных ионных растворов. Параметры теории для диаграмм состояний систем MgO–Al2O3–B2O3, CaO–Al2O3–B2O3, CaO–MgO–B2O3 приведены выше. Недостающие для расчетов энергетические параметры теории (для диаграмм, содержащих FeO) приведены в [8, 17].
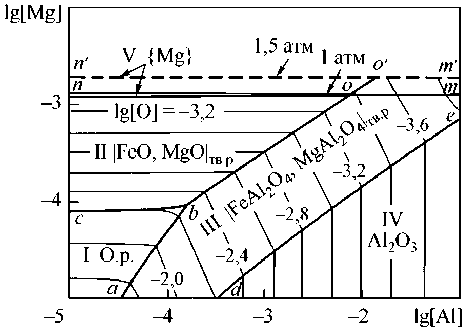
На рис. 2 приведены диаграммы раскисления железа сплавами Mg–B–Al и Ca–B–Al. На полях диаграмм указаны названия фаз. Так, на рис. 2а в области I указаны составы жидкого металла, содержащего 0,001 мас. % бора, равновесного с оксидным расплавом (FeO, Al 2 O 3 , B 2 O 3 , MgO), в области II – с твердым раствором оксидов на основе MgO, в области III – с твердым шпинельным раствором, в области IV – с корундом. На линии no заданы составы металла, равновесного с твердым раствором оксидов и парами магния при давлении p Mg = 1 атм. Аналогично линия n′o′ – для 1,5 атм. На линии om заданы составы металла, равновесного со шпинельным твердым раствором и парами магния при давлении 1 атм, на линии o′m′ – для 1,5 атм. Тонкими линиями на ПРКМ нанесены изотермы кислорода в логарифмических координатах. На осях рис. 2а нанесены концентрации компонентов в логарифмических координатах. Аналогичные обозначения и на рис. 2б (для случая раскисления кальцием, алюминием и бором).
На рис. 3 приведена ПРКМ системы Fe–Mg–Ca–Al–B–O при 1600 °С и фиксированных концентрациях [Mg] = 0,001 и [B] = = 0001 мас. %. Газовая фаза состоит из двух компонентов – паров магния и кальция. При общем давлении 1 атм p Mg = 0,83 атм,
а)
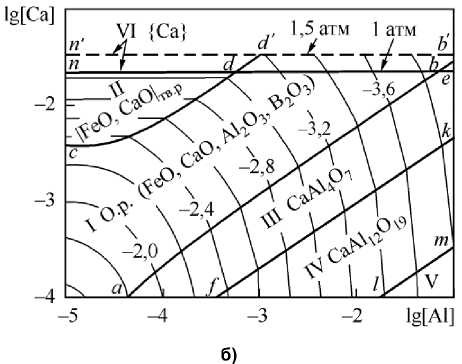
Рис. 2. Поверхности растворимости компонентов в металле (ПРКМ) при T = 1600 °С, [B] = 0,001 мас. % систем: а) Fe–Mg–Al–B–O; б) Fe–Ca–Al–B–O (V – Al 2 O 3 )
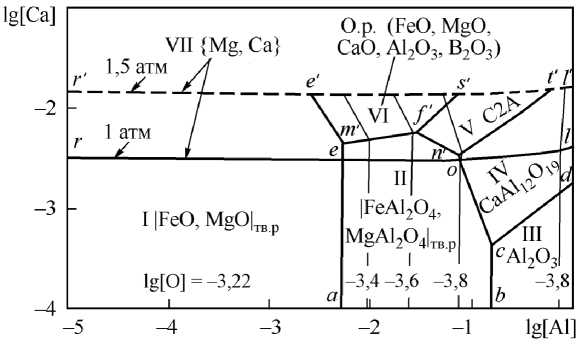
Рис. 3. ПРКМ системы Fe–Mg–Ca–Al–B–O, T = 1600 °С, [Mg] = 0,001, [B] = 0,001 мас. % (С2A – CaAl 4 O 7 )
p Ca = 0,17 атм (линия reol ). В глубине металла возможно гидростатическое повышение давления. При общем давлении 1,5 атм p Mg = 0,83 атм, p Ca = 0,67 атм (линия r′e′s′t’l′ ).
Из рис. 2 и 3 видно, что равновесные по бору составы металла не содержат чистой фазы бора. Бор может входить в состав металлических расплавов и в небольших количествах расходоваться на раскисление металла. Основными же неметаллическими включениями будут магнезиальная шпинель, биалюминат кальция и жидкие оксидные включения (при [Ca] ≈ 0,001–0,005 и [Al] = 0,01–0,03 мас. %).
Заключение
Разработана методика расчета составов равновесного металла и шлака, при которых в основном бор не должен расходоваться на участие в оксидных фазах, а будет находиться в жидком металле. Построены диаграммы состояний систем MgO–Al 2 O 3 –B 2 O 3 , CaO–Al 2 O 3 –B 2 O 3 , CaO–MgO–B 2 O 3 при 1600 °С с использованием теории субрегулярных ионных растворов. Впервые построены поверхности растворимости компонентов для термодинамических систем Fe–Mg–Al–B–O, Fe–Ca– Al–B–O, Fe–Mg–Ca–Al–B–O при высоких температурах. Изучено влияние общего давления на растворимость магния и кальция в жидком железе.
Статья выполнена при поддержке Правительства РФ (Постановление № 211 от 16.03.2013 г.), соглашение № 02.A03.21.0011.
Список литературы Термодинамическое моделирование процессов взаимодействия кальция, магния, алюминия и бора с кислородом в металлических расплавах
- Барадынцева, Е.П. Влияние микролегирования бором на прокаливаемость сталей / Е.П. Барадынцева, Н.А. Глазунов, О.В. Роговцова // Литье и металлургия. - 2016. - № 3 (84). - С. 70-74.
- Лякишев, Н.П. Борсодержащие стали и сплавы / Н.П. Лякишев, Ю.Л. Плинер, С.И. Лаппо. - М.: Металлургия, 1986. - 191 с.
- Новое применение бора в металлургии / В.В. Парусов, А.Б. Сычков, И.В. Деревянченко, М.А. Жигарев // Вестник МГТУ им. Г.И. Носова, 2005. - № 1 (9). - С. 15-17.
- Потапов, А.И. Технологические особенности легирования стали бором / А.И. Потапов, А.Е. Семин // Известия высших учебных заведений. Черная металлургия, 2012. - № 55 (9). - С. 68-69.
- Перспективы выплавки стали с повышенной прокаливаемостью за счет бора / Л.Б. Исаева, И.Е. Лев, Н.М. Великонская, А.Г. Безшкуренко // Сборник тезисов IX Международной научно-практической конференции «Литье 2013», Украина, Запорожье, 2013. - С. 261-262.
- Козлов, Д.В. Возможности применения бористых сталей в существующих и перспективных ядерных реакторах / Д.В. Козлов, В.Д. Рисованный // Известия Самарского научного центра РАН. - 2012. - Т. 14, № 4 (4). - С. 966-970.
- Нестеренко, А.М. Размерно-геометрические спектры легирования стали бором и медью / А.М. Нестеренко, А.Б. Сычков // Фундаментальные и прикладные проблемы черной металлургии: сб. науч. тр. - Днепропетровск: Bision, 2004. - Вып. 7. - С. 181-183.
- Михайлов, Г.Г. Термодинамическое моделирование фазовых равновесий в оксидных системах, содержащих B2O3 / Г.Г. Михайлов, Л.А. Макровец, Л.А. Смирнов // Вестник ЮУрГУ. Серия «Металлургия». - 2014. - № 14 (4). - С. 11-16.
- Михайлов, Г.Г. Термодинамический анализ реакций взаимодействия марганца, кремния, магния, кальция, алюминия с кислородом в борсодержащем расплаве на основе железа / Г.Г. Михайлов, Л.А. Макровец, Л.А. Смирнов // Вестник ЮУрГУ. Серия «Металлургия». - 2015. - Т. 15, № 2. - С. 5-12.
- Лысенкова, Е.В. Образование нитридов титана в стальных расплавах - термодинамические расчеты на основе уточненных справочных данных / Е.В. Лысенкова, А.Я. Стомахин // Известия высших учебных заведений. Черная металлургия. - 2015. - Т. 58, № 6. - С. 439-443.
- Диаграммы состояния силикатных систем. Справочник. Выпуск четвертый. Тройные окисные системы / В.П. Барзаковский, В.В. Лапин, А.И. Бойкова, Н.Н. Курцева. - Л.: Наука, Ленинград. отд-ние, 1974. - 514 с.
- Hamzawy, E.M.A. Vitrification and devitrification phenomena in the ternary MgO-Al2O3-B2O3 system / E.M.A. Hamzawy, H. Darwish // Ceramics International. - 2008. - Vol. 34. - P. 1965-1969.
- Kiss, S.J. The influence of B2O3 on spinel formation in the Al2O3-MgO-B2O3 system / S.J. Kiss // Sci. Ceram.; Proc. 12th Int. Conf. Saint-Vincent, 23-30 June 1983, Faenza, 1984. - Vol. 12. - P. 195-198.
- Sokolov, V.A. Synthesis and properties of flux-cast refractories in Al2O3-MgO-B2O3 system / V.A. Sokolov, T.Ya. Malysheva, M.D. Gasparyan // Refractories and Inductrial ceramics. - 2008. - Vol. 49, no. 2. - P. 146-149.
- The Effects of Gravity on the Combustion Synthesis of B2O3-Al2O3-MgO Glass Ceramic Composites / A.R. Manerbino, H.C. Yi, J.Y. Guignt et al. // 12th International Proceedings of the Experimental Methods for Microgravity Materials Science, ASM International, April 2, 2000. Document ID: 20010064835/ - https://ntrs.nasa.gov/ search.jsp?R=20010064835.
- Fletcher, B.L. Phase Equilibria in the System CaO-MgO-B2O3 at 900°C / B.L. Fletcher, J.R. Stevenson, A. Whitaker // Journal of the American Ceramic Society, 1970. - Vol. 53, no. 2. - P. 95-97. - 10.1111/j.1151-2916. 1970.tb12018.x
- DOI: 10.1111/j.1151-2916.1970.tb12018
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем / Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. - М.: Издат. Дом МИСИС. - 2009. - 519 с.
- Bůžek, Z. Základní termodynamické údaje o metalurgických reakcích a o interakcích prvků v soustavách významných pro hutnickou teorii a praxi / Z. Bůžek // Hutnické aktuality. - 1979. - Vol. 20, no. 1-2. - P. 3-111.
- Балковой, Ю.В. Параметры взаимодействия первого порядка в расплавах на основе железа: обзор. информ. / Ю.В. Балковой, Р.А. Алеев, В.К. Баканов. - М.: Черметинформация, 1987. - 42 с.
- Steelmaking Data Sourcebook, The Japan Society for the Promotion of Science, The 19th Committee on Steelmaking, Gordon and Breach Science Publishers, New York. NY, 1988. - P. 288-289.
- Evolution Mechanisms of MgO•Al2O3 Inclusions by Cerium in Spring Steel Used in Fasteners of High-Speed Railway / L.J. Wang, Y.Q. Liu, Q. Wang, K.C. Chou // ISIJ International. - 2015. - Vol. 55, no. 5. - P. 970-975.
- Park, J.H. Control of MgO•Al2O3 Spinel Inclusions in Stainless Steels / J.H. Park, H. Todoroki // ISIJ International, 2010. - Vol. 50, no. 10. - P. 1333-1346.


