Термодинамическое описание фазовых равновесий в системе Cu2O-CeO2-Ce2O3-La2O3
Автор: Самойлова Ольга Владимировна, Михайлов Геннадий Георгиевич, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 1 т.17, 2017 года.
Бесплатный доступ
С использованием теорий совершенных ионных растворов и субрегулярных ионных растворов проведено термодинамическое моделирование линий ликвидуса для двойных оксидных фазовых диаграмм и поверхностей ликвидуса для тройных оксидных фазовых диаграмм, составляющих систему Cu2O-CeO2-Ce2O3-La2O3. Линия солидуса, ограничивающая существование твердого раствора в системе CeO2-La2O3, рассчитывалась с использованием теории регулярных ионных растворов. В ходе работы определены параметры применяемых моделей и температурные зависимости констант равновесия реакций перехода веществ из твердого состояния в жидкое, используемые для расчета фазовых диаграмм исследуемых систем. Большинство систем (Cu2O-CeO2, Cu2O-Ce2O3, Cu2O-La2O3, CeO2-Ce2O3, Ce2O3-La2O3, Cu2O-CeO2-Ce2O3, Cu2O-Ce2O3-La2O3) представляют собой диаграммы эвтектического типа с одной точкой эвтектики. Для вышеперечисленных систем, включающих Cu2O как компонент, характерны достаточно низкие температуры эвтектического равновесия. Система CeO2-La2O3 характеризуется наличием твердого раствора и точкой на линии ликвидуса, имеющей нулевой интервал кристаллизации. Фазовые диаграммы Cu2O-CeO2-La2O3 и CeO2-La2O3-Ce2O3 характеризуются наличием обширной области равновесия оксидного расплава с твердым раствором |CeO2, La2O3|тв.р.
Система cu2o-ceo2-ce2o3-la2o3, термодинамическое моделирование, фазовые равновесия
Короткий адрес: https://sciup.org/147157068
IDR: 147157068 | УДК: 669.35 | DOI: 10.14529/met170102
Thermodynamic description of phase equilibria in the Cu2O-CeO2-Ce2O3-La2O3 system
Thermodynamic modeling of liquidus lines for binary oxide phase diagrams and liquidus surfaces for ternary oxide phase diagrams that make up the Cu2O-CeO2-Ce2O3-La2O3 system was performed using the theories of ideal ionic solutions and subregular ionic solutions. Solidus line, limiting the existence of a solid solution in the CeO2-La2O3 system, was calculated using the theory of regular ionic solutions. The values of parameters of the used theories and the temperature dependence of the equilibrium constants of transition from solid to liquid, used to calculate the phase diagrams of the investigation systems, were determined during this work. Most of the systems (Cu2O-CeO2, Cu2O-Ce2O3, Cu2O-La2O3, CeO2-Ce2O3, Ce2O3-La2O3, Cu2O-CeO2-Ce2O3, Cu2O-Ce2O3-La2O3) are eutectic type diagrams with one eutectic point for each diagram. For the above systems including Cu2O as a component, it was concluded that these systems are characterized by sufficiently low eutectic equilibrium temperatures. The CeO2-La2O3 system is characterized by the presence of a solid solution and a point on the liquidus line, having a zero crystallization interval. Phase diagrams Cu2O-CeO2-La2O3 and CeO2-La2O3-Ce2O3 are characterized by a vast area of the equilibrium of oxide melt with the solid solution |CeO2, La2O3|ss.
Текст научной статьи Термодинамическое описание фазовых равновесий в системе Cu2O-CeO2-Ce2O3-La2O3
Использование редкоземельных элементов (РЗМ) в качестве элементов-раскислителей при производстве меди и сплавов на ее основе [1, 2] требует данных не только по термодинамике процессов, происходящих в металлическом расплаве, но также и сведений о сопряженном с жидким металлом оксидном шлаковом расплаве, содержащем оксиды РЗМ.
В литературе практически не встречается данных о диаграммах состояния систем вида «оксид меди Cu2O – оксид/оксиды РЗМ». Целью данной работы является построение двойных и тройных диаграмм состояния, входящих в систему Cu 2 O–CeO 2 –Ce 2 O 3 –La 2 O 3 .
Подробно методика моделирования диаграмм состояния оксидных систем приведена в работах [3, 4]. Расчет должен опираться на координаты (состав и температура) наиболее надежно определенных характерных точек на диаграммах: точек эвтектических, перитектических, фазовых переходов (например, плавления веществ в исследуемой системе) и т. п. Таким образом, для моделирования диаграмм состояния необходимы сведения о температу- рах и теплотах плавления веществ исследуемой системы. В табл. 1 приведены данные для веществ, составляющих систему Cu2O–CeO2– Ce2O3–La2O3. В табл. 2 приведены температурные зависимости констант равновесия процесса перехода веществ из твердого состояния в жидкое, рассчитанные по формуле (использованы сведения из табл. 1):
оо
AmHT о A тнт о lg Кц л =--m--+--m .
пл 2,3026 RT 2,3026 RTm о
Здесь K пл – константа равновесия перехода твердого вещества в жидкое состояние; A mH O o - теплота плавления вещества,
Tm
Дж/моль; Tmo – температура плавления веще- ства, К; R – универсальная газовая постоянная, R = 8,314 Дж/моль·К.
Для моделирования линий ликвидуса фазовых диаграмм Cu 2 O–CeO 2 , Cu 2 O–Ce 2 O 3 , Cu 2 O–La 2 O 3 , CeO 2 –Ce 2 O 3 , Ce 2 O 3 –La 2 O 3 и поверхностей ликвидуса фазовых диаграмм Cu 2 O–CeO 2 –Ce 2 O 3 , Cu 2 O–Ce 2 O 3 –La 2 O 3 использовалось приближение теории совершенных ионных растворов [3]. Согласно этой теории
Таблица 1
Данные о температурах и теплотах плавления веществ
|
Вещество |
o Tm , С |
A mH O o , Дж/моль Tm |
|
Cu 2 O |
1242 [5] |
64300 [5] |
|
CeO 2 |
2397 [6] |
79549 [7] |
|
Ce 2 O 3 |
2210 [8] |
83736 [7] |
|
La2O3 |
2301 [9] |
78000 [9] |
Таблица 2 Температурные зависимости для констант равновесия, характеризующих процесс перехода вещества из твердого состояния в жидкое
|
Вещество |
lg K |
|
Cu 2 O |
- 3359/ T + 2,217 |
|
CeO 2 |
- 4155/ T + 1,556 |
|
Ce 2 O 3 |
- 4374/ t + 1,762 |
|
La2O3 |
- 4074/ t + 1,5 83 |
Таблица 3
Сведения о координатах эвтектического равновесия в исследуемых системах
Для указанных выше систем в литературе практически нет данных о виде фазовых диаграмм. Для системы CeO2–Ce2O3 по результатам проведенного авторами работы [10] моделирования имеются сведения о наличии эвтектического превращения при температуре 1803 °С. Имеются данные о наличии соединения Cu2O·La2O3 (CuLaO2) в системе Cu2O–La2O3 [11–14]. Практически все исследователи указывают на твердофазный распад данного соединения, то есть на то, что это соединение не может находиться в равно- весии с оксидным расплавом. Только в работе [14] в ячейке EMF при температурах порядка 1012 °С появилась жидкая фаза, однако авторы работы никак не объясняют данный результат и, тем более, не связывают его с плавлением CuLaO2 или образованием эвтектики с участием этого соединения. По результатам проведенного нами моделирования соединение CuLaO2 распадается при температуре 1100 °С без выхода на линию ликвидуса.
Результаты расчета поверхностей ликвидуса фазовых диаграмм систем Cu 2 O–CeO 2 – Ce 2 O 3 и Cu 2 O–Ce 2 O 3 –La 2 O 3 приведены на рис. 1 и 2 соответственно.
Моделирование линии ликвидуса системы CeO2–La2O3 проводилось с использованием приближения теории субрегулярных ионных растворов [3], согласно которому активности компонентов раствора равны:
1g ax =V i 1g x i +
V i Г 3 x 2 x 2 S iii2 + x i x 2 ( 2 - 3 x i ) 6 1122 + x 2 ( 1 - 3 x i ) S i222
2,3026 RT
;
1g a 2 =V 2 1g x 2 +
V 2 Г x i3 ( i - 3 x 2 ) S iii2 + x 2 x 2 ( 2 - 3 x 2 ) S ii22 + 3 x 2 x 2 6 i222
2,3026 RT
где ν i – число катионов в молекуле компонента; x i – ионная доля компонента; Q ijkl – ские параметры теории, Дж/моль; Т – температура, К; R – универсальная газовая R = 8,314 Дж/моль·К.
энергетиче-постоянная,
Ce2O3
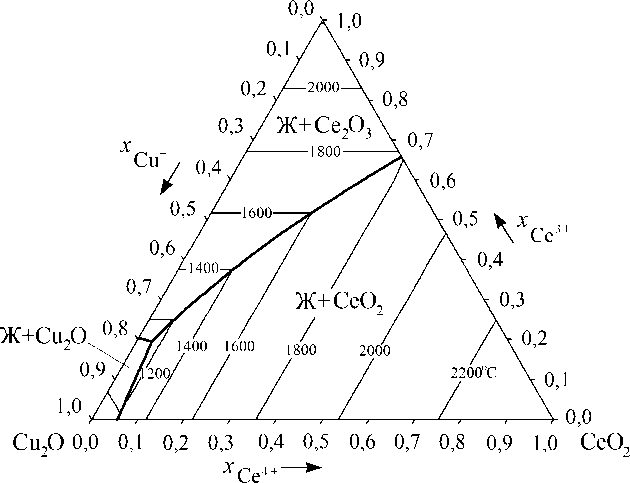
Рис. 1. Результаты расчета поверхности ликвидуса фазовой диаграммы системы Cu 2 O–CeO 2 –Ce 2 O 3
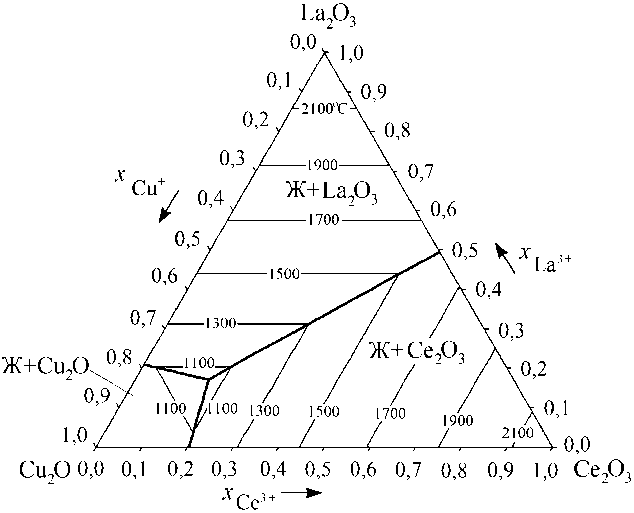
Рис. 2. Результаты расчета поверхности ликвидуса фазовой диаграммы системы Cu 2 O–Ce 2 O 3 –La 2 O 3
Моделирование линии солидуса, ограничивающей область существования твердого раствора в системе CeO 2 –La 2 O 3 , проводилось с использованием теории регулярных ионных растворов [3], согласно которой активности равны:
1g ax = Vj 1g xx + V 1 x 2 Q12 ; (4)
-
1 1 1 2,3026 RT
1g a 2 = v2 1g x 2 + V 2 x 1 Q 12 , (5)
-
2 2 2 2,3026 RT
где ν i – число катионов в молекуле компонента; x – ионная доля компонента; Q 12 – энергетический параметр теории, Дж/моль; Т – температура, К; R – универсальная газовая постоянная, R = 8,314 Дж/моль·К.
В ходе моделирования фазовой диаграммы CeO 2 –La 2 O 3 с использованием нескольких характерных точек для поиска энергетических параметров применяемых моделей составлялась система нелинейных уравнений, которая решалась с использованием метода Ньютона. После того, как энергетические параметры были найдены, линии ликвидуса и солидуса рассчитывались целиком.
Результаты моделирования фазовой диаграммы системы CeO 2 –La 2 O 3 приведены на рис. 3. При моделировании учитывалась возможность образования твердых растворов в данной системе [15]. Согласно результатам расчета линия ликвидуса системы CeO 2 –La 2 O 3
характеризуется точкой минимума, имеющей нулевой интервал кристаллизации, что совпадает с данными работы [16]. Энергетические параметры теории субрегулярных ионных растворов оказались равными (Дж/моль): Q 1112 =–20 816; Q 1122 =–16679; Q 1222 =–61445. Энергетический параметр теории регулярных ионных растворов равен Q 12 = –6843 Дж/моль.
Для расчета поверхностей ликвидуса систем Cu 2 O–CeO 2 –La 2 O 3 (рис. 4) и CeO 2 –La 2 O 3 – Ce 2 O 3 (рис. 5) использовалась совокупность теорий совершенных ионных растворов, субрегулярных ионных растворов и регулярных ионных растворов. Для системы Cu 2 O–CeO 2 –La 2 O 3 вводились дополнительные перекрестные энергетические параметры теории субрегулярных ионных растворов, которые подбирались методом последовательных итераций. Численно эти параметры оказались равны (Дж/моль): Q 1123 =–20565; Q 1223 =–51538; Q 1233 =–30722.
Таким образом, по результатам моделирования при добавлении в систему с простой эвтектикой Cu 2 O–CeO 2 третьего компонента La 2 O 3 , фазовая диаграмма тройной оксидной системы Cu 2 O–CeO 2 –La 2 O 3 характеризуется обширной областью равновесия оксидного расплава с твердым раствором |CeO 2 , La 2 O 3 | тв.р . Диаграмма состояния системы CeO 2 –La 2 O 3 – Ce 2 O 3 также характеризуется наличием области равновесия оксидного расплава с твердым раствором |CeO 2 , La 2 O 3 | тв.р .
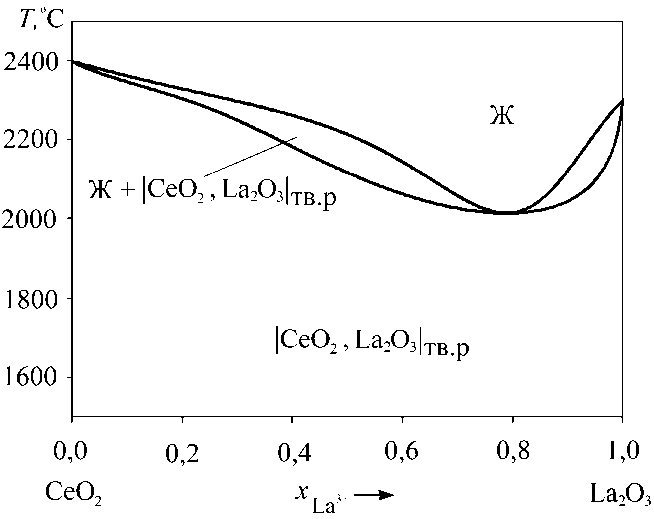
Рис. 3. Результаты расчета фазовой диаграммы системы CeO 2 –La 2 O 3
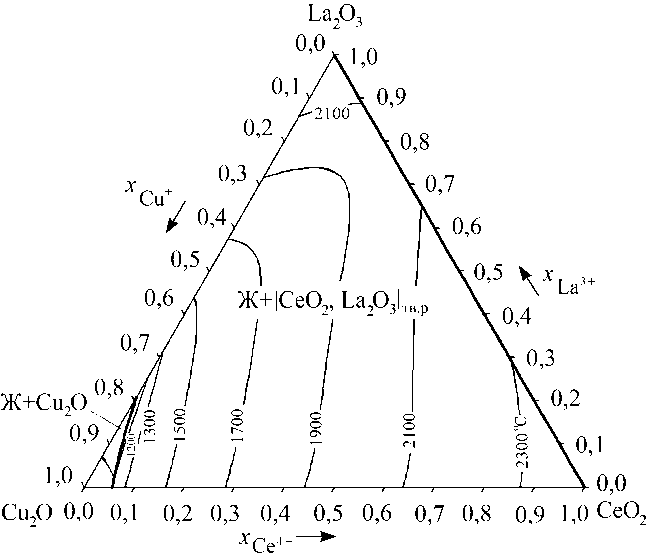
Рис. 4. Результаты расчета поверхности ликвидуса фазовой диаграммы системы Cu 2 O–CeO 2 –La 2 O 3
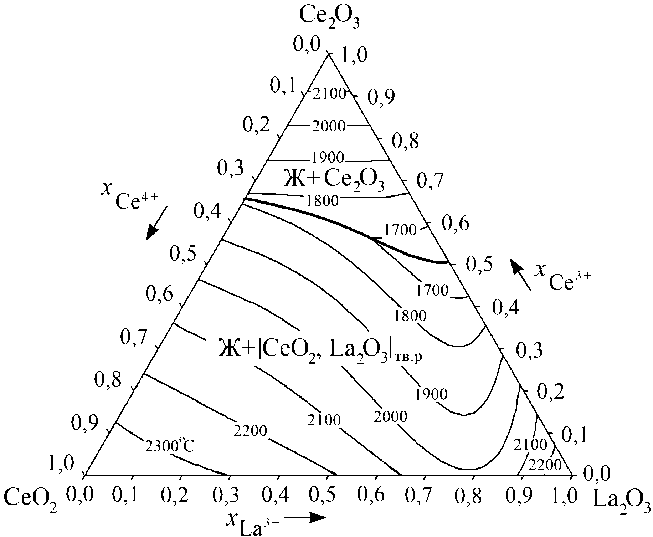
Рис. 5. Результаты расчета поверхности ликвидуса фазовой диаграммы системы CeO 2 –La 2 O 3 –Ce 2 O 3
Выводы
Проведено термодинамическое описание фазовых равновесий в двойных и тройных диаграммах состояния, составляющих систему Cu2O–CeO2–Ce2O3–La2O3. Определены термодинамические модели и их параметры, необходимые для описания фазовых диаграмм ис- следуемых систем. По результатам расчета показано, что системы Cu2O–CeO2, Cu2O– Ce2O3, Cu2O–La2O3, CeO2–Ce2O3, Ce2O3–La2O3, Cu2O–CeO2–Ce2O3, Cu2O–Ce2O3–La2O3 представляют собой диаграммы эвтектического типа с одной точкой эвтектики. Для вышеперечисленных систем, включающих Cu2O как компонент, характерны достаточно низкие температуры эвтектического равновесия, которое смещено по составу в сторону больших концентраций оксида меди. Также показано, что соединение CuLaO2 в системе Cu2O–La2O3 распадается при температуре 1100 °С без выхода на линию ликвидуса. Системы CeO2– La2O3, Cu2O–CeO2–La2O3 и CeO2–La2O3–Ce2O3 характеризуются наличием твердого раствора |CeO2, La2O3|тв.р.
Работа осуществлена при финансовой поддержке РФФИ, грант № 16-38-60144 мол_а_дк.
Список литературы Термодинамическое описание фазовых равновесий в системе Cu2O-CeO2-Ce2O3-La2O3
- Куликов, И.С. Раскисление металлов/И.С. Куликов. -М.: Металлургия, 1975. -504 с.
- Судавцова, В.С. Влияние лития, бора, магния и иттрия на активность кислорода в жидкой меди/В.С. Судавцова, М.В. Михайловская, А.В. Калмыков//Расплавы. -1987. -Т. 1, № 2.-С. 43-46.
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. -М.: Издат. Дом МИСиС, 2009. -520 с.
- Михайлов, Г.Г. Фазовые равновесия в многокомпонентных системах с жидкими цветными металлами/Г.Г. Михайлов, Е.А. Трофимов, А.Ю. Сидоренко. -М.: Издат. Дом МИСиС, 2014. -158 с.
- Химическая энциклопедия: в 5 т./под ред. И.Л. Кнунянца. -М.: Сов. энцикл, 1990. -Т. 2. -671 с.
- Мордовин, О.А. Определение температур плавления окислов редкоземельных элементов/О.А. Мордовин, Н.И. Тимофеева, Л.Н. Дроздова//Неорганические материалы. -1967. -Т. III, № 1. -С. 187-189.
- Физико-химические свойства окислов. Справочник/под ред. Г.В. Самсонова. -М.: Металлургия, 1969. -456 с.
- Sata, T. Some material properties of cerium sesquioxide/T. Sata, M. Yoshimura//J. Ceram. Assoc. Japan. -1968. -Vol. 76, no. 4. -P. 116-122.
- Ushakov, S.V. Direct measurements of fusion and phase transition enthalpies in lanthanum oxide/S.V. Ushakov, A. Navrotsky//Journal of Materials Research. -2011. -Vol. 26, no. 7. -P. 845-847 DOI: 10.1557/jmr.2010.79
- Zinkevich, M. Thermodynamic modelling of the cerium-oxygen system/M. Zinkevich, D. Djurovic, F. Aldinger//Solid State Ionics. -2006. -Vol. 177. -P. 989-1001 DOI: 10.1016/j.ssi.2006.02.044
- Thermodynamic stability of ternary oxides in Ln-M-O (Ln = La, Pr, Nd; M = Co, Ni, Cu) systems/A.N. Petrov, V.A. Cherepanov, A.Yu. Zuyev, V.M. Zhukovsky//Journal of Solid State Chemistry. -1988. -Vol. 77, no. 1. -P. 1-14 DOI: 10.1016/0022-4596(88)90083-7
- LaCuO2.5+x and YCuO2.5+x delafossites: materials with triangular Cu2+δ planes/R.J. Cava, H.W. Zandbergen, A.P. Ramirez et al.//Journal of Solid State Chemistry. -1993. -Vol. 104, no. 2. -P. 437-452 DOI: 10.1006/jssc.1993.1179
- Kucharski, R. Reduction and oxidation of simple oxocuprates/R. Kucharski, Z. Gontarz//Journal of Thermal Analysis and Calorimetry. -2000. -Vol. 60, no. 1. -P. 219-227 DOI: 10.1023/A:1010121913036
- Jacob, K.T. Phase relations in the system Cu-La-O and thermodynamic properties of CuLaO2 and CuLa2O4/K.T. Jacob, K.P. Jayadevan//Journal of Materials Science. -2002. -Vol. 37, no. 8. -P. 1611-1620 DOI: 10.1023/A:1014957910889
- Minkova, N. Isomorphic substitutions in the CeO2-La2O3 system at 850 °C/N. Minkova, S. Aslanian//Crystal Research and Technology. -1989. -Vol. 24, no. 4. -P. 351-354 DOI: 10.1002/crat.2170240402
- Measurement and calculation of the ZrO2-CeO2-LaO1.5 phase diagram/Y. Du, M. Yashima, T. Koura et al.//Calphad. -1996. -Vol. 20, no. 1. -P. 95-108 DOI: 10.1016/0364-5916(96)00017-X


