Термодинамическое описание системы Cu2O-SiO2
Автор: Трофимов Евгений Алексеевич, Михайлов Геннадий Георгиевич, Жихарев Владилен Михайлович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 36 (169), 2009 года.
Бесплатный доступ
Посредством термодинамических расчётов построены несколько вариантов фазовых диаграмм системы Cu2O-SiO2, которые могут быть использованы для анализа имеющихся литературных данных. Результаты расчёта сопоставлены с экспериментальными данными.
Диаграмма состояния, оксид меди, оксид кремния, термодинамические расчёты
Короткий адрес: https://sciup.org/147156624
IDR: 147156624 | УДК: 669.33+541.123
Thermodynamic analysis of the Cu2O-SiO2 system
Using the thermodynamic calculations, several variants of the phase diagrams of the Cu2O-SiO2 system were plotted. The diagrams plotted can be used for analysis of available literary data. The results of the calculations can be correlated with the experimental data.
Текст научной статьи Термодинамическое описание системы Cu2O-SiO2
Система Cu2O-SiO2 является основой медерафинировочных шлаков. Несмотря на то, что попытки термодинамического описания этой системы предпринимались неоднократно, удовлетворительной модели фазовых равновесий, реализующихся в системе Cu2O-SiO2, описывающей состояние системы в широком интервале температур и концентраций, до сих пор не создано.
Настоящая работа посвящена изучению возможностей термодинамического описания системы Cu2O-SiO2 при температурах выше 1000 °C посредством различных модельных теорий строения шлаковых расплавов. В ходе работы предпринята попытка расчёта диаграммы состояния бинарной системы Cu2O-SiO2, опираясь на различные модельные представления. Для расчёта диаграмм использовались значения термодинамических функций плавления индивидуальных веществ (табл. 1), заимствованные из справочника [1]. Для подбора модельных параметров и оценки достоверности результатов расчёта в работе использованы данные справочника [2].
Таблица 1
Термодинамические характеристики плавления оксидов
|
Вещество |
Энтальпия плавления, АЯПЛ, Дж/моль |
Температура плавления, Т, °C |
|
Си2О, куприт |
64300 |
1242 |
|
SiO2, тридимит |
9002 |
1680 |
|
SiO2, кристобалит |
7704 |
1720 |
В ходе работы изучены возможности использования некоторых наиболее распространённых подходов. Результаты расчётов представлены на рис. 1 и 2.
В ходе расчёта по теории совершенных ионных расплавов считалось, что расплав состоит из ионов: положительных - Си+ и отрицательных -О2- и SiO44-. Интересно отметить, что расчет, проведённый исходя из предположения, что расплав состоит из ионов Cu+, Si4+ и О2", приводит к следующим координатам точки эвтектики: Т= 793 °C, 65,9 мол. % SiO2.
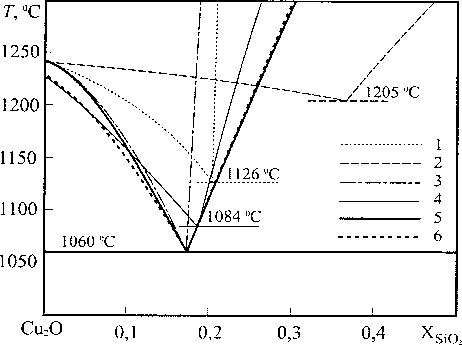
Рис. 1. Окрестности точки эвтектики на диаграмме состояния системы Cu2O-SiO2: 1 - результаты расчёта по теории совершенных ионных расплавов; 2 -результаты расчёта по теории фаз с коллективной системой электронов; 3 - результаты расчёта по теории субрегулярных ионных расплавов; 4 - расчёт посредством уравнений Маргулиса, проведённый авторами работы [6]; 5 ~ расчёт посредством уравнений Маргулиса, проведённый авторами настоящей работы; 6 - данные экспериментального исследования, приведённые в справочнике [2]
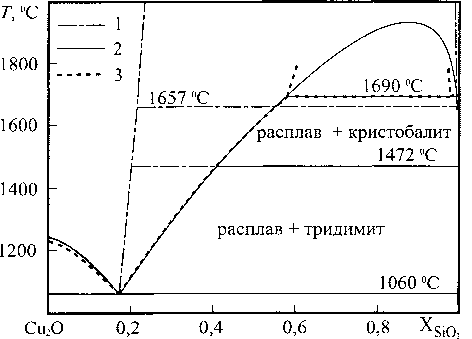
Рис. 2. Диаграмма состояния системы Cu2O-SiO2: 1 - результаты расчёта по теории субрегулярных ионных расплавов; 2 - расчёт посредством уравнений Маргулиса, проведённый авторами настоящей работы; 3 - данные экспериментального исследования, приведённые в справочнике [2]
При использовании приближения теории фаз с коллективной системой электронов (АТ. Пономаренко), активности оксидов меди и кремния в расплаве рассчитывались по формулам:
_ 2 _ 2
^Си2О - aCu * аО ’ aSiO2 ~ ^Si ' аО ’ где дСи, asi, ао - атомные активности соответствующих элементов в шлаке, которые рассчитываются по теории АТ. Пономаренко следующим образом:
«i = Q т,,
( к
= ycj6 ” , )
Sy =0,5(х^-Х^)2, где Cj, Cj - атомные доли элементов в шлаке, R - универсальная газовая постоянная (R = 0,00831 кДж/моль), Т - температура (К), Хь Щ - энергетические параметры элементов, из которых образуется расплав. В табл. 2 представлены значения параметров, рекомендованные автором теории в работе [3] и использованные в ходе нашего расчёта. Некоторое изменение значений параметров помогает добиться большего совпадения результатов расчёта с экспериментальными данными, однако, в любом случае применение этого подхода не позволяет рассчитывать координаты купола расслаивания, наличие которого характерно для изучаемой системы.
Таблица 2 Параметры теории строения фаз с коллективной системой электронов
|
Элемент i |
Си |
О |
Si |
|
Xi по [3], кДж/моль |
418 |
1255 |
172 |
В соответствии с использованным приближением теории субрегулярных ионных расплавов активности компонентов оксидного расплава можно вычислить по формулам следующего вида [4]:
lg ах = vx Igxj -bviPxf х| Qxxn +
+ ххх| (2 - 3x02im + XI (1 - 3x0 g1222]/2,3^T, lg «2 = V2 lgX2 +У2 [*1 (1 - 3x2)21112 +
+ x j x2(2 — 3x0g! 122 + 3xj x 2 21222]/2,ЗЛТ, где к - число катионов, которые образуются при диссоциации молекулы компонента шлака, число катионов в молекуле компонента шлака (для Си2О v = 2, для SiO2 v = 1), X! и х2 - катионные доли ионов Си+ и Si4+, a Q - энергетические параметры теории.
Определённый в ходе работы набор значений параметров: QXXn = -38 100 Дж/моль, 21122 = = 318 000 Дж/моль, 2i222= 59 3 00 Дж/моль.
Согласно подходу, связанному с использованием модифицированных уравнений Маргулиса третьего порядка [5], коэффициенты активности компонентов рассчитываются по формулам следующего вида:
In Y, = 0,5^^ + w^Xj-Q^^jpXjXp + >1 . j=lp=l
/=1 Hp=^
где yz - коэффициент активности /-го компонента, х - мольные доли компонентов в растворе, Wy - параметры взаимодействия, зависящие от температуры:
wy =cuiT + dll.
Отметим, что в работе [6] сделана попытка использования уравнений Маргулиса для расчёта диаграммы состояния системы Cu2O-SiO2. Однако значения, представленные в табл. 3, по нашему мнению, позволяют лучше описывать экспериментальные данные, приведённые в справочнике [2].
Таблица 3
Параметры взаимодействия для расчёта по уравнениям Маргулиса
|
н |
С |
d |
|
Си2О—SiO2 |
55 672 |
-27,06 |
|
SiO2-Cu2O |
25 445 |
-23,52 |
Работа проведена по научной программе Федерального агентства по образованию - «Развитие научного потенциала высшей школы (2009-2010 годы)», код проекта - 375 и при поддержке РФФИ, грант № 07-08-00365.
Список литературы Термодинамическое описание системы Cu2O-SiO2
- Физико-химические свойства окислов: справ./Г.В. Самсонов, А.Л. Борисова, Т.Г. Жидкова и др. М.: Металлургия, 1978. 472 с.
- Диаграммы состояния силикатных систем: справ. Вып. 1: Двойные системы/H.A. Торопов, В.П. Барзаковский, В.В. Лапин, H.H. Курцева. Л.: Наука. Ленингр. отд., 1969. 822 с.
- Пономаренко A.Г. Вопросы термодинамики фаз переменного состава, имеющих коллективную электронную фазу. II. Оценка энергетических параметров/A.Г. Пономаренко, Э.П. Мавренова//Журн. физ. химии. 1974. Т. 48, № 7. С. 1672-1674.
- Михайлов Г.Г. Термодинамика раскисления стали/Г.Г. Михайлов, Д.Я. Поволоцкий. М.: Металлургия, 1993. 144 с.
- Chuang Y.Y. Extantion of the associated solution model to ternary metal-sulfur melts: Cu-Ni-S/Y.Y. Chuang, Y.A. Chang//Met. Trans. 1982. V. 13B, № 9. P. 379.
- Сорокин М.Л. Термодинамика системы Cu-O-SiO2/М.Л. Сорокин, H.A. Андрюшечкин, A.Г. Николаев//Цветные металлы. 1997. № 6. С. 16-19.


