Термохимический реактор восстановительных атмосфер с окислением части продуктов паровой конверсии метана
Автор: Дубинин Алексей Михайлович, Черепанова Екатерина Владимировна, Тупоногов Владимир Геннадьевич, Грицук Светлана Александровна, Емельянова Анастасия Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Энергетика @vestnik-susu-power
Рубрика: Теплоэнергетика
Статья в выпуске: 1 т.18, 2018 года.
Бесплатный доступ
Разработана конструкция термохимического реактора для бескислородной паровой конверсии метана с частичным окислением продуктов конверсии с целью обеспечения автотермичности процесса. Реактор разделен на нижнюю зону слоя с каталитической насадкой, в которой происходит конверсия метана, и верхнюю, где организован отвод из реактора части продуктов конверсии и окисление оставшейся части для обеспечения необходимой температуры слоя. Представлены результаты экспериментальных исследований реактора, включающие определение вертикальной эффективной теплопроводности псевдоожиженного слоя электрокорунда, заторможенного алюмо-никелевой каталитической насадкой КСН-2, температуры и состава продуктов конверсии. Разработана стационарная одномерная модель паровой конверсии метана в однородном псевдоожиженном слое, заторможенном каталитической насадкой. Расчетный и экспериментальный составы продуктов конверсии метана при соотношении CH4:H2O=1:1 и температуре на выходе из слоя около 1000 °С удовлетворительно совпадают. Продукты конверсии могут применяться в качестве восстановительных атмосфер, например, при переделе железорудного сырья.
Метан, водяной пар, псевдоожиженный слой, электрокорунд, катализатор, распределение температуры в слое, эффективная теплопроводность слоя
Короткий адрес: https://sciup.org/147232661
IDR: 147232661 | УДК: 621.785.062 | DOI: 10.14529/power180102
Reducing-atmosphere thermochemical reactor with partial oxidation of methane steam reforming products
A thermochemical reactor has been designed for oxygen-free steam reforming of methane with partial oxidation of reforming, which ensures an autothermal process. The reactor consists of a lower zone which contains a bed with catalytic packing where methane is reformed; and an upper zone some of the conversion products are withdrawn from the reactor and the rest is oxidized to maintain the desired bed temperature. We herein present experimental results which include the identified effective vertical thermal conductivity of the fluidized electro-corundum bed inhibited by the KSN-2 aluminum-nickel catalytic packing of KSN-2; the temperature and composition of the reforming products are identified as well. We have developed a stationary one-dimensional model of how methane is steam-reformed in a homogeneous fluidized bed while inhibited catalytic packing. The model is in a satisfactory agreement with experimental results when it comes to the compositions of methane reforming products at a CH4:H2O=1:1 ratio; the same applies to the bed-exit temperature of about 1000 °C. Reforming products can be used as reducing atmospheres, for example, in iron ore processing.
Текст научной статьи Термохимический реактор восстановительных атмосфер с окислением части продуктов паровой конверсии метана
Восстановительные газы получают в крупнотоннажных реакторах шахтного типа, производя конверсию природного газа (метана) водяным паром, добавляя кислород к исходной смеси, который расходуется на полное окисление определенной части метана, что позволяет осуществлять процесс авто-термично, без подвода теплоты извне [1, с. 23, 27]. Однако добавление кислорода к исходной смеси не только приводит к существенному удорожанию получаемого газа, но и ухудшает его состав продуктами полного сгорания метана, что требует для восстановительных процессов очистки газа от CO2 и H2O дорогостоящими способами. Добавление к исходной смеси CH4: H2O = 1:1 кислорода в количестве 0,6 объема на один объем исходного метана, как требуют условия теплового баланса автотермического процесса для поддержания в реакционном объеме температуры 1000 °C, снижает восстановительный потенциал (H2 + CO)/(CO2 + H2O) в 20 раз. Содержание окисляющих компонентов (CO2 + H2O) > 10 % и CH4 >5 % в горячем газе не позволяет использовать его для прямого восстановления железорудных окатышей. Осушка газа охлаждением в скрубберах несколько улучшает состав атмосферы, но требует дополнительной затраты теплоты на его последующий подогрев до 1000 °C перед вводом в агрегат для восстановления железорудных окатышей. Энергоэффективные аппараты для конверсии метана предложены в [2, 3] и проходят исследовательскую стадию.
В работе [4] разработана достаточно сложная конструкция реактора с горячими байпасами и двумя слоями крупнокускового катализатора, что позволяет обеспечить наибольший выход водорода на единицу сырья.
Для увеличения температуры на катализаторе в реторте трубчатой печи предлагается использовать несколько последовательно чередующихся слоев ингибитор-катализатор [5]. При понижении температуры на катализаторе до уровня, при котором возможно выпадение сажи, конверсия прерывается, а неравновесные продукты поступают выше для нагрева в слой ингибитора. Чередование слоев позволяет предотвратить выпадение сажи и разрушение катализатора.
Для выравнивания температуры в объеме реактора предлагается [6] применение гидродинамической интенсификации газового потока, например, в режиме псевдоожижения гранул катализатора, что требует существенного усложнения конструкции реактора.
В работе [7] значения максимальной степени конверсии метана дымовыми газами, полученные теоретически, подтверждаются экспериментальными значениями.
Для построения кинетической модели предлагается [8, 9] механизм реакции паровой конверсии метана, состоящий из одиннадцати стадий. Мольное отношение H2O/CH4 равно двум. Построенная модель адекватно отображает экспериментальные данные.
Скорость подъема пузырей в кипящем слое, размещенном над каталитической насадкой, рассчитывается по методике [10]. Она зависит от рабочей, минимальной скорости псевдоожижения и избыточной порозности псевдоожиженного слоя для прохода пузырей. Пузыри играют определяющую роль в процессе окисления части продуктов конверсии воздухом для увеличения температуры в слое.
В публикации [11] предлагается процесс низкотемпературного производства водорода с одновременным уменьшением выхода диоксида углерода. Представлена экспериментальная установка. В работе [12] моделируется процесс парокислородной конверсии метана, который сравнивается с паровой конверсией метана. Делается вывод о меньшем расходе метана на единицу продукции.
Паровая конверсия метана при отношении CH4:H2O=1:1 рассматривается в работе [13]. Показано, что наибольший выход Н2 получается в адиабатном реакторе. Приведены испытания паровой конверсии метана, полученного из биомассы, с целью производства синтез-газа с высокой теплотой сгорания [14].
В данной публикации исследуется работа реактора с псевдоожиженным слоем упрощенной конструкции, в котором за счет особенностей псевдоожиженного слоя: интенсивного перемешивания твердой фазы и менее интенсивного перемешивания газа, – осуществляется процесс автотермической паровой конверсии метана [15].
Экспериментальные исследования на модели реактора
В разработанной конструкции реактора процессы конверсии и частичное окисление продуктов происходят позонно в реторте реактора, как показано на рис. 1 экспериментальной модели реактора. В реторте 17 с внутренним диаметром 0,18 м помещена кассета из катализатора 5 КСН-2 высотой 0,7 м, в межкусковых объемах которой циркулируют частицы мелкодисперсного электрокорунда размером 0,32 мм, являющегося промежуточным теплоносителем. В псевдоожиженный над насадкой слой частиц 7 погружена фурма, состоящая из трубы 9 диаметром 82 мм, «рубашки» 10 с перфорациями 8. Под газораспределительную решётку 2 подводится водяной пар с метаном. Часть х = 0,25 продуктов конверсии, образующихся в катализаторе в результате стехиометрической эндотермической реакции
^i
CH4 + H2O — CO + 3H2, (1) отводится по трубе 9 для использования, а другая часть (1 — х) = 0,75 расходуется на окисление воздухом с целью обеспечения теплотой реакции конверсии метана, подогрев продуктов этой же реакции и тепловые потери. Теплота переносится в объем каталитической насадки разогретыми частицами мелкодисперсного материала. Воздух для протекания экзотермической реакции окисления части (1 — х) продуктов паровой конверсии метана, описываемой стехиометрическим уравнением
CO + 3H2 + 2(O2 + 3,76N2) =
= CO2 + 3H2O + 7,52N2, (2) подводится через перфорации 8 . Продукты окисления отводятся из реактора через камеру 11 . С целью предотвращения загрязнения продуктов конверсии метана продуктами из камеры окисления части синтез-газа нисходящим потоком газа (CO2, H2O и N2) [16, с. 221], расстояние между отверстиями для выхода воздуха 8 (см. рис. 1) и нижним торцом трубы 9 для отвода продуктов паровой конверсии метана принималось 300 мм [17, с. 20].
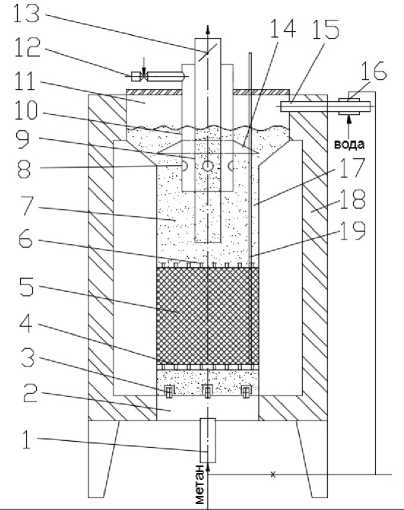
Рис. 1. Схема экспериментального термохимического реактора: 1 – штуцер для ввода парометановой смеси; 2 – газораспределительная беспровальная камера; 3 – беспровальные колпачки; 4 – решетка; 5 – каталитическая насадка КСН-2; 6 – решетка; 7 – псевдоожиженный слой; 8 – перфорации; 9 – внутренняя труба для отвода продуктов паровой конверсии метана; 10 – рубашка; 11 – сборная камера; 12 – штуцер для ввода воздуха; 13 – клапан; 14 – усеченный конус; 15 – штуцер для отвода продуктов сгорания; 16 – теплообменник; 17 – реторта; 18 – тепловая изоляция;
19 – чехол для термопары
Водяной пар получается в теплообменнике 16 или поступает от другого источника. Усеченный конус 14 способствует лучшему перемешиванию продуктов конверсии с воздухом и, как следствие, более полному окислению [18]. Для замера температуры по высоте катализатора использован чехол 19 из тонкостенной легированной трубки, заваренной с нижнего торца, внутри которого перемещалась Х-A термопара (погрешность измерений – 1,5 %). Клапан 13 предназначен для перераспределения долей х и (1-х) между камерами в процессе эксперимента. Расход природного газа с Qh = 35 590 кДж/м3 (объем воздуха и продуктов сгорания при а _ 1: vh = 9,44; vh Г = 10,59 м3/м3) равнялся 3,5 м3/ч, водяного пара - 2,8 кг/ч, воздуха -30 м3/ч. Расходы воздуха и природного газа определялись по ротаметру с относительной погрешностью 2,5 %, водяного пара – дроссельной шайбой с погрешностью 3 %. Соотношение объемных расходов H2O: CH4 = 1:1 на входе в реактор контро- лировалось по составу продуктов конверсии на выходе трубы 9 по балансовому выражению
Гп+гсо+2гсо а = -, гм+гсо+гсо2
а сажевыделение, моль С/моль М, – по составу продуктов паровой конверсии метана из баланса по углероду:
д С _ ^—г н^ +г со +г со^ +г м ) l-r H? .
Состав продуктов конверсии и окисления
многократно определялся на хроматографе с погрешностью 4 %. Влажность продуктов конверсии определяли измерителем влажности по температуре точки росы.
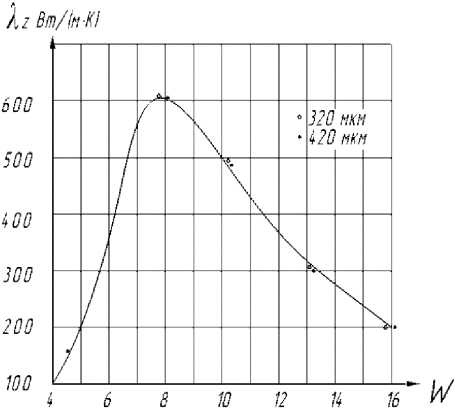
Рис. 2. Зависимость вертикальной составляющей коэффициента теплопроводности заторможенного катализатором КСН-2 псевдоожиженного слоя от числа псевдоожижения. 320 мкм и 420 мкм – размеры частиц электрокорунда
Экспериментальное поле температуры, представленное на рис. 2, показывает существенную неравномерность температуры по высоте катализатора: на нижнем торце камеры с катализатором – 575 °C, а на верхнем – 1000 °C. Полученные в экспериментах продукты паровой конверсии метана на выходе имели следующий состав:
Гп _ 1,76; гС02 _ 1,398; Гн? _ 72,043;
гм _ 2,449; гсо _ 22,35 (% объёмные), а продукты сгорания:
Гсо2 _ 7,8; Го2 _ 0,26; г^ _ 64,24;
гп _ 25,7; гсо _ 2,0 (% объёмные).
Химический недожог q3 составлял 7 %. Восстановительный потенциал
( Гн2 + Гсо )/( Г п + Гсо2 ) _
_ (72,043 + 22,35)/(1,76 + 1,398) _ 29,9;
гм < 5 %; гС02 + гп _ 3,158 < 10 %.
Такой газ можно использовать в качестве восстановительной атмосферы.
Моделирование реактора
Процесс паровой конверсии метана по реакции (1) сопровождается прямой _ к
CO + H2O + 3H2 - CO2 + 4H2
и обратной реакцией водяного газа
к
CO2+4H2-CO + H2O + 3H2, где K2 и K3 - константы скоростей соответствующих реакций. Поэтому в равновесных продуктах паровой конверсии метана при отношении CH4:H2O_ 1:1 всегда присутствует диоксид углерода от 7 % при температуре 500 °C до 0,1 % при 1000 °C [19].
Эндотермический эффект реакции (1) qzl _ _ 12 912 кДж на 1 кг метана, поступившего в реакцию. Теплота, необходимая для протекания ре- акции и компенсации тепловых потерь, выделяется при окислении в кольцевом зазоре между ретортой 17 и «рубашкой» 10 части (1 — х) продуктов конверсии в потоке воздуха, выходящего из перфораций 8 по реакции (2) с экзотермическим эффектом qx2 _ 63 056 кДж на 1 кг метана, поданного в реакцию (1), и переносится в объем каталитической насадки посредством эффективного коэффициента теплопроводности Az Вт/(м^К).
При полном перемешивании мелкодисперсных частиц по сечению реторты стационарную задачу о распределении температуры и концентрации метана вдоль оси z в каталитической насадке можно считать одномерной и описать следующей системой нелинейных уравнений:
d2t
Яz ^z? _ 9xl • Kl • 5 • Гм • Рм • Е +
+т • Спк • CnK(t) ^z;
г м dw + w dr M _ —К5Г , е dz е dz
где плотность метана
Рм _ РМ н.у -273 • Р/(273 + t)Po скорость продуктов конверсии w _ ^пк/рПК;
плотность продуктов конверсии
Р пк = Р . (1 ■ -Р. ■••"■• ... ; ■ (7)
константа скорости реакции (1)
Ki = 87,5 exp[—65 500/(8,31Г)]
взята из [20].
Левая часть уравнения (5) выражает приход мощности за счет вертикальной составляющей эффективной теплопроводности заторможенного насадкой псевдоожиженного слоя мелкодисперсных частиц в объем каталитической насадки. Правая часть уравнения – расход мощности на эндотермическую реакцию и подогрев продуктов этой реакции.
Уравнение (6) представляет собой баланс массы между конвективным притоком реагирующей массы метана в левой части и убылью ее в результате химических превращений в правой части уравнения. Диффузионным потоком массы ввиду его малости по сравнению с конвективным пренебрегаем. Порядок реакции по концентрации метана равен единице. Уравнение (7) выражает зависимость плотности продуктов конверсии не только от температуры и давления, а также от увеличения объема продуктов конверсии в два раза при уменьшении концентрации метана в продуктах конверсии от 0,5 до 0.
Граничные условия к уравнениям (5) и (6): при z = 0:
концентрация метана на входе гм = гм . исх = 0,5; d£l
Л^ ^|х-0 + ^М + ^П = = m • Спк ' CnK(t|z=o) ' t|z=o;
при z = Н:
[9 x2 (1 — 9 з — 9 s)](1 - х) =
— „ (1 ГМ.кон 1 + 2гМ.ИсхА I = Qr! 1----) + ^ ^М.исх !+2^М.кон'
-
+ [ C nC( t| z=H ) ' (1 — х) + х ' GlK^z^// ) 1 ' t| z=H .
Граничное условие на входе в насадку (z = 0) представляет собой уравнение баланса мощности, поступающей через 1 м2 сечения реторты эффективной теплопроводностью с нижнего торца кассеты с катализатором, а также с поступающими под насадку метаном и водяным паром и расходуемой на нагрев продуктов конверсии до температуры на нижнем торце насадки. Истинные теплоемкости продуктов конверсии CnK(t) и окисления Cnc(t) определялись из уравнений (1) и (2) с использованием [21].
На верхнем торце насадки (z = Н) граничное условие устанавливает равенство между теплотой, выделяющейся при окислении части (1 — х) продуктов конверсии (с учетом химического недожога и тепловой потери в окружающую среду), а также подводимой с воздухом в левой части и теплотой, расходуемой на эндотермическую реакцию (1), подогрев продуктов этой реакции и продуктов сгорания до температуры на верхнем торце насадки в правой части уравнения.
Множитель f 1 — г М.кон • 1+2г М.исх А — фактиче- х ^ М.исх 1+2^ М.кон'
ская степень конверсии метана, где множитель 1+2гМ.исх компенсирует эффект разбавления кон-1+2^М.кон центрации метана Гм.кон в процессе реагирования за счет увеличения объема продуктов реакции (1) в два раза. Все величины, входящие в приведенные уравнения, отнесены к 1 кг метана, вводимого в реактор по уравнению (1).
В расчетах принимались следующие значения параметров: гм . исх = 0,5; давление в реакторе р = р0 = 0,1 МПа (р0 - атмосферное); теплота, вносимая в реактор с водяным паром Qn = 551, метаном - qm = 44 и воздухом - qb = 391 кДж на 1 кг метана, вводимого в реактор; удельные потери с химическим недожогом q = 0,07 (7 %), в окружающую среду Q = 0,18 (18 %); удельная площадь поверхности катализатора 5 = 258 м2/м3, его порозность е = 0,345; доля продуктов конверсии, отводимых на полезное использование х = 0,25; высота кассеты с катализатором Н = 0,7 м; диаметр реторты 0,18 м; внутренний диаметр трубы для отвода продуктов конверсии 82 мм; размер частиц электрокорунда 0,32 мм; размер цилиндрических частиц алюмо-никелевого катализатора КСН-2 18 х 18 х 4 мм с отверстием 4 мм; массовая скорость продуктов конверсии СПК, отнесенная к площади сечения пустой реторты, равна 0,06 кг/(м 2 • с). Число псевдоожижения W = 9.
Необходимая масса метана для образования 1 кг продуктов конверсии m = 0,47 кг/кг. При возврате физической теплоты продуктов окисления и конверсии в реактор через производство пара, подогрев воздуха и метана, доля x существенно возрастает.
Для решения уравнения (5) предварительно определялась зависимость эффективного коэффициента теплопроводности в продольном направлении Zz заторможенного каталитической насадкой КСН-2 псевдоожиженного слоя от числа псевдоожижения (отношения рабочей к минимальной скорости псевдоожижения). Для этого в реакторе была проведена серия экспериментов при подаче в реактор только воздуха. В межкусковых объёмах промышленного катализатора КСН-2 ожижались частицы электрокорунда размером 0,32 мм или 0,42 мм. Температура стенки реторты составляла 850 °С, высота слоя катализатора – 0,7 м, число псевдоожижения воздуха - Ж = 4 - 18. Величина xz определялась путем наложения на поле экспериментальной зависимости t(z) с рассчитанной из уравнения (5) t * (z) при различных значениях Zz и одинаковых значениях W . При максимальном совпадении температур t(z) и t * (z) значение Xz принималось таким же, какое соответствовало расчетной температуре t * (z) при одном и том же числе псевдоожижения. Результаты представлены на рис. 2, из которого видно, что Xz от числа W проходит через максимальное значение 600 Вт/(м·К) при числе W = 8. С увеличением W частицы корунда выносятся из насадки и Zz уменьшается.
Ре з у л ьта ты ра с че тов з а в исим ос ти те м пе ра тур ы и кон центра ц и и м ета на от в ыс оты ка та лит ичес кой на са д ки по у ра в нен ия м (5) и (6) с у пом ян утыми граничными условиями и A z = 400, 500, 600, 700 и 1000 Вт/(м∙К) при числе W = 9 представлены на рис. 3. Вид н а с и л ьная н е ра в ном е рнос ть те м пер а т уры в ос е в ом напра вл е н ии. Че м в ыше Az, тем неравномерность те м пе ра т уры по в ыс оте м еньше . Н а рис . 3 на не с е ны и экс перим е нтал ьно полу че нные з на чени я те м пе ра т у ры по в ыс оте на с адк и пр и W — 9 , которые ук л а ды в а ются м е ж д у те мпе ра т урами, вычисленными при Xz — 500 и 600 Вт/(м^К) (т. е. Az = 550 Вт/(м<К ) ), что у д ов л е творительно согл а суе тся с данными, пре дста в л ен ным и на рис. 2, где Az = 550 Вт/(м^К) та к ж е с оотв е тс тву е т числу псевдоожижения W = 9.
К онцентраци и ос та л ь ных ком пон ен тов в проду к та х ко нв е рс и и на в ы х од е из ре а к тора опре дел ял и сь из ура вне н ия м а те р иа л ь ного ба л анса реакции (1) по концентрации гМ . кон, и з кот орого в идно, что на 1 моль CH4 р а с х од уетс я 1 м ол ь H2O, а из 1 моля CH4 получа е тс я 1 м ол ь CO и 3 моля H2. Ч и сл о м ол ей прод у ктов кон в е рс ии п ри кон ц е н тр ации метана на выходе гМ . кон — 4/(1 + 2гМ . кон), число молей метана на выходе
ММ.коН — 4 • гм.кон/(1 + 2 ^ М. к о н ).
Фактическое число молей прореагировавшего метана равно 1 — ММ . кон.
Число молей оксида углерода:
МСО = 1 - ММ кон .
Число молей водорода:
М н2 = 3(1 — М м^он ).
Число молей водяного пара:
МН2О — ММ.кон .
Общее число молей смеси на выходе:
М — Е М1 — МСО + МН2+ МН2О + ММ.кон .
Объемные доли компонентов смеси, м 3 /м 3 :
Г ео — МСО/М ; ГН2— МН2/М ; ГН2О — МН2О/М ;
Г м — М м.кон /М.
Концентрация диоксида углерода:
ГСО 2
К Р^СО^Н 2 О
,
Г Н
где КР - константа равновесия реакции водяного газа, находится из [17, с. 20].
Расчетный состав продукта конверсии близок к экспериментальному при температуре 1000 °С на верхнем торце кассеты с катализатором (см. таблицу). Расчетный состав продуктов паровой кон- версии метана удовлетворительно совпадает с экспериментальным. Наибольшие расхождения по диоксиду углерода и воде. Загрязнение продуктов конверсии продуктами полного сгорания не про-
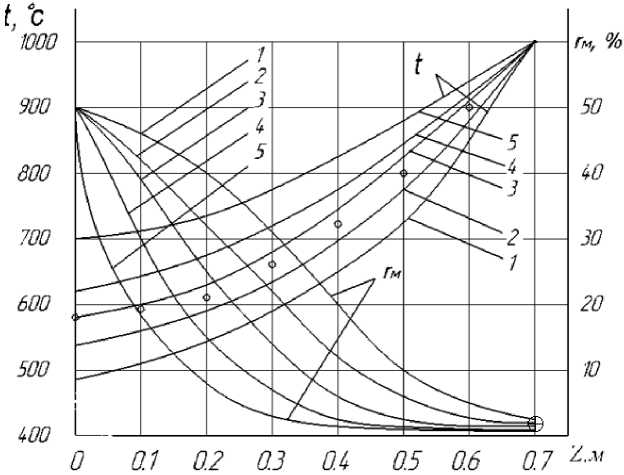
Рис. 3. Распределение температуры и концентрации метана по высоте реактора при W = 9. Кривые 1, 2, 3, 4, 5 соответствуют λ z = 400, 500, 600, 700 и 1000 Вт/(м∙К). Точки ○ – экспериментально замеренная температура. г М - концентрация метана (% объемные). Точка ® - экспериментально замеренная концентрация метана на выходе из реактора
Сравнение экспериментально полученного состава продуктов паровой конверсии метана с расчетным при температуре 1000 °С
|
Компоненты смеси на выходе |
Г м |
ГН 2 |
Гсо |
ГСО 2 |
Гн2о |
|
Эксперимент, % объемн. |
2,449 |
72,043 |
22,35 |
1,398 |
1,76 |
|
Расчет, % объемн. |
2,44 |
70,935 |
23,66 |
0,495 |
2,47 |
исходило. Состав получаемого газа удовлетворяет требованиям, предъявляемым к восстановительным атмосферам. Хотя реактор конструктивно прост, но имеет недостаток из-за добавления в продукты сгорания 1 моля водяного пара на 1 моль метана, поскольку окисляется не метан, а продукты паровой конверсии метана, что увеличивает потерю с уходящими продуктами сгорания.
Заключение
Эффективность работы реактора в значительной степени определяется коэффициентом переноса теплоты Az. Чем больше величина Az, тем выше средняя температура, а следовательно, и скорость реакций. Обратное влияние на распределение температур и концентраций оказывает увеличение массовой скорости продуктов конверсии.
Значения Az достаточны для переноса теплоты из верхних слоев аппарата в нижние и поддержания там температуры на высоком уровне 600–1000 °C.
В продуктах, выводимых из камеры сгорания, имеется водяной пар, уменьшающий термический КПД аппарата на 5,5 %.
Исключено проникновение продуктов полного сгорания в камеру отвода продуктов конверсии за счет нисходящего потока газа в плотной фазе в камере сгорания. Метан появляется в продуктах газификации из-за реакции гидрогенизации углерода. Хорошо проходит только под высоким давлением 2–20 МПа.
Перемешивание твердой фазы и связанный с ним перенос теплоты носят диффузионный характер, поэтому система описана дифференциальным уравнением второго порядка конвективного теплопере-носа со стоками теплоты. Присутствие в продуктах CO2 и H2O в небольших количествах связано с тем, что реакции не успевают дойти до равновесия.
Разработана конструкция термохимического реактора паровой конверсии метана с заторможенным катализатором псевдоожиженным слоем для получения восстановительных атмосфер.
Экспериментально показано, что эффективный коэффициент осевой теплопроводности заторможенного насадкой слоя электрокорунда, ожижаемого продуктами конверсии и воздухом, практически совпадают при одинаковых числах псевдоожижения. При Ж = 9 значение Az составляет около 550 Вт/(м∙К).
Состав продуктов конверсии:
Н2 = 72,043; CO = 22,35; гСО2 = 1,398;
CH4 = 2,449; H2O = 1,76 (% объёмные)
пригоден для процессов восстановления железорудных окатышей, так как (СО2 + H2O) < 10 %, (H2 + СО)/(СО2 + H2O) > 10, а CH4 < 5 %.
Разработана расчетная модель реактора, удовлетворительно описывающая экспериментальные данные, при помощи которой рассчитываются все параметры, необходимые для проектирования реакторов промышленного назначения.
Список литературы Термохимический реактор восстановительных атмосфер с окислением части продуктов паровой конверсии метана
- Производство технологического газа для синтеза аммиака и метанола из углеводородных газов / под ред. А.Г. Лейбуш. - М.: Химия. - 1971. - 286 с.
- Оптимальные параметры реактора с заторможенным насадкой циркуляционным псевдоожиженным слоем для паровой конверсии метана / А.М. Дубинин, С.Е. Щеклеин, В.Г. Тупоногов и др. // Международный научный журнал «Альтернативная энергетика и экология». - 2015. - № 13-14 (177-178). - С. 103-108. DOI: 10.15518/isjaee.2015.13-14.010
- Писаренко, Е.В. Энерго- и ресурсосберегающий процесс получения синтез-газа из природного газа в производстве метанола / Е.В. Писаренко, В.Н. Писаренко // Теоретические основы химической технологии. - 2011. - Т. 45, № 1. - С. 371-377.
- Мещеряков, Г.В. Конверсия природного газа для совместных производств метанол-водород, метанол-аммиак / Г.В. Мещеряков, Ю.А. Комиссаров // Вестник МИТХТ. - 2011. - Т. 6, № 4. - С. 72-76.
- Igumnov, V.S. Technical and technological methods of realization of steam catalytic conversion of natural gas with a methane-watr proportion close to stoichiometric ratio / V.S. Igumnov // Hydrogen Material Science and Chemistry of Carbon Nanomaterials / T.V. Veziglu et al. (eds). - Springer, 2007. - P. 555-561. DOI: 10.1007/978-1-4020-5514-0_70
- Oxidative coupling of methane: Process design, development and operation in mini-plant scale / S. Stünkel, H. Trivedi, H.-R. Godini et al. // Chemie Ingenieur Technik. - 2012. - No. 11. - P. 1989-1996.
- DOI: 10.1002/cite.201200052
- Hoang, D.L. Kinetic and modeling study of methane steam reforming over sulfide nickel catalyst on a gamma alumina support / D.L. Hoang, S.H. Chan, O.L. Ding // Chemical Engineering Journal. - 2005. - Vol. 112. - P. 1-11.
- DOI: 10.1016/j.cej.2005.06.004
- Xu, J. Methane steam reforming, methanation and water gas shift: I. Intrinsic Kinetics / Xu J., Froment G.F. // AIChE J. - 1989. - Vol. 35, no. 1. - P. 88-96.
- DOI: 10.1002/aic.690350109
- Xu, J. Methane steam reforming: II. Diffusional limitations and reactor / J. Xu, G.F. Froment // The journal of the American Institute of Chemical Engineers (AlChE). - 1989. - Vol. 35, no. 1. - P. 97-103.
- DOI: 10.1002/aic.690350110
- Kehoe, P.W. Pressure fluctuation in sluggins fluidized beds / P.W. Kehoe, J.F. Davidcon // The journal of the American Institute of Chemical Engineers (AlChE). - 1973. - Vol. 69, no. 128. - P. 34-40.
- Progress in low temperature hydrogen production with simulaneous CO2 abatement / H. Chen, Y. Ding, N.T. Cong et al. // Chemical Engineering Research and Design. - 2011. - Vol. 89, iss. 9. - P. 1774-1782.
- DOI: 10.1016/j.cherd.2010.06.008
- Integrated auto-thermal oxidate coupling and steam reforming of methane. Part 1: Design of dual-function catalyst particle / T.P. Tiemersma, A.S. Chaudhari, F. Gallucci et al. // Chemical Engineering Science. - 2012. - Vol. 82. - P. 200-214.
- DOI: 10.1016/j.ces.2012.07.048
- Fernandez, J.R. Modeling of sorption enhanced steam methane reforming in an adiabatic fixed bed reactor] / J.R. Fernandez, J.C. Abanades, R. Murillo // Chemical Engineering Science. - 2012. - Vol. 84. - P. 1-11.
- DOI: 10.1016/j.ces.2012.07.039
- Hiblot, H. Steam reforming of methane in a synthesis gas from biomass gasification / H. Hiblot // International Journal of Hydrogen Energy, 2016. - Vol. 41. - P. 18329-18338.
- DOI: 10.1016/j.ijhydene.2016.07.226
- А.С. 992079 СССР. Генератор эндотермических атмосфер / А.М. Дубинин, А.П. Баскаков, В.Б. Шойбонов. - № 3260865/22-02; заявл. 06.01.81; опубл. 30.01.83, Бюл. № 4.
- Кунии, Д. Промышленное псевдоожижение. США, 1969 / Д. Кунии, О. Левеншпиль; пер. с англ. под ред. М.Г. Слинько и Г.С. Яблонского. - М.: Химия, 1976. - 448 с.


