Тяжелое желудочно-кишечное кровотечение как проявление гранулематозного полиангиита (гранулематоза Вегенера)
Автор: Фролова Н.Ф., Ветшева М.С., Лосс К.Э., Подкорытова О.Л., Волгина Г.В., Брацун О.И., Воронова Н.Е., Назарова И.Н.
Журнал: Московский хирургический журнал @mossj
Статья в выпуске: 3 (55), 2017 года.
Бесплатный доступ
Гранулематоз с полиангиитом (гранулематоз Вегенера) (ГПА) представляет собой первичный васкулит неизвестного этиологии, характеризу- ющийся гранулематозным некротизирующим воспалением мелких артерий и вен. Консенсус Chapel Hill классифицировал ГПА как васкулит с по- ражением небольших сосудов антинейтрофильными цитоплазматическими антителами (cANCA). Классическое проявление болезни, описанное Вегенером в 1936 году, включает в себя поражение верхних и нижних дыхательных путей и гломерулонефрит, оно может влиять на любой другой орган. Это приводит к неоднородности клинических проявлений. Хотя участие желудочно-кишечного тракта встречается редко, но поражается не только толстая, но и тонкая кишка, что вызывает серьезное осложнение ГПА.
Гранулематоз с полиангиитом, кровотечение из желудочно-кишечного тракта
Короткий адрес: https://sciup.org/142212749
IDR: 142212749 | УДК: 616.33-073.75
Текст научной статьи Тяжелое желудочно-кишечное кровотечение как проявление гранулематозного полиангиита (гранулематоза Вегенера)
Гранулематозный полиангиит Вегенера (ГПА), со старым, привычным названием Гранулематоз Вегенера (ГВ) – это полигенетический системный васкулит ассоциированный с выработкой антинейтрофильных цитоплазматических антител (АNCA), поражающий сосуды мелкого калибра с развитием некротизирующего васкулита с образованием гранулем и характеризующимся отсутствием (или небольшим количеством) отложения иммунных депозитов, потреблением комплемента (малоиммунные - pauci- иммунный васкулит). При ГПА в 85% случаев, имеется гиперпродукция ANCA со специфичностью к протеиназе-3 (PR-3, с- ANCA). Для него характерна воспалительная клеточная инфильтрация и некроз стенки кровеносных сосудов, с образованием гранулематозной воспалительной реакцией, приводящая к ишемическим изменениям в органах и тканях, что и объясняет многообразие клинических проявлений и поражение жизненно важных органов [1].
Для гранулематозного полиангиита Вегенера характерно множественное поражение жизненно важных органов. В зависимости от характера вовлечённых в патологический процесс органов, выделяют локальную, генерализован- ную форму заболевания. В случае поражения почек, легких, сердца, суставов, и достаточно редко, только в 5-15% случаях, поражение органов желудочно-кишечного тракта (ЖКТ), говорят о генерализованной стадии заболевания, имеющей тяжелый прогноз [2, 3].
В седьмом пункте Бермингемской шкалы активности васкулита (BVAS), оценивается тяжесть вовлечения ЖКТ, что указывает на высокую степень активности генерализованной формы ГПА. Поражении ЖКТ, которое проявляется болями в животе, диареей, иногда кровотечением, вследствие развития ишемических язв желудка и кишечника, вплоть до перфорации. Описаны синдром Budd Chiari, панкреатит, холецистит, перитонит, асцит, патология печени (гепатомегалия), как правило, поражение желудочно-кишечного тракта представлены ишемическим поражением или перфорацией кишки [4–7].
За последние десятилетия в мире отмечена тенденция к увеличению распространенности АNCA-АВ. Заболеваемость АNCA-АВ в частности ГПА, колеблется от 4 до 250 случаев на 100 000 населения в год. Пик заболеваемости приходится на 45–55 лет, мужчины болеют несколько чаще, чем женщины. Распространенность АNCA-АВ (р-АNCA)
наиболее высока в странах Северной Европы, в то время, как частота АNCA-АВ (с-АNCA) и вероятность поражения почек возрастают в южных широтах и странах Азии. Наибольшая заболеваемость АNCA-АВ отмечена в Швеции: 300 на 1 млн. жителей, при этом антитела к с-АNCA выявляют только у 35% больных. В то же время, в Японии у 91% больных обнаруживают антитела к р-АNCA, и не было зарегистрировано ни одного случая с-АNCA. Заболеваемость АNCA-АВ в Российской Федерации не установлена [8–10].
Клинические проявления системных васкулитов определяются типом, размером и локализацией пораженных сосудов, а также тяжестью иммуновоспалительных изменений и характеризуются сложными патогенетическими механизмами, разнообразностью клинико-иммунологических форм, прогрессирующим течением. Несмотря на проводимую патогенетическую терапию, вероятность летальных исходов при данной патологии остается очень высокой. С учетом поражения жизненно важных органов, фатальностью лечения необходима быстрая диагностика и своевременное начало патогенетической терапии [11].
В патогенезе развития некротизирующего васкулита активное принимают В-клетки и плазмоциты, которые производят АNCA. Цитоплазматические АNCA-антигены высвобождаются на поверхности нейтрофилов и активируют альтернативный путь комплемента, вызывающий некротическое воспаление сосудов. Происхождение АNCA до настоящего времени не известно, но они связаны с генетически-детерминированной HLA-специфичностью [12, 13]. Вместе с тем в 10% случаев даже при активном васкулите АNCA не обнаруживаются. Так же выделяют изолированный почечный васкулит, при котором отсутствуют системные проявления, но имеется клиника гломерулонефрита (ГН), с гиперпродукцией АNCA-АТ. Отсутствие АNCA, не исключает диагноза АNCA-АВ. С другой стороны, АNCA могут быть обнаружены у больных с другими аутоиммунными заболеваниями, воспалительными заболеваниями кишечника, туберкулезом, инфекционным эндокардитом, эхинококкозе, опухолях легких.
Прогноз при АNCA-АВ в отсутствии лечения неблагоприятный и большинство пациентов умирают в течение первого года болезни, вследствие неуклонного прогрессирования заболевания в виде развития - тяжелого повреждения легких и легочного кровотечения; острого панкреатита; некрозов слизистой кишечника с профузным кровотечением; поражение ЦНС (цереброваскулит, полинейропатия); поражение сердечно-сосудистой системы (перикардит); быстропрогрессирующим гломерулонефритом (БПГН) с неизбежным развитием терминальной хронической почечной недостаточности (ТХПН). Даже при применении патогенетической терапии, включающей стандартные иммуносупрессивные препараты (кортикостероиды, циклофосфамид), кумулятивная 5-летняя выживаемость составляет около 70%, причем 25% из выживших пациентов, остаются на постоян- ной заместительной почечной терапии (диализ-зависимые). Известно, что АNCA-АВ свойственно рецидивирующее течение, несмотря на патогенетическую терапию [14,15].
Большинство желудочно-кишечных проявлений ГВ, о которых говорится в литературе, являются острыми и часто катастрофическими. Pagnoux С. с соавторами отмечает, что оперативное лечение у пациентов с некротизирующими васкулитами только ухудшает прогноз и снижает показатели выживаемости [16].
Мы представляем клинический случай гранулематозного полиангиита Вегенера с поражением почек, легких, ЛОР-органов с тяжелым вовлечением желудочно-кишечного тракта, который проявился профузным желудочно-кишечным кровотечением.
История болезни
Больная В. 56 лет госпитализирована в ГКБ №52 по каналу перевод из ГКБ им. В.В. Вересаева 16.06.2017
Анамнез заболевания:
До марта 2017 года считала себя здоровой. В конце марта 2017 года перенесла ОРВИ, осложнившуюся средним гнойным отитом, перфорацией барабанной перепонки. Проходила лечение в ГКБ им. С.П. Боткина с диагнозом «острый 2-сторонний гнойный отит, невропатия лицевого нерва». 23.05.17 выполнена ревизия левой барабанной полости. 17.05.17 - шунтирование барабанной полости. Выписана домой 30.05.17. 01.06.17 обратилась в диагностическое отделение ГКБ им. С.П. Боткина в связи с болями в животе. Выполнена ЭГДС, диагностирован эрозивный гастрит, принимала противоязвенную терапию. С 03.06.17 отмечалось повышение Т тела до 38 oС, усилился парез лицевой мускулатуры, в связи с чем 05.06.17 госпитализирована в терапевтическое отделение ГКБ им. В.В. Вересаева с предварительным диагнозом: «острая невропатия лицевого нерва слева с поражением дистального участка на фоне острого гнойного среднего отита, осложнившегося мастоидитом, фаза восстановления». При обследовании: лабораторно отмечается быстрое нарастание азотемии: мочевина 6,5-15 ммоль/л, креатинин 111-507 мкмоль/л, прогрессирующая анемия: Нв 120-67 г/л, лейкоциты 8-10,6*10/9, тромбоцитопения 183-80*10/9, в общем анализе мочи: 1010, белок 0,99 г/л, лейкоциты 30-31 в п/зр, эритроциты 2-3 в п/зр, цилиндры 0-1 в п/зр.
По данным ЭХО-КГ: полости не расширены, нарушении локальной сократимости не выявлено, миксоматозная дегенерация створок МК. В правой плевральной полости следы жидкости. Рентгенография органов грудной клетки 11.06.17: 2-сторонняя плевропневмония. МСКТ височных костей от 06.06.17: КТ-картина полисинусита, левостороннего гайморита. МСКТ легких от 14.06.17: 2-сторонний фиброз, 2-сторонняя пневмония, плеврит. УЗИ плевральных полостей от 11.06.17: выпот в плевральных полостях с 2-х
сторон 400-500 мл. УЗИ плевральных полостей от 14.06.17: нарастание выпота в плевральных полостях – справа 600 мл, слева 1 л. Консультирована нефрологом: следует проводить дифференциальный диагноз с гранулематозом Вегенера и сепсисом с развитием полиорганной недостаточности. В стационаре проводилась антибактериальная терапия. Лабораторно отмечен рост С-РБ, лихорадка до 38,5 oС , что потребовало замены антибактериальной терапии. Направлены анализы крови на АNCA. 08.06.17 произведен прокол левой гайморовой пазухи. 14.06.17 проведена плевральная пункция с диагностической целью: эвакуировано 400 мл жидкости желтоватого цвета. 15.06.17 получен положительный результат исследования крови на АNCA – выявлено повышения титра антитела к пероксидазе-3 (более 200). 15.06.17 переведена в ОРИТ в связи с нарастанием дыхательной недостаточности. Проводились сеансы НИИВЛ. 15.06.17 начата пульс-терапия солумедролом в дозе 750 мг\сут.
16.06.2017 в связи с прогрессированием почечной недостаточности переведена в ОРИТ №2 ГБУЗ «ГКБ № 52 ДЗМ».
При поступлении: состояние тяжелое. Сознание ясное. По шкале Глазго 15 баллов. Тяжесть состояния по шкале АРАСНЕ II 18 баллов. Жалобы на слабость. Кожные покровы и видимые слизистые бледные, чистые, высыпаний нет. Суставы не изменены. Признаков варикозно- расширенных вен нижних конечностей не визуализируется. Дыхание самостоятельное, эффективное. Речевая одышка. Начата инсуфляция увлажненного О2- 2-3 л\мин. SpО2 - 99%. Над легкими выслушивается жесткое дыхание, несколько ослабленное над нижними отделами с обеих сторон, хрипов нет. Тоны сердца приглушены, ритм правильный. АД 105\63 мм рт.ст., ЧСС 79 в мин. По ЭКМ-ритм синусовый. Живот не вздут, участвует в акте дыхания, доступен глубокой пальпации во всех отделах. Перистальтика выслушивается. Печень и селезенка не пальпируются. Поясничная область не изменена, на пальпацию не реагирует. Почки не пальпируются. Диурез по мочевому катетеру 500 мл/сут.
По данным лабораторного обследования:
Общий анализ крови: Hb - 88 г/л, L-20 109/л, Tr - 155 109/л, п/яд – 1, с/яд-90, мон-2%, лф-6%, СОЭ-2 мм/ч.
Биохимический анализ крови: креатинин плазмы крови – 597 мкмоль/л, мочевина- 26 ммоль/л, ЛДГ 663 Ед\л, общий белок 55 г\л, альбумин 26 г\л, мочевая кислота – 662 мкмоль/л, билирубин общ. - 10,3 мкмоль/л, АСТ-22,6 ЕД/л, АЛТ-2,7 ЕД/л, ГГТ-38,6 ЕД/л, ЩФ-179 ЕД/л, холестерин – 2,98 мкмоль/л, панкр.амилаза – 32,4 ЕД/л, С-РБ – 90 мг/мл, калий 4,1 ммоль\л, натрий 130 ммоль\л, глюкоза крови 14 ммоль\л, КОС: рН 7,41, ВЕ 0,6 ммоль\л.
Иммунологическое исследование:
Антитела к протеиназе-3 IgG – 14,8 (норма <20 МЕ/мл), Антитела к МПО – 5,1(норма <20 МЕ/мл), IgM – 153 (норма 130-170 мг/дл), IgA – 139 (норма 210-290 мг/дл), IgG – 924 (норма 1200-1400 мг/дл)
Коагулограмма: ФБ- 3,34 г/л, ПВ- 34,7сек., АЧТВ 37,4 с, МНО 3,17., ТВ- 18,7 сек.
Протеинограмма: общий белок 44,9 г/л: альбумин 53,2%, альфа-1-11,7%, альфа-2- 7,4%, бета-1- 4,0%, бета-2- 2,9%, гамма 20,8%.
Общий анализ мочи: уд. вес-1015, белок-0,7 г/л, лейкоциты – 206 кл/мкл, эритроциты – 5936 кл/мкл
Инструментальные методы обследования:
УЗИ внутренних органов: Заключение: Диффузные изменения п/железы, асцит, диффузные изменения паренхимы почек, двухсторонний гидроторакс.
ЭХО-КГ: Общая систолическая функция миокарда левого желудочка удовлетворительная. Зон нарушения локальной сократимости не выявлено. Нарушение функции диастолического расслабления миокарда ЛЖ. Незначительная симметричная гипертрофия миокарда ЛЖ. Полости сердца не расширены. Эхо-признаки умеренной легочной гипертензии. СДЛА – 55 mm Hg.ТР 1 ст. Уплотнение корня аорты, колец и створок аортального и митрального клапанов. Митральная недостаточность легкой степени. Следы перикардиальной жидкости.
ЭКГ: Ритм синусовый. ЧСС 68 в минуту. ЭОС вертикальное направление.
Рентгенография органов грудной клетки: Заключение: Рентген-картина застойных явления в малом круге кровообращения. Отек легких? Дифференцировать с двусторонними полисегментарными инфильтративными изменениями
В ОРИТ №2, на основании анамнеза, клинико-инструментальных и лабораторных данных был установлен клинический диагноз:
Основной: АNCA-ассоциированный васкулит (Гранулематоз Вегенера), с поражением ЛОР-органов (2-сторонний средний отит, мастоидит), поражения почек (БПГН с ОПН), легких (2-сторонняя пневмония, пневмонит).
Осложнения: Быстропрогрессирующий гломерулонефрит (БПГН), ОПН. Уремия. Анемия. 2-сторонний гнойный средний отит. Ревизия левой барабанной полости-23.05.17. Шунтирование левой барабанной полости - 17.05.17. Двусторонняя пневмония. Двусторонний гидроторакс. Состояние после пункции плевральной полости.
С учетом наличия характерного симптомокомплекса: поражения ЛОР органов, анемия, лихорадка, активный нефритический синдром с нарастающей почечной недостаточностью, двухсторонний легочный процесс, серологически- АТ к ПР3 более 200, незамедлительно принято решение о проведение патогенетической терапии высокими дозами кортикостероидов, высокообъёмными плазмаобменами, цитостатиками, учитывая наличие диализ-потребной почечной недостаточности – сеансы гемодиализа.
16.06.17, 17.06.17, 18.06.17 – проведено две процедуры каскадного плазмообмена, без использования донорской плазмы, с одновременным введением иммуноглобулина
(И.Г. Вена): 16.06.17 – 5 гр., 17.06.17 – 5 гр., 18.06.17 – 10 гр.; 19.06.17 введено 600 мг циклофосфана; продолжена антибактериальная терапия (бакперазон 2 гр х 2 р\сут, линезо-лид 600 мг х 2 р\сут).
Однако 19.06.17 течение заболевания осложнилось развитием желудочно-кишечного кровотечения (отмечалось снижение уровня гемоглобина до 57 г/л, при ЭГДС - эрозивно-язвенный гастрит – Forest 3, на фоне атрофии слизистой. Множественные острые язвы 12 п.к. Умеренно выраженный дуоденит). В этот же день по данным МСКТ органов грудной клетки выявлено двухстороннее массивное кровоизлияние в легочную ткань (рис.1), в связи с чем с 19.06.17 начаты сеансы плазмаобмена с замещением свежезамороженной плазмы объемом замещения до 3,0 литров и в/в введение метилпреднизолона 125 мг перед процедурой, продолжено лечение гемодиализом без применения гепарина.
Учитывая тяжелую гемическую гипоксию на фоне анемии неоднократно проводилась гемотрансфузия эритроцитарной взвеси. На фоне проводимого лечения дыхательная недостаточность не прогрессирует - на фоне инсуфляции кислорода 5 л/минуту сатурация и газы крови в норме. Тем не менее в общем анализе крови сохраняется анемия тяжелой степени (Нв 55-45 г/л), неоднократно отмечалась примесь крови в стуле, сменившаяся меленой.
Выполнена колоноскопия - эрозивно-язвенный колит с признаками кровотечения на момент осмотра, активное поступление крови через Баугиниеву заслонку (рис.2). Для оценки гемостаза пациентка неоднократно консультирована гемостезиологом, выполнялись исследования ТЭГ, с гемостатической целью производилась трансфузия криопреципитата. Учитывая тяжелое состояния больной, развитие смертельного осложнения основного заболевания – профузного желудочно-кишечного кровотечения, для определения дальнейшей тактике ведения пациентки проведен консилиум, который принял решение, что в настоящий момент тяжесть состояния пациентки обусловлена обширным поражением ЖКТ на фоне активности системного васку- лита в виде множественных эрозий желудка, всех отделов толстой и, вероятно, тонкой кишки с активным кровотечением. С учетом объема поражения, оперативное лечение не показано.
Необходимо продолжить патогенетическую терапию в виде ежедневных плазмаобменов с предварительным в/в введение метилпреднизолона. Ежедневное динамическое наблюдение хирургов. К терапии добавлены - Де-нол 480 мг/сут, сульфосалазин 2000 мг/сут. Продолжена инфузия омепразола 160 мг/сут через шприцевой дозатор, парентеральное питание. Контроль ЭГДС, колоноскопии.
На фоне проводимой терапии к 13 суткам пребывания в ОРИТ №2 отмечалась четкая положительная динамика в виде прекращения мелены, повышения уровня гемоглобина крови до 80 г/л, нормализации показателей коагулограммы - МНО 1,48, АЧТВ 30,1 сек, ПТИ 71,43%, данных ЭГДС в динамике (эрозивный гастрит на фоне атрофии слизистой, рубцовая деформация желудка, язва луковицы 12 перстной кишки, бульбит, умеренно выраженный дуоденит). Также мы видели четкую положительную динамику в легких (рис. 3), снижение уровня креатинина плазмы крови 150 мкмоль/л, восстановления диуреза до 2200 мл/сут, прекращения сеансов гемодиализа.
При стабилизации состояния пациентка для дальнейшего лечения была переведена во 2-е нефрологическое отделение, где была продолжена патогенетическая терапия (преднизолон в/в), активная гастропротективная терапия, гипотензивная терапия, коррекция анемии. Была продолжена активизация пациентки с положительной динамикой, консультирована логопедом. Пациентке была выполнена ЭГДС-контроль - диффузный эрозивный дуоденит, очаговый бульбит, острые эрозии антрального отдела желудка, очаговый гастрит. По сравнению с предыдущим ЭГДС положительная динамика. Была консультирована гастроэнтерологом, скорректирована гастропротективная терапия.
25.07.17 выполнена ЭГДС в динамике - острая язва луковицы 12 перстной кишки в стадии открытого дефекта,
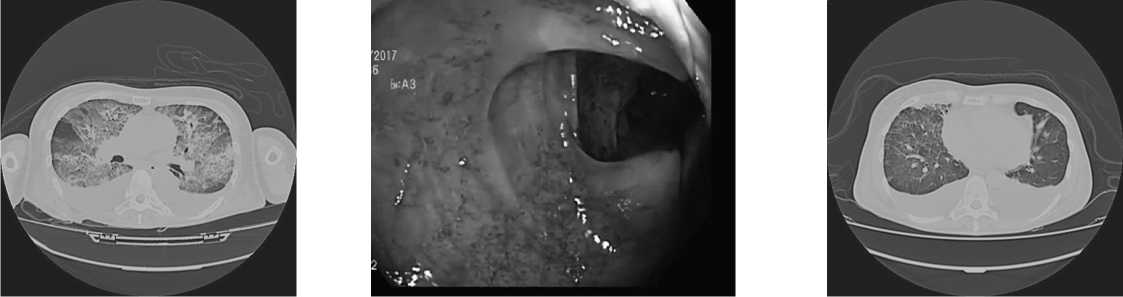
Рис. 1. МСКТ легких 19.06.17
Рис. 2. Колоноскопия 22.06.17
Рис. 3. МСКТ легких 26.06.17
геморрагический гастрит, рубцовая деформация луковицы 12 перстной кишки, кандидоз пищевода. После чего была назначена противогрибковая терапия. При контроле МСКТ органов грудной клетки выраженная положительная динамика, умеренные интерстициальные изменения легких (рис.4). Лабораторно стабилизация уровня азотемии – креатинин 148 мкмоль/л, в продолжении заместительной почечной терапии не нуждается, уровень гемоглобина повысился до 99 г/л, уменьшилась активность нефритического синдрома. Лабораторно сохраняется иммунологическая активность – АТ к МПО повышение в 3 нормы (66,4 Ме/л). В связи с сохраняющейся активностью основного заболевания 18.07.17 был введен циклофосфан в дозе 500 мг в/в (2-е введение). Введение перенесла удовлетворительно. При контроле лабораторных данных без отрицательной динамики. Достигнут запланированный клинический результат на стационарном этапе лечения. 30.07.17 пациентка выписана на амбулаторный этап наблюдения и лечения у нефролога КДНО.
Обсуждение и выводы
Системные аутоиммунные заболевания могут вызывать множество желудочно-кишечных осложнений, которые являются одной из основных причин тяжести заболевания, а иногда и смерти пациента, особенно если они вовремя не диагностируются и не проводится патогенетическая терапия.
Гранулематоз с полиангитом характеризуется некротизирующим васкулитом и гранулематозным воспалением. Болезнь имеет склонность к поражению верхнего и нижнего дыхательного тракта, и почек, но у 10 - 25 % больных выявляется поражение желудочно-кишечного тракта [17,18]. Васкулит может вызывать локальные или диффузные патологические изменения в желудочно-кишечном тракте. Эти изменения достаточно разнообразны - язвы, подслизистый отек, кровоизлияние, динамическую непроходимость, ишемию брыжейки кишечника, обструкцию кишечника и опасную для жизни перфорацию. Диагноз желудочно-кишечных осложнений во многом зависит от клинической картины заболевания. Все это вызывает серьезную угрозу жизни пациентов. Дифференциальный диагноз должен охватывать другие воспалительные заболевания, особенно болезнь Крона. Нельзя не учитывать и побочные эффекты иммуносупрессивного лечения, как причины кишечных осложнений.
Патогенетическая терапия, широко используемая для лечения ГПА, эффективна при лечении пациентов с желудочно-кишечным поражением, как проявлением основного заболевания, хотя некоторые осложнения, такие, например, как перфорация полого органа, требуют хирургического вмешательства.
Список литературы Тяжелое желудочно-кишечное кровотечение как проявление гранулематозного полиангиита (гранулематоза Вегенера)
- Jennette J.C., Falk R.J., Bacon P.A. et al. 2012 revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides -Arthritis Rheum. -65 (1): 2013; 1-11
- Nadeau SE. Neurologic manifestations of systemic vasculitis. Neurol Clin. 2002; 20 (1):123-150
- Grant SC, Levy RD, Venning MC, Ward C, Brooks NH. Wegener's granulomatosis and the heart. Br Heart J. 1994; 71 (1):82-86
- Бекетова Т.В. АНЦА-ассоциированные системные васкулиты. Под редакцией академика РАН Насонова Е.Л. Москва, 2015 46-48 с./ENG
- Strivens RL, Bateman A, Arden NK, Edwards CJ. Intestinal perforation and jejunal haemorrhage due to Wegener's granulomatosis. Clin Exp Rheumatol. 2005; 23 (1):124
- Geraghty J, Mackay IR, Smith DC. Intestinal perforation in Wegener's granulomatosis. Gut. 1986; 27(4):450-451
- Akca T, Colak T, Caglikulekci M, Ocal K, Aydin S. Intestinal perforation in Wegener's granulomatosis: a case report. Ulus Travma Derg. 2005; 11 (4):348-351
- Watts RA, Lane SE, Bentham G, Scott DGI Epidemiology of systemic vasculitis -a 10-year study. -Arthritis Rheum 2000; 43: 4 22-427
- Fujimoto S, Watts R, Kobayashi S, et al. Comparison of the epidemiology of anti-neutrophil cytoplasmic antibodyassociated vasculitis between Japan and the UK. -Rheumatology 2011; 50:1916-1920
- Бекетова Т.В. АНЦА-ассоциированный системный васку-лит. Нефрология. Национальное руководство/гл.ред.Н.А.Мухин. -М.: ГЭОТАР-Медиа, 2014
- Hilhorst М. et al. Connective tissue growth factor and the cicatrization of cellular crescents in ANCA-associated glomerulonephritis. -NDT. Volume 30, Issue 8 Pp. 1291-1299
- Lionaki, S. et al. Classification of antineutrophil cytoplasmic autoantibody vasculitides: the role of antineutrophil cytoplasmic autoantibody specificity for myeloperoxidase or proteinase 3 in disease recognition and prognosis. -Arthritis Rheum. 64, 2012; 3452-3462
- Lyons, P. A. et al. Genetically distinct subsets within ANCA-associated vasculitis. N. -Engl. J. Med. 367, 214-223 (2012)
- Merkel P.A. et al. The OMERACT core set of outcome measures for use in clinical trials of ANCA-associated vasculitis. -J Rheumatol. 2011 Jul;38(7):1480-6 DOI: 10.3899/jrheum.110276
- Pagnoux C, Hogan S, Chin H, et al. Predictors of treatment resistance and relapse in antineutrophil cytoplasmic antibody-associated small-vessel vasculitis: Comparison of two independent cohorts. -Arthritis Rheum. 2008;58:2908-18 DOI: 10.1002/art.23800
- Pagnoux C, Mahr A, Cohen P, Guillevin L. Presentation and outcome of gastrointestinal involvement in systemic necrotizing vasculitides: analysis of 62 patients with polyarteritis nodosa, microscopic polyangiitis, Wegener granulomatosis, Churg-Strauss syndrome, or rheumatoid arthritis-associated vasculitis. Medicine (Baltimore) 2005; 84 (2):115-128
- Prz Gastroenterol. 2016; 11 (4): 270-275, 10.5114/pg.2016.57887
- Sahin M, Cure E, Goren I, et al. Wegener’s granulomatosis presenting with acute renal failure and gastric ulcer. Case Rep Clin Prac Rev. 2006; 7:236-9


