Точность неинвазивного измерения сердечного выброса на основе оценки времени транзита пульсовой волны при аортокоронарном шунтировании на работающем сердце
Автор: Смткин Алексей Анатольевич, Хуссейн А., Захаров В.И., Изотова Н.Н., Кузьков В.В., Киров М.Ю.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Анестезиология и реаниматология
Статья в выпуске: 2 т.20, 2016 года.
Бесплатный доступ
Цель. Оценка точности измерения сердечного выброса неинвазивной системой esCCO, основанной на определении времени транзита пульсовой волны, в сравнении с транспульмональной термодилюцией в периоперационном периоде аортокоронарного шунтирования без искусственного кровообращения. Материал и методы. В исследование включены 20 пациентов, которым выполняли плановое аортокоронарного шунтирования без искусственного кровообращения. На пяти последовательных интраоперационных и трех послеоперационных этапах одновременно определяли сердечный выброс на основе оценки времени транзита пульсовой волны и методом транспульмональной термодилюцией. Проведен анализ согласованности абсолютных значений сердечного выброса и способности отслеживать его динамику сердечного выброса. Результаты. Всего получено 153 пары данных сердечного выброса. По данным анализа Бланда - Альтмана, средняя интраоперационная разница между методами составила 1,2 л/мин с границами согласованности ± 2,9 л/ мин и процентной ошибкой 64%. Интраоперационный анализ полярной диаграммы показал повышенное значение угловой разницы (6,9 °) и радиальных границ согласованности (± 70,4 °) и сниженную полярную конкордантность (55%). В послеоперационном периоде согласованность между методами улучшилась со средней разницей 0,4 л/мин, границами согласованности ± 2,3 л/мин и процентной ошибкой 41%. Послеоперационная способность отслеживать динамику СВ также улучшилась (угловая разница 3,2º, угловые границы согласованности ± 39º, полярная конкордантность 81%). Выводы. Низкая точность и воспроизводимость измерения сердечного выброса неинвазивной системой esCCO и недостаточная способность технологии отслеживать динамику сердечного выброса во время аортокоронарного шунтирования без искусственного кровообращения не позволяют рекомендовать интраоперационное использование этого метода как альтернативу термодилюционным методикам. После операции система esCCO показала более высокую согласованность с термодилюционной методикой и улучшила способность отслеживать динамику сердечного выброса.
Сердечный выброс, гемодинамика, время транзита пульсовой волны, транспульмональная термодилюция
Короткий адрес: https://sciup.org/142140732
IDR: 142140732 | DOI: 10.21688-1681-3472-2016-2-104-110
Reliability of non-invasive cardiac output monitoring based on pulse wave transit time in off-pump coronary artery bypass grafting
Aim: The study was designed to evaluate the accuracy of cardiac output (CO) measurements based on pulse wave transit time (PWTT) as compared to transpulmonary thermodilution (TPTD) in perioperative off-pump coronary artery bypass grafting (OPCABG). Methods: 20 patients scheduled for elective OPCABG were enrolled for a prospective study. Parallel measurements of CO by using PWTT (COPWTT) and TPTD (COTPTD) were carried out at five stages intraoperatively and at three stages postoperatively. Also analyzed was the agreement between CO absolute values and its ability to monitor cardiac output dynamics. Results: All in all, 153 pairs of CO data were obtained. According to Bland-Altman analysis, the mean intraoperative difference between the methods was 1.2 L/min, with boundaries of agreement reaching ± 2.9 L/min and a percentage error amounting to 64%. The intraoperative analysis of a polar plot revealed an increased angular difference of 6.9° and radial boundaries of agreement of ± 70.4º, and a decreased polar concordance rate (55%). The postoperative analysis of the data showed better agreement between the methods: mean difference was 0.4 L/min with boundaries of agreement of ± 2.3 L/min and percentage error of 41%. The postoperative trending ability was also more accurate (angular difference of 3.2º, angular boundaries of agreement ± 39°, polar concordance rate 81%). Conclusion: Poor accuracy and reproducibility of non-invasive COPWTT and its insufficient trending ability to monitor cardiac output during off-pump coronary artery bypass grafting makes it impossible to recommend this technology to be used intraoperatively as an alternative to transpulmonary thermodilution technique. The calibration and trending ability of COPWTT improved after OPCAB.
Текст научной статьи Точность неинвазивного измерения сердечного выброса на основе оценки времени транзита пульсовой волны при аортокоронарном шунтировании на работающем сердце
В последнее десятилетие в медицинской практике значительно возрос интерес к малоинвазивным и неинвазивным лечебно-диагностическим методикам, в том числе в анестезиологии и интенсивной терапии [1, 2]. Такой подход позволяет минимизировать риск осложнений, связанных с потенциально опасными инвазивными процедурами. В то же время снижение инвазивности не должно отражаться на точности и своевременности оценки мониторируемых по-
Статья доступна по лицензии Creative Commons Attribution 4.0.
казателей, что также напрямую влияет на безопасность пациента и качество лечения.
Недавно в клинической практике стал доступным метод мониторинга сердечного выброса – estimated continuous cardiac output (esCCO), основанный на оценке времени транзита пульсовой волны (ВТПВ). Система esCCO определяет ВТПВ как временной интервал между моментом появления зубца R на электрокардиограмме (ЭКГ) и началом пульсовой волны на плетизмограмме пульсоксиметра. Измеренные ВТПВ, артериальное давление (инвазивное или неинвазивное) и частота сердечных сокращений могут быть использованы для расчета сердечного выброса (СВ) согласно следующей формуле [1]:
СВ = K X (а X ВТПВ + в) X ЧСС, где СВ – сердечный выброс; α – константа, которая была определена в предыдущих клинических исследованиях технологии esCCO; β – переменная, являющаяся производной пульсового давления; K – коэффициент калибровки, основанный на биометрических характеристиках пациента, включающих рост, вес, пол и возраст; ВТПВ – время транзита пульсовой волны; ЧСС – частота сердечных сокращений.
Доступная в настоящий момент версия системы esCCO имеет возможность первичной калибровки на основе биометрических данных пациента, снабжена автоматическим алгоритмом, анализирующим качество сигнала, и не требует дополнительной «внешней» калибровки, что в комбинации с измеряемым неинвазивно артериальным давлением (АД) позволяет проводить непрерывную оценку СВ полностью неинвазивно [2]. Однако клиническая эффективность этой системы требует проверки в различных гемодинамических условиях.
Целью исследования явилась оценка точности измерения СВ системой esCCO при ее калибровке на основе неинвазивно измеряемого артериального давления в сравнении с транспульмональной термодилюцией (ТПТД) у пациентов в периоперационном периоде аортокоронарного шунтирования без искусственного кровообращения (АКШ без ИК).
Материал и методы
Исследование проведено на базе Первой городской клинической больницы имени Е.Е. Волосевич и кафедры анестезиологии и реаниматологии Северного государственного медицинского университета г. Архангельска. В проспективном порядке с января по май 2014 года в исследование включили 20 пациентов с ишемической болезнью сердца (оценка по шкале ASA II – III класс), требующей хирургической реваскуляризации миокарда. Критерии исключения из исследования: возраст пациентов менее 18 и более 80 лет, предоперационная фракция выброса менее 35%, тяжелая дисфункция клапанов, существенное поражение периферических артерий, постоянная форма фибрилляции предсердий или другие значимые аритмии, необходимость использования двух лучевых артерий в качестве шунтов и проведение симультанных хирургических вмешательств (например, каротидная эндартерэктомия, коррекция аневризмы желудочка и др.).
В операционной всем пациентам начинали рутинный мониторинг гемодинамики, включавший неинвазивное измерение артериального давления (НИАД), ЭКГ с анализом сегмента ST и пульсоксиметрию (LifeScope BSM-6701K, Nihon Kohden Corporation, Токио, Япония).
Начальную калибровку системы esCCO проводили до индукции анестезии, используя ЭКГ, пульсоксиметрию, НИАД и биометрические характеристики пациента (возраст, пол, рост и вес). Повторная калибровка esCCO автоматически активировалась на каждом этапе исследования при повторных измерениях НИАД непосредственно перед началом термодилюционного измерения сердечного выброса.
С целью инвазивного мониторинга гемодинамики и оценки СВ методом транспульмональной термодилюции (СВТПТД) после индукции анестезии осуществлялась катетеризация внутренней яремной вены катетером 8,5F и бедренной артерии термодилюционным катетером 5F (Pulsiocath PV2015L20, Pulsion), который соединялся с монитором PiCCO2 (Pulsion Medical Systems, Германия). Термодилюционные измерения проводили путем троекратного ведения 15 мл холодного (<4 °C) 5%-го раствора глюкозы через центральный венозный катетер. Среднее значение трех измерений с вариациями менее 10% использовали для последующего анализа данных.
Регистрировали одновременно средний результат трех измерений СВТПТД и СВ на основе ВТПВ (СВВТПВ), значение которого записывали в момент окончания последнего из трех термодилюционных измерений. Параллельное измерение СВТПТД и СВВТПВ выполняли после индукции анестезии, после стернотомии, в момент стабилизации поверхности сердца, после восстановления кровотока по шунтам, в конце операции, через 2, 4 и 6 ч после операции. Для оценки влияния системного сосудистого сопротивления на точность и воспроизводимость измерения СВ с помощью технологии esCCO регистрировали индекс системного сосудистого сопротивления (ИССС), используя монитор PiCCO2.
Статистический анализ проводили, используя пакет программ SPSS (версия 14.0, SPSS Inc., Чикаго), MedCalc Software (версия 12.3, MedCalc Software bvba, Бельгия) и программного обеспечения SigmaPlot (версия 11.0, Systat Software, Inc., США). Характер распределения данных оценивали, используя тест Шапиро – Уилка. Данные представлены в виде среднего значения и среднеквадратичного отклонения или медианы и 25-го – 75-го процентилей.
Для оценки корреляции СВТПТД и СВВТПВ в зависимости от типа распределения данных вычисляли коэффици- енты корреляции r-Пирсона или rho-Спирмена. С целью определения согласованности СВТПТД и СВВТПВ для всех пар данных, взятых вместе, для интра- и послеоперационных пар данных и для каждого этапа в отдельности использовали анализ Бланда – Альтмана с оценкой средней разницы двух методов и границ согласованности (±1,96 среднеквадратичного отклонения средней разницы). Расчет процентной ошибки выполняли следующим образом: 1,96 х среднеквадратичное отклонение средней разницы методов / среднее значение сердечного выброса по данным двух методов х 100% [3]. Для оценки точности и воспроизводимости измерений esCCO в отношении разных диапазонов истинного значения СВ (по данным ТПТД) выполняли отдельный анализ Бланда – Альтмана для пар данных с СВТПТД ≥ 3,5 и < 3,5 л/мин.
Для оценки способности системы esCCO отслеживать тенденцию изменений СВ после вычисления разницы СВ ( Δ СВ) между двумя последовательными измерениями для каждого метода ( Δ СВВТПВ и Δ СВТПТД соответственно), путем вычитания значения на предшествующем этапе из значения на последующем, использовали полуполярную диаграмму [4]. Согласно рекомендации Critchley et al., из дальнейшего анализа исключили данные центральной зоны полярной диаграммы со значениями Δ CO <0,5 л/мин, представляющими «статистический шум» [4]. На основе данных полуполярной диаграммы рассчитывали угловую разницу, радиальные границы согласованности и полярную конкордантность. Способность отслеживать динамику СВ считалась приемлемой при условии, что угловая разница была в пределах ± 5 °, радиальные границы согласованности – в пределах ± 30 ° и полярная конкордантность при радиальной границе в 30 ° составляла 95% и выше [4]. Результаты тестов считали статистически значимыми при р <0,05.
Результаты
Основные характеристики пациентов (n = 20) представлены в виде средней ± среднеквадративного отклонения медианы (25-го – 75-го процентилей) или процентов.
|
Возраст (разброс), лет |
50–77 |
|
Пол (муж./жен.), % |
65/35 |
|
Рост, см |
165±10 |
|
Масса, кг |
82,1±2,1 |
|
Площадь поверхности тела, м2 |
1,92±0,27 |
|
Индекс массы тела, кг/м2 |
22±1 |
|
Предоперационная фракция изгнания |
0,56±0,11 |
|
Количество шунтов |
3 (3–4) |
а
б
Среднее СВ^, и СВТПТД (л/мин)
в
3- * + +1,96 СКО
X s+n * +°
О у _________________Среднее л Д °«
-1,96 СКО
._
2 4 6 8 1012
Среднее СВвтпв и СВТПТД (л/мин)
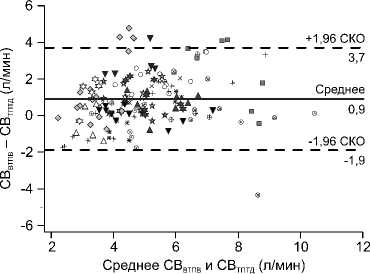
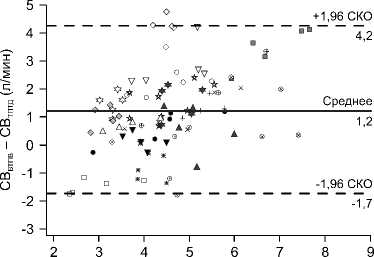
Рис. 1. Диаграмма Бланда – Альтмана: а – для всех включенных пар данных; б – для интраоперационных пар данных; в – для послеоперационных пар данных. Каждый маркер отображает отдельную пару данных, каждый тип маркера соответствует отдельному пациенту. Непрерывная горизонтальная линия показывает значение средней разницы между СВВТПВ и СВТПТД. Пунктирная линия показывает верхнюю и нижнюю 95%-ю границу согласованности. СВВТПВ – сердечный выброс, полученный на основе времени транзита пульсовой волны; СВТПТД – сердечный выброс, полученный на основе транспульмональной термодилюции; СКО – среднеквадратичное отклонение
Fig. 1. Bland-Altman plot: a – for all data pairs included; б – for intraoperative data pairs; в – for postoperative data pairs. Each marker presents an individual data pair; each marker type corresponds to an individual patient. A solid horizontal line shows the value of mean difference between COPWTT and COTPTD. A dotted line demonstrates an upper and lower 95 % boundary of agreement. COPWTT is cardiac output based on pulse wave transit time; COTPTD is cardiac output based on transpulmonary thermodilution; CKO is mean root square deviation
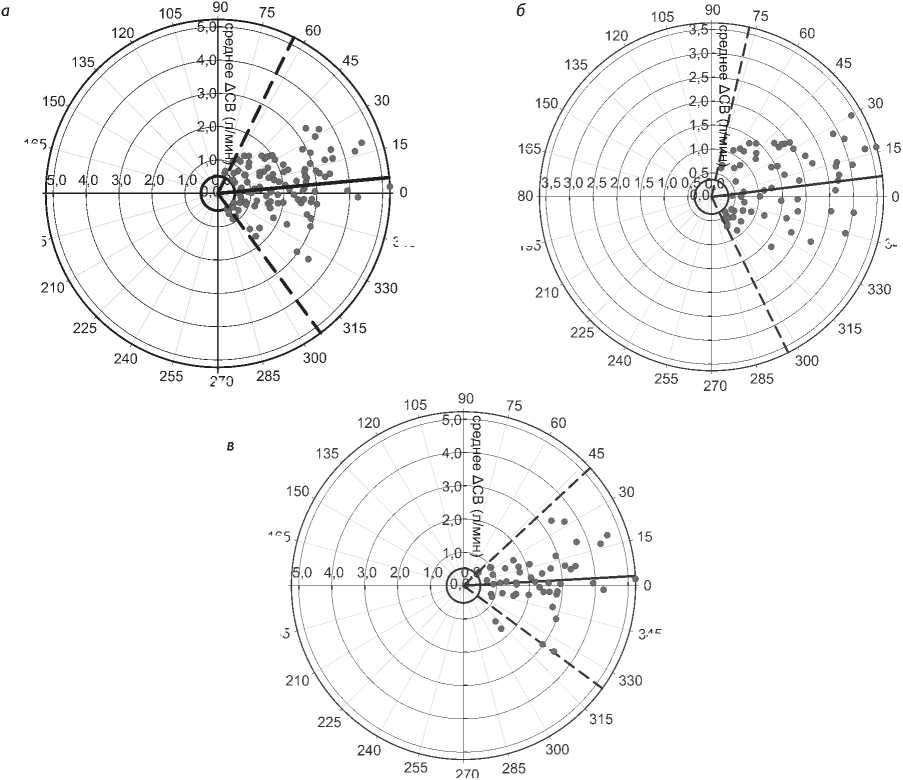
Рис. 2. Полярная диаграмма: а – для всех включенных пар данных; б – для интраоперационных пар данных; в – для послеоперационных пар данных. Расстояние от центра диаграммы отражает среднее изменение сердечного выброса, а угол отображает согласованность методов. Утолщенное кольцо в центре отражает центральную зону исключения (среднее Δ СВ <0,5 л/мин). Толстая линия отображает средний полярный угол (угловую разницу), а пунктирная линия показывает радиальные границы согласованности. Δ СВ – изменение сердечного выброса
Fig. 2. Polar plot: a – for all data pairs included; б – for intraoperative data pairs; в – for postoperative data pairs. A distance from the plot center is a mean cardiac output deviation, while an angle shows the agreement of methods. A thickened ring in the center means the central zone of exclusion (average Δ CO <0.5 L/min). A thick line represents an average polar angle (angle difference) and a dotted line demonstrates radial boundaries of agreement. Δ СВ is a change of cardiac output
Интраоперационно четырем пациентам потребовалась вазопрессорная поддержка э федрином в максимальной дозе 5 мг на этапе фиксации поверхности сердца или восстановления кровотока по шунтам.
Всего в исследовании получено 153 пары данных СВ. Результаты СВВТПВ получены в 95,6% измерений. В семи случаях возникли трудности в определении СВ методикой esCCO в связи с эпизодами аритмий или низким качеством сигнала ЭКГ или пульсоксиметрии. При суммарном анализе всех этапов выявили умеренно выраженную корреляцию СВТПТД и СВВТПВ (rho = 0,63, р <0,01). Для всех включенных пар данных средняя разница между неинвазивным СВВТПВ и СВТПТД составила 0,9 л/мин с границами согласованности ± 2,8 л/мин и процентной ошибкой 57% (рис. 1, а). В табл. 2 представлены корреляции, результаты анализа Бланда – Альтмана и процентные ошибки двух методов оценки СВ на разных этапах исследования. Выявлена значительная корреляция между неинвазивным СВВТПВ и СВТПТД после стернотомии, на момент восстановления кровотока по шунтам и на всех этапах послеоперационного периода с завышением СВВТПВ в сравнении с СВТПТД на всех этапах исследования и процентной ошибкой в пределах 32–71%.
В процессе исследования значения ИССС варьировали в пределах 2 180-2 800 дин х с х см-5 х м-2. Вместе с тем вариации средних различий СВ двух методов на этапах исследования и вариации процентных ошибок не коррелировали со значением ИССС.
Изолированный анализ интра- и послеоперационных пар данных выявил, что интраоперационно среднее различие между неинвазивным СВВТПВ и СВТПТД составило 1,2 л/мин с границами согласованности ± 2,9 л/мин и процентной ошибкой 64% (рис. 1, б ). Между тем в послеоперационном периоде среднее различие СВ между методами составило 0,4 л/мин с границами согласованности ± 2,3 л/мин и процентной ошибкой 41% (рис. 1, в ).
Анализ пар данных с нормальными и низкими референтными значениями СВ (СВТПТД ≥ 3,5 л/мин и СВТПТД<3,5 л/мин соответственно) выявил, что при нормальном референтном значении СВ среднее различие между методами составило 0,7 л/мин с границами согласованности ± 2,7 л/мин и процентной ошибкой 48%. При низком референтном значении СВ среднее различие между методами возрастало до 1,3 л/мин с границами согласованности ± 3,2 л/мин и процентной ошибкой 89%.
На рис. 2, а представлена полуполярная диаграмма для всех включенных в исследование пар данных. Угловая разница составила 5,2 ° с радиальными границами согласованности ± 58,6 °. При радиальной границе 30 ° полярная конкордант-ность составила 69%. Дискретный анализ интра- и послеоперационных этапов выявил низкую интраоперационную способность отслеживать динамику СВ с угловой разницей 6,9 °, радиальными границами согласованности ± 70,4 ° и полярной конкордантностью 55% (рис. 2, б ). В послеоперационном периоде способность отслеживать тенденции изменений СВ улучшилась, о чем свидетельствуют угловая разница 3,2 °, радиальные границы согласованности ± 39 ° и полярная конкор-дантность 81% (рис. 2, в ).
При оценке точности неинвазивного измерения АД анализ Бланда – Альтмана показал, что, в сравнении с инвазивным измерением АД, неинвазивная методика занижает пульсовое давление в среднем на 9,5 мм рт. ст. с границами согласованности ± 21,8 мм рт. ст. и процентной ошибкой 44%.
Обсуждение
В периоперационном периоде АКШ без ИК неинвазивная методика оценки сердечного выброса, основанная на определении ВТПВ, демонстрирует недостаточную согласован- ность и способность отслеживать тенденцию изменений сердечного выброса в сравнении с ТПТД.
В настоящий момент в клинической практике применяют ряд мониторных систем измерения СВ, использующих малоинвазивные или полностью неинвазивные технологии. Такие устройства позволяют повысить безопасность пациента прежде всего за счет уменьшения осложнений со стороны потенциально опасных инвазивных процедур. Однако уменьшение инвазивности часто приводит к увеличению погрешности измерений [5]. Это в свою очередь ограничивает использование неинвазивных систем у нестабильных пациентов, для которых точность мониторинга один из ключевых моментов успешной терапии.
В основе технологии esCCO лежит идея о зависимости скорости распространения пульсовой волны от величины ударного объема и сердечного выброса. Производное скорости распространения пульсовой волны – ВТПВ определяется как временной интервал между появлением зубца R на ЭКГ и началом роста пульсовой волны на плетизмограмме пульсоксиметра [6]. Алгоритм, используемый в системе esCCO, основан на допущении, что ударный объем пропорционален пульсовому давлению и податливости сосудистой стенки, определяемой биометрическими характеристиками пациента (полом, возрастом, весом, ростом) и ВТПВ [6].
Анализ Бланда – Альтмана всех полученных пар данных показал, что система esCCO в неинвазивном варианте умеренно завышает СВ со средней разницей 0,9 л/мин и процентной ошибкой 57%, что значительно превышает клинически приемлемые пределы (см. рис. 1, а ). Также наблюдалось завышение СВ на каждом этапе исследования с процентной ошибкой в пределах 32–71% (табл. 2). В других исследованиях по оценке точности неинвазивной системы esCCO получены сходные результаты со средней разницей от 0,13 до 1,6 л/мин и процентной ошибкой 49–80% в зависимости от референтного метода измерения СВ [7–9]. Низкую согласованность методов можно объяснить рядом факторов. ВТПВ обратно пропорционально ударному объему, поэтому система esCCO может умеренно завышать значение СВ из-за ошибочной недооценки истинного ВТПВ, особенно в фазу изометрического сокращения, определяя этот период от момента появления зубца R на ЭКГ до открытия аортального клапана. Так, Sugo и соавторы, оценивая СВ с помощью эхокардиографии, продемонстрировали, что вариации продолжительности фазы, предшествующей изгнанию, составляют примерно половину от ВТПВ [10]. Несмотря на более сложную идентификацию зубца Q на ЭКГ, сдвиг стартовой точки от зубца R к зубцу Q, возможно, позволит повысить точность технологии esCCO.
Сосудистое сопротивление также может влиять на точность малоинвазивных методик [11]. Ранее проведенные исследования показали умеренное воздействие сосудистого сопротивления на точность технологии esCCO [7, 12]. В этом исследовании вариация ИССС составила 22%. Однако это не повлияло на согласованность методов оценки сердечного выброса.
Отдельный анализ интра- и послеоперационных пар данных выявил, что после операции система esCCO показала меньшую процентную ошибку в сравнении с интраоперационными данными (рис. 1, б , в ). Эти различия можно объяснить более стабильной гемодинамикой в послеоперационном периоде. Кроме того, отдельный анализ пар данных с нормальным ( ≥ 3,5 л/мин) и низким СВТПТД выявил значительно более высокую процентную ошибку (89%) системы esCCO при низком значении референтного показателя СВ в сравнении с 48% в подгруппе с нормальным СВТПТД. Высокую процентную ошибку выявили и среди пациентов с низким СВ при оценке других малоинвазивных методов измерения сердечного выброса [13, 14].
Другим возможным источником ошибки может быть определение АД неинвазивным методом. Ранее проведенные исследования показали, что осциллометрическое измерение АД недооценивает истинное значение, измеренное инвазивным методом, при этом в наибольшей степени занижается значение систолического АД [15]. В этом исследовании неинвазивное измерение АД с помощью плечевой манжеты приводило к недооценке измеренного инвазивным путем пульсового давления со средней разницей –9,5 мм рт. ст. и процентной ошибкой 44%.
Способность новых систем мониторинга отслеживать динамику СВ может рассматриваться как альтернатива измерению абсолютных значений СВ. Тем не менее неинвазивный вариант системы esCCO продемонстрировал недостаточную способность отслеживать изменения СВ в сравнении с методом ТПТД, что выразилось в угловой разнице 5,2 ° и полярной конкордантности 69% (рис. 2, а ). Важно отметить, что в послеоперационном периоде при более стабильной гемодинамике система esCCO эффективнее отслеживала тенденции изменений СВ, с более точной калибровкой исследуемых методов относительно друг друга и более высокой полярной конкордантностью, в сравнении с интраоперационным периодом (рис. 2, б , в ). Ранее выполненные исследования также показали недостаточную способность системы esCCO отслеживать динамику СВ [2, 7]. Вероятно, это связано с низкой чувствительностью и нелинейностью изменений пульсового давления в ответ на изменение объема циркулирующей крови.
Исследование имеет ряд ограничений. Во-первых, в качестве референтного мы использовали метод термодилюции, наиболее широко применяемый, но не обладающий абсолютной точностью. Кроме того, проводили исследование пациентов в условиях АКШ без ИК, для которых характерны относительно ограниченные изменения сердечного выброса. В связи с этим необходимы дальнейшие исследования для оценки эффективности технологии esCCO у различных групп пациентов и в различных гемодинамических условиях.
Заключение
Низкая точность и воспроизводимость измерения сердечного выброса на основе оценки времени транзита пульсовой волны и недостаточная способность отслеживать динамику сердечного выброса во время АКШ на работающем сердце не позволяют рекомендовать интраоперационное использование данного метода в качестве альтернативы термодилюционным методикам. В то же время в послеоперационном периоде система esCCO продемонстрировала более высокую согласованность с термодилюционной методикой и улучшенную способность отслеживать динамику сердечного выброса. Учитывая, что система esCCO умеренно завышает истинное значение сердечного выброса, низкий показатель сердечного выброса по данным esCCO следует рассматривать как сигнал для дальнейших диагностических мероприятий.
Финансирование
Исследование получило частичную грантовую поддержку от компании Nihon Kohden.
Список литературы Точность неинвазивного измерения сердечного выброса на основе оценки времени транзита пульсовой волны при аортокоронарном шунтировании на работающем сердце
- Gosling R.G., Budge М.М. Terminology for describing the elastic behavior of arteries//Hypertension. 2003. Vol. 41 (6). P. 1180-2.
- Ishihara H., Sugo Y., Tsutsui M., Yamada T., Sato T., Akazawa T., Sato N., Yamashita K., Takeda J. The ability of a new continuous cardiac output monitor to measure trends in cardiac output following implementation of a patient information calibration and an automated exclusion algorithm//J. Clin. Monit. Comput. 2012. Vol. 26 (6). P. 465-71 DOI: 10.1007/s10877-012-9384-7
- Critchley L.A., Critchley J.A. A meta-analysis of studies using bias and precision statistics to compare cardiac output measurement techniques//J. Clin. Monit. Comput. 1999. Vol. 15 (2). P. 85-91.
- Critchley L.A., Yang X.X., Lee A. Assessment of trending ability of cardiac output monitors by polar plot methodology//J. Cardiothorac. Vasc. Anesth. 2011. Vol. 25 (3). P. 536-46 DOI: 10.1053/j.jvca.2011.01.003
- Peyton P.J., Chong S.W. Minimally invasive measurement of cardiac output during surgery and critical care: a meta-analysis of accuracy and precision//Anesthesiology. 2010. Vol. 113 (5). P. 1220-35 DOI: 10.1097/ALN.0b013e3181ee3130
- Sharwood-Smith G., Bruce J., Drummond G. Assessment of pulse transit time to indicate cardiovascular changes during obstetric spinal anaesthesia//Br. J. Anaesth. 2006. Vol. 96 (1). P. 100-5.
- Bataille B., Bertuit M., Mora M., Mazerolles M., Cocquet P., Masson B., Moussot P.E., Ginot J., Silva S., Larché J. Comparison of esCCO and transthoracic echocardiography for non-invasive measurement of cardiac output intensive care//Br. J. Anaesth. 2012. Vol. 109 (6). P. 879-86 DOI: 10.1093/bja/aes298
- Sinha A.C., Singh P.M., Grewal N., Aman M., Dubowitz G. Comparison between continuous non-invasive estimated cardiac output by pulse wave transit time and thermodilution method//Ann. Card. Anaesth. 2014. Vol. 17 (4). P. 273-7 DOI: 10.4103/0971-9784.142059
- Fischer M.O., Balaire X., Le Mauff de Kergal C., Boisselier C., Gérard J.L., Hanouz J.L., Fellahi J.L. The diagnostic accuracy of estimated continuous cardiac output compared with transthoracic echocardiography//Can. J. Anaesth. 2014. Vol. 61 (1). P. 19-26 DOI: 10.1007/s12630-013-0055-z
- Sugo Y., Sakai T., Terao M., Ukawa T., Ochiai R. The comparison of a novel continuous cardiac output monitor based on pulse wave transit time and echo Doppler during exercise//Conf. Proc. IEEE. Eng. Med. Biol. Soc. 2012. Vol. 2012. P. 236-9. DOI: 10.1109/EMBC.2012.6345913.
- Biancofiore G., Critchley L.A., Lee A., Bindi L., Bisà M., Esposito M., Meacci L., Mozzo R., DeSimone P., Urbani L., Filipponi F. Evaluation of an uncalibrated arterial pulse contour cardiac output monitoring system in cirrhotic patients undergoing liver surgery//Br. J. Anaesth. 2009. Vol. 102 (1). P. 47-54 DOI: 10.1093/bja/aen343
- Ishihara H., Tsutsui M. Impact of changes in systemic vascular resistance on a novel non-invasive continuous cardiac output measurement system based on pulse wave transit time: a report of two cases//J. Clin. Monit. Comput. 2014. Vol. 28 (4). P. 423-7 DOI: 10.1007/s10877-013-9529-3
- Maeda T., Yoshitani K., Inatomi Y., Ohnishi Y. Inaccuracy of the FloTrac/Vigileo™ system in patients with low cardiac index//J. Cardiothorac. Vasc. Anesth. 2014. Vol. 28 (6). P. 1521-6 DOI: 10.1053/j.jvca.2014.04.013
- Mayer J., Boldt J., Schöllhorn T., Röhm K.D., Mengistu A.M., Suttner S. Semi-invasive monitoring of cardiac output by a new device using arterial pressure waveform analysis: a comparison with intermittent pulmonary artery thermodilution in patients undergoing cardiac surgery//Br. J. Anaesth. 2007. Vol. 98 (2). P. 176-82.
- Ribezzo S., Spina E., Di Bartolomeo S., Sanson G. Noninvasive techniques for blood pressure measurement are not a reliable alternative to direct measurement: a randomized crossover trial in ICU//Scientific. World. Journal. 2014. Vol. 2014. P. 353628 DOI: 10.1155/2014/353628


