Топографическое распределение и возможная роль про- и антивоспалительных субпопуляций макрофагов в разных типах атеросклеротических поражений
Автор: Шишкина Валентина Сергеевна, Ильинская Ольга Петровна, Челомбитько Мария Александровна, Васильева Тамара Викторовна, Федоров Артем Валерьевич, Тарарак Эдуард Михайлович
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.22, 2014 года.
Бесплатный доступ
Проведен анализ распределения и возможной роли субпопуляций макрофагов (Мф) про- (М1) и антивоспалительного (М2) фенотипа в развитии атеросклеротического поражения. Морфогистологическую оценку типов поражений проводили согласно классификации ВОЗ. В каждом образце с помощью иммуногистохимического окрашивания выявляли Мф М1 (MCP1+ - клетки) и М2 (CD206+ и CD163+ - клетки). Показали, что во всех типах поражений присутствуют обе субпопуляции Мф, численное соотношение между которыми может существенно меняться в разных областях и типах бляшек. Субпопуляция Мф М1 численно преобладает в областях инфильтрации клетками воспаления и активного поглощения липидов, а М2 - в зонах репарации межклеточного матрикса и ангиогенеза. Проведена количественная оценка распределения обеих субпопуляций в клинически наиболее значимых областях поражений, предрасположенных к разрыву - фиброзных покрышках (адлюминальные фиброзные слои) и плечах. Достоверной разницы по содержанию Мф М1 и М2 в плечах выявлено не было. В фиброзных покрышках атером, фиброатером и осложненных поражений по сравнению с фиброзными и фиброкальцинозными обнаружена достоверно более интенсивная инфильтрация Мф обеих субпопуляций. Сделано заключение, что баланс сил между про- и антивоспалительной субпопуляциями Мф существенно влияет на процессы формирования атеросклеротического поражения и развитие осложнений при атеросклерозе.
Атеросклероз, сонные артерии, про- и антивоспалительные субпопуляции макрофагов
Короткий адрес: https://sciup.org/143177005
IDR: 143177005
Distribution and possible role of pro- and anti-inflammation macrophage subpopulations in different types of carotid atherosclerotic plaques
The analysis of the distribution and the possible role of macrophage subpopulations of (Mf) pro-(M1) and anti-inflammatory (M2) phenotype in the development of atherosclerotic lesions was conducted. Morphohistological assessment of the lesions types was performed according to the WHO classification. In each sample Mf M1 (MCP1 + - cells) and M2 (CD206+ and CD163+ - cells) were detected by immunohistochemical staining. The analysis revealed that in all types of lesions both subpopulations of Mf are present, and the numerical ratio between them can vary significantly in different areas and types of the plaques. Subpopulation Mf M1 mainly concentrates in areas of infiltration by inflammatory cells and active absorption of lipids, and M2 - in the areas of reparation of the intercellular matrix and angiogenesis. Quantitative evaluation of the distribution of both subpopulations in clinically more significant areas of plaques most prone to rupture or thrombosis - in the fibrous caps (adluminal fibrous layers) and shoulders...
Текст научной статьи Топографическое распределение и возможная роль про- и антивоспалительных субпопуляций макрофагов в разных типах атеросклеротических поражений
Введение. В последние годы сформировалось представление о том, что макрофаги (Мф) в зависимости от получаемых ими сигналов могут изменять свой фенотип, проявляя как про-, так и антивоспалительную активность. In vitro провоспа-лительные Мф (М1) развиваются в ответ на стимуляцию IFNγ, TNFα и LPS, что повышает секрецию ими различных провоспалительных цитокинов, в основном IL-12 и MCP1 и ведет к снижению ими секреции IL-10. Деятельность таких клеток обеспечивает Tх1-зависимый иммунный ответ и она направлена, в основном, на стимуляцию процесса воспаления [1, 2, 3]. Напротив, антивоспалитель-ные Мф (М2) развиваются в ответ на действие IL-4, IL-13, IL-10, TGF-b, стимулируя их к высокой продукции антивоспалительных цитокинов, в основном IL-10 и угнетению секреции IL-12, тем самым способствуя подавлению воспалительной реакции и восстановлению ткани [1, 2, 3]. Кроме того, in vivo Мф М2 стимулируют ангиогенез и усиливают перестройку и репарацию ткани путём синтеза факторов, стимулирующих пролиферацию гладкомышечных клеток и фибробластов, а также синтез ими соединительнотканного матрикса [4].
Известно, что морфологическая основа атеросклеротических поражений, развивающихся в интиме артерий человека - это результат сложного взаимодействия различных типов клеток, как пришедших из кровеносного русла (моноцитов (Мц), Мф, лимфоцитов и др.), так и стромального компонента сосудистой стенки (эндотелия, гладкомышечных клеток и др.). Проникновение в субэндотелиальное пространство Мц периферической крови, их последующая макрофагальная дифференцировка и активация в интиме – это ключевые моменты развития атеросклеротических бляшек (АСБ) [5]. По данным последних исследований в АСБ присутствуют как про-, так и антивоспалительные Мф. Эти супопуляции Мф были выявлены в различных эндартерэктоми-рованных образцах артерий человека, а также в бляшках аорт атеросклеротических моделей мышей [3, 6, 7, 8, 9]. Однако, роль этих субпопуляций в процессе формирования, прогрессии и дестабилизации атеросклеротического поражения до сих пор остается мало изученной.
Цель исследования – изучение распределения про- и антивоспалительных субпопуляций Мф М1 и М2 в различных областях и типах атеросклеротических поражений внутренних сонных артерий человека и их возможной роли в формировании и дестабилизации АСБ.
Материалы и методы исследования. Материалом исследования служили пораженные атеросклерозом участки внутренних сонных артерий человека, изъятые в ходе операций каротидной эндартерэктомии в отделении неотложной сосудистой хирургии института скорой помощи им. Н.В.Склифосовского. Исследовано 16 таких образцов от 10 мужчин (средний возраст 59 ± 6 года) и 6 женщин (средний возраст 73 ± 5 года) с верифицированным гемодинамически значимым каротидным стенозом (степень стеноза 69 ± 14%). Биоптаты, состоявшие из интимы и медии, содержали 27 АСБ удлиненной формы с участками поражений разных типов от липидного пятна/ полосы до осложненного поражения, которые разрезали поперек на фрагменты шириной 5 – 7 мм (n = 66) и замораживали в парах жидкого азота. Для морфологического и иммуногистохимического анализа готовили криосрезы, часть из которых после фиксации в смеси метанол: хлороформ: ледяная уксусная кислота (6:3:1) окрашивали для общеморфологической оценки типов поражений гематоксилин-эозином, по Ван-Гизону и масляным красным О. Типы атеросклеротических поражений классифицировали по Г. Стари [10].
Другую часть криосрезов использовали для иммуногистохимического выявления различных антигенов с помощью непрямого пероксидазного метода с использованием авидин-биотинового комплекса. Для идентификации типов клеток использовали мышиные моноклональные антитела в разведении 1:100 (DAKO, Дания) против специфических клеточных маркеров: CD14 (Мц), HAM56 (Мф человека), vWF (эндотелиальные клетки), CD3 (Т-лимфоциты – Т-Лц) и SM-aktin (гладкомышечные клетки). Субпопуляции Мф выявляли согласно принятой на сегодняшний день схеме, используя мышиные моноклональные антитела в разведении 1:100 (BD, Франция): против маркера провоспали-тельных Мф – MCP-1 (моноцит-хемотаксический фактор 1) и против двух маркеров антивоспа-лительных Мф – СD206 (маннозный рецептор) и CD163 (гемоглобиновый – гаптоглобиновый рецептор – маркер регуляторных М2) [6, 11]. Криосрезы атеросклеротических поражений после инкубации с первыми антителами фиксировали 10% забуференным формалином (Биовитрум, Россия), обрабатывали 3% перекисью водорода для ингибирования эндогенной пероксидазы и инкубировали с биотинилированными козьими поликлональными антителами к мышиным IgG в разведении 1:200 (Vector, США). Последующее выявление мест связывания антител с антигенами проводили с помощью коньюгата авидина D с пероксидазой хрена (Vector, США), а визуализацию – с помощью стандартного набора на основе диаминобензидина (Vector, США).
Измерение и подсчет различных морфометрических параметров проводили на цифровых микрофотоснимках гистологических срезов в программе ImageJ. В первой части исследования анализировали топографию распределения Мф М1 и М2 на срезах в неизмененной интиме сосуда и при различной степени прогрессии атеросклеротического поражения. Во второй части работы была проведена количественная оценка распределения Т-Лц, Мц, Мф М1 и М2 в участках АСБ наиболее предрасположенных к разрыву и тромбозу – в покрышке и плечах. При этом проводили подсчет числа клеток каждого типа, приходящихся на общую площадь участка среза в 1мм2.
Рис. 1. Поперечные гистологические срезы внутренней сонной артерии. А – фрагмент неизмененной интимы, окраска по Ван-Гизону, ядра окрашены гематоксилином; Б – фрагмент липидной полосы, липиды окрашены масляным красным О, ядра – гематоксилином; рамки ограничивают области, представленные далее (В, Г, соответственно). В, Г – распределение Мц и Мф М1 и М2 на последовательных срезах тех же фрагментов неизмененной интимы и начального атеросклеротического поражения – липидного пятна. Иммунопероксидазный (АВС-kit) метод окрашивания с помощью моноклональных антител против специфических клеточных маркеров: В-а, Г-а – CD14 (Мц); В-б, Г-б – HAM56 (Мф человека); В-в, Г-в – MCP1 (Мф М1); В-г, Г-г – CD206 (Мф М2). Клетки, содержащие перечисленные антигены, имеют коричневое окрашивание. Буквенные обозначения: И – интима, М – медия, Пс – просвет сосуда. А, Б, В, Г. Ув. 200.
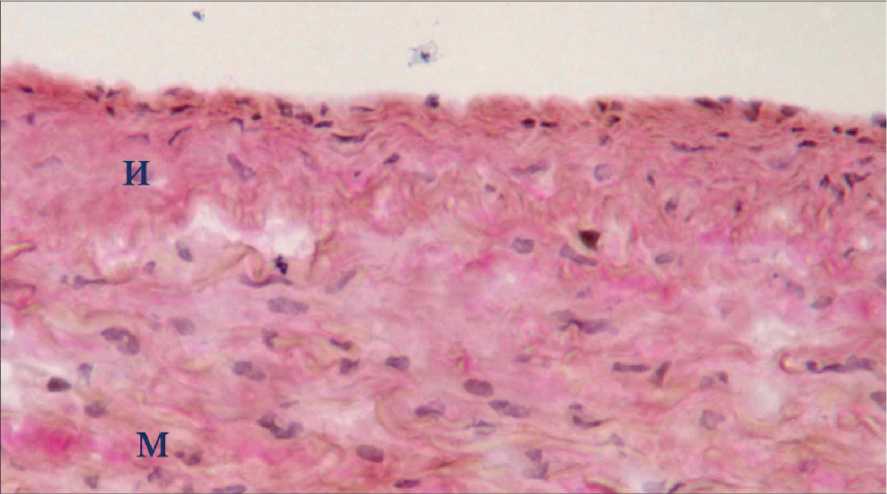
Рис. 1А.
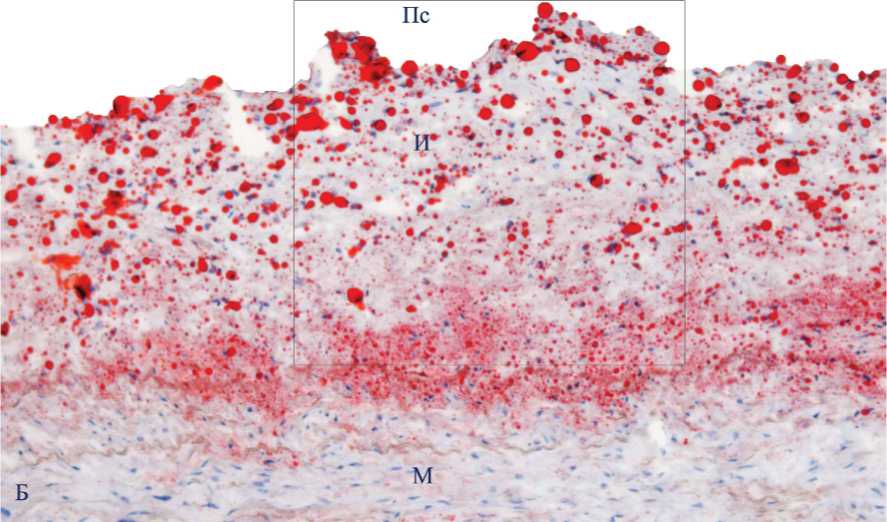
Рис. 1Б.
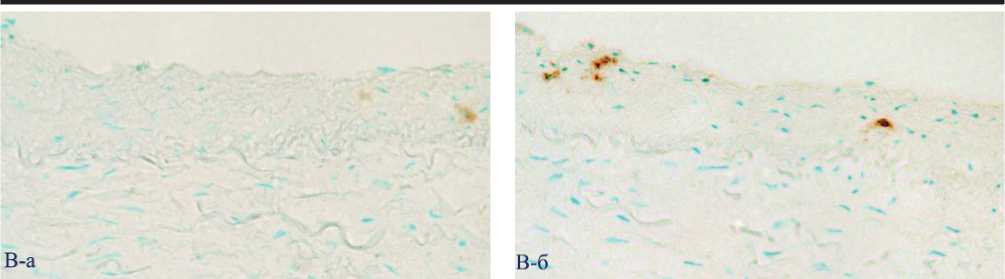
Рис. 1В-а.
Рис. 1В-б.

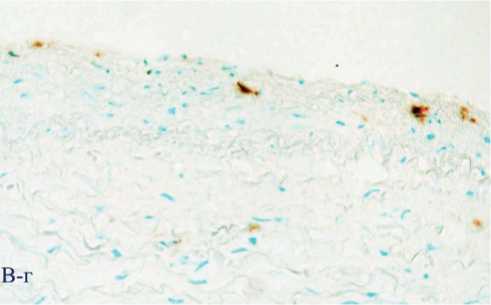
Рис. 1В-г.
Рис. 1В-в.
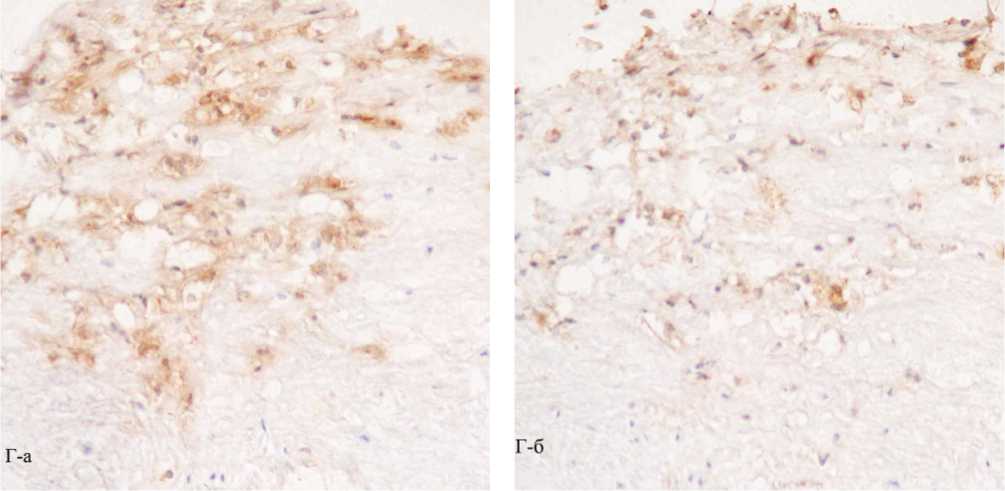
Рис. 1Г-а. Рис. 1Г-б.
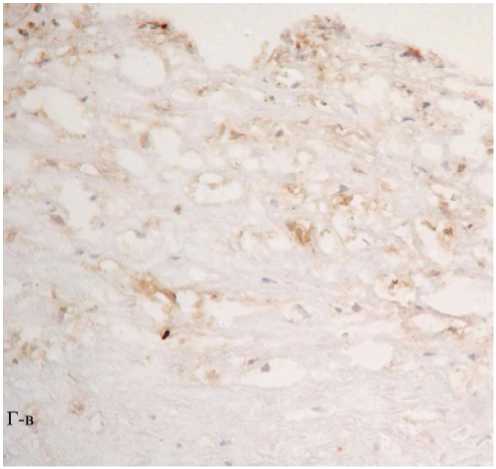
Рис. 1Г-в.
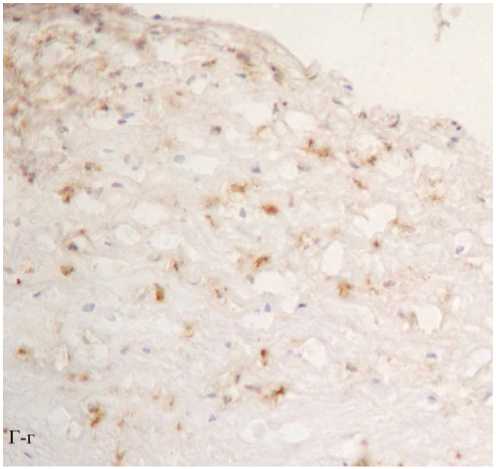
Рис. 1Г-г.
Статистическую обработку полученных цифровых значений проводили с помощью программы STATISTICA 7.0, используя двусторонний непараметрический критерий Манна-Уитни при статистической достоверности р <0,05.
Результаты исследования и их обсуждение. Гистологический анализ операционного материала позволил выявить следующие типы атеросклеротических поражений внутренних сонных артерий, которые были в дальнейшем подвергнуты иммуногистохимическому исследованию: липидные пятна/полоски – 4, атеромы – 3, фиброатеромы – 13, фиброзные поражения – 22, фиброкальцинозные – 7, осложненные – 13. Всего было исследовано 66 отдельных фрагмента сосудов, в том числе 4 участка неизмененной интимы.
После иммуногистохимического окрашивания срезов сонных артерий был проведен сравнительный анализ топографического распределения про- и антивоспалительных Мф в нормальной интиме и указанных выше типах атеросклеротических поражений. В неизмененной интиме были обнаружены лишь единичные Мц/ Мф, представленные CD14+, HAM56+ и CD206+-клетками, соответственно (рис. 1А, и В (а – г)). В липидных пятнах/полосах интима была значительно инфильтрирована Мц и Мф (рис. 1Б и Г (а - г)), имеющими как про- (MCP1+-клетки), так и антивоспалительный иммунофенотип (CD206+ и CD163+-клетки). При этом достоверного различия по количеству М1 и М2 Мф в липидной полосе выявлено не было (табл . 1).
Полученные нами данные согласуются с результатами ранее опубликованных работ. Показано, что в неизмененной артериальной стенке всегда присутствуют резидентные Мф, выполняющие гомеостатические функции, а в случае воспаления первыми реагирующие на изменившиеся условия. Проникновение в интиму модифицированных липопротеидов (модЛП) стимулирует местную воспалительную реакцию с интенсивной инфильтрацией Т-Лц и Мц и является начальной стадией развития поражения (липидное пятно/полоса) [5]. При этом в сосудах происходит поляризация активации Т-Лц и Мф по про- или антивоспалительному пути [12]. Нами было обнаружено, что в липидном пятне/полосе присутствуют Мф М1 и М2, что указывает на существенную роль обеих субпопуляций в развитии этой стадии поражения. Этот факт подтверждают экспериментальные данные других исследователей, показавших в условиях in vitro, что Мф М1 необходимы для активного фагоцитоза модЛП и стимуляции воспалительной реакции [3], а Мф М2 – для клиренса апоптотических клеток и секреции цитокинов и ферментов, участвующих в реорганизации матрикса и стимулирующих фиброз [12, 13]. В нашем исследовании в липидном пятне/полосе CD206+ и CD163+ Мф М2 были представлены в равных долях. А суммарное количество Мф М2 в липидном пятне/полосе по сравнению с Мф М1 (MCP1+- клетки) было в 2,3 раза больше (табл. 1). Следует отметить, что эти данные отличаются от тех, что получены в модели атеросклероза у мышей, у которых ранние липидные бляшки в стенке аорты были инфильтрированы только Мф М2 [8].
Таблица 1.
Распределение субпопуляций Мф М1 и М2 в липидных пятнах/полосках (M ± m).
|
Макрофаги |
М1 |
М2 |
P |
||
|
Маркер |
(1) MCP1 |
(2) CD206 |
(3) CD163 |
p1-2 |
p1-3 |
|
Количество маркированных клеток/мм2 ткани |
|||||
|
Липидное пят-но/полоса |
117,8 ± 30,5 |
155,3 ± 39,4 |
115,6 ± 28,1 |
р> 0,05 |
р> 0,05 |
Примечание: MCP1 – моноцитарный хемотаксический белок (маркер М1 Мф); CD206 – маннозный рецептор (маркер М2 Мф) и CD163 – рецептор к гемоглобину – гаптоглобину (маркер М2 регуляторных Мф).
Анализ результатов иммуногистохимического исследования последовательных срезов атеросклеротических поражений и их сопоставление с данными, полученными при окраске на липиды, показал, что про- и антивоспалительные Мф существенно отличаются по содержанию липидных включений и локализации внутри поражений. Подавляющее большинство пенистых клеток с липидными включениями несли маркер Мф НАМ56 (рис. 2. А, Б). При этом Мф М1 (MCP1+ – клетки) содержали значительные включения липидов (рис. 2 А, В) и были расположены в основном в типичных местах скопления пенистых клеток: в плечах бляшек, внутри липидных ядер, над ними или по их периферии, в то время как Мф М2 (CD206+– и CD163+– клетки) содержали незначительные липидные включения (рис. 2 А, Г и Д) и находились в наиболее стабильных областях поражений: фиброзных покрышках и/или в участках с высоким содержанием межклеточного матрикса. Можно отметить, что большинство Мф М1 (MCP1+ – клеток) солокализовались с HAM56+Мф (рис. 2 Б, В), а обе функциональные подгруппы Мф М2 (CD206+– и CD163+– клетки) – как с HAM56+ Мф (рис. 2 Б, Г, Д), так и с CD14+ Мц. Описанные результаты согласуются с данными, полученными группой исследователей ранее. Так была продемонстрирована солокализация MCP1+– и пенистых клеток [6], а также описано, что Мф M2 (CD68+CD206+– клетки) располагаются дальше от липидного ядра, чем Мф М1 (CD68+CD206-– клетки), и более слабо поглощают липиды [11].
Различия в локализации М1 и М2 субпопуляций Мф можно объяснить специфическими особенностями их функциональной активности, которая исследована в экспериментах in vitro [12]. В частности показано, что Мф М1 активно фагоцитирует окисленные ЛНП и секретирует ряд металлопротеаз (MMP1, 3 и 9) и провоспалитель-ных цитокинов (IL-1β, 6, 8, 12 и TNF-α), вследствие чего, по мнению ряда авторов, могут участвовать в формировании атеро-некротического ядра [2,
-
14, 15]. Эти факты вполне согласуются с тем, что в нашем исследовании Мф М1 мы обнаружили в основном вокруг атеронекротического ядра и других местах скопления липидов. Что касается Мф М2, то для них характерно участие в клиренсе апоптотирующих клеток, а также синтез антивоспалительных (IL-4, 10, 13; CCL18, 22, 24) и других факторов, в частности TGF-β, стимулирующих гладкомышечные клетки к пролиферации и синтезу внеклеточного матрикса, что способствует образованию фиброзной ткани [12]. Эти наблюдения могут объяснять факт расположения Мф М2 в основном в областях, обедненных липидами и в фиброзной ткани.
Следует отметить, что при исследовании следующих за липидной полосой прогрессирующих стадий развития АСБ, так называемых выраженных поражений – атером, фиброатером, фиброкальцинозных и осложненных поражений [10], наряду с уже описанной картиной распределения Мф были обнаружены специфические зоны локализации субпопуляции Мф М2. Значительные скопления Мф М2, как CD206+, так и CD163+, были выявлены в местах расположения новообразованных сосудов. Это можно объяснить участием Мф М2 в процессах ангиогенеза вследствие способности этих клеток синтезировать VEGF и эндотелин [16]. Кроме того, в участках с расположением геморрагий мы обнаружили Мф М2 преимущественно регуляторного типа (CD163+ – клетки), а в покрышках над пристеночными тромбами – CD206+ – клетки. Известно, что появление геморрагий в АСБ ведет к разрушению внеклеточного матрикса и дестабилизации поражения, поэтому присутствие скоплений CD163+ – клеток в этих областях можно объяснить наряду с их участием в утилизации гемоглобина, также секрецией атеропротекторного IL-10, который является участником негативной регуляции воспалительного процесса [16]. Выявленный нами факт преимущественного скопления CD206+ - клеток в покрышках поражений с пристеночными тромба- ми можно объяснить синтезом ими факторов (IL-4, 10 и 13), активность которых направлена, прежде всего, на ингибирование активации эндотелия и стимуляцию гладкомышечных клеток к синтезу матрикса [12].
В выраженных атеросклеротических поражениях была проведена количественная оценка распределения Т-Лц, Мц и субпопуляций Мф М1 и М2 в наиболее значимых, т.е. предрасположенных к разрыву, тромбозу, возникновению геморрагий участках АСБ – фиброзной покрышке и плечах, левом и правом. Мы показали, что как в плечах, так и в покрышках всех типов АСБ присутствовали обе субпопуляции Мф, т.е. М1 (MCP1+) и М2 (CD206+ и CD163+). В участках плеч наиболее сильная ин- фильтрация М1 и М2 Мф была выявлена в фибро-атеромах и осложненных поражениях, однако и в плечах остальных типов поражений содержание обеих субпопуляций было высоким и достоверной разницы между разными типами поражений по М1 и М2 Мф выявлено не было. Полученные результаты свидетельствуют о высокой воспалительной активности таких участков для всех типов поражений. Что касается фиброзных покрышек атером, фиброатером и осложненных поражений, то они были инфильтрированы достоверно большим количеством Т-Лц, Мц и Мф по сравнению с фиброзной тканью поверхностных (адлюминальных) слоев фиброзных и фиброкальцинозных бляшек, что соответствует ранее опубликованным данным
Рис. 2. Распределение субпопуляций Мф на последовательных поперечных гистологических срезах атеромы внутренней сонной артерии, сопоставление с локализацией липидов. А – окраска на липиды масляным красным О, ядра окрашены гематоксилином; рамка ограничивает область, представленную далее (Б – Д, соответственно). Б – Д – распределение Мф М1 и М2 на последовательных поперечных срезах того же фрагмента АСБ. Иммунопероксидазный (АВС-kit) метод окрашивания с помощью моноклональных антител против специфических клеточных маркеров: Б – HAM56 (Мф человека), В – MCP1 (Мф М1), Г – CD206 (Мф М2) и Д – CD163 (Мф М2 регуляторного типа). Клетки, содержащие перечисленные антигены, имеют коричневое окрашивание. Буквенные обозначения: Пк – пенистые клетки. А, Б, В, Г Ув. 200.
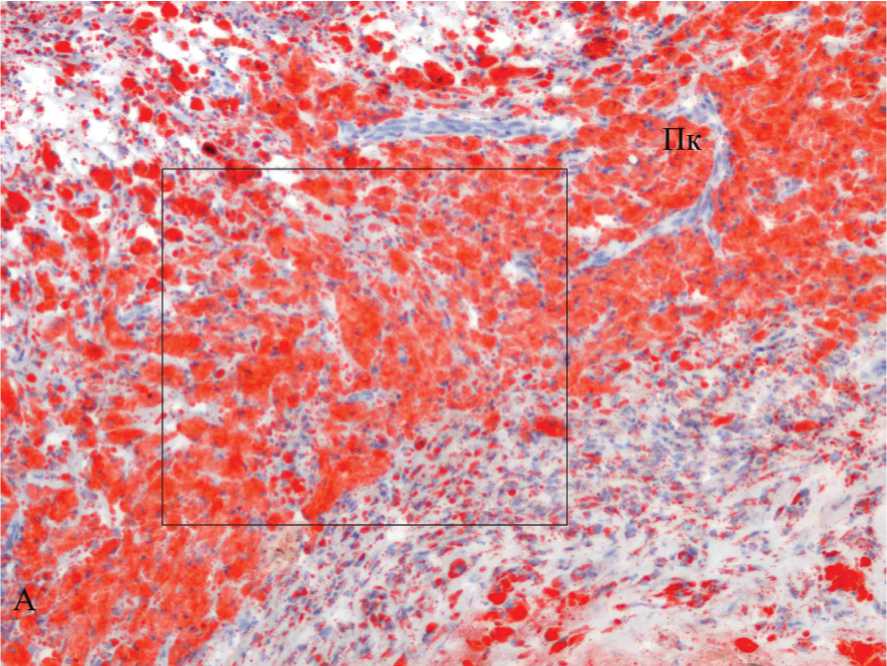
Рис. 2А.
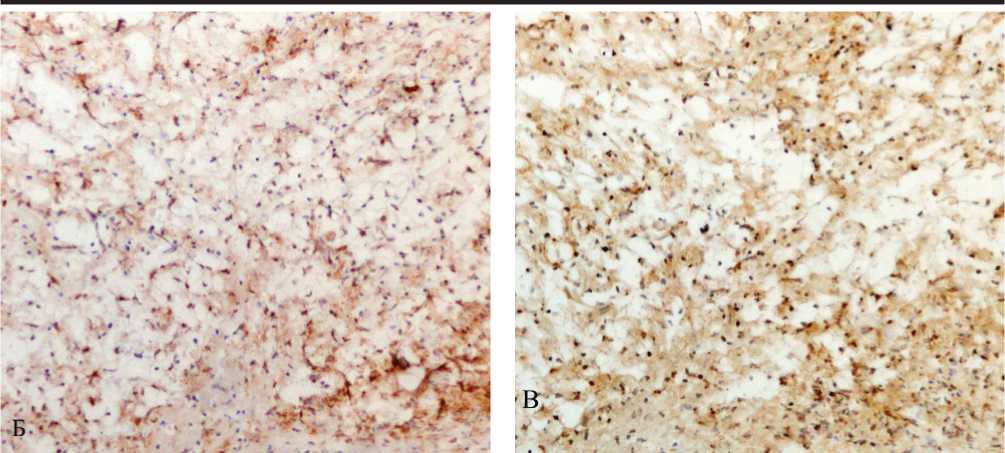
Рис. 2Б.
Рис. 2В.
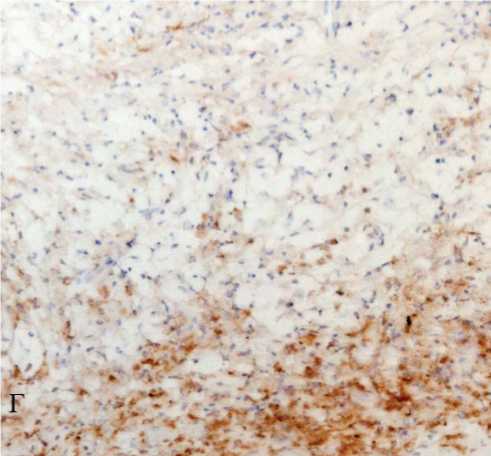
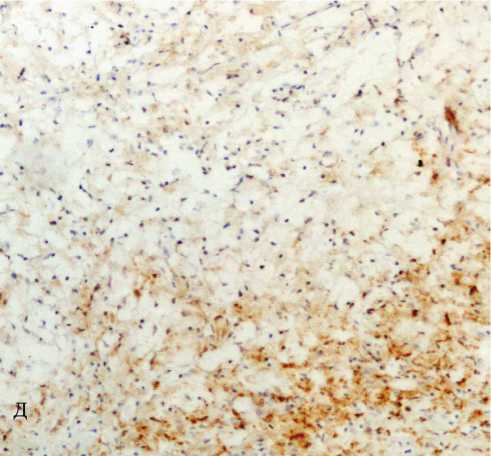
Рис. 2Г.
Рис. 2Д.
-
[5 ]. Однако в литературе на сегодняшний день отсутствуют сведения о распределении субпопуляций Мф М1 и М2 в адлюминальных областях разных типов поражений. Результаты подсчетов содержания Мф М1 и М2 в этих областях разных типов поражений представлены в таблице 1. Достоверно самое низкое содержание Мф М1 обнаружено в адлюминальных фиброзных слоях фиброкальцинозных поражений. В аналогичных структурах фиброзных поражений содержание таких клеток также было низким и достоверно отличалось от содержания их в покрышках фи-броатером и осложненных поражениий – в 2,5 и
-
2 раза, соответственно. Содержание же Мф М1 в фиброзных покрышках атером было высоким, однако достоверных различий с остальными типами поражений кроме фиброкальцинозных выявлено не было.
Исследование распределения функциональных подтипов антивоспалительных Мф М2 (CD206+ и CD163+ - клеток) в адлюминальных фиброзных слоях АСБ разных типов выявило ряд специфических особенностей (табл. 2). Так, в фиброзных и фиброкальцинозных поражениях содержание Мф CD206+ в этих областях было достоверно ниже по сравнению с покрышками фиброатером
Таблица 2.
Распределение субпопуляций Мф М1 и М2 в покрышках (адлюминальных фиброзных слоях) атеросклеротических поражений разных типов (M ± m).
|
Макрофаги |
Маркер |
Типы поражений по Stary (2000), (n = 58) |
р< 0,05 |
||||
|
1. Атерома (n=3) |
2. Фиброа-тер. (n=13) |
3. Фиброзн. (n=22) |
4. Фибро-кальц. (n=7) |
5. Осложнен. (n=13) |
|||
|
Кол-во маркированных клеток/мм2 ткани |
|||||||
|
М1 |
MCP1 |
194,1 ± 116,4 |
163,9 ±38,0 |
66,9 ± 13,1 |
27,4 ± 4,2 |
131,3 ± 28,0 |
3 – 2, 5 4 – 1, 2, 3, 5 |
|
М2 |
CD206 |
141,4 ± 56,8 |
218,6 ± 27,7 |
82,1 ± 9,9 |
76,8 ± 24,0 |
201,1 ± 26,0 |
3 – 2 ,5 4 – 2, 5 |
|
CD163 |
195,2 ± 93,4 |
204,5 ± 37,9 |
56,1 ± 7,6 |
110,9 ± 49,5 |
182,2 ± 32,9 |
3 – 1, 2, 5 4 – 2 |
|
Примечание: MCP1 – моноцитарный хемотаксический белок (маркер М1 Мф), CD206 – маннозный рецептор (маркер М2 Мф) и CD163 – рецептор к гемоглобину – гаптоглобину (маркер М2 регуляторных Мф).
(в 2,7 и 2,9 раз, соответственно) и осложненных поражений (в 2,5 и 2,6 раза, соответственно). Достоверно более низкое количество антивоспа-лительных CD163+- Мф было также выявлено в адлюминальных слоях фиброзных поражений по сравнению с покрышками атером, фиброатером и осложненных поражений, соответственно в 3,5, 3,6 и 3,3 раза. Средние значения содержания этих клеток были характерны для аналогичных областей фиброкальцинозных поражений, где их число в 1,8 раза было ниже, чем в покрышках фиброатером. Фиброзные и фиброкальцинозные поражения не отличались по содержанию в их поверхностных фиброзных слоях М2 Мф (CD206+ – клеток), однако различались по количеству Мф регуляторного типа CD163+ - М2, а также прово-спалительных MCP1+- М1. Так, в адлюминальных областях фиброзных поражений по сравнению с фиброкальцинозными наблюдалось более низкое содержание CD163+-Мф и более высокое – провоспалительных MCP1+- клеток. Эти различия могут отражать более высокую степень провоспалительной активности в адлюминальных слоях фиброзных бляшек по сравнению с фибро-кальцинозными. Интенсивная инфильтрация как про- так и антивоспалительными Мф покрышек нестабильных поражений – фиброатером и осложненных поражений, по сравнению со стабильными, т.е. фиброзными и фиброкальцинозными, свидетельствует об идущих в них более активных воспалительных процессах, которые способствуют дестабилизации АСБ вследствие деградации внеклеточного матрикса, ведущей к возможному истончению и разрыву фиброзных покрышек – наиболее опасному в клиническом отношении осложнению при атеросклерозе.
Выводы:
-
1) Во всех типах атеросклеротических поражений обнаружены Мф как про- (MCP1+), так и ан-тивоспалительного фенотипа (CD206+ и CD163+);
-
2) на ранней стадии развития поражения (липидное пятно/полоса) Мф М1 и М2 присутствуют в равном соотношении, что указывает на существенную роль обеих субпопуляций в инициации процесса атерогенеза в интиме;
-
3) в выраженных атеросклеротических поражениях (атерома, фиброатерома, осложненное поражение) в областях, богатых липидными включениями или инфильтрированных клетками воспаления, локализуются в основном провоспа-лительного типа Мф М1 (MCP1+ – клетки);
-
4) в стабильных поражениях (фиброзных и фиброкальцинозных), а также в фиброзных областях атером и фиброатером преимущественно локализуются Мф антивоспалительного фенотипа М2 (CD206+ и CD163+ – клетки);
-
5) достоверной разницы по содержанию Мф М1 и М2 в плечах АСБ разных типов выявлено не было;
-
6) обнаружена достоверно более интенсивная инфильтрация Мф обеих субпопуляций адлюминальных фиброзных слоев (фиброзных покрышек) в атеромах, фиброатеромах и осложненных поражениях по сравнению с фиброзными и фиброкальцинозными.
Полученные в работе результаты позволяют сделать заключение, что баланс сил между про- и антивоспалительной субпопуляциями Мф М1 и М2 существенно влияет на процессы формирования атеросклеротического поражения и развитие осложнений при атеросклерозе.
Работа выполнена при финансовой поддержке Правительства г. Москвы, Госконтракт №
8/3-280н-10 от 27 мая 2010 г. и гранта РФФИ № 13-04-00463 А от 2013 г.
Список литературы Топографическое распределение и возможная роль про- и антивоспалительных субпопуляций макрофагов в разных типах атеросклеротических поражений
- Geissmann F., Manz M.G., et al. Development of monocytes, macrophages and dendritic cells//Science. 2010. № 327. P. 656-661.
- Ley K., Miller Y.I., Hedrick C.C. Monocyte and macrophage dynamics during atherogenesis//Arterioscler. Thromb. Vasc. Biol. 2011. № 31. P. 1506-1516.
- Wolfs I.M., Donners M.M., de Winther M.P. Differentiation factors and cytokines in the atherosclerotic plaque micro-environment as a trigger for macrophage polarization//Thromb Haemost. 2011. Т. 106, № 5. P. 763-771.
- Wynn T.A., Fibrotic disease and the T(H)1/T(H)2 paradigm//Nat. Rev. Immunol. 2004. № 4. P. 583-594.
- Libby P., Lichtman A.H., Hansson G.K. Immune effector mechanisms implicated in atherosclerosis: from mice to humans//Immunity. 2013. Т. 38, № 6. P. 1092-1104.
- Bouhlel M.A., Derudas B., et al. PARg activation primes human monocytes into alternative M2 macrophages with anti-inflammatory properties//Cell Metabolism. 2007. № 6. P. 137-143.
- Wilson H.M., Macrophages heterogeneity in atherosclerosis -implications for therapy//J Cell Mol Med. 2010. Т. 14, № 8. P. 2055-2065.
- Khallou-Laschet J., Varthaman A., et al. Macrophage plasticity in experimental atherosclerosis//PLoS ONE. 2010. № 5.
- Shaikh S., Brittenden J. et al. Macrophage subtypes in symptomatic carotid artery and femoral artery plaques//Eur. J. Vasc. Endovasc. Surg. 2012. № 44. P. 491-497.
- Stary H.C. Natural history and histological classification of atherosclerotic lesions: an update//Arterioscler. Thromb. Vasc. Biol. 2000. T 20, № 5. P. 1177-1178.
- Chinetti-Gbaguidi G., Baron M., et al. Human atherosclerotic plaque alternative macrophages display cholesterol handling but phagocytosis because of distinct activities of the PARy and LXRa pathways//Circ Res. 2011. Т. 108, № 8. P. 985-995.
- Butcher M.J., Galkina E.V. Phenotypic and functional heterogeneity of macrophages and dendritic cell subsets in the healthy and atherosclerosis-prone aorta//Frontiers in Physiology. 2012. Т. 3, № 44. P. 1-13
- Thorp E., Subramanian M., Tabas I. The role of macrophages and dendritic cells in the clearance of apoptotic cells in advanced atherosclerosis//Eur. J. Immunol. 2011. Т. 41, № 9. P. 2515-2518.
- Moore K.J., Tabas I. Macrophages in the pathogenesis of atherosclerosis//Cell. 2011. № 145. P. 341-355.
- Murray P.J., Wynn T.A. Protective and pathogenic functions of macrophage subsets//Nat. Rev. Immunol. 2011. № 11. P. 723-737.
- Mantovani A., Garlanda C., Locati M. Macrophage diversity and polarization in atherosclerosis: a question of balance//Arterioscler. Thromb. Vasc. Biol. 2009. № 29. P. 1419 -1423.


