Трансформация модифицированных полихлорбифенилов штаммом Rhodococcus wratisla viensis КТ112-7 в условиях засоления
Автор: Егорова Д.О.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 3, 2018 года.
Бесплатный доступ
Показано, что штамм Rhodococcus wratislaviensis КТ112-7 способен разлагать смесь соединений, образованную после химической модификации коммерческой смеси полихлорированных бифени-лов марки Совол, в условиях засоления. Смесь состоит из тетра- и пентахлорированных бифени-лов, гидрокси-полихлорированных бифенилов, аминоэтокси-полихлорированных бифенилов и гидроксиаминоэтокси-полихлорированных бифенилов. Установлено, что величина деструкции данной смеси штаммом R. wratislaviensis КТ112-7 в присутствии в среде 60 г/л хлорида натрия составляет 73.8%. В условиях засоления среды штамм КТ112-7 проявляет деградативную активность ко всем модифицированным и не модифицированным конгенерам полихлорбифенилов, представленных в смеси. Разложение данных соединений происходило с образованием и накоплением в среде хлорированных и гидроксилированных бензойных кислот, а также катехола.
Полихлорированные бифенилы, соз, штаммы-деструкторы, химическая модификация
Короткий адрес: https://sciup.org/147227029
IDR: 147227029 | УДК: 5
The transformation of modified polychlorinated biphenyls by the Rhodococcus wratislaviensis strain КТ112-7 in the saline conditions
The strain Rhodococcus wratislaviensis KT112-7 was able to decompose a mixture of compounds formed after the chemical modification of a commercial mixture of polychlorinated biphenyls «Sovol», under conditions of salinity. The mixture consists of tetra- and pentachlorinated biphenyls, hydroxy-polychlorinated biphenyls, aminoethoxy-polychlorinated biphenyls, and hydroxyaminoethoxy-polychlorinated biphenyls. It was found that the destruction of this mixture by the strain of R. wratislaviensis KT112-7 in the presence of 60 g/l sodium chloride was 73.8%. Under conditions of salinization, the strain KT112-7 exhibits degradative activity to all the modified and unmodified congeners of polychlorinated biphenyls present in the mixture. The decomposition of these compounds occurred with the formation and accumulation the chlorinated and hydroxylated benzoic acids, and catechol.
Текст научной статьи Трансформация модифицированных полихлорбифенилов штаммом Rhodococcus wratisla viensis КТ112-7 в условиях засоления
Полихлорированные бифенилы (ПХБ) – группа искусственно синтезированных хлорароматиче-ских соединений, обладающих высоким уровнем стабильности к физическому, химическому и биологическому воздействию [Трегер, 2013]. ПХБ производили в ХХ в. в виде коммерческих смесей, содержащих в своем составе 40–60 конгенеров [Erikson, Kaley, 2011]. Широкое применение смесей полихлорбифенилов в промышленности привело к значительному загрязнению данными соединениями различных объектов окружающей среды [Ross, 2004; Murugan, Vasudevan, 2018]. Согласно Стокгольмской конвенции, ратифицированной РФ в 2011 г., полихлорированные бифенилы должны быть уничтожены к 2028 г. [ ; ]. При этом территории, загрязненные ПХБ, должны быть восстановлены.
ПХБ состоят из двух ароматических колец, соединенных С-С связью, и ионов хлора, расположенных в качестве заместителей в количестве от 1 до 10 [Erikson, Kaley, 2011]. По результатам многочисленных исследований установлено, что био-
доступность ПХБ находится в обратной зависимости от степени хлорирования их молекулы, а реакционная способность при химическом воздействии – в прямой зависимости от степени хлорирования молекулы [Pieper, 2005; Field, Sierra-Alvarez, 2008; Горбунова и др., 2011]. При химической переработке коммерческих смесей ПХБ образуются различные варианты модифицированных конгенеров, содержащих в составе молекулы в качестве заместителей гидрокси-, аминоэтокси-, полигликолок-си-группы и ряд других [Егорова и др., 2011, 2013; Горбунова и др., 2014]. Кроме того, известно, что в процессе трансформации хлорбифенилов высшими растениями в окружающей среде образуются производные, содержащие гидрокси-группы в составе молекулы полихлорбифенилов [Tehrani, Van Aken, 2014]. Таким образом, в окружающей среде присутствуют не только ранее синтезированные конгенеры ПХБ, но и их модифицированные производные, содержащие в своем составе различные химические группы.
В настоящее время известно значительное количество штаммов аэробных бактерий, способных разлагать хлорированные бифенилы [Pieper, 2005; Field, Sierra-Alvarez, 2008; Agullo et al., 2017]. Однако штаммов, способных трансформировать модифицированные конгенеры ПХБ, изучено ограниченное количество [Francova et al., 2004; Tehrani et al., 2012; Егорова и др., 2013; Горбунова и др., 2014; Mizukami-Murata et al., 2016]. Стоит учитывать, что трансформация ПХБ и их производных в естественных условиях осложняется присутствием ряда негативных экологических факторов, таких как высокие или низкие температуры, низкая влажность, высокая соленость среды [Margesin, Schinner, 2001]. Однако примеров бактериальной деструкции модифицированных ПХБ в условиях, отличных от оптимальных, в литературе не найдено.
Цель настоящей работы – изучение особенностей трансформации смеси химически модифицированных полихлорбифенилов штаммом Rhodococcus wratislaviensi s КТ112-7 в условиях засоления.
Материалы и методы исследования
Штамм-деструктор . В работе использован штамм Rhodococcus wratislaviensi s КТ112-7, выделенный ранее из отходов соледобывающего предприятия [Егорова и др., 2013]. Штамм R. wratisla-viensi s КТ112-7 осуществляет разложение хлорированных бифенилов, бензоата и орто -фталата в условиях засоления среды [Егорова и др., 2013, 2018].
Модифицированные полихлорбифенилы. Смесь модифицированных полихлорированных бифенилов, обозначенная как GTI-2013, предоставлена для исследования сотрудниками Института органического синтеза им. И.Я. Постовского УрO РАН. Смесь GTI-2013 образована в результате взаимодействия коммерческой смеси ПХБ марки Совол (35 конгенеров, содержащих от 4 до 6 заместителей) с 2-аминоэтанолом в присутствии KOH при 110–115°С в течение 7.5 ч. [Горбунова и др., 2014]. Смесь GTI-2013 содержит тетра- и пентахлорбифенилы, не вступившие в реакцию, а также хлорбифенилы с гидрокси- и аминоэтоксигруппами в качестве заместителей.
Деструкция модифицированных ПХБ . Деструкцию проводили в эксперименте с отмытыми клетками. Бактериальную культуру штамма КТ112-7 предварительно выращивали в МСР [Raimond, 1961] с бифенилом (1 г/л) и хлоридом натрия в концентрации 60 г/л до ОП 600 =1.0. Оптическую плотность измеряли на BioSpec-mini (“Shimadzu”, Япония) при длине волны 600 нм. Культивирование осуществляли в колбах Эрленмейера объемом 250 мл в 100 мл жидкой среды при 28ºС и аэрации на круговой качалке Environmental Shaker-Incubator ES-20/60 (“BioSan”, Латвия) со скоростью 180 об/мин. Отмытые дважды в МСР, содержащей 6% NaCl, клетки (1 мл, ОП 600 =2.0) переносили во флаконы с тефлоновыми крышками. Смесь модифицированных полихлорбифенилов GTI-2013 вносили в виде ацетонового раствора до конечной концентрации 0.47 мг/мл. Флаконы встряхивали на круговой качалке Environmental Shaker-Incubator ES-20/60 (“BioSan”, Латвия) (180 об/мин) при 28ºС. Эффективность деструкции смеси GTI-2013 оценивали через 2, 4 и 6 сут.
Анализ количества компонентов смеси GTI-2013 проводили методом ГХ-МСД и ГХ-ПИД в гексановых экстрактах [Горбунова и др., 2014].
Идентификацию компонентов проводили на основании базы масс-спектров NIST05 и калибровочных хроматограмм ГСО 7821-2000 «Совол».
Анализ продуктов деструкции . Продукты деструкции определяли в культуральной жидкости, освобожденной от бактериальных клеток центрифугированием (9660g, 3 мин., центрифуга miniSpin (“Eppendorf”, Германия)), методом ВЭЖХ. ВЭЖХ-анализ проводили на жидкостном хроматографе LC-20AD Prominence (“Shimadzu”, Япония) с УФ-детектором SPD-20A при 205 нм и колонкой Supelco C18 (150 x 4.6 мм) (“Sigma-Aldrich”, США) в системе ацетонитрил – 0.1%-ный H 3 PO 4 (70:30). Идентификацию проводили на основании сравнения времени удержания на колонке исследуемых и стандартных соединений.
Кинетические параметры деструкции . Эффективность деструкции смеси модифицированных хлорбифенилов оценивали в процентах согласно формуле
Д (%)=(С t ×100)/C 0 , где Д – эффективность деструкции, %; С t – концентрация смеси GTI-2013 через определенный промежуток времени (2, 4, 6 сут.); C 0 – концентрация смеси GTI-2013 в начальный момент времени.
Удельную скорость деструкции смеси GTI-2013 рассчитывали по формуле
V t = (C 0 -C t )/t , где С 0 – концентрация смеси GTI-2013 в начальной момент времени, C t – концентрация смеси GTI-2013 через 6 сут. эксперимента, t –время деструкции, ч.
Статистическая обработка результатов . Все эксперименты проводили в трехкратной повторности. Полученные данные обрабатывали с использованием стандартных пакетов компьютерных программ Microsoft Excel.
Результаты и их обсуждение
В результате ранее проведенных исследований установлено, что штамм Rhodococcus wratislavien-si s КТ112-7 осуществляет трансформацию моно- и дихлорированных бифенилов при концентрации хлорида натрия в среде в диапазоне от 0 до 50 г/л, а незамещенного бифенила при концентрации NaCl в среде до 100 г/л [Егорова и др., 2013, 2018]. При этом уровень деструкции хлорированных бифенилов был выше, чем у известных штаммов-деструкторов родов Rhodococcus , Aquami-crobium , Bacillus и Pseudomonas [Pieper, 2005; Field, Sierra-Alvarez, 2008; Agullo et al., 2017]. Также ранее показано, что штамм R. wratislavien-si s КТ112-7 разлагает модифицированные хлорированные бифенилы при физиологическом уровне солености среды [Егорова и др., 2013; Горбунова и др., 2014].
В настоящем исследовании установлено, что штамм R. wratislaviensi s КТ112-7 осуществляет трансформацию смеси GTI-2013, состоящую из тетра- и пента-хлорбифенилов, а также из модифицированных хлорбифенилов, содержащих в молекуле гидрокси- и аминоэтокси-группы в присутствии в среде 60 г/л NaCl (рис. 1, 2). Деструкция смеси за 6 сут. составила 73.8% (рис. 1), что на 5% ниже, чем аналогичный показатель в условиях отсутствия засоления среды. Рядом работ показано, что повышение уровня засоленности среды негативно сказывается на деградативной активности аэробных штаммов [Margesin R., Schinner, 2001; Плотникова и др., 2006; Егорова и др., 2018]. Таким образом, полученный результат согласуется с известной закономерностью.
Динамика убыли смеси GTI-2013 под действием культуры штамма R. wratislaviensis КТ112-7 имеет вид вогнутой кривой и описывается степенным уравнением y = -0.0043x3 + 0.042x2 – 0.1542x + 0.47, c величиной достоверности аппроксимации R2=1.0.
При отсутствии солевого стресса, характер кривой, описывающей убыль данной смеси штаммом КТ112-7, имеет аналогичный вид и описывается также уравнением третьей степени [Горбунова и др., 2014]. Анализ кинетических параметров деструкции смеси GTI-2013 показал, что при культивировании в присутствии 6%-ного хлорида натрия удельная скорость деструкции составила 0.056 (мг/л)/сут., тогда как, при разложении в изотонических условиях, данный показатель, в пересчете за первые 6 сут. культивирования, составлял 0.067 (мг/л)/сут. По-видимому, гипертоническая среда оказывает влияние на активность ферментов деструкции, но не на принцип их работы.
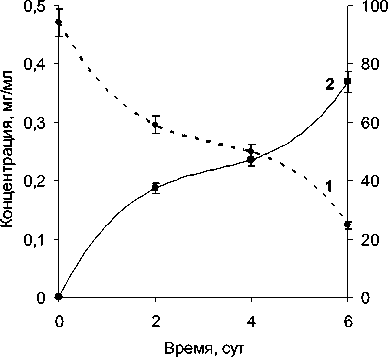
Рис. 1 . Динамика разложения смеси GTI-2013 штаммом R. wratislaviensi s КТ112-7:
1 – изменение концентрации смеси в культуральной среде, 2 – уровень деструкции
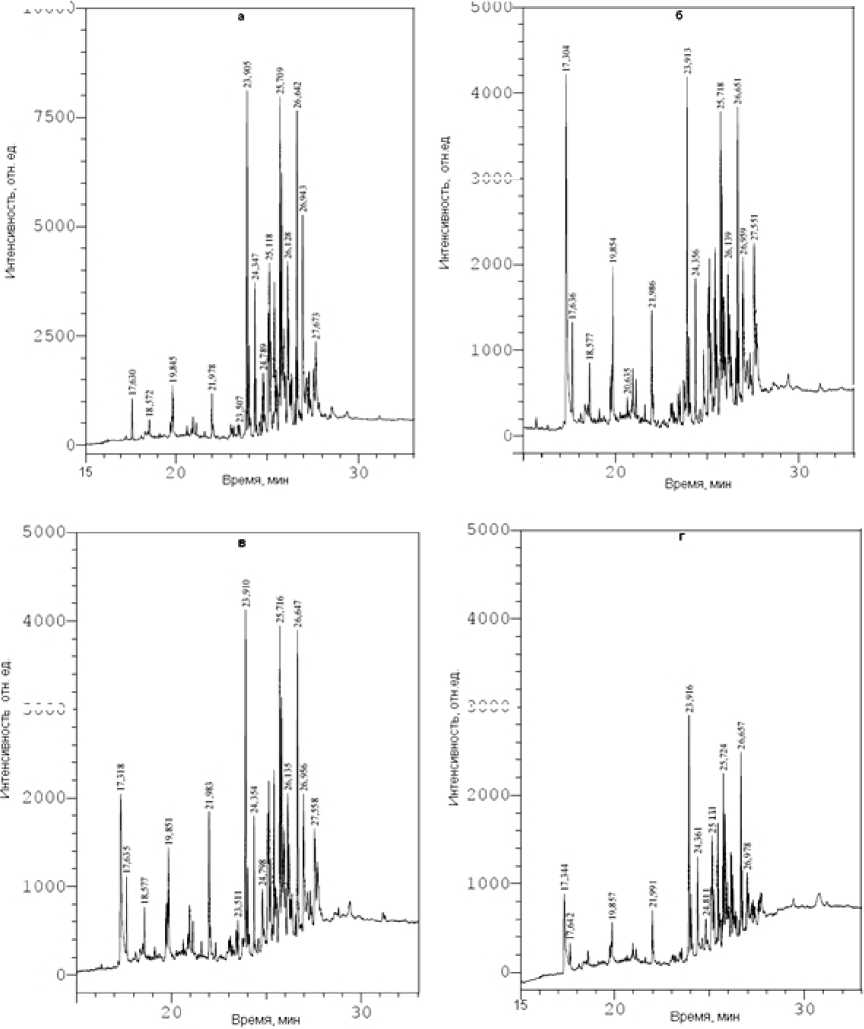
Методом газовой хроматографии с пламенноионизационным и масс-спектрометрическим детектированием установлено, что штамм R. wra-tislaviensi s КТ112-7 разлагает все соединения, представленные в смеси GTI-2013, а именно тетра-и пентахлорбифенилы, гидроксиполихлор-бифенилы, аминоэтоксиполихлорбифенилы и гидроксиа-миноэтоксиполихлорбифенилы (рис. 2). Ранее было показано, что при разложении данной смеси в изотонических условиях, штамм КТ112-7 в первую очередь трансформирует производные ПХБ с аминоэтоксигруппой [Горбунова и др., 2014]. Однако при культивировании в гипертонических условиях подобной закономерности не выявлено.
Основную долю смеси GTI-2013 составляют гидроксилированные полихлорированные бифенилы [Горбунова и др., 2014]. На рисунке 2 им соответствует ряд наиболее высоких пиков с временем удержания 23.5–27.5 мин. Анализ профиля хроматограмм показывает, что штамм R. wratislaviensis КТ112-7 проявляет разную активность к гидрокси- лированным три-, тетра- и пента-хлорбифенилам. При этом на доступность субстрата, по-видимому, влияет не только количество атомов хлора в молекуле гидрокси-ПХБ, но и их расположение. Известно, что штаммы Burkholderia xenovorans LB400 и Comamonas testosteroni B-356 предпочтительнее окисляют гидроксихлорбифенилы, содержащие заместителей в одном кольце молекулы 10000
3000-
3000-
3000-1
Рис. 2. Хроматограмма смеси GTI-2013 до начала бактериальной деструкции (а) и через 2 сут. (б), 4 сут. (в) и 6 сут. (г) разложения штаммом КТ112-7
Аналогичная закономерность отмечена для штамма Sphingomonas sp. N-9, однако данный штамм проявлял высокую ферментативную активность к (моно-тетра)хлорированным моногидроксибифенилам, и в меньшей степени трансформи-
[Francova et al., 2004; Mackova et al., 2007]. Штамм B. xenovorans LB400 эффективно разлагает монохлорированные гидроксибифенилы, проявляет меньшую активность в отношении дихлориро-ваных моногидроксибифенилов и не трансформирует трихлорированные моногидроксибифенилы [Tehrani et al., 2012, 2014].
ровал пента- и гексахлорированные моногидроксибифенилы [Mizukami-Murata et al., 2016]. Расположение гидрокси-группы также влияет на эффективность бактериальной трансформации гидрокси-ПХБ. В работе Bhalla с коллегами [2016]
показано, что наиболее токсичными являются дии три-хлорированные гидроксибифенилы, содержащие гидрокси-группу во втором или четвертом положении на кольце молекулы бифенила.
Бактериальная трансформация бифенила и его модифицированных производных протекает под действием ферментативного комплекса, обусловливающего окисление молекулы через стадии гидроксипроизводных до формирования (хлор)бен-зойных и (хлор)пентадиеновых кислот [Sondossi et al., 1991; Pieper, 2005]. При дальнейшем разложе-
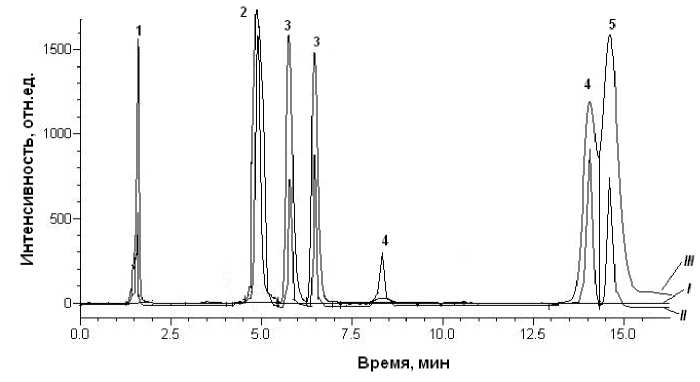
Рис. 3 . Хроматограмма (условия ВЭЖХ) смеси промежуточных продуктов, образовавшихся в результате бактериальной деструкции смеси GTI-2013 штаммом R. wratislaviensis КТ112-7:
0 сут. ( I ), 2 сут. ( II ), 6 сут. ( III ): 1 – катехол, 2 – гидроксибензойная кислота, 3 – моно-хлорбензойные кислоты, 4 – ди-хлорбензойные кислоты, 5 – три-хлорбензойные кислоты
Аналогичные результаты были получены при разложении данной смеси модифицированных ПХБ в изотонических условиях [Горбунова и др., 2014]. Однако известно, что повышение уровня осмолярности среды приводит к снижению скорости трансформации хлорированных бензойных кислот – метаболитов ПХБ [Егорова и др., 2018]. Количественный анализ показал, что в настоящем исследовании происходит накопление метаболитов (хлор- и гидроксибензойных кислот), образующихся при трансформации модифицированных ПХБ. Однако наличие гидроксибензойных кислот, являющихся предшественниками соединений основного обмена клетки, позволяет предположить, что при разложении смеси гидрокси- и амноэтокси-полихлорированных бифенилов штаммом R. wra-tislaviensi s КТ112-7 в присутствии 60 г/л хлорида натрия не накапливаются соединения, токсичные для окружающей среды.
Заключение
В результате проведенных исследований изучены особенности трансформации химически моди-фицирвоанных полихлорированных бифенилов штаммом R. wratislaviensi s КТ112-7 в условиях засоления среды.
нии (хлор)бензойных кислот в качестве метаболитов образуются гидроксибензойные кислоты и (хлор)катехолы [Егорова и др., 2013].
При анализе культуральной жидкости методом высокоэффективной жидкостной хроматографии установлено, что при разложении смеси GTI-2013 штаммом R. wratislaviensi s КТ112-7 в условиях засоления образуются хлорированные и гидроксилированные бензойные кислоты, а также катехол (рис. 3).
Показано, что содержание в среде 60 г/л хлорида натрия приводит к незначительному снижению эффективности разложения смеси гидрокси- и аминоэтокси-полихлорированных бифенилов. Установлено, что штамм КТ112-7 эффективно разлагает все модифицированные конгенеры ПХБ, представленные в смеси, а также не модифицированные тетра- и пентахлорбифенилы. Основными метаболитами являются хлорированные и гидроксилированные бензойные кислоты, а также катехол. При этом высокое содержание хлорида натрия в среде приводит к накоплению метаболитов в культуральной жидкости.
Таким образом, полученные результаты свидетельствуют об эффективной деструкции смеси химически модифицированных полихлорбифенилов штаммом R. wratislaviensi s КТ112-7 в условиях засоления и позволяют рекомендовать данный штамм для использования в разработках биотехнологий, направленных на переработку полихлорированных бифенилов в различных условиях среды.
Работа выполнена в рамках государственного задания. Номер госрегистрации темы: 01201353249. Тема: «Молекулярные механизмы адаптации микроорганизмов к факторам среды».
Список литературы Трансформация модифицированных полихлорбифенилов штаммом Rhodococcus wratisla viensis КТ112-7 в условиях засоления
- Горбунова Т.И. и др. Пример междисциплинарного подхода к проблеме обезвреживания техногенных полихлорбифенилов // Доклады Академии наук. 2014. Т. 454, № 4. С.411-416. DOI: 10.7868/S086956521404015X
- Горбунова Т.И. и др. Полихлорирбифенилы. Проблемы экологии, анализа и химической утилизации. М.: Красанд, 2011. 400 с.
- Егорова Д. О. и др. Деструкция ароматических углеводородов штаммом Rhodococcus wratis-lavensis KT112-7, выделенным из отходов соледобывающего предприятия // Прикладная биохимия и микробиология. 2013. Т. 49, № 3. С. 267-278. DOI: 10.7868/S0555109913030070
- Егорова Д.О. и др. Бактериальная деструкция смеси, полученной при химической модификации поли-хлорированных бифенилов полиэтиленгликолями // Биотехнология. 2013. № 4. С. 56-64.
- Егорова Д.О. и др. Особенности разложения хлорированных бифенилов штаммом Rhodococcus wratislaviensis КТ112-7 в условиях засоления // Прикладная биохимия и микробиология. 2018. Т. 54, № 3. С. 253-263. 10.7868/ S0555109918030042. DOI: 10.7868/S0555109918030042
- Егорова Д.О. и др. Утилизация полихлорбифе-нилов с использованием химических и биологических процессов // Доклады Академии наук. 2011. Т. 441, № 3. С. 328-331.
- Трегер Ю. СОЗ - стойкие и очень опасные // The Chemical Journal. 2013. № 1. С. 30-34.
- Agullo L., Pieper D.H., Seeger M. Handbook of Hydrocarbon and lipid Microbiology / ed. N.T. Kenneth. Berlin; Heidelberg: Springer, 2017. P. 1-28.
- Bhalla R., Tehrani R., Van Aken B. Toxicity of hy-droxylated polychlorinated biphenyls (HO-PCBs) using the bioluminescent assay Microtox // Ecotoxicology. 2016. Vol. 25. P. 1438-1444.
- Erikson M.D., Kaley II R.G. Applications of poly-chlorinated biphenyls // Environmental Science Pollution Reserch. 2011. Vol. 18(2). P. 135-151.
- DOI: 10.1007/s11356-010-0392-1
- Field J.A., Sierra-Alvarez R. Microbial transformation and degradation of polychlorinated biphenyls // Environmental Pollution. 2008. Vol. 155, № 1. P. 1-12.
- Frankova K. et al. Ability of bacterial biphenyl di-oxygenases from Burkholderia sp. LB400 and Co-mamonas testosteroni B-356 to catalyse oxygenation of ortho-hydroxychlorobiphenyla formed from PCBs by plants // Environmental Pollution. 2004. Vol. 127. P. 41-48.
- Makova M. et al. Biotransformation of PCBs by plants and bacteria - consequences of plant-microbe interactions // European Journal of Soil Biology. 2007. Vol. 43. P. 233-241.
- Margesin R., Schinner F. Biodegradation and bioreme-diation of hydrocarbons in extreme environments // Applied Microbiology Biotechnology. 2001. Vol. 56. P. 650-663.
- DOI: 10.1007/s002530100701
- Mizukami-Murata S. et al. Detoxification of hydroxy-lated polychlorobiphenyls by Sphingomonas sp. strain N-9 isolated from forest soil // Chemosphere. 2016. Vol. 165. P. 173-182.
- Murugan K., Vasudevan N. Intracellular toxicity by PCBs and role of VBNC bacterial strains in biodegradation // Ecotoxicology Environmental Safety. 2018. Vol. 157. P. 40-60.
- DOI: 10.1016/j.ecoenv.2018.03.014
- Pieper D.H. Aerobic degradation of polychlorinated biphenyls. // Applied Microbiology Biotechnology. 2005. Vol. 67, № 2. P. 170-191.
- DOI: 10.1007/s00253-004-1810-4
- Raymond R.L. Microbial oxidation of n-paraffinic hydrocarbons // Developments in Industrial Microbiology. 1961. Vol. 2. P. 23-32.
- Ross G. The public health implications of polychlori-nated biphenyls (PCBs) in the environment // Ecotoxicology Environmental Safety. 2004. Vol. 59. P. 275-291.
- DOI: 10.1016/j.ecoenv.2004.06.003
- Sandossi M. et al. Metabolism of hydroxibiphenyl and chloro-hydroxybiphenyl by biphenyl/chlorobiphe-nyl degrading Pseudomonas testosteroni, strain B-356 // Journal of Industrial Microbiology. 1991. Vol. 7. P. 77-88.
- Tehrani R. et al. Biodegradation of mono-hydro-xylated PCBs by Burkholderia xenovorans // Biotechnology Letters. 2012. Vol. 34. P. 2247-2252.
- Tehrani R., Lyv M.M., Van Aken B. Transformation of hydroxylated derivatives of 2,5-dichlorobiphenyl and 2,4,6-trichlorobiphenyl by Burkholderia xenovorans LB400 // Environmental Science Pollution Reserch. 2014. Vol. 21. P. 6346-6353.
- Tehrani R., Van Aken B. Hydroxylated polychlori-nated biphenyls in the environment: sources, fate, and toxicities // Environmental Science Pollution Reserch 2014. Vol. 21. P. 6330-6345.
- DOI: 10.1007/s11356-013-1742-6


