Транскатетерная артериальная эмболизация при кровотечениях из верхних отделов желудочно-кишечного тракта
Автор: Багдасаров Валерий Вартанович, Багдасарова Елена Анатольевна, Чернооков Александр Иванович, Атаян Андрей Александрович, Карчевский Евгений Викторович, Багдасарова Дарья Валерьевна
Журнал: Хирургическая практика @spractice
Рубрика: Оригинальные исследования
Статья в выпуске: 3, 2015 года.
Бесплатный доступ
Цель исследования: продемонстрировать возможности использования транскатетерной артериальной эмболизации при кровотечениях из верхних отделов желудочно-кишечного тракта. Материалы и методы: представлены результаты наблюдения 445 больных с острым желудочно-кишечным кровотечением из верхних отделов желудочно-кишечного трактаза период с 2009 по 2014 г. Результаты: Изменение хирургической тактики лечения ЖКК привело к снижению послеоперационной летальности с 22,9% в 2009-2011 гг. до 6,5% в 2012-2014 гг. заключение: Транскатетерная артериальная эмболизация из-за минимальной инвазивности, отсутствии наркоза, лапаротомии, эффективности и безопасности, а также возможности повторного выполнения, особенно у мультиморбидных пациентов и больных пожилого возраста, показала себя эффективной в контроле кровотечения и снижения смертности.
Кровотечение, язва, эндоскопический гемостаз, транскатетерная артериальная эмболизация, the general гомоцистеин
Короткий адрес: https://sciup.org/142211637
IDR: 142211637
Текст научной статьи Транскатетерная артериальная эмболизация при кровотечениях из верхних отделов желудочно-кишечного тракта
Большой и до конца не решенной проблемой неотложной хирургии в начале ХХI века остается острое кровотечение из верхних отделов желудочно-кишечного тракта, связанное со значимой смертностью. Еще до недавнего времени 35-55% пациентам с массивным острым желудочно-кишечным кровотечением (ЖКК) из верхних отделов требовалось экстренное хирургическое вмешательство, что соотносится со смертностью в 20%, которая достигала 50% у пожилых больных с тяжелыми сопутствующими заболеваниями [1, 2].
Эпидемиологические данные указывают о дальнейшем «старении» и увеличении мультиморбидности пациентов с ЖКК, что значительно маскирует несомненные успехи в их лечении. Опубликованная частота возникновения желудочно-кишечных кровотечений (ЖКК) колеблется от 62 до 172 случаев на 100.000 взрослых в год [3]. Наиболее спорным вопросом остается тактический подход к лечению ЖКК. Недавно состоявшийся пленум Российского общества хирургов в Воронеже (5-6 июня 2014 г), посвященный ЖКК, подтверждает этот тезис.
Применение инновационных технологий, в том числе ми-ниинвазивных, доказало свою эффективность в различных областях медицины [4-6] . Эндоскопический гемостаз признан первым методом в линии выбора лечебной тактики при ЖКК. В случае применения современных методов эндоскопического гемостаза, по данным разных авторов, удается добиться адекватного гемостаза от 87% до 98% случаев [7], но в 10-30% у этих пациентов может возникнуть рецидив кровотечения [8]. И до сих пор неизвестно, где та граница, за которой могут помочь артериальная эмболизацияили операция.
При неэффективности эндоскопического гемостаза, рецидиве кровотечения, неприменимости операции, как следствие, нестабильности гемодинамики, угрозе для жизни пациента, некоторые авторы [9, 10] считают транскатетерную артериальную эмболизацию (ТАЭ) методом спасения, особенно среди больных высокого операционного риска после неудачного эндоскопического лечения. Очевидное преимущество ТАЭ, по данным этих авторов, состоит в избегании лапаротомии у критических пациентов, наркоза, уменьшающейся смертности и инфекционных осложнений. Неотложная хирургия действи- тельно оказалось необходимой в 5% случаев из-за массивного кровотечения или его рецидива в случае неудачи эндоскопического гемостаза [11]. У многих из этих пациентов мультимор-бидность часто была причиной негативного исхода.
При хирургическом вмешательстве на высоте кровотечения смертность варьирует в пределах 20-40% [12, 13]. Кровотечения в верхние отделыжелудочно-кишечного тракта при хроническом кистозном панкреатите являются относительно редкими и вызывают значительные трудности для диагностики и лечения. Сложной эндоскопическойпроблемой является отсутствие явного источника кровотечения при неоднократныхи безрезультатныхэндоскопических исследованиях.
Появление и дальнейшее развитие эндоваскулярных интервенционных методик из-за её минимальной инвазивности, возможности повторного проведения, эффективности и безопасности особенно у мультиморбидныхпациентов пожилого возраста, слабых, и с нестабильным кровяным давлением и больных после операции, рецидив является плохим прогностическим фактором при кровотечениях из верхних отделов желудочно-кишечного тракта, с уровнем смертности в 44-60%. За последние годы эндоваскулярные вмешательствасыгрализна-чительнуюрольвэкстренномлечениизаболевания,существенно изменили тактику лечения пациентов с ЖКК [14, 15].
Цель: Оптимизировать тактику лечения при ЖКК из верхних отделов желудочно-кишечного тракта с использованием эндоваскулярных интервенционных методик.
Материал и методы исследования
В основной группе (2012-2014 гг.) у больных с язвенным гастродуоденальным кровотечением применяли разработанный нами лечебно-диагностический алгоритм: 1)эндоскопический гемостаз под наркозом с уточнением риска рецидива кровотечения (по шкале Rockall); 2) при неуверенном или при безуспешном эндоскопическом гемостазе, а также при рецидиве кровотечения с необходимостью переливания ≥3-4единиц эритроцитарной массы в течение 24 часов–ТАЭ; 3) при отсутствии эффекта от ТАЭ –хирургическое лечение.
Оценку тяжести состояния пациентов определяли по интегральным системам-шкалам APACHE-IIи SOFA. Наиболее простым инструментом оценки операционного риска является динамическое изменение индекса Алговера (ИА) – увеличение индекса в динамике коррелировало с неблагоприятным исходом (rho = 0,65, p< 0,001).
В контрольной группе (2009-2011 г) использовали традиционную активную хирургическую тактику- при неустойчивом эндоскопическом гемостазе или при рецидиве кровотечения –хирургическое лечение.
Всем больным при эзофагодуоденоскопии с ЖКК проводили оценку кровотечения поJ.Forrest.Ориентировочную степень кровопотери на момент госпитализации определяли по индексу Алговера. Для стратификации больных по степени риска рецидива кровотечения (от 4 до11 баллов) использовали прогностическую шкалу Rockall. К группе высокого риска рецидива кровотечения относили пациентов, набравших 6 и больше баллов.
В основной группе (192 б-х) эндоскопический гемостаз у больных с язвеннымгастродуоденальным кровотечением сопровождался обязательной внутривенной инфузией ингибиторов протоннойпомпы (нексиумболюсно160 мг, затем 8-12 мг/ч в течение 72 часов).
При ангиографии в 58% наблюдениях использовали подмышечный доступ, в 27% –феморальныйи в 15% –радиаль-ный доступ. Выполнялась последовательно селективная и суперселективная катетеризация селезеночной, левой желудочной, гастродуоденальной артерии (ГДА) и ее ветвей–a. pancreaticoduodenalis sup. ant. et post. И ветви верхней брыжеечной артерии – a.pancreaticoduodenalis inf. ant. et post . При этом выявляли прямые и косвенные признаки кровотечения: экс-травазацию контрастированной крови, тромботическую окклюзию сосудов, регионарный артериальный спазм, аневризмы ветвей чревного ствола, а также признаки локальной гиперваскуляризации и периартериальной диффузии контрастированной крови. Для исключения «слепой» эмболизации, во время гастродуоденоскопи и метили сточник кровотечения клипсами, которые являлись «дорожной картой», что значительно облегчало поиск заинтересованной артерии при отсутствии прямых признаков кровотечения. С целью эндоваскулярной окклюзии использовались стентграфт, микроспирали Гиатур-ко, микросферы (размером от 300 до500 мкм), сферические и цилиндрические эмболы «Эмбокс-Ц» и «сэндвичи» (спирали Гиантурко с микросферами).
Результаты и их обсуждение
Эндоскопический гемостаз был первым в линии выбора лечебной тактики у наших пациентов с ЖКК. Рецидив ЖКК в первые трое суток был связан с трудностями эндоскопического гемостаза и не соблюдением протокола по блокаде протонного насоса. Повторные попытки эндоскопического гемостаза предпринимали только у крайне тяжелых больных и при очень высоком риске оперативного вмешательства. Хирургическое лечение в контрольной группе было вторым методом выбора после эндоскопического гемостаза, что улучшало эффективность у данных пациентов, однако в показателях летальности уменьшения не наблюдали.
При первичном эндоскопическом вмешательстве устойчивый гемостаз наблюдали у 21(11,0%) пациента. Повторные эндоскопические вмешательства выполнены у 142 (74,0%) больных.
У пациентов основной группы после эндоскопического гемостаза, терапия высокими в/в дозами ингибиторов протонной помпы (нексиум 160 мг болюсно и далее 8 мг/ч) существенно снизило частоту рецидивов, но не имело существенного эффекта относительно смертности.
В основной группе, особенно у пожилых пациентов, после эндоскопического лечения гемостаз достигнут у 87,0%. Неконтролируемые кровотечения по нашим данным составили около 13% наблюдений. При возникновении рецидива жизненные показатели часто были нестабильны, и в результате, вторичное эндоскопическое исследование под наркозом провести было трудно, тем более выполнить хирургическое вмешательство.
Из 192 больных основной группы у 32(16,7%) рецидив кровотечения или его высокий риск являлись показанием к проведению транскатетерной артериальной эмболизации (ТАЭ) – в течение 12-36 ч с момента остановки кровотечения.
Наблюдение №1: Б-й С., 43 лет, поступил в клинику 04.06.2014г. с жалобами на слабость, рвоту с примесью крови, черный стул, сильное головокружение. Из анамнеза: 5 лет тому назад ему была выполнена панкреатоцистоеюностомия по поводу кистозного панкреатита.Hb при поступлении 59,2 г/л. При ЭГДС обнаружена кровоточащая язва на задней стенкелу-ковицы двенадцатиперстной кишки.Оценка по ForrestIA. Под наркозом выполнен эндоскопический гемостаз. Рецидив кровотечения через 2 часа. Повторный эндоскопический гемостаз неэффективен. Проведена попытка артериальной эмболизации, которая технически не увенчалась успехом. Больному выполнена экстренная операция- технически сложная гастродуо-денотомия (за месяц до поступления больному была выполнена операция – ушивание кровоточащей язвы двенадцатиперстной кишки в районной больнице Подмосковья). На операции с трудом удалось выделить антральный отдел с луковицей 12 п.к. Проведено ушивание кровоточащей язвы 12-перстной кишки. В послеоперационном периоде через 3 суток у больного возникла несостоятельность в области дуоденопластики с формированием свища. Через 5 суток возник повторный рецидив профузного дуоденального кровотечения. Состояние больного тяжелое. Индекс Алговера 1,2. В связи с нестабильной гемодинамикой и техническими сложностями при выполнении предыдущей операции с развитием несостоятельности дуоде-нопластики, а также значительными трудностями предстоящей операции, больному решено повторить ангиографию чревного ствола с эндоваскулярным гемостазом.Выполнена селективная ангиография из левого подмышечного доступа (ориентиром для селективной катетеризации были клипсы, установленные при гастроскопии) с эмболизацией микросферами ПВА Cook (рис.1), которая на этот раз оказалась успешной (рис. 2, 3). Кровотечение остановилось и больной был переведен в профильное хирургическое отделение. После выполнения эмболизации больному проводили консервативную инфузионную, противо- язвенную (нексиум 160мг\сут) терапию, гемотрансфузии. На фоне проводимого лечения рецидивов кровотечения не было. Свищ закрылся на 14 день.
Приведенное наблюдение свидетельствует о том, как ТАЭ оказалась эффективным альтернативным методом лечения у пациента с рецидивом после эндоскопического и хирургического лечения.
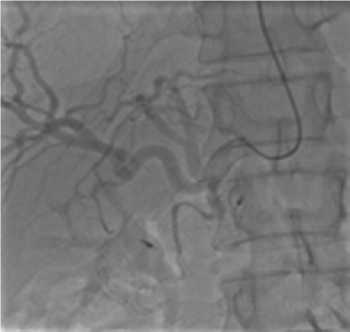
Рис. 1. Диагностический проводник селективно проведен в a.gastroduodenalis.На рисунке видны клипсы («дорожная карта»), установленные в ходе выполнения эндоскопического гемостаза, которые позволяют определить место кровотечения и кровоснабжающую артериальную ветвь
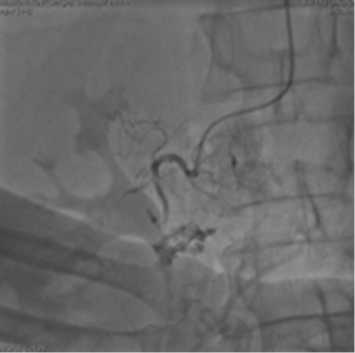
Рис. 2. Селективная катетеризация a. gastroduodenalis . Экстравазация контраста
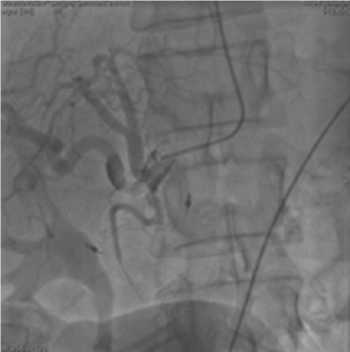
Рис. 3. Ангиограмма после эмболизациимикросферами.Экстравазата нет
Наблюдение №2: Больной Г., 64 л., находился на лечении с 11.01.14 по 28.01.14.Поступил 11.01.14 с жалобами на одышку, сухой кашель, отеки рук и ног, увеличение живота. Со слов больного, длительное время страдает ишемической болезнью сердца и бронхиальной астмой, сахарным диабетом 2 типа. Жалобы беспокоят в течение недели. Госпитализирован в кардиологическое отделение, проводилось лечение. 18.01.14 у больного появилась клиника желудочно-кишечного кровотечения, выполнена ЭГДС: источником кровотечения является острая язва передней стенки луковицы 12-перстной кишки. Попытка эндоскопического гемостаза неэффективна. Выполнена операция: Лапаротомия, дуоденотомия, прошивание язвы 12-перстной кишки, назоинтестинальное дренирование, дренирование брюшной полости. Диагноз: острая язва луковицы 12-перстной кишки, осложненная кровотечением. Послеоперационный период протекал тяжело, проводилась комплексная интенсивная терапия в отделении реанимации. 27.01.14 у больного возник рецидив кровотечения из верхних отделов желудочно-кишечного тракта. При диагностической ЭГДС определено, что источником рецидивного кровотечения является язва луковицы 12-перстной кишки. Учитывая тяжелое состояние больного, ранее выполненный эндоскопический гемостаз и прошивание острой язвы луковицы 12-перстной кишки, решено выполнить эндоваскулярный гемостаз. Выполнена ангиография, целиакография, селективная катетеризация желудочно-двенадцатиперстной артерии (рис. 4) с эмболизацией микроспиралью Гиантурко (рис. 5).
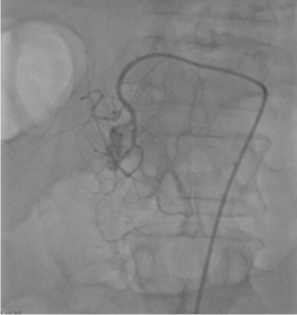
Рис. 4. Экстравазация контраста в зоне язвенного дефекта 12-перстной кишки
Несмотря на проводимую консервативную терапию, прогрессировала сердечно-сосудистая недостаточность и 28.01.14 больной умер. На секции: признаков повторного рецидива желудочно-кишечного кровотечения не обнаружено. У больного с ИБС, сахарным диабетом II типа смерть наступила от острой сердечно-сосудистой недостаточности.
Это наблюдение демонстративно тем, что у пожилого муль-тиморбидного больного была выбрана некорректная тактика. После безуспешного эндоскопического гемостаза, необходимо было применить эндоваскулярный гемостаз. Выполненная
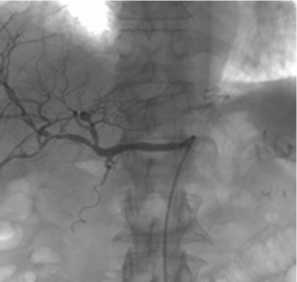
Рис. 5. Ангиограмма после эмболизации a. gastroduodenalis микроспиралью Гиантурко операция усугубила состояние тяжелого больного и привела к негативному исходу.
В контрольной группе (до 2012 г) оперировано 39 (37,9%) больных. Стандартным вмешательством при желудочнокишечном кровотечении являлось прошивание или иссечение кровоточащей язвы,селективной ваготомией(дуоденальная язва) с вариантами дренирующих операций.
В основной группе (с 2012 г) показанием к операции являются такие ЖКК, когда с помощью эндоскопического гемостаза и транскатетерной артериальной эмболизации невозможно было добиться дефинитивного гемостаза.
При рецидиве ЖКК (на 3-5 сутки) повторяли эндоскопический гемостаз с обязательным назначением ингибиторов протонной помпы. В случае нестабильной гемодинамики применяли ТАЭ. При отсутствии успеха больного оперировали.
Мы не сравнивали ТАЭ и хирургические вмешательства в лечении массивных ЖКК из-за сложностей проведения контролируемого исследования в экстренных условиях. Тем не менее, использование ТАЭ поддержано высоким уровнем технического и клинического успеха. Очевидное преимущество ТАЭ состоит в миниинвазивности, исключении наркоза, лапаротомии у критических больных, уменьшающейся смертности и инфекционных осложнений. Успешная эмболизация(прекращение кровотечения -клинический эффект) составила 93%. Выбор ТАЭ как альтернативу в лечении ЖКК после эндоскопической неудачи позволяет сделать выбор в том случае, когда хирургическое лечение будет более сложным, особенно у пациентов с факторами риска рецидива кровотечения и смертности, которые также относятся к пациентам высокого операционного риска. В большинстве наблюдений, эмболизация уменьшает необходимость хирургического вмешательства у больных, чье выживание зависит от сопутствующих заболеваний.
Гистологические исследования после эндоскопического исследования показали, что изменения слизистой наблюдались как в области язвы, так и на расстоянии в зависимости от диаметра эмболизированной артерии и развитости коллатералей.
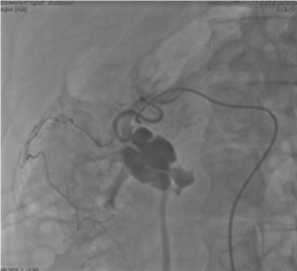
Рис. 6. Экстравазация контрастного вещества с контрастированием ложной кисты головки поджелудочной железы.
При локализации язвы в 12-перстной кишке на передней или боковой стенках основным вариантом операции было иссечение кровоточащей язвы, а при локализации источника кровотечения на задней стенке – прошивание язвы с экстрадуоде-нальной лигатурой a. gastroduodenali s у 5 больных, а ставшую настоящим раритетом ваготомию применяем крайне редко.
Таким образом, в результате применяемого лечебного алгоритма экстренное оперативное вмешательство потребовалось у 7,8% пациентов.
Источниками кровотечения при кистозном панкреатите у 3 больных была селезеночная артерия и у 5-х больных ветви гастродуоденальной артерии.
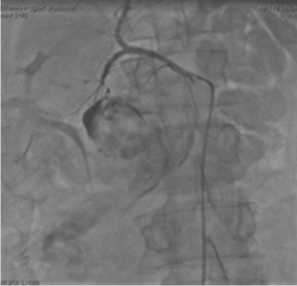
Рис. 7. Эмболизации спиралями и микросферами («сэндвич»). Отмечается полное прекращение кровотечения в кисту
Наблюдение №3: Больной Е., 43 л, поступил 29.01.14 с жалобами на тошноту, рвоту, боли в эпигастральной области. Болеет около 3 дней, когда после нарушения диеты появились тошнота, рвота, боли в животе. Злоупотребляет алкоголем, страдает хроническим панкреатитом. 03.02.14 у больного возникла клиника внутрибрюшного кровотечения, по этому поводу в срочном порядке выполнена операция: лапаротомия, вскрытие псевдокисты головки, остановка кровотечения, дренирование. 16.02.14 у больного возникповторный рецидив кровотечения в псевдокисту головки поджелудочной железы с прорывом в 12-ти перстную кишку (рис. 6). Учитывая тяжесть состояния пациента и ранее выполненную операцию, решено выполнить ангиографию с эмболизацией. Выполнена рентгенэндо-васкулярная окклюзия ветвей гастродуоденальной артерии (а. pancreatoduodenalis sup. ant. et post.) (рис. 7). От дальнейшего лечения отказался. Выписан с рекомендациями контрольной явки для решения вопроса об оперативном лечении.
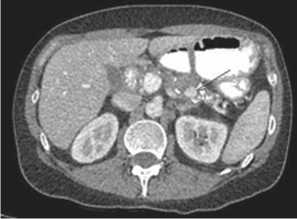
Рис. 8. СКТ-признаки хронического кальцифицирующего панкреатита, мешотчатая аневризма селезеночной артерии
Наблюдение №4: Больная В., 46 лет, поступила в ГКБ №7 30.05.14 с жалобами на тупую боль в эпигастрии, слабость, тошноту, рвоту. Считает себя больной в течение 2 недель, когда отметила появление болей в эпигастрии, а также стула темновишневого цвета. При обследовании установлено, что у больной (по данным ультразвукового исследования органов брюшной полости) имеется псевдокиста хвоста поджелудочной железы с признаками кровотока в ней, а также (данные эзофагогастродуоденоскопии) гемобилия. При поступлении в стационар состояние больной средней тяжести, кожные покровы бледные. Уровень гемоглобина крови – 84г\л. Выполнена компьютерная томография органов брюшной полости, на которой установлено, что у больной имеются признаки хронического кальцифицирующего панкреатита, а также мешотчатая аневризма селезеночной артерии (рис 8, 9).Удалось добиться эффективного эндоваскулярного гемостаза. За время наблюдения данных за рецидив кровотечения не получено. Также не было данных за ишемическое поражение органов брюшной полости (за счет эмболизации ствола артерии) (рис. 10). Больная подготовлена к операции: лапаротомия, резекция тела-хвоста поджелудочной железы со спленэктомией. Интраоперационно установлено, что кровоток в полость псевдокисты поджелудочной железы отсутствует.
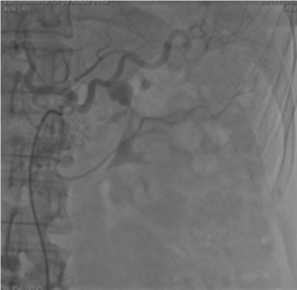
Рис. 9. В проекции поджелудочной железы контрастируются две полости, кровоснабжаемые из селезеночной артерии
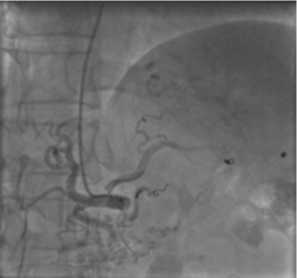
Рис. 10. Суперселективная катетеризация селезеночной артерии, окклюзия артерии спиралями Гиантурко
Хирургическая тактика при неварикозных ЖКК, применяемая нами в течение последних лет, совпадает с принципами лечения гастродуоденальных кровотечений, которые представлены в Международном Консенсусе (2010 год) по ведению больных с язвенным кровотечением.
Изменение хирургической тактики лечения ЖКК привело к снижению послеоперационной летальности с 22,9% в 20092011 гг. до 6,5% в 2012-2014 гг.
Выводы
Неудачная либо неприменимая эндоскопия у гемодинамически нестабильных пациентов, должна предполагать срочную транскатетерную артериальную эмболизацию, тогда как реэндоскопия должна быть применена в первую очередь у стабильных пациентов.
Список литературы Транскатетерная артериальная эмболизация при кровотечениях из верхних отделов желудочно-кишечного тракта
- Defreyne L., Vanlangenhove P, De Vos M. Embolization as a first approach with endoscopic allyunmanageable acute nonvariceal gastrointestinal hemorrhage.//Radiology, 2001, 218, 739-748.
- Loffroy R., Guiu B. Role of transcatheter arterial embolization for massive bleeding from gastroduodenal ulcers.//World J Gastroenterol 2009 December 21; 15(47): 5889-5897.
- National Institute for Health and Clinical Excellence (2012) Acute upper gastrointestinal bleeding: management. . London: National Institute for Health and Clinical Excellence.
- Восканян С.Э., Каркищенко В.Н., Колышев И.Ю., Шабалин М.В., Марисов Л.В. Лазерные технологии в медицине//Спортивная медицина: наука и практика. 2014. №3. С. 62-71
- Литвиненко А.С., Добровольский О.Б., Куршев В.В., Веселова Л.В., Дятчина Г.В. Влияние экстракорпоральной ударно-волновой терапии на динамику болевого синдрома у спортсменов при заболеваниях опорно-двигательного аппарата//Спортивная медицина: наука и практика. 2014. №2. С. 32-41
- Безуглов Э.Н., Ачкасов Е.Е., Усманова Э.М., Куршев В.В., Султанова О.А., Заборова В.А., Суворов В. Г., Седерхольм Л. А. Применение тромбоцитарных факторов роста при лечении повреждений латеральных связок голеностопного сустава у футболистов//Спортивная медицина: наука и практика. 2013. №1. С. 31-35
- Lang D, Teo EK, Tan A, Ibrahim S, Tan PS, Ang TL, Fock KM. A comparison of surgery versus transcatheter angiographic embolization in the treatment of nonvariceal upper gastrointestinal bleeding uncontrolled by endoscopy.//Eur J. Gastroenterol Hepatol 2012; 24: 929-938.
- Barkun A, Sabbah S, Enns R. The Canadian Registry on Nonvariceal Upper Gastrointestinal Bleeding and Endoscopy (RUGBE): Endoscopic hemostasis and proton pump inhibition are associated with improved outcomes in a real-life setting.//Am J. Gastroenterol 2004;99:1238-46.
- Sheasgreen Ch., Leontiadis Grigorios I. Recent advances on the management of patients with non-variceal upper gastrointestinal bleeding.//Annals of Gastroenterology (2013) 26, 191-197.
- Loffroy R., Estivalet L., Cherblanc V., Sottier D., Guiu B., Cercueil J.-P., Krause D. Transcatheter embolization as the new reference standard for endoscopically unmanageable upper gastrointestinal bleeding.//World J GastrointestSurg 2012 October 27; 4(10): 223-227.
- Liou T.C., Lin S.C., Wang H.Y., Chang W.H. Optimal injection volume of epinephrine for endoscopic treatment of peptic ulcer bleeding.//Wld J. Gastroenterol., 2006, 12,3108-3113.
- Cheynel N., Peschaud F., Hagry O. Bleeding gastroduodenal ulcer: results of surgical management.//Ann. Chir., 2001, 126, 232-235.
- Квашин А.И., Атаманов С.А., Мельник А.В., Быков А.О., Пом-кин А.А., Ширкин М.Г., Портнягин А.Ф., Пачерских Ф.Н. Эндоваскулярный гемостаз при дуоденальном кровотечении.//Международный журнал интервенционной кардиоангиологии. 2012. №31. С.19-25.
- Barkun A.N, Bardou M, Ernst J. International consensus recommendations on the management of patients with nonvariceal upper gastrointestinal bleeding.//Ann Intern Med 2010;152:101-113.
- Yong-Li Wang, Ying-Sheng Cheng, Li-Zhen Liu, Zhong-Hui He and Kun-Hong Ding. Emergency transcatheter embolization in patients with acute massive duodenal ulcer bleeding.//World J Gastroenterol. 2012 September 14; 18(34): 4765-4770.


