Транскраниальная электроимпульсная терапия в лечении хронического болевого синдрома
Автор: Крайнюков П.Е., Ким Е.А., Гудантов Р.Б., Мезникова А.В., Борисова А.В., Зыкова В.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Обзоры литературы
Статья в выпуске: 4 т.19, 2024 года.
Бесплатный доступ
Обоснование: хронический болевой синдром у пациентов с комбинированными минно-взрывными травмами, травматическими ампутациями конечностей, обширными ожогами и пр. в настоящее время особенно актуален. Представлен анализ современных литературных данных по электрофизиотерапии хронической боли, который позволит выбрать оптимальный метод лечения данной категории пациентов.Цель: изучить литературные данные и провести сравнительный анализ используемых в настоящее время методов транскраниальной электрофизиотерапии болевого синдрома, что позволит улучшить результаты лечения пациентов с хроническим болевым синдромом.Материалы и методы: выполнен анализ статей, обзоров, исследований в современной научной медицинской литературе по проблеме. Сбор материалов проводился в электронных библиотеках ВМедА им. С.М.Кирова, Первого МГМУ им. И.М.Сеченова, использованы статьи информационных ресурсов: NCBI, PCM; Springer; Elsevier, EMBASE, Web of Science и PsychINFO, Elibrary и др.Результаты: в литературе выявлено большое многообразие методов транскраниальной электрофизиотерапии, используемых в клинической практике в терапии хронического болевого синдрома. Методы систематизируются на основании: характера вмешательства (инвазивные, неинвазивные), параметров электрического тока (постоянный, переменный, непрерывный или импульсный).Заключение: методы неинвазивной транскраниальной электрофизиотерапии могут быть более эффективными и предпочтительными для лечения хронического болевого синдрома по сравнению с другими методами по ряду причин: неинвазивность, безопасность, простота, снижение боли за счет регуляции нейропластичности, регуляция эмоционального состояния.
Транскраниальная электроимпульсная терапия, электрофизиотерапия, электросон, транскраниальная электростимуляция, болевой синдром, ноцицепторы, нейропластичност
Короткий адрес: https://sciup.org/140308705
IDR: 140308705 | DOI: 10.25881/20728255_2024_19_4_125
Transcranial electric pulse therapy in the treatment of chronic pain syndrome
Rationale: chronic pain syndrome in patients with combined mine-explosive injuries, traumatic limb amputations, extensive burns, etc., is currently especially relevant. The presented analysis of modern literature data on electrophysiotherapy of chronic pain in this category of patients.Objective: to study the literature data and conduct a comparative analysis of the currently used methods of transcranial electrophysiotherapy of pain syndrome, which will improve the results of treatment of patients with chronic pain syndrome.Materials and methods: the analysis of articles, reviews, and studies in the modern scientific medical literature on the voiced problem is carried out. The collection of materials was carried out in the electronic libraries of the kirov university, the first sechenov Moscow state medical university, articles from information resources were used: ncbi, pcm; springer; elsevier, embase, web of science and psychinfo, elibrary, etc.Results: a wide variety of transcranial electrophysiotherapy methods used in clinical practice in the treatment of chronic pain syndrome has been revealed in the literature. The methods are systematized based on: the nature of the intervention (invasive, non-invasive), the parameters of the electric current (direct, alternating, continuous or pulsed).Conclusion: methods of noninvasive transcranial electrophysiotherapy may be more effective and preferable for the treatment of chronic pain syndrome compared to other methods for a number of reasons: noninvasiveness, safety, simplicity, pain reduction due to regulation of neuroplasticity, regulation of emotional state.
Текст обзорной статьи Транскраниальная электроимпульсная терапия в лечении хронического болевого синдрома
электричестве и физиологии в 1902 г. объединили экспериментальные исследования французского физика S.A.N. Leduc (1853–1939 гг.) с воздействием электричества на головной мозг. Опытным путем он определил наиболее эффективный импульсный ток частотой 100 ГЦ, с интервальным межимпульсным соотношением прямоугольной формы 1:10. При апробации действия электронаркоза на себе он позже охарактеризовал состояние «как во сне – ни двигаться, ни говорить не мог». Исторически это явление «электросна» получило название «ток Ледюка». Изыскания S.A.N. Leduc исходят из теории отечественного физиолога, создателя науки о высшей нервной деятельности, «отца» отечественной физиологической школы – И.П. Павлова, который считал, что внутреннее

торможение и сон являются единым процессом по своей организации, с разницей, что внутреннее торможение охватывает лишь отдельные группы клеток головного мозга, а при развитии сна торможение распространяется по коре головного мозга и спускается в подкорковые образования [4]. И.П. Павлов назвал активным сон, развивающийся при воздействии тормозных условных раздражителей, противоположным ему является пассивный сон, возникающий в результате прекращения или резкого ограничения афферентных импульсов в кору больших полушарий [5]. Вплоть до 50-х гг. прошлого столетия исследование электроимпульсной стимуляцией головного мозга человека продолжалось в основном отечественными учеными: А.Т. Болотовым, А.Е. Щербаком, Ф. Белявским, О. Ковалевским, А.Н. Обросовым, В.Г. Ясногородскими др. В 1967 г. в г. Граце (Австрия), состоялся первый симпозиум по электросну и электроанестезии, где было высказано мнение, что электросон на самом деле не вызывает сон, а является побочным действием тормозного эффекта электростимуляции. Поэтому название электросна было изменено на краниальную электростимуляционную терапию (CET). В 1969 г. был принят термин – трансцеребральная электротерапия (TCET), которую впоследствии переименовали в краниальную электротерапию Cranial Electrotherapy Stimulation (CES).
В результате двадцатилетних исследований на базе Института физиологии им. И.П. Павлова РАН, в начале 1980-х гг. группа отечественных ученых (Ковалевский А.В., Газеева И.В., Гайсина А.В. и др.) под руководством профессора В.П. Лебедева, совершили прорыв в мировой электрофизиологии, открыв селективную активацию антиноцицептивных систем головного мозга под влиянием электрического тока.
Используемые методики электрофизиотерапии в мире при лечении болевого синдрома.
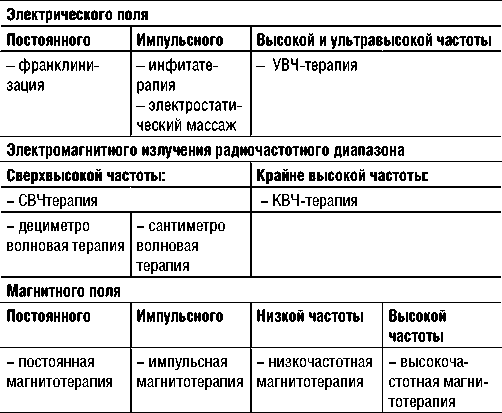
В современной медицине реформация методик электротерапии болевого синдрома происходит параллельно с учением о патофизиологии боли, и определяет направленность терапии, исходя из важнейших параметров электрического тока (постоянный, переменный, непрерывный или импульсный) [6; 7], табл. 1:
К примеру, супрессия возбудимости ноцицепторов, в т.ч. и их проводников, реализуется с помощью методики электрофореза локальных анестетиков, ультразвука (при определенных условиях). Подавление возбудимости ноцицептивных волокон происходит при помощи лазеротерапии, анодной гальванизации и др. [8]. Обезболивающие действия вторичного характера, отчетливо наблюдаются при использовании лечебных физических факторов (локальный холод, инфракрасное излучение, тепло, сверхвысокочастотные электромагнитные потоки и др.), с влиянием на звенья патогенеза физических причин болевой реакции – увеличение чувствительности ноцицепторов, развитие периневрального отека с локализацией алгоген-ных медиаторов (гистамин, серотонин, ацетилхолин, про-
Табл. 1. Методы применения электрического тока в клинической физиотерапии [7]
Постоянный электрический ток
Непрерывного действия: Импульсного действия:
– гальванизация
– лекарственный электрофорез
– электросонтерапия
– транскраниальная электроанальгезия
– электростимуляция
– диадинамотерапия
– короткоимпульсная электроанальгезия
Переменного электрического тока
Низкой частоты:
Средней частоты:
– местная дарсонвализация
– амплипульстерапия
– интерференцтерапия
– флюктуоризация
– ультратонотерапия
стагландины, субстанция Р, нейрокинин А и др.). В 1965 г. Р. Мезлак (с соавт.) представили теорию «входных ворот», где отмечается система контроля афферентных входов через обратные связи; как механизм, реализующего обезболивающее действие. Через влияние на «входной блок,» предложены методики: диадинамического тока, акупунктурная анальгезия, короткоимпульсная электроаналгезия (чрескожная электронейростимуляция, и др.) [9].
Стимуляция электроимпульсами головного мозга или транскраниальная электроимпульсная стимуляция представлены, исходя из инвазивного и неинвазивного характера вмешательства.
Инвазивные методы предусматривают электродную имплантацию в ткань головного мозга:
-
• Глубокая стимуляция мозга (DBS) – воздействие на активирующие нейроны центров боли перивен-трикулярное и периакведуктальное серое вещество (PVG/PAG) и ростральную переднюю поясную кору (ACC) высокочастотными электрическими импульсами [10]. В терапии фантомной боли, при ампутациях конечностей, описаны положительные результаты при электростимуляции таламической области (DBS), Abreu et al. указывают на снижение болевого синдрома

у пациентов в диапазоне от 50,6 до 76,4%, участвовавших в исследовании [11].
-
• Стимуляция моторной коры (MCS) – электронейростимуляция, путем расположения активного электрода в прецентральной извилине или центральной борозде. В зависимости от расположения электрода в анатомическом пространстве головного мозга выделяют два метода MCS – субдуральная MCS и эпидуральная MCS. Первые сообщения об успешном клиническом использовании MCS при хронической боли датируются началом 1990-х гг. [12]. И хотя точный механизм анальгетического действия остается не до конца понятными, метод MCS хорошо описан в терапии хронических болевых состояний (центральную постинсультная боль (CPSP), тройничная невралгия, спинальная посттравматическая боль и пр. [13].
Ряд исследований, связанных с инвазивными методиками в терапии болевого синдрома, показали неблагополучные результаты или даже были остановлены до полного сбора данных [14]. Инвазивность в структуры головного мозга предполагает определённый риск осложнений, негативных эффектов: судорожный синдром (18%), раневые инфекции (12%), кровотечения, эпидуральные гематомы и дуральные рубцы [6].
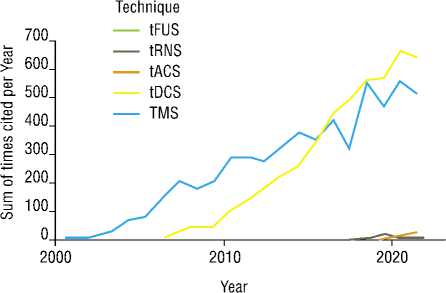
По данным анализа зарубежных источников Xiong H.Y. еt al. (2022) показательна прогрессия за последние 20 лет актуальности и востребованности проблем по исследованию неинвазивных транскраниальных мето-дик(NIBS) в терапии хронической боли (Рис. 1).
Развитие анальгетического эффекта электростимуляции NIBS многоуровневое: с активацией на нейрональном уровне нейрогуморальных связей – синаптических нейромедиаторов, на сетевом межклеточном уровне нейронных цепей, изменяется нейропластичность, дисбаланс возбуждения и торможения нервных центров при передаче и обработке болевого импульса[10]. Perocheau D., и соавт. (2014) в своем исследовании по нейровизуализации боли показали взаимосвязь хронической боли с изменениями в нейронных сетях, включая пути восприятия, сенсибилизации и регуляции боли.
Неинвазивные методы опосредованы чрескожной электростимуляцией:
-
• транскраниальная стимуляция постоянным током (tDCS). Основа метода –электромодуляция нейрональных центров под воздействием импульсов постоянного тока низкой амплитуды (от 0,5 до 2 мА). Импульсы постоянного тока подаются через кожные электроды (анодный, катодный) [16]. В tDCS используется слабый ток, не вызывая потенциалов действия, но меняя потенциал покоя мембраны нейронов. При анодной стимуляции возникает деполяризация клеточной мембраны, увеличивая возбудимость коры головного мозга, катодная – гиперполяризует мембрану нейрона и подавляет возбудимость [17]. Однако, описанные изменения в мембранном потенциале окончательно не объясняют наблюдаемый стойкий анальгетический эффект [18]. В работе Lefaucheur J.P. и соавт. (2017) описывается tDCS влияние на межнейрональном уровне. Авторы отметили фоновую медиаторную активность серотонина, дофамина, ацетилхолина, клеточных мембранных каналов, натрия и кальция с возникновением tDCS зависимой аналгезии на уровне межсинаптических связей «кора-кора» и «кора-подкорка» при воздействии на таламические центры [19].
-
• Транскраниальная стимуляция переменным током (tACS). Особенность переменного тока – изменение направления и величины в единицу времени, по закону синуса графически отображается как синусоида Возможность синусоидальной стимуляции с фиксированной амплитудой и частотой методологически описывается в регуляции интенсивности болевого синдрома [20]. В межнейрональном взаимодействии направленные ионные токи через синапсы происходят в определенных ритмических электроимпульсных колебаниях, (мозговые волны) с параметрами частоты от 0,02 до 600 Гц. Альфа-активность (8–12 Гц), дельта (1–4 Гц), тета (4–8 Гц), мю (8–13 Гц), бета (13–30 Гц), гамма (30–150 Гц). Arendsen L.J. и соавт. (2018) в исследовании по взаимосвязи между альфа-активностью и
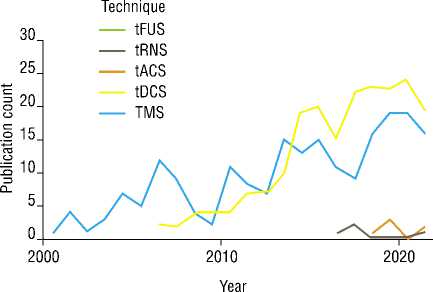
Рис. 1. Количество исследований за последние 20 лет по изучению NIBS в терапии хронической боли [15].

болью, определили возможность tACS в подавлении боли и подтвердили, что супрессия нейронных колебаний в альфа– и гамма – диапазонах при болевой стимуляции могут регулировать восприятие боли, но только когда интенсивность и вероятность предстоящего болевого стимула была в эксперименте неизвестна [20]. Метод tACS пока представлен в экспериментальной медицине.
Повторная транскраниальная магнитная стимуля-ция(rTMS) основана на способности динамических магнитных полей индуцировать электрическую активность, и позволяет воздействовать на определенные нейрональные локусы и группы коры головного мозга и межнейронных сетях. При этом магнитная стимуляция может в достаточной степени деполяризовать нейроны вызывая потенциалы действия. Такая эффективность импульсной магнитной рестимуляции имеет накопительный характер. Посредством регулярного, повторного воздействия активизируется большее количество нейронов, развиваются кумулятивные изменения нейропластичности с повышением уровня эндогенных опиоидов. В настоящее время оказываемый анальгетический эффект rTMS указан многими авторами в качестве дополнительного метода лечения у пациентов с хроническими рефрактерными болевыми синдромами, после инсульта (таламическая/стволовая), при травмах и невропатиях периферического генеза [21]. Перспективное значение rTMS описывается во множестве представленных источниках.
Краниальная электротерапия (CES) – метод с минимальным уровнем побочных эффектов, одобрен международными сообществами для лечения боли, депрессии, тревожного расстройства и бессонницы. CES до сих пор называют электросном в некоторых регионах мира. В настоящее время большинство устройств CES ограничивают интенсивность стимула до менее 1,0 миллиампера при 0,5 или 100 Гц от источника 9 вольт. CES не обеспечивает достижения глубокого сна, но положительная эффективность описывается в независимости от бодрствования пациентов. Чрескожное воздействие импульсного электрического напряжения низкой амплитуды (<1 мА), в одних методиках выполнялось через электроды, наложенные на мочки ушей [22]. Другими авторами транскраниальная стимуляция осуществлялось с помощью постоянного импульсного тока низкой частоты (1–150 Гц) и малой силы (до 10 мА) при глазнично-сосцевидном или лобно-сосцевидном расположении электродов [23]. Исследования показали, что CESповышает уровни нейромедиаторов в крови (бета-эндорфин, серотонин), и действует через подкорково-стволовые образования, расположенные вблизи основания мозга, а именно: таламус, гипоталамус, гипофиз, ретикулярная формация ствола, лимбическая система [24]. Результаты такого муль- тилокального действия в виде седативного, обезболивающего эффекта, снижение поведенческих реакций на хроническую боль (эмоциональная лабильность, депрессия, улучшение когнитивных функций) указаны в терапии хронической боли (фибромиалгия, нейропатическая боль после травмы спинного мозга и др.) [25]. Также CES импульсные токи оказывают нормализующее действие на сердечно-сосудистую систему в целом, улучшая центральную гемодинамику, микроциркуляцию, благоприятно воздействует на психологический и неврологический статус больных, перенесших церебральный инсульт. Выделяют 3 эффективных диапазона частот CES [26]: малые (5–12 Гц) оказывают седативное, успокаивающее действие, с восстановлением баланса процессов торможения/возбуждения, и влияют на выработку серотонина; средние (70–80 Гц) оказывают анальгези-рующее действие при хронических болях, повышают уровень эндогенных опиатов, дофамина, адреналина, норадреналина; высокие (90–120 Гц) оказывают транквилизирующий, гипотензивный и седативный результаты. На частотах 90–120 Гц электроимпульсы стимулируют работу гипофиза, вызывая повышение секреции адренокортикотропного гормона. Taylor A.G. и соавт. (2013) в рандомизированных, двойных слепых, контролируемых клинических исследованиях указали эффективную анальгезию CES у пациентов с фибромиалгией [27], Tan G. и соавт. (2011) – при травматической невропатической боли спинного мозга [28], Barclay T.H. и соавт. (2014) – у пациентов с тревожным расстройством и коморбидной депрессией [29].
-
• Транскраниальный фокусированный ультразвук (tFUS). Сравнительно новая методика описывается в двух режимах – высокоинтенсивный (HIFU) (с энергией более 5 Вт/см2) и низкоинтенсивный (LIFU) (с энергией 0,125–3,0 Вт/см2) фокусированный ультразвук [30]. HUFI описан в терапии болевого синдрома радикального или паллиативного лечения больных с опухолевыми новообразованиями различной локализации. Действие HUFI основано на 2 интерстициальных механизмах в фокусированной зоне действия: термическая абляция (превращение механической энергии в тепловую) и акустическая кавитация [31]. По характеру действия на клетки ультразвук низких интенсивностей обладает энергетическим влиянием в меньшей степени, чем высокой, однако такая ультразвуковая энергия (1–3 МГц; 0,2–0,6 Вт/см2; 0,5–5 мин.) усиливает скорости циркуляции крови в тканях, повышает температуру тела на 0,5–1,5 °С, увеличивает проницаемость клеточных мембран с эффектом до 6–10 час. Tyler W.J. (2011) также отметил влияние низкоинтенсивного ультразвукового излучения на акустически зависимую проницаемость мембранных ионных (кальциевых, натриевых и калиевых) каналов нейронов [32]. Высокая пространственная точность
LIFU позволяет использовать акустическую энергию для обратимой модуляции активности глубоких структур мозга [33]. Badran B.W. и соавт. (2020) продемонстрировали возможность методом LIFU влиять на болевую чувствительность при воздействии на таламус под контролем МРТ, с точкой фокуса на правую переднюю часть таламуса у 19 добровольцев, и отметили, что два 10-минутных сеанса оказывали антиноцицептивный эффект на болевую стимуляцию по сравнению c плацебо [34].
-
• Неинвазивная кортикальная электростимуляция со сниженным сопротивлением (RINCE). Основное отличие от других методов состоит в том, что используются определенные частоты тока, которые, за счет пониженного сопротивления кожи и свода черепа, обеспечивают более глубокое проникновение в кору головного мозга [35] для низкочастотной кортикальной модуляции, и как полагают, повышает передачу сигнала и эффективность стимуляции [36]. Неинвазивная кортикальная электростимуляция у пациентов с фибромиалгией обеспечивала умеренное улучшение боли, утомляемости и сна и лечение хорошо переносилось [37]. При наблюдении за пациентами с фибромиалгией, прошедших курс RINCE, в отдаленном периоде отмечалось значительное улучшение [38].
-
• Транскраниальная случайная шумовая стимуляция (tRNS). Принцип стохастического резонанса в переменном токе, используемый в методике tRNS [39] активизирует процессы возбуждения коры головного мозга, где случайная генерация частот от 0 до 640 Гц повышает возбудимость моторных отделов коры головного мозга [40; 41]. Доказательства, подтверждающие эффективность tRNS как единственного вмешательства для лечения хронической боли в настоящее время ограничены [42].
Основное направление в настоящее время занимают методы транскраниальной электростимуляции с преимущественным низкочастотной импульсной сложномоду-лируемой модуляцией, исходя из ее преимущественных характеристик: близость к физиологичной электро-импульсной активности головного мозга, сниженным сопротивлением тканей, отсутствием раздражения кожи, доминирующая эффективность анальгезии за счет ритмичности и упорядоченности импульсов.
Сохраняющаяся актуальность старейшего метода электросна (CES) объясняется его простотой и безопасной результативностью. Использование импульсации П-образной формы, малой силы (до 10 мА), с длительностью импульсов (0,8–0,5 мс), низкой частоты (от 1 до 160 Гц) признано безопасным и близким к электрофизиологическим параметрам человеческого головного мозга [43]. Применение электро-сонтерапии в лечении больных эпилепсией, обеспечивало вегетативный и гуморальный гомеостаз с нормализацией возбуждающих– тормозных процессов ЦНС, увеличением секреции эндорфинов лимбической системой, с анальгези-рующим и седативным эффектами [44].
Близкие по эффективности результаты электросон-терапии на эндорфиновый профиль больных ревматоидным артритом, описывается в работе Кошуковой Г.Н. и др. (2016), где отмечено высокое анальгезирующее действие электросна [45].
Изучение вариаций электрического импульса (величина, направление, форма, длительность импульса, период действия, скважность и др.), локуса действия в структуре ЦНС, механизмов формирования хронического болевого синдрома, а также селективное влияние на систему процессов антиноцицепции, явилось основой в разработке и внедрению отечественными учеными метода транскраниальной электростимуляции (ТЭС) эндорфинэргических механизмов головного мозга [46].
При ТЭС в отличие от электросна используются биполярные импульсы П-образной или синусоидальной формы до 150 Гц со среднечастотным заполнением (5–10 кГц), либо однополярные импульсы прямоугольной формы частотой до 3 кГц. При этом отмечены изменения биоэлектрической активности мозга с селективной активизацией опиоидной системы, подкорковых структур [47].
Схожим с ТЭС механизмом действия обладает ме-зодиэнцефальная модуляция (МДМ) [48]. Как и в предыдущих методиках здесь используется слабоинтенсивное электрическое потенцирование с точкой приложения на срединные структуры головного мозга. МДМ выгодно отличает от прочих транскраниальных электростимуляций используемая широта в низкочастотном диапазоне от 20 до 100 Гц, возможность генерировать как прямоугольные, так и треугольные, М-образные, полукруглые, трапециевидные импульсы, имеющие свои особенности. Для П – образной модуляции преобладающее значение имеют анальгетические, бронхолитические и репаративные эффекты, треугольная модуляция вызывает транквилизирующие, седативное влияние [49]. В настоящее время описаны методики МДМ с вариацией различных форм с целью достижения большей эффективности. С целью наибольшего влияния на мезодиэнцефальную зону и усиления седативного эффекта при МДМ анодный электрод располагают на область лба, акатодный электрод на затылочную область.
Выводы
Методики NIBS могут быть более эффективными и предпочтительными для лечения фантомной и нейропатической боли по сравнению с другими методами по ряду причин:
-
1. Неинвазивность, безопасность, простота. Электросон, ТЭС, МДМ, в отличие от инвазивных методов, таких как глубокая стимуляция мозга, или электростимуляция периферических нервов, не требует хирургического вмешательства. Это снижает риск осложнений, таких как инфекции, кровоизлияния и эпидуральные гематомы, которые могут возникать при инвазивных методах. К тому же, электросон имеет минимальные
-
2. Снижение боли за счет регуляции нейропластичности. Влияя на нейропластичность головного мозга, изменяя активность нейрональной сети, транскраниальная электростимуляция активирует эндогенные механизмы подавления боли через регуляцию системы антиноцицепции нейромедиаторов, таких как эндорфины и серотонин и др.
-
3. Широта диапазона частот и форм электроимпульсов. Использование различных частот и форм импульсов для достижения конкретных терапевтических эффектов – низкие частоты (5–12 Гц) оказывают седативное действие, помогая при эмоциональной лабильности и тревоге, которые могут сопутствовать фантомной боли, в то время как более высокие частоты (70–80 Гц) эффективно подавляют хроническую боль, способствуя высвобождению эндогенных опиоидов. Это особенно важно при лечении фантомной боли, где нейропластичность и нарушение работы нейромедиаторных систем играют ключевую роль в поддержании болевых ощущений.
-
4. Регуляция эмоционального состояния. Хроническая боль зачастую сопровождается тревогой и депрессией, что отягощает и усложняет лечение. Электросон одновременно воздействует на эмоциональные и болевые компоненты, улучшая психоэмоциональный паттерн пациентов. Это комплексное действие делает методику предпочтительной для пациентов с хроническими болевыми синдромами.
побочные эффекты, по сравнению с медикаментозными методами лечения. Медикаментозная терапия, особенно при хронической боли, может приводить к множеству нежелательных последствий, тогда как NIBS является неинвазивным методом и может применяться на регулярной основе без значительного риска для пациента, что доказано безопасным длительным использованием в терапии, не требующим каких – то особых, дополнительных условий.
Представленные клинические исследования показывают эффективность электроимпульсной терапии в лечении хронической боли, в том числе фантомной боли, особенно у пациентов, перенёсших травматические ампутации. Исследования подтверждают значительное снижение болевых ощущений при использовании этих методик, что делают их предпочтительными и доступными для долгосрочного контроля болевого синдрома.
Список литературы Транскраниальная электроимпульсная терапия в лечении хронического болевого синдрома
- Yong RJ, Mullins PM, Bhattacharyya N. Prevalence of chronic pain among adults in the United States. Pain. 2022. 163(2): e328-e332. doi: 10.1097/j.pain.0000000000002291.
- Юдин В.Е., Ярошенко В.П., Косухин Е.С. и др. Фантомно-болевой синдром: клиника, диагностика, лечение // Вестник Медицинского института непрерывного образования. – 2023. – Т.3. – №1. – С.39-43. doi: 10.36107/2782-1714_2023-3-1-39-43.
- Энциклопедический Словарь Ф.А. Брокгауза и И.А. Ефрона: В 86 полутомах с иллюстрациями и дополнительными материалами. – С.-Петербург, 1890-1907.
- Кершбаум Х., Чугунова Е.И. Учение И.П. Павлова о высшей нервной деятельности // Рос. мед.-биол. вестн. им. акад. И.П. Павлова. – 2014. – №3.
- Федоров В.К. Учение И.П. Павлова о сне и его целебной роли. Архивная копия от 13.07.2020 на Wayback Machine: стенограмма публичной лекции из цикла «И.П. Павлов и его учение». Ленинград, 1951. – 40 с.
- Henssen D, Kurt E, van Walsum A, et al. Motor cortex stimulation in chronic neuropathic orofacial pain syndromes: a systematic review and meta-analysis. SciRep. 2020; 10(1): 7195. doi: 10.1038/s41598-020-64177-z.
- Сорокин C.A. Использование электрических токов и электромагнитных полей в терапии. Владимир: Изд-во Владим.гос.ун-та, 2006. – 36 с.
- Абрамович С.Г. Физиотерапия боли. Иркутск: Курортная медицина, 2021. – С.5-18.
- Разумова А.Н, Стародубова В.И., Пономаренко Г.Н. Санаторно- курортное лечение: национальное руководство. – Москва: ГЭОТАР-Медиа, 2021. – 752 с.
- Knotkova H, Hamani C, Sivanesan E, et al. Neuromodulationforchronicpain. Lancet. 2021; 397(10289): 2111-2124. doi: 10.1016/S0140-6736(21) 00794-7.
- Abreu V, Vaz R, Chamadoira C, et al. Thalamic deep brain stimulation for post-traumatic neuropathic limb pain: Efficacy at five years’ follow-up and effective volume of activated brain tissue. Neurochirurgie. 2022; 68(1): 52-60. doi: 10.1016/j.neuchi.2021.06.006.
- Ramos-Fresnedo A, Perez-Vega C, Domingo RA, et al. Motor Cortex Stimulation for Pain: A Narrative Review of Indications, Techniques, and Outcomes. Neuromodulation. 2022; 25(2): 211-221. doi: 10.1016/j. neurom.2021.10.025.
- Lopes PSS, Campos ACP, Fonoff ET, et al. Motor cortex and pain control: exploring the descending relay analgesic pathways and spinal nociceptive neurons in healthy conscious rats. BehavBrainFunct. 2019; 15(1): 5. doi: 10.1186/s12993-019-0156-0.
- Radic JA, Beauprie I, Chiasson P, et al. Motor Cortex Stimulation for Neuropathic Pain: A Randomized Cross-over Trial. Can J Neurol Sci. 2015; 42(6): 401-9. doi: 10.1017/cjn.2015.292.
- Xiong HY, Zheng JJ, Wang XQ. Non-invasive Brain Stimulation for Chronic Pain: State of the Art and Future Directions. Front Mol Neurosci. 2022; 15: 888716. doi: 10.3389/fnmol.2022.888716.
- Nitsche MA, Paulus W. Excitability changes induced in the human motor cortex by weak transcranial directcurrent stimulation. J Physiol. 2000; 527(3): 633-9. doi: 10.1111/j.1469-7793.2000.t01-1-00633.x.
- Lefaucheur JP, Wendling F. Mechanisms of action of tDCS: A brief and practical overview. NeurophysiolClin. 2019; 49(4): 269-275. doi: 10.1016/j.neucli.2019.07.013.
- Navarro-López V, Del-Valle-Gratacós M, Fernández-Vázquez D, et al. Transcranial direct current stimulation in the management of phantom limb pain: a systematic review of randomized controlled trials. Eur J Phys Rehabil Med. 2022; 58(5): 738-748. doi: 10.23736/S1973-9087.22.07439-1.
- Lefaucheur JP, Antal A, Ayache SS, et al. Evidence-based guidelineson the therapeuticuse of trans cranial direct current stimulation (tDCS). Clin Neurophysiol. 2017; 128(1): 56-92. doi: 10.1016/j.clinph.2016.10.087.
- Arendsen LJ, Hugh-Jones S, Lloyd DM. Transcranial Alternating Current Stimulation at Alpha Frequency Reduces Pain When the Intensity of Pain is Uncertain. JPain. 2018; 19(7): 807-818. doi: 10.1016/j.jpain.2018.02.014.
- Sonmez AI, Camsari DD, Nandakumar AL, et al. Accelerated TMS for Depression: A systematic review and meta-analysis. Psychiatry Res. 2019; 273: 770-781. doi: 10.1016/j.psychres.2018.12.041.
- Annalena P, Till H, Jan L, et al. Efficacy of cranial electrotherapy stimulation in patients with burning mouth syndrome: a randomized, controlled, double-blind pilot study. Front Neurol. 2024; 15: 1343093. doi: 10.3389/ fneur.2024.1343093.
- Суюндуков Р.Р., Полетаев В.С., Кузина О.В. Влияние электросна на показатели активности вегетативного отдела нервной системы. Молодежь и современная наука: Междунар. междисциплинар. науч.-практ. конф., г. Самара, 15 июня 2021 г. – Самара: Инсома-пресс, 2021. – С.98-112.
- Barclay TH, Barclay RD. A clinical trial of cranial electrotherapy stimulation for anxiety and comorbid depression. J Affect Disord. 2014; 164: 171-7. doi: 10.1016/j.jad.2014.04.029.
- Ching PY, Hsu TW, Chen GW, et al. Efficacy and Tolerability of Cranial Electrotherapy Stimulation in the Treatment of Anxiety: A Systemic Review and Meta-Analysis. Front Psychiatry. 2022; 13: 899040. doi: 10.3389/ fpsyt.2022.899040.
- Савченкова А.В., Войткевич Е.Г., Погонышев В.А. Электросонтерапия. Молодой исследователь 2024: сборник статей IV Международной научно-практической конференции, Пенза, 30 января 2024 года. – Пенза: Наука и Просвещение, 2024. – С.28-31.
- Taylor AG, Anderson JG, Riedel SL, et al. A randomized, controlled, double-blind pilot study of the effects of cranial electrical stimulation on activity in brain pain processing regions in individuals with fibromyalgia. Explore. 2013; 9: 32-40. doi: 10.1016/j.explore.2012.10.006.
- Tan G, Rintala DH, Jensen MP, et al. Efficacy of cranial electrotherapy stimulation for neuropathic pain following spinal cord injury: a multi-site randomized controlled trial with a secondary 6-month open-label phase. J Spinal Cord Med. 2011; 34(3): 285-96. doi: 10.1179/2045772311Y.0000000008.
- Barclay TH, Barclay RD. A clinical trial of cranial electrotherapy stimulation for anxiety and comorbid depression. J Affect Disord. 2014; 164: 171-7. doi: 10.1016/j.jad.2014.04.029.
- Amanda R, et al. Low Intensity Focused Ultrasound for Non-invasive and Reversible Deep Brain Neuromodulation-A Paradigm Shift in Psychiatric Research. Front Psychiatry. 2022; 13: 825802. doi: 10.3389/fpsyt.2022. 825802.
- Bachu VS, Kedda J, Suk I, et al. High-Intensity Focused Ultrasound: A Review of Mechanisms and Clinical Applications. Ann Biomed Eng. 2021; 49(9): 1975-1991. doi: 10.1007/s10439-021-02833-9.
- Tyler WJ. Noninvasive neuromodulation with ultrasound? A continuum mechanics hypothesis. Neuroscientist. 2011; 17: 25-36. doi: 10.1177/ 1073858409348066.
- Folloni D, Verhagen L, Mars RB, et al. Manipulation of subcortical and deep cortical activity in the primate brain using transcranial focused ultrasound stimulation. Neuron. 2019; 101: 1109.e5–16.e5. doi: 10.1016/j.neuron. 2019.01.019.
- Badran BW, Caulfield KA, Stomberg-Firestein S, et al. Sonication of the anterior thalamus with MRI-guided transcranial focused ultrasound, (tFUS) alters pain thresholds in healthy adults: a double-blind, sham-controlled study. Brain Stimul. 2020; 13: 1805-12. doi: 10.1016/j.brs.2020.10.007.
- Szymoniuk M, Chin JH, Domagalski Ł, et al. Brain stimulation for chronic pain management: a narrative review of analgesic mechanisms and clinical evidence. Neurosurg Rev. 2023; 46(1): 127. doi: 10.1007/ s10143-023-02032-1.
- O’Connell NE, Marston L, Spencer S, et al. Non-invasive brain stimulation techniques for chronic pain. Cochrane Database Syst Rev. 2018; 4(4): CD008208. doi: 10.1002/14651858.CD008208.pub5.
- Hargrove JB, Bennett RM, Simons DG, et al. A randomized placebo-controlled study of noninvasive cortical electrostimulation in the treatment of fibromyalgia patients. PainMed, 2012; 13(1): 115-24. doi: 10.1111/ j. 1526-4637.2011.01292.x.
- Hargrove JB, Bennett RM, Clauw DJ. Long-term outcomes in fibromyalgia patients treated with noninvasive cortical electrostimulation. Arch Phys Med Rehabil. 2012; 93(10): 1868-71. doi: 10.1016/j.apmr.2012.04.006.
- Маляев В.С., Вадивасова Т.Е., Анищенко В.С. Стохастический резонанс, стохастическая синхронизация и индуцированный шумом хаос в осцилляторе Дуффинга // Известия вузов. ПНД. – 2007. – №5.
- Moret B, Donato R, Nucci M, Cona G, Campana G. Transcranial randomnoise stimulation (tRNS): a wide range of frequencies is needed for increasing cortical excitability.Sci Rep. 2019; 9(1): 15150. doi: 10.1038/ s41598-019-51553-7.
- Paulus W. Transcranial electrical stimulation (tES – tDCS; tRNS, tACS) methods. NeuropsycholRehabil. 2011; 21(5): 602-17. doi: 10.1080/ 09602011.2011.557292.
- Xiong HY, Zheng JJ, Wang XQ. Non-invasive Brain Stimulation for Chronic Pain: State of the Art and Future Directions. Front MolNeurosci. 2022; 15: 888716. doi: 10.3389/fnmol.2022.888716.
- Ишков А.С., Солодимова Г.А., Тимонина Е.А., Колдов А.C. Повышение качества физиотерапии импульсным электрическим током. – Пенза: Труды Международного симпозиума «Надежность и качество». 2015. Т.2.
- Шалькевич Л.В., Кудач А.И., Волотовская А.В. и др. Физические методы в лечении и реабилитации пациентов с эпилепсией // Здравоохранение. – 2017. – №12. – С.3-12.
- Кошукова Г.Н., Буглак Н.П. Влияние электросон-терапии на эндорфиновый профиль больных ревматоидным артритом // Вестник физиотерапии и курортологии. – 2016. – №1.
- Липатова А.С., Поляков П.П., Каде А.Х. и др. Влияние транскраниальной электростимуляции на выносливость крыс с разной устойчивостью к стрессу // Биомедицина. – 2018. –№1.
- Красильникова Р.Г., Черепахина Н.Л., Романовская С.В. Основы общей физиотерапии. Москва: ГБОУ ВПО РНИМУ им. Н.И.Пирогова, 2015. – С.24-27.
- Пономаренко Г.Н. Медицинская реабилитация: учебник. Москва: ГЭОТАР-Медиа, 2021. – 368 с.
- Волотовская А.В., Войченко Н.В., Сущеня Е.А. и др. Мезодиэнцефальная модуляция – современный метод транскраниальной электротерапии: учеб-метод. пособие. Минск: БелМАПО, 2022. – 23 с.


