Транскрипционная активность генов, регулирующих дифференцировку Т-хелперов в отдалённые сроки у хронически облучённых людей
Автор: Никифоров В.С., Котикова А.И., Блинова Е.А., Аклеев А.В.
Рубрика: Научные статьи
Статья в выпуске: 3 т.32, 2023 года.
Бесплатный доступ
Целью настоящей работы явилось изучение экспрессии генов TBX21, RORC, GATA3, NFKB1, MAPK8 и STAT3, ответственных за регуляцию дифференцировки различных субполуляций Т-хелперов, у лиц, подвергшихся хроническому радиационному воздействию. Объектом исследования служили клетки периферической крови, полученные от 120 человек, подвергшихся хроническому облучению в широком диапазоне доз на реке Тече. Средняя накопленная поглощённая доза облучения красного костного мозга у обследованных облучённых лиц, составила 742,7±78,6 мГр (диапазон доз: 73,5-3516,1 мГр), в группе сравнения 17,4±2,2 мГр (диапазон доз: 0,0-55,5 мГр). Анализ субпопуляционного состава Т-хелперов (Th1, Th2, Th17) проводился методом проточной цитофлуориметрии. Оценка относительного содержания мРНК генов TBX21, RORC, GATA3, NFKB1, MAPK8 и STAT3 была осуществлена при помощи ПЦР-ВР. Проведённое исследование позволило отметить снижение относительного количества Т-хелперов 2 типа в популяциях Т-хелперов центральной памяти в группе хронически облучённых людей по сравнению с группой сравнения. В составе популяции Т-хелперов центральной памяти показано статистически значимое увеличение относительного количества Т-хелперов 1 типа в зависимости от накопленной поглощённой дозы облучения красного костного мозга. Изменений со стороны экспрессии мРНК исследуемых генов отмечено не было. Анализ связи экспрессии мРНК GATA3, MAPK8, STAT3, RORC, TBX21 и относительного количества клеток в субпопуляциях Т-хелперов 1, 2 и 17 типов у обследованных людей статистически значимых закономерностей не выявил.
Экспрессия генов, транскрипционная активность, транскрипционные регуляторы дифференцировки т-хелперов, т-хелперы, th1, th2, th17, хроническое радиационное воздействие, малые и средние дозы
Короткий адрес: https://sciup.org/170200555
IDR: 170200555 | УДК: 616-001.28:575 | DOI: 10.21870/0131-3878-2023-32-3-14-25
Transcriptional activity of genes regulating T-helpers differentiation in the accidentally exposed population of the Southern Urals
The objective of this work was to study the expression of the TBX21, RORC, GATA3, MAPK8, and STAT3 genes responsible for the regulation of the differentiation of various T-helper subpopulations in individuals chronically exposed to radiation. The object of the study was peripheral blood cells obtained from 120 people chronically exposed to radiation in a wide range of doses on the Techa River. The mean cumulative absorbed dose to red bone marrow in the examined exposed individuals was 742.7±78.6 mGy (dose range: 73.5-3516.1 mGy), in the comparison group - 17.4±2.2 mGy (dose range: 0.0-55.5 mGy). The subpopulation composition of T-helpers (Th1, Th2, Th17) was analyzed by flow cytofluorimetry. The relative mRNA content of the TBX21, RORC, GATA3, NFKB1, MAPK8, and STAT3 genes was estimated by RT-PCR. The study made it possible to note a decrease in the relative number of T-helper 2 in the populations of T-helper central memory in the group of chronically exposed people compared to the comparison group. In the population of T-helpers of central memory, a statistically significant increase in the relative number of T-helpers 1 was shown, depending on the accumulated absorbed dose to red bone marrow. No changes in mRNA expression of the studied genes were observed. The analysis of the relationship between the expression of GATA3, MAPK8, STAT3, RORC, TBX21 mRNA and the relative number of cells in subpopulations of T-helper types 1, 2, and 17 in the examined people did not reveal statistically significant patterns.
Текст научной статьи Транскрипционная активность генов, регулирующих дифференцировку Т-хелперов в отдалённые сроки у хронически облучённых людей
Многочисленные данные свидетельствуют об иммуномодулирующем эффекте ионизирующего излучения, выражающемся в количественных и функциональных изменениях Т-клеточного звена, формировании воспалительного иммунного профиля, нарушении баланса в содержании субпопуляции Т-лимфоцитов, изменении экспрессии генов сигнальных молекул, в том числе ци-токинового профиля [1], что, в свою очередь, может вносить вклад в развитие отдалённых соматико-стохастических последствий радиационного воздействия, прежде всего, лейкозов и злокачественных опухолей.
В ранее проведённых исследованиях у жителей прибрежных сёл реки Течи, подвергшихся низкоинтенсивному хроническому радиационному воздействию вследствие сбросов жидких радиоактивных отходов ПО «Маяк» в реку Течу, в отдалённом периоде регистрировались изменения в иммунной системе, выражавшиеся в снижении количества лейкоцитов (главным образом, за счёт нейтрофилов и лимфоцитов) в крови, повышении лизосомальной активности нейтрофилов, некоторой супрессии внутриклеточного кислородзависимого метаболизма моноцитов и смещении баланса системы цитокинов в сторону провоспалительного ответа [2, 3].
Популяция Т-хелперов является высоко гетерогенной и динамичной. Благодаря внешним и внутренним стимулам происходит активация сигнальных внутриклеточных путей, обуславливающих дифференцировку наивных CD4+ Т-клеток в различные подмножества Т-хелперных клеток.
Под воздействием ионизирующего излучения может дифференциально изменяться экспрессия транскрипционных факторов, что отражается на соотношении различных субпопуляций Т-хелперов [4]. В свою очередь, дисбаланс различных субпопуляций Т-хелперов (Th1, Th2, Th17) является одной из причин развития воспалительного процесса.
На сегодняшний день молекулярно-генетические изменения в Т-клеточном звене иммунной системы, а также роль этих изменений в патогенезе отдалённых эффектов облучения (в частности, онкологических заболеваний) наряду с другими механизмами изучено недостаточно [5].
В связи с этим, цель исследования заключалась в оценке транскрипционной активность генов TBX21, RORC, NFKB1, GATA3, MAPK8 и STAT3, ответственных за дифференцировку субпопуляций Т-хелперов 1, 2 и 17 типов у лиц, подвергшихся хроническому радиационному воздействию.
Материалы и методы
Предмет и объект исследования. Исследование субпопуляционного состава Т-хелперов (Th1, Th2 и Th17) и транскрипционной активности генов у облучённых людей было проведено в отдалённые сроки (спустя более 60 лет) после начала хронического радиационного воздействия.
Материалом для исследования служили образцы периферической крови, собранные в стерильные вакуумные пробирки Tempus Blood RNA Collection Tubes (Applied Biosystem, США), содержащие транспортную среду для стабилизации РНК в биопробах. Взятие крови осуществлялось из локтевой вены утром натощак. Образцы хранились в биобанке лаборатории молекулярно-клеточной радиобиологии ФГБУН УНПЦ РМ ФМБА России при температуре минус 80 °С.
Кровь была получена от 120 жителей прибрежных сёл реки Течи, подвергшихся хроническому радиационному воздействию вследствие сбросов жидких радиоактивных отходов ПО «Маяк». Нарушение технологического процесса переработки и хранения радиоактивных отходов явилось причиной загрязнения окружающей среды радионуклидами (90Sr, 89Sr, 137Cs, 95Zr, 95Nb, 144 Ce, 104Ru): в 1949-1956 гг. было сброшено в реку Течу 1,15 x 10 17 Бк жидких радиоактивных отходов), в связи с чем население загрязнённых территорий подверглось внутреннему и внешнему облучению.
В результате защитных мероприятий и распада короткоживущих радионуклидов мощность дозы внешнего облучения, а также внутреннего облучения мягких тканей, тимуса и периферических лимфоидных органов существенно снизилась и после 1960 г. не превышала 0,01 мГр/год для всех, кто проживал на прибрежных территориях. Иная картина облучения была у красного костного мозга (ККМ), поскольку главный вклад в формирование дозы вносил долгоживущий остео-тропный 90Sr, обеспечивающий хроническое облучение с монотонно снижающейся мощностью дозы, которая к 1985 г. у всех облучённых была менее 0,01 мГр/год [6]. Таким образом, у облучённых людей значительно преобладали поглощённые дозы на ККМ, тогда как дозы на тимус и периферические лимфоидные органы были на порядок ниже (табл. 1).
При формировании обследованной группы были использованы следующие критерии включения в исследование:
-
1) облучённые лица из когорты реки Течи – проживавшие в одном из 41 сёл, расположенных на побережье реки Течи, в период с 01.01.1950 по 31.12.1960 гг.;
-
2) наличие рассчитанной индивидуальной поглощённой накопленной дозы облучения ККМ, тимуса и периферических лимфоидных органов.
Критерии исключения:
-
1) наличие у обследованных лиц онкологических, аутоиммунных, острых или хронических (период обострения) воспалительных заболеваний на период обследования;
-
2) приём противоопухолевых препаратов, антибиотиков, стероидных гормонов из подкласса кортикостероидов в течение последних 6 мес. до исследования;
-
3) рентгенологическое обследование в течение последних 6 мес.
На основании сформулированных критериев были выделены две основные группы обследуемых лиц:
-
1) группа облучённых лиц с индивидуальными накопленными дозами облучения ККМ 70 мГр и более (далее – основная группа) – 66 человек;
-
2) группа сравнения – лица, проживающие в сходных социально-экономических условиях, но с интенсивностью облучения ККМ, не превышавшей 1 мГр/год, и накопленной дозой менее 70 мГр за весь период жизни – 54 человека.
Основные характеристики исследуемых групп представлены в табл. 1. Исследуемые группы включали лиц пожилого возраста: среднее значение возраста для хронически облучённых лиц составило 73,2 ± 0,5 год (диапазон: 67,0-84,0 лет), для группы сравнения – 68,8 ± 0,9 лет (диапазон: 60,0-87,0 лет). В двух группах подавляющее большинство образцов крови было получено от женщин. Обследуемые группы состояли из лиц, принадлежавших к двум этническим группам: славяне (в основном русские, а также украинцы и белорусы) и тюрки (в основном татары и башкиры).
Таблица 1 Характеристика исследуемых групп
|
Показатель |
Основная группа |
Группа сравнения |
|
Объём выборки |
N=66 |
N=54 |
|
N (%) |
||
|
мужчины ол женщины славяне Этническая группа тюрки |
17 (30,6) 37 (69,4) 26 (47,0) 28 (51,0) |
24 (42,0) 42 (58,0) 20 (32,0) 46 (64,0) |
|
M±SE (min-max) |
||
|
Возраст, лет Доза облучения ККМ, мГр Доза облучения тимуса и периферических лимфоидных органов, мГр |
73,2±0,5 (67,0-84,0) 742,7±78,6 (73,5-3716,1) 97,7±9,91 (5,1-355,3) |
68,8±0,9 (60,0-87,0) 17,4±2,2 (0-55,3) 7,5±1,3 (0-39,5) |
Все пациенты подписывали добровольное информированное согласие на проведение исследования, одобренное этическим комитетом УНПЦ РМ ФМБА России.
Количественная оценка экспрессии генов. Выделение РНК проводили на колонках с помощью набора GeneJET Stabilized and Fresh Whole Blood RNA Kit (Thermo Scientific™, США) по стандартной методике. Информацию о концентрации и чистоте выделенных образцов РНК получали с помощью спектрофотометра NanoDrop 2000С (Thermo Scientific, США). Отношение оптических плотностей, измеренных при A260/280 для РНК, выделенной из всех образцов крови, составило 2,0±0,05. Исходным количеством для анализа было 100 нг/мкл РНК каждого образца. Реакцию обратной транскрипции для синтеза кДНК проводили с использованием коммерческого набора реагентов High-Capacity cDNA Reverse Transcription Kit (Applied Biosystem, США). Относительное количественное содержания мРНК определяли с помощью ПЦР в режиме реального времени с использованием амплификатора CFX96 Touch (Bio-Rad Laboratories, США).
Количественную оценку экспрессии анализируемых генов проводили по методу 2-ΔΔСt [7]. Данные оценивали относительно уровней мРНК генов «домашнего хозяйства» (housekeeping genes) ACTB и B2M. Анализ кривых амплификации производили в программе Bio-Rad CFX Manager 2.1 (Bio-Rar Laboratories, США) методом пороговой линии. Расчёт проводился с учётом трёх повторов для каждого гена. В работе были использованы коммерческие наборы праймеров/зон-дов от Applied Biosystems, США: STAT3 (Hs00374280_m1), GATA3 (Hs00231122_m1), MAPK8 (Hs01548508_m1), NFKB1 (Hs00765730_m1), ACTB (4333762F), B2M (4333766F), часть праймеров были синтезированы ООО «ДНК-синтез» (Россия): TBX21 (Forward: 5'-GGCTCCAGATGTTCTTCGCTA-3', Reverse: 5'-GGATGGGCTTCCTCTTCTCA-3', Probe: FAM-BHQ1 – 5'-CACGACCAGGAATTTGACCCTCCA-3'), FOXP3 (Forward: 5'-CCTTCACGTTCAACATCAAGC-3', Reverse: 5'-GCTCTGGGTACAGGTCCTCATC-3', Probe: FAM-BHQ1 – 5'-CCAGTCCCGTGAAACGCCCA-3'), RORC (Forward: 5'-GAATCAAGGAAATACGAGAACAAGAC-3', Reverse: 5'-CTTCATCCCCTCGGTCTTTG-3', Probe: FAM-BHQ1 – 5'-CGACTCAGCCACCTCTGACTACTGCC-3').
Оценка субпопуляций Т-хелперов. Схема исследования субпопуляционного состава Т-хелперов периферической крови облучённых лиц методом проточной цитометрии подробно описана в статье [8].
Для анализа субпопуляций Т-хелперов применялась следующая тактика гейтирования: выявление Т-хелперов проводилось по наличию на поверхности клеток CD3 и CD4 маркеров. Далее популяция CD3+CD4+-клеток разделялась на субпопуляции Т-хелперов на разной стадии дифференцировки по наличию поверхностных маркеров CD45RA и CD62L, а именно Т-хелперов центральной памяти с фенотипом CD3+CD4+CD45RA-CD62L+ и Т-хелперов эффекторной памяти с фенотипом CD3+CD4+CD45RA-CD62L-. В популяциях Т-хелперов центральной памяти и Т-хелперов эффекторной памяти определялись субпопуляции различных Т-хелперов по наличию маркеров CCR4, CCR6, CXCR3 и CXCR5 [9]. Характеристика исследуемых субпопуляций Т-хелперов представлена в табл. 2.
Таблица 2
Фенотипы исследуемых субпопуляций Т-хелперов в периферической крови облучённых лиц
|
Фенотип клеток |
Наименование субпопуляции Т-хелперов |
|
CXCR5–CXCR3+CCR6–CCR4– |
Т-хелперы 1 (Th1) |
|
CXCR5–CXCR3–CCR6–CCR4+ |
Т-хелперы 2 (Th2) |
|
CXCR5–CXCR3–CCR6+CCR4– |
Т-хелперы 17 (Th17) |
Статистическая обработка результатов. Статистический анализ данных исследования проводили с применением стандартных методов математико-статистической обработки с использованием пакетов программ прикладного статистического анализа (Statistica v. 10.0 и SigmaPlоt v. 12.5). Для оценки межгрупповых различий значений признаков применяли U-критерий Манна-Уитни. Определение вида зависимости исследуемых показателей проводилось с использованием корреляционного анализа по Спирмену. Для всех критериев и тестов различия признавали статистически значимыми при p<0,05.
Результаты и обсуждение
Оценка представленности трёх субпопуляций Т-хелперов (Th1, Th2 и Th17) в популяциях Т-хелперов центральной памяти (Т ем ) и Т-хелперов эффекторной памяти (Т ем ) у обследуемых лиц представлены на рис. 1А и 1Б соответственно.
Как следует из рис. 1А, в группе облучённых лиц было обнаружено слабое статистически значимое снижение содержания относительного количества субпопуляций Т-хелперов 2 (р=0,04) в популяции Т-хелперов центральной памяти относительно группы сравнения. Для других популяций Т-хелперов различий выявлено не было. При этом не наблюдалось различий в общем относительном количестве Т-хелперов (СО3+СО4+-клетки): медиана в группе сравнения составила 40,45% (25-75% - 34,00 - 46,69), в основной группе - 36,41% (25-75% - 32,37 - 41,97), p=0,06, что скорее указывает на перераспределение клеточных субпопуляций внутри популяции Т-хелперов, без признаков иммунодефицитных состояний у облучённых лиц.
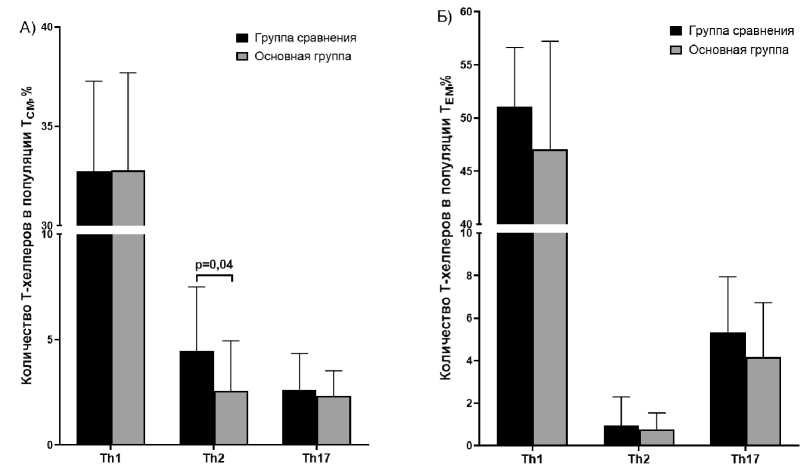
Рис. 1. Относительное количество субпопуляций Т-хелперов в популяциях Т-хелперов центральной памяти (Т ем ) (А) и Т-хелперов эффекторной памяти (Т ем ) (Б) у обследуемых лиц.
В результате корреляционного анализа было показано, что в составе популяции Т-хелперов центральной памяти статистически значимо увеличивалось относительное количество Т-хелперов 1 в зависимости от накопленной поглощённой дозы облучения ККМ (R=0,20, p=0,04). При этом, для указанной субпопуляции не было отмечено возрастных зависимостей в обеих исследуемых группах.
В составе популяции Т-хелперов эффекторной памяти не было выявлено статистически значимых дозовых зависимостей в содержании различных субпопуляций Т-хелперов периферической крови облучённых лиц.
Воздействие ионизирующего излучения вызывает изменение направления дифференцировки Т-хелперов, что приводит к дисбалансу клеточных подтипов Th1 и Th2, что в свою очередь может способствовать развитию иммуноопосредованных заболеваний: доминирующий Th2-от-вет связан с атопическими заболеваниями, а усиление Th1-ответа играет роль в развитии хронических воспалительных и аутоиммунных заболеваний, таких как ревматоидный артрит и сахарный диабет [10]. Сообщается, что облучение в высоких дозах ионизирующего излучения индуцирует стойкий иммунный ответ Th2, одновременно подавляя иммунный ответ Th1 у экспериментальных животных и выживших после атомной бомбардировки [11]. Однако эффекты, вызываемые воздействием малых и средних доз радиации, остаются спорными: ранее сообщалось, что облучение в дозе 50 мГр способствует повышению уровней мРНК цитокинов Th1 (IFN-γ) и Th2 (IL-4 и IL-5) в CD4+ T-клетках мышей [12]. В то же время в эксперименте показано, что облучение мышей в дозе 75 мГр приводит к ингибированию Th2 и активации Th1-ответа [13], а обследование иранских лаборантов-радиологов, получивших дозу облучения ниже 50 мЗв, также демонстрирует иммунологический сдвиг в сторону Th1-ответа и супрессию ответа Th2 [14].
Направление дифференцировки наивных Т-клеток в клетки Th1 или Th2 имеет решающее значение для Т-зависимого иммунного ответа. Так, например, одна из ведущих ролей в дифференцировке Th2 принадлежит цитокину IL-4, который заставляет наивные Т-клетки дифференцироваться в эффекторные клетки Th2 [15]. При этом ранее в исследованиях хронически облучённых жителей прибрежных сёл реки Течи было показано статистически значимое снижение концентрации данного цитокина в периферической крови [3], что может быть причиной снижения количества клеток Th2 у этих же облучённых лиц.
Однако не только цитокиновое окружение определяет направление дифференцировки Т-клеток. Изменение экспрессии транскрипционных факторов, участвующих в дифференцировке Т-хелперов, может существенно влиять на представленность различных субпопуляций. Например, сдвиг баланса Th1/Th2 может быть объяснён тем, что облучение в диапазоне малых доз приводит к активации транскрипционного фактора Stat4 в клетках Th1 и при этом ингибирует ключевой фактор транскрипции GATA3 в клетках Th2 [13].
Таким образом, в основе дисбаланса субпопуляций Th1/Th2 могут лежать изменения экспрессии транскрипционных факторов [13]. В связи с этим на втором этапе работы у обследованных лиц была проанализирована транскрипционная активность генов, участвующих в регуляции дифференцировки Т-хелперов. Результаты исследования представлены на рис. 2.
При сравнении двух выборок не было установлено статистически значимых различий в экспрессии мРНК исследуемых генов.
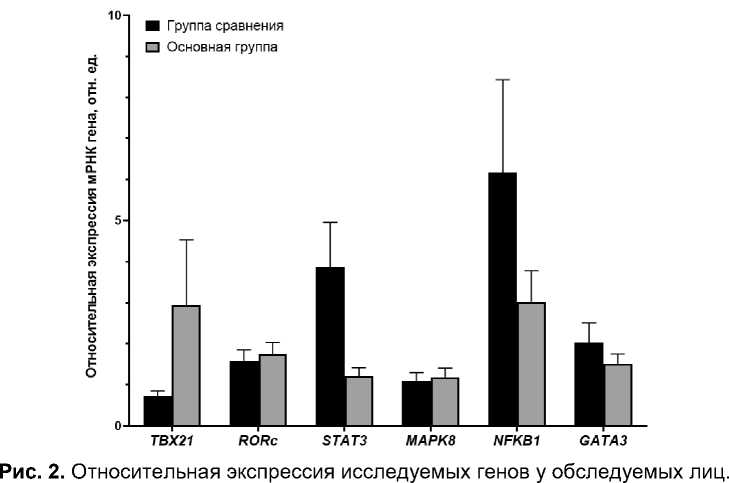
Необходимо отметить, что ранее полученные данные на расширенной выборке (264 человека) в исследовании, посвященном изучению кооперативной работе генов в отдалённые сроки после облучения, демонстрировали статистически значимое снижение транскрипционной активности гена NFKB1 в группе хронически облучённых людей [16].
Для изучения характера распределения показателей транскрипционной активности генов TBX21, STAT3 и NFKB1, подразумевающего оценку доли хронически облучённых людей, имеющих выраженные изменения в экспрессии мРНК, был проведён частотный анализ.
Результаты анализа представлены в табл. 3, где видно, что вариабельность индивидуальных значений относительного содержания мРНК генов TBX21, STAT3 и NFKB1 в двух группах была сопоставима.
Таблица 3
Частота отклонений от референтных значений (95% ДИ) относительного содержания мРНК генов TBX21, STAT3 и NFKB1 в обследованных группах
|
Ген |
Частота отклонений от референтных значений, абс. (%) |
||||
|
Группа сравнения N=54 |
Облучённые лица N=66 |
Уровень значимости, p |
|||
|
<2,5% |
>97,5% |
<2,5% |
>97,5% |
||
|
TBX21 |
1 (1,85) |
1 (1,85) |
1 (1,51) |
4 (6,06) |
0,252 |
|
STAT3 |
1 (1,85) |
1 (1,85) |
2 (3,03) |
0 (0) |
0,681 |
|
NFKB1 |
1 (1,85) |
1 (1,85) |
1 (1,51) |
1 (0,62) |
0,887 |
В рамках настоящей работы нами не было отмечено статистически значимых связей относительного содержания мРНК исследуемых генов с дозовыми характеристиками (накопленной поглощённой дозой облучения ККМ, тимуса и периферических лимфоидных органов).
Данные об изменении экспрессии генов вследствие воздействия малых доз ионизирующего излучения в клетках крови человека показывают высокую степень сложности транскрипционных изменений. В ряде работ показано нарушение регуляции сигнальных путей, находящихся под контролем транскрипционных факторов, регулирующих дифференцировку CD4+-клеток, в моделях как in vitro , так и in vivo после острого радиационного облучения в диапазоне малых и средних доз [17]. Однако, в литературе крайне мало сведений о функционировании внутриклеточных путей в отдалённые сроки после хронического радиационного воздействия.
Воздействие малых и высоких доз оказывает влияние на различные биологические процессы в иммунокомпетентных клетках. Так, уже при дозе в 5 мГр наблюдается активация цитокиновых и хемокиновых сигнальных путей, ответственных за иммунные и воспалительные процессы [18]. В работе, посвящённой изучению отдалённых последствий аварии на ЧАЭС, у облучённых людей [19] отмечается изменение экспрессии 116 генов, имеющих отношение к интерферонам, интерлейкинам, колониестимулирующим факторам и факторам роста, что напрямую свидетельствует о смещении иммунного баланса в сторону воспалительных ответов у данной категории лиц.
Ранее для этих же лиц была показана активация транскрипционного фактора NFkB1, которая имела высокую степень корреляции с содержанием ряда цитокинов, таких как IL-1 и IL-6 [20]. Примечательно, что подобные эффекты были характерны для лиц, имеющих различные клинические формы злокачественных новообразований. Так, повышенное содержание мРНК генов семейства NFkB, а именно NFκB1, NFκB2 и Rel, было зафиксировано спустя 20 лет при обследовании лиц, облучённых вследствие аварии на ЧАЭС, с раком предстательной железы [21], щитовидной железы [22], молочной железы и лейкозом [23].
Индуцированные ионизирующим излучением изменения в экспрессии генов характерны для различных подмножеств лимфоцитов у облучённых людей [24]. Ранний ответ клетки после облучения в диапазоне малых доз (5 мГр) заключался в репрессии генов, который был характерен в большей степени для клеток CD4+. Репрессированные гены были вовлечены, по большей части, в окислительное фосфорилирование и биосинтез белка.
Анализ связи экспрессии мРНК, исследуемых в рамках настоящей работы генов с относительным количеством клеток Th1, Th2 и Th17 в субпопуляциях Т-хелперов центральной и эффекторной памяти, не позволил отметить статистически значимых закономерностей.
Таким образом, в результате проведённого исследования, у облучённых лиц выявлено снижение относительного количества клеток Th2, однако изменений в количестве мРНК генов, кодирующих транскрипционные факторы дифференцировки Т-хелперов, на данном этапе работы обнаружено не было.
Заключение
Исследование, проведённое через 60-70 лет после начала хронического облучения, позволило отметить в лимфоцитах периферической крови снижение относительного количества Т-хелперов 2 типа в популяции Т-хелперов центральной памяти у лиц, с поглощённой дозой облучения красного костного мозга 742,7 ± 78,6 (диапазон: 73,5-3716,1 мГр), при этом не регистрировалось снижение общего количества Т-хелперов в исследуемой группе, что, вероятно, указывает на адаптационные механизмы, проявляющиеся в перераспределении различных субпопуляций Т-хелперов. Также наблюдалось дозозависимое увеличение количества Т-хелперов 1 типа в периферической крови облучённых лиц. Подобные изменения внутри популяции Т-хелперов могут служить маркером некоторого провоспалительного сдвига у облучённых лиц, однако для подтверждения данной гипотезы необходимы дальнейшие исследования.
Не было выявлено статистически значимых различий в транскрипционной активности генов-регуляторов дифференцировки Т-хелперов: GATA3, STAT3, TBX21, MAPK8 и RORC между обследуемыми группами людей.
Анализ связи экспрессии регуляторов транскрипции и относительного количества субпопуляций Т-хелперов у обследованных людей не позволил отметить статистически значимых закономерностей.
Список литературы Транскрипционная активность генов, регулирующих дифференцировку Т-хелперов в отдалённые сроки у хронически облучённых людей
- Li H.H., Wang Y.W., Chen R., Zhou B., Ashwell J.D., Fornace A.J.Jr. Ionizing radiation impairs T cell activation by affecting metabolic reprogramming //Int. J. Biol. Sci. 2015. V. 11, N 7. P. 726-736.
- Аклеев А.А. Иммунный статус человека в отдалённом периоде хронического радиационного воздействия //Медицинская радиология и радиационная безопасность. 2020. Т. 65, № 4. С. 29-35.
- Кодинцева Е.А., Аклев А.А., Блинова Е.А. Цитокиновый профиль лиц, подвергшихся хроническому радиационному воздействию, в отдалённые сроки после облучения //Радиационная биология. Радиоэкология. 2021. Т. 61, № 5. С. 506-514.
- Beauford S.S., Kumari A., Garnett-Benson C. Ionizing radiation modulates the phenotype and function of human CD4+ induced regulatory T cells //BMC Immunol. 2020. V. 21, N 1. P. 18. DOI: 10.1186/s12865-020-00349-w.
- ICRP, 2012. ICRP statement on tissue reactions and early and late effects of radiation in normal tissues and organs - threshold doses for tissue reactions in a radiation protection context. ICRP Publication 118 //Ann. ICRP. 2012. V. 41, N 1/2. P. 1-322.
- Дёгтева М.О., Напье Б.А., Толстых Е.И., Шишкина Е.А., Бугров Н.Г., Крестинина Л.Ю., Аклеев А.В. Распределение индивидуальных доз в когорте людей, облучённых в результате радиоактивного загрязнения реки Течи //Медицинская радиология и радиационная безопасность. 2019. Т. 64, № 3. С. 46-53.
- Livak K.J., Schmittgen T.D. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T)) method //Methods. 2001. V. 25, N 4. P. 402-408.
- Котикова А.И., Блинова Е.А., Аклеев А.В. Субпопуляционный состав Т-хелперов в периферической крови хронически облучённых лиц в отдалённом периоде //Медицина экстремальных ситуаций. 2022. № 2. С. 65-73.
- Кудрявцев И.В., Борисов А.Г., Кробинец И.И., Савченко А.А., Серебрякова М.К., Тотолян А.А. Хемокиновые рецепторы на Т-хелперах различного уровня дифференцировки: основные субпопуляции //Медицинская иммунология. 2016. Т. 18, № 3. С. 239-250.
- Hirahara K., Nakayama T. CD4+ T-cell subsets in inflammatory diseases: beyond the Th1/Th2 paradigm //Int. Immunol. 2016. V. 28, N 4. P. 163-71.
- Park H.R., Jo S.K., Paik S.G. Factors effecting the Th2-like immune response after gamma-irradiation: low production of IL-12 heterodimer in antigen-presenting cells and small expression of the IL-12 receptor in T cells //Int. J. Radiat. Biol. 2005. V. 81, N 3. P. 221-231.
- Cho S.J., Kang H., Hong E.H., Kim J.Y., Nam S.Y. Transcriptome analysis of low-dose ionizing radiation-impacted genes in CD4+ T-cells undergoing activation and regulation of their expression of select cytokines //J. Immunotoxicol. 2018. V. 15, N 1. P. 137-146.
- Gao H., Dong Z., Gong X., Dong J., Zhang Y., Wei W., Wang R., Jin S. Effects of various radiation doses on induced T-helper cell differentiation and related cytokine secretion //J. Radiat. Res. 2018. V. 59, N 4. P. 395-403.
- Karimi G., Balali-Mood M., Alamdaran S.A., Badie-Bostan H., Mohammadi E., Ghorani-Azam A., Sadeghi M., Riahi-Zanjani B. Increase in the Th1-cell-based immune response in healthy workers exposed to low-dose radiation - immune system status of radiology staff //J. Pharmacopuncture. 2017. V. 20, N 2. P. 107-111.
- Dong C., Flavell R.A. Cell fate decision: T-helper 1 and 2 subsets in immune responses //Arthritis Res. 2000. V. 2, N 3. P. 179-188.
- Nikiforov V.S., Akleyev A.V. mRNA expression of GATA3, FOXP3, TBX21, STAT3, NFKB1, and MAPK8 transcription factors in humans and their cooperative interactions long-term after exposure to chronic radiation //Biology Bulletin. 2022. V. 49, N 6. P. 588-595.
- Bazyka D., Ilienko I., Golyarnik N., Belyaev O., Lyaskivska O. Gene expression and cellular markers of occupational radiation exposure in Chernobyl shelter construction workers //Health Phys. 2020. V. 119, N 1. P. 37-43.
- El-Saghire H., Thierens H., Monsieurs P., Michaux A., Vandevoorde C., Baatout S. Gene set enrichment analysis highlights different gene expression profiles in whole blood samples X-irradiated with low and high doses //Int. J. Radiat. Biol. 2013. V. 89, N 8. P. 628-638.
- Albanese J., Martens K., Karanitsa L.V., Schreyer S.K., Dainiak N. Multivariate analysis of low-dose radiation-associated changes in cytokine gene expression profiles using microarray technology //Exp. Hematol. 2007. V. 35, N 4. P. 47-54.
- Hosoi Y., Miyachi H., Matsumoto Y., Enomoto A., Nakagawa K., Suzuki N., Ono T. Induction of interleukin-1 beta and interleukin-6 mRNA by low doses of ionizing radiation in macrophages //Int. J. Cancer. 2001. V. 96, N 5. P. 270-276.
- Savli H., Szendroi A., Romics I., Nagy B. Gene network and canonical pathway analysis in prostate cancer: a microarray study //Exp. Mol. Med. 2008. V. 40, N 2. P. 176-185.
- Cine N., Tarkun I., Canturk N., Gunduz Y., Sunnetci D., Savli H. Whole genome expression, canonical pathway and gene network analysis in the cases of papillary thyroid cancer //European Society of Human Genetics Conference Proceedings. 2012. V. 20, N 1. P.192.
- Savli H., Akkoyunlu R.U., Cine N., Gluzman D.F., Zavelevich M.P., Sklyarenko L.M., Koval S.V., Sunnetci D. Deregulated levels of the NF-kB1, NF-kB2, and Rel genes in Ukrainian patients with leukemia and lymphoma in the post-Chernobyl period //Turk. J. Haematol. 2016. V. 33, N 1. P. 8-14.
- Gruel G., Voisin P., Vaurijoux A., Roch-Lefevre S., Gregoire E., Maltere P., Petat C., Gidrol X., Voisin P., Roy L. Broad modulation of gene expression in CD4+ lymphocyte subpopulations in response to low doses of ionizing radiation //Radiat. Res. 2008. V. 170, N 3. P. 335-344.


