Транскрипционный фактор BRN-3 и рак предстательной железы, связь с особенностями гормональной рецепции и с уровнем активации AKT/M-TOR сигнального пути
Автор: Спирина Людмила Викторовна, Горбунов Алексей Константинович, Кондакова Ирина Викторовна, Слонимская Евгений Анатольевич, Усынин Е.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 1 т.17, 2018 года.
Бесплатный доступ
Введение. Транскрипционные факторы POU4F1 (нейрогенные факторы Brn-3α) играют значимую роль в развитии злокачественных новообразований. Цель исследования - изучение экспрессии транскрипционного фактора Brn-3α, андрогеновых (AR) и эстрогеновых рецепторов (ER) в ткани доброкачественной гиперплазии и рака предстательной железы и определении связи с уровнем активации AKT/mTOR сигнального пути. Материал и методы. В исследование было включено 30 больных местнораспространенным раком предстательной железы (РПЖ) T2-3N0M0, 15 пациентов с доброкачественной гиперплазией предстательной железы (ДГПЖ). Определение уровня экспрессии генов Brn-3α, AR, ERα, а также компонентов AKT/m-TOR сигнального пути проводилось методом ПЦР в реальном времени. Результаты. Показано, что увеличение экспрессии гена ядерного белка Brn-3α сопровождалось ростом уровня мРНК ERα в ткани рака предстательной железы. Экспрессия AR была высока в обеих группах больных. Выявлена активация AKT/m-TOR сигнального каскада: отмечены высокие уровни экспрессии AKT, а также m-TOR в трансформированных клетках. Однако отмечено отсутствие изменений фосфатазы PTEN при развитии патологических процессов предстательной железы. Заключение. Транскрипционный фактор Brn-3α связан с развитием РПЖ, что сопровождается повышением экспрессии ERα, протеинкиназы AKT и m-TOR.
Транскрипционный фактор brn-3α, рак предстательной железы, сигнальный путь akt/m-tor
Короткий адрес: https://sciup.org/140254158
IDR: 140254158 | УДК: 616.65-006.6:576.3:577.2:577.1 | DOI: 10.21294/1814-4861-2018-17-1-26-31
Transcription factor BRN-3 and prostate cancer, relation with hormone receptors and AKT/M-TOR signaling pathway activation
Introduction. The transcription factor Brn-3α (product of the POU4F1) plays a significant role in carcinogenesis. The purpose of the study was to investigate Brn-3α, AR, ERα expressions in tissues of benign prostatic hyperplasia and prostate cancer as well as to determine their association with AKT/mTOR signaling pathway activation. Material and methods. The study included 30 patients with locally advanced prostate cancer and 15 patients with benign prostatic hyperplasia. The expression levels of Brn-3α, AR, ERα and the components of AKT/m-TOR signaling pathway were determined using RT-PCR assay. Results. Overexpression of Brn-3α in prostate cancer tissues was found to be associated with high level of ERα mRNA. High expression of AR was revealed in tissues of benign prostatic hyperplasia and prostate cancer. High expression levels of AKT, m-TOR and PTEN were observed in prostate cancer tissues. However, no significant changes in PTEN mRNA level were found in tissues of prostatic hyperplasia. Conclusion. Brn-3α transcription factor was associated with prostate cancer and accompanied with high expression levels of ERα, AKT and m-TOR.
Текст научной статьи Транскрипционный фактор BRN-3 и рак предстательной железы, связь с особенностями гормональной рецепции и с уровнем активации AKT/M-TOR сигнального пути
Введение . Транскрипционные факторы POU4F1 (нейрогенные факторы Brn-3 a ) играют значимую роль в развитии злокачественных новообразований. Цель исследования – изучение экспрессии транскрипционного фактора Brn-3 α , андрогеновых (AR) и эстрогеновых рецепторов (ER) в ткани доброкачественной гиперплазии и рака предстательной железы и определении связи с уровнем активации AKT/mTOR сигнального пути. Материал и методы . В исследование было включено 30 больных местнораспространенным раком предстательной железы (РПЖ) T2–3N0M0, 15 пациентов с доброкачественной гиперплазией предстательной железы (ДГПЖ). Определение уровня экспрессии генов Brn-3 α , AR, ER α , а также компонентов AKT/m-TOR сигнального пути проводилось методом ПЦР в реальном времени. Результаты. Показано, что увеличение экспрессии гена ядерного белка Brn-3 a сопровождалось ростом уровня мРНК ER α в ткани рака предстательной железы. Экспрессия AR была высока в обеих группах больных. Выявлена активация AKT/m-TOR сигнального каскада: отмечены высокие уровни экспрессии AKT, а также m-TOR в трансформированных клетках. Однако отмечено отсутствие изменений фосфатазы PTEN при развитии патологических процессов предстательной железы. Заключение. Транскрипционный фактор Brn-3 α связан с развитием РПЖ, что сопровождается повышением экспрессии ER α , протеинкиназы AKT и m-TOR.
В развитии гормонозависимых опухолей человека большое значение имеют транскрипционные факторы POU4F1, также известные как нейрогенные факторы Brn-3 α [1]. Они представляют собой важные ядерные белки, регулирующие процессы пролиферации и дифференцировки клетки. Полагают, что транскрипционный фактор Brn-3 α вовлечен в различные процессы онкогенеза, в частности, участвуя в проведении апоптотических сигналов и контролируя скорость клеточного цикла [2]. Кроме того, определено влияние данного показателя на уровень экспрессии рецепторов половых гормонов: эстрогенов (ER) и андрогенов (AR) [3].
Рецепторы стероидных гормонов входят в большое семейство внутриклеточных рецепторов, которые активируются под действием соответствующих лигандов. ER и AR являются их основными представителями. ER имеют 2 подтипа: ER α и ER β . Каждый из них кодируется отдельным геном, при этом имеются сведения о преимущественной экспрессии того или иного подтипа рецептора в разных тканях [3]. Известна роль ER α в качестве важного регулятора интенсивности процессов ангиогенеза гормонозависимых опухолей [4]. Изменение уровня и экспрессии стероидных гормонов найдено в злокачественных новообразованиях
различных локализаций [5]. В первую очередь к ним относят рак предстательной железы (РПЖ), рак молочной железы и др. Известно, что роль AR различается в разных типах опухоли. Например, рецепторы являются стимуляторами опухолевого роста при раке мочевого пузыря, предстательной железы, в то время как в печени они является супрессорами опухолевого роста [6].
Ключевым сигнальным каскадом, обеспечивающим регуляцию процессов пролиферации и апоптоза опухолевых клеток при действии AR и ER, является AKT/m-TOR путь [7–9]. К его значимым компонентам относят протеинкиназы AKT, m-TOR, PTEN и др. Известно, что мужчины с доброкачественной гиперплазией предстательной железы (ДГПЖ) имеют больший риск развития РПЖ [10]. В настоящее время превалирует точка зрения об общности патогенетических процессов, лежащих в основе развития ДГПЖ и РПЖ [11]. В частности, показано, что высокая экспрессия AR характерна для обоих видов патологий.
Цель исследования – изучение экспрессии транскрипционного фактора Brn-3 α , AR, ER α в ткани доброкачественной гиперплазии и рака предстательной железы, а также оценка уровня активации AKT/mTOR сигнального пути.
Материал и методы
В исследование было включено 30 больных местнораспространенным РПК T2–3N0M0 и 15 пациентов с доброкачественной гиперплазией предстательной железы, проходивших лечение в клиниках НИИ онкологии Томского НИМЦ. Объ- емы диагностики и лечения больных соответствовали рекомендуемым алгоритмам, утвержденным Министерством здравоохранения и социального развития РФ. Проведение данной работы одобрено этическим комитетом НИИ онкологии Томского НИМЦ.
Материалом для исследования являлись образцы гиперплазированной и опухолевой ткани, полученные при проведении диагностической биопсии, а также нормальная ткань простаты, которая была получена при оперативном вмешательстве у больных раком мочевого пузыря.
Для исследования экспрессии молекулярных показателей и выделения мРНК образцы тканей помещали в раствор RNAlater (Ambion, USA) и сохраняли при температуре –80ºС (после 24-часовой инкубации при +4ºС).
Определение уровня экспрессии генов Brn-3α, AR, ERα, а также компонентов AKT/m-TOR сигнального пути
РНК выделяли с помощью набора RNeasy mini Kit, содержащего ДНКазу I (Qiagen, Germany). Для оценки количества выделенной РНК на спектрофотометре NanoDrop-2000 (Thermo Scientific, USA) оценивали концентрацию и чистоту выделения РНК. Концентрация РНК составила от 80 до 250 нг/мкл, А260/А280=1,95–2,05; А260/ А230=1,90–2,31. Целостность РНК оценивалась при помощи капиллярного электрофореза на приборе TapeStation (Agilent Technologies, USA) и набора R6K ScreenTape (Agilent Technologies, USA). RIN составил 5,6–7,8.
Таблица 1 Последовательность праймеров исследованных генов Ген Ампликон Последовательность POU4F1 NM_006237 AR NM_000044 ER NM_000125 4E-BP1 294 п.н. 190 п.н. 386 п.н. 244 п.н. 181 п.н. 152 п.н. 267 п.н. 244 п.н. 160 п.н. F 5′- CACGCTCTCGCACAACAA-3′ R 5′- ATCCGCTTCTGCTTCTGTCT-3′ F 5′- GAGGGACAGCAGGCAGA-3′ R 5′- GCTATCAGAACACACACACACACT-3′ F 5′- TCCTGATGATTGGTCTCGTCT-3′ R 5′- GATGTGGGAGAGGATGAGGA-3′ F 5′- CAGCCCTTTCTCCCTCACT -3′ NM_004095.3 AKT1 NM_001014431.1 С-RAF NM_002880.3 GSK3b NM_001146156.1 70S kinase alpha NM_001272042.1 m-TOR NM_004958.3 R 5′- TTCCCAAGCACATCAACCT -3′ F 5′- CGAGGACGCCAAGGAGA -3′ R 5′- GTCATCTTGGTCAGGTGGTGT -3′ F 5′- TGGTGTGTCCTGCTCCCT -3′ R 5′- ACTGCCTGCTACCTTACTTCCT -3′ F 5′- AGACAAGGACGGCAGCAA -3′ R 5′- TGGAGTAGAAGAAATAACGCAAT -3′ F 5′- CAGCACAGCAAATCCTCAGA -3′ R 5′- ACACATCTCCCTCTCCACCTT -3′ F 5′- CCAAAGGCAACAAGCGAT-3′ R 5′- TTCACCAAACCGTCTCCAA -3′ PDK1 NM_001278549.1 187 п.н. F 5′- TCACCAGGACAGCCAATACA -3′ R 5′- CTCCTCGGTCACTCATCTTCA -3′ GAPDH NM_001256799.2 138 п.н. F 5′- GGAAGTCAGGTGGAGCGA-3′ R 5′-GCAACAATATCCACTTTACCAGA-3′ Примечание: NM – номер последовательности РНК в NCBI Nucleotide Database ; F – прямой праймер; R – обратный праймер. СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2018; 17(1): 26–31 27
Уровень экспрессии генов оценивали при помощи количественной обратно-транскриптазной ПЦР в режиме реального времени (RT-qPCR) с использованием красителя SYBR Green на ам-плификаторе iCycler (Bio-Rad, USA). Для получения кДНК на матрице РНК проводили реакцию обратной транскрипции с помощью набора OT m-MuLV-RH (БиоЛабмикс, Россия) со случайными гексануклеотидными праймерами в соответствии с инструкцией к набору. ПЦР ставили в трех репликах в объеме 25 мкл, содержащем 12,5 мкл БиоМастер HS-qPCR SYBR Blue (БиоЛабмикс, Россия), 300 нM прямого и обратного праймеров и 50 нг кДНК. Двухшаговая программа амплификации включала 1 цикл – 94ºС, 10 мин – предварительная денатурация; 40 циклов – 1-й шаг 94ºС, 10 сек и 2-й шаг, – 20 сек при температуре 60ºС. Праймеры были подобраны с использованием программы Vector NTI Advance 11,5 и базы данных NCBI (табл. 1). В качестве референсного гена использовали ген «домашнего хозяйства» фермента GAPDH (glyceraldehydes-3-phosphate dehydrogenase), и уровень экспрессии каждого целевого гена нормализовали по отношению к экспрессии GAPDH.
Статистическую обработку результатов проводили с применением пакета программ Statistica 8.0. Результаты определения экспрессии генов представлены как среднее значение ± ошибка среднего.
Результаты и обсуждение
Показано увеличение экспрессии мРНК транскрипционного фактора Brn-3 α в 4,13 раза в ткани РПЖ по сравнению с ДГПЖ (рис. 1). Это свидетельствует о том, что в трансформированных клетках простаты происходит увеличение экспрессии данного маркера, что влияет на уровень рецепторов стероидных гормонов. Этот факт подтверждается также экспериментальными данными, полученными D.C. Berwick et al. [2]. Авторами доказано влияние данного показателя на рост транскрипционной активности рецепторов ER и AR.
В ткани РПЖ отмечен рост экспрессии ER α в 30,33 раза по сравнению с тканью аденомы (табл. 2). При этом выявлено, что в обеих группах больных отмечен высокий уровень мРНК AR. Полученные данные свидетельствуют о том, что для злокачественных опухолей предстательной железы характерно повышение экспрессии как ER,
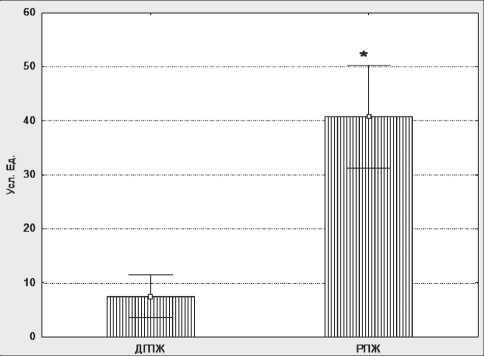
Рис. 1. Экспрессия гена транскрипционного фактора Brn-3 α в ткани ДГПЖ и РПЖ. Примечание: * – различия статистически значимы по сравнению с показателями у больных ДГПЖ (p<0,05)
так и AR в отличие от ДГПЖ. Имеются сведения, что пролиферация опухолевых клеток простаты в условиях in vitro происходит под влиянием активирующих сигналов ER α , определяя особенности течения заболевания [12, 13]. Выявленный факт является молекулярной особенностью трансформированных клеток, и его значимость еще предстоит оценить.
При сравнительном анализе экспрессии генов компонентов AKT/m-TOR сигнального пути в патологических процессах предстательной железы отмечена активация данного сигнального каскада, доказательством которой является повышенный уровень экспрессии протеинкиназы AKT (табл. 3). В ткани рака предстательной железы зафиксировано увеличение этого показателя в 4,9 раза по сравнению с ДГПЖ. Дополнительным доказательством высокой активности AKT/m-TOR сигнального пути при злокачественных новообразованиях явилось повышение уровня мРНК m-TOR в 8,4 раза. Стоит отметить, что сходные значения уровня фосфатазы PTEN наблюдались как при ДГПЖ, так и при раке предстательной железы.
Дополнительные сведения, подтверждающие связь молекулярных маркеров с наличием патологических изменений в ткани предстательной железы, были получены при проведении корреляционного анализа (рис. 2). Так, при изучении корреляционных зависимостей в ткани ДГПЖ выявлены связи молекулярных показателей с ядерным
Таблица 2
Экспрессия генов андрогеновых (AR) и эстрогеновых рецепторов (ER) при патологии предстательной железы
Показатель, усл. ед.
ДГПЖ
Рак предстательной железы
AR
173,0 ± 79,6
151,87 ± 23,0
ER
2,62 ± 1,19
79,47 ± 20,17*
Примечание: * – различия статистически значимы по сравнению с показателями у больных ДГПЖ (p<0,05).
Таблица 3
Экспрессия генов компонентов AKT-m-TOR сигнального пути при патологии предстательной железы
|
Показатель, усл. ед. |
ДГПЖ |
Рак предстательной железы |
|
PTEN |
Компоненты AKT/m-TOR сигнального пути 193,5 ± 75,9 |
234,01 ± 24,9 |
|
AKT |
2,15 ± 0,59 |
10,53 ± 3,3* |
|
GSK-3-beta |
0,95 ± 0,48 |
12,6 ± 5,69 |
|
PDK1 |
5,75 ± 3,78 |
2,9 ± 1,0 |
|
c-RAF |
13,63 ± 8,1 |
25,19 ± 8,28 |
|
m-TOR |
Протеинкиназа m-TOR и ее субстраты 3,69 ± 1,32 |
30,99 ± 13,8* |
|
70 S6 |
3,45 ± 1,74 |
18,35 ± 11,11 |
|
4E-BP1 |
1,48 ± 0,58 |
3,93 ± 1,94 |
Примечание: * – различия статистически значимы по сравнению с показателями у больных ДГПЖ (p<0,05).
фактором Brn-3 α . Уровень его экспрессии зависел от мРНК гена 4E-BP1 (r=0,9; p=0,001) и от мРНК m-TOR (r=0,8; p=0,001). Также подтверждена значимость AR в развитии предопухолевых заболеваний простаты. Отмечены корреляции между экспрессией AR, экспрессией c-Raf (r=0,7; p=0,001), 70 S6 киназой (r=0,95; p=0,001) и PTEN (r=0,8; p=0,014). Вероятно, повышение экспрессии AR, приводящее к активации AKT/m-TOR сигнального пути, сочетается с высоким уровнем мРНК PTEN.
При РПЖ отмечена прямая зависимость экспрессии Brn-3α от уровня мРНК 4EBP1 (r=0,4; p=0,01) и мРНК AR (r=0,28; p=0,018). При этом отмечены отрицательная зависимость между экспрессией AR и PDK1 при РПЖ (r=–0,42; p=0,001), а также положительные зависимости между AR, уровнем мРНК c-RAF (r=0,57; p=0,001) и 70 S6 киназой (r=0,5; p=0,001). Интересным является факт сопряженности между экспрессией PTEN и AR (r=0,66; p=0,001), а также Brn-3α (r=0,29 p=0,001). При корреляционном анализе выявлено влияние эстрогеновых рецепторов в ткани РПЖ на уровень активации AKT/m-TOR сигнального пути, что подтверждается связями между экспрес- сией ERα и AKT (r=0,57; p=0,01), а также с c-RAF (r=0,57; p=0,01), GSK-3β (r=0,40; p=0,015) и PDK1 (r=0,28; p=0,01).
Заключение
Развитие доброкачественной гиперплазии предстательной железы связано с увеличением экспрессии AR, что определяет в дальнейшем возникновение злокачественной патологии. Выявлено, что в трансформированных клетках железы в этих условиях возрастает экспрессия ядерного фактора Brn-3α, который способствует росту уровня мРНК ERα. Изменение гормональной рецепции при развитии опухолевой патологии сопровождается повышением активности AKT/m-TOR сигнального каскада на фоне исходных значений мРНК гена PTEN. Стоит отметить, что зафиксирован факт усиления связей между компонентами сигнального каскада, рецепторами гормонов и Brn-3 α в развитии патологических процессов предстательной железы. Резюмируя полученные данные, можно полагать, что изучаемые молекулярные маркеры ассоциированы с развитием злокачественных новообразований, определяя особенности их течения.
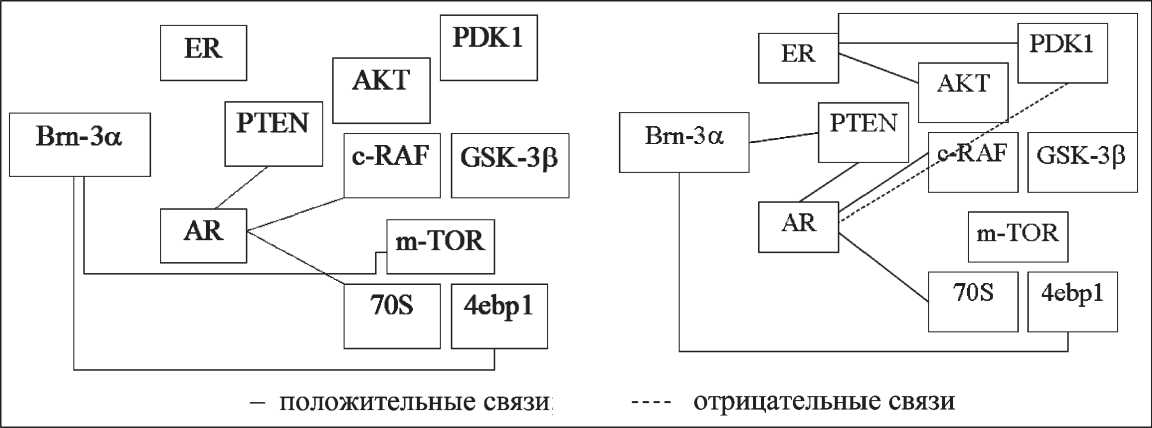
Рис. 2. Корреляционные связи между молекулярными маркерами в ткани ДГПЖ (А) и в ткани РПЖ (Б)
Список литературы Транскрипционный фактор BRN-3 и рак предстательной железы, связь с особенностями гормональной рецепции и с уровнем активации AKT/M-TOR сигнального пути
- Budhram-Mahadeo V., Fujita R., Bitsi S., Sicard P., Heads R. Co-expression of POU4F2/Brn-3b with p53 may be important for controlling expression of pro-apoptotic genes in cardiomyocytes following ischaemic/hypoxic insults. Cell Death Dis. 2014; 5: 1503. DOI: 10.1038/cddis.2014.452
- Berwick D.C., Diss J.K., Budhram-Mahadeo V.S., Latchman D.S. A simple technique for the prediction of interacting proteins reveals a direct Brn-3a-androgen receptor interaction. J Biol Chem. 2010 May 14; 285 (20): 15286-95. DOI: 10.1074/jbc.M109.071456
- Stoica J., Franke F.T., Wellstein A., Szubaiko F., List H.-J., Reiter R., Morgan E., Martin M.B., Stoica A. Estradiol Rapidly Activates Akt via the ErbB2 Signaling Pathway. J Biol Chem. 2010 May 14; 285 (20): 15286-95. DOI: 10.1074/jbc.M109.071456
- Vamesu S. Angiogenesis and ER/PR status in primary breast cancer patients: an analysis of 158 needle core biopsies. Rom J Morphol Embryol. 2007; 48 (1): 25-31.
- Ahmad N., Kumar R. Steroid hormone receptors in cancer development: A target for cancer therapeutics. Cancer Lett. 2011 Jan 1; 300 (1): 1-9. DOI: 10.1016/j.canlet.2010.09.008


