Твердофазная металлизация железо-ванадиевых концентратов, получаемых из титаномагнетитовых руд
Автор: Асанов А.В., Рощин А.В., Рощин В.Е.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 13 (189), 2010 года.
Бесплатный доступ
Рассмотрены процессы, протекающие при твердофазной металлизации железо-ванадиевых концентратов. Прослежена последовательность превращений в концентратах. Определена температура восстановления металлов из их оксидов и продолжительность выдержки для восстановления железа.
Металлизация, железо-ванадиевый концентрат
Короткий адрес: https://sciup.org/147156643
IDR: 147156643 | УДК: 669.053.2+661.88
Solid-phase metallization of ferro-vanadium concentrates
The article considers the processes proceeding at solid-phase metallization of ferrovanadium concentrates. The sequence of transformations in concentrates is tracked. Temperatures of reduction of metals from oxides and duration of holding for iron reduction are defined.
Текст научной статьи Твердофазная металлизация железо-ванадиевых концентратов, получаемых из титаномагнетитовых руд
Запасы титаномагнетитовых руд на Южном Урале оцениваются десятками миллиардов тонн, однако их переработка традиционными методами невозможна вследствие высокого содержания в них оксидов титана. Так, в месторождениях Мед-ведёвско-Копанской группы, запасы которых оцениваются в 6 млрд т, в среднем содержится 20 % железа, 8,7 % TiO2 и 0,24 % V2O5. При обогащении руд этих месторождений получают концентраты двух видов - железо-ванадиевый и ильменитовый. Типичный состав железо-ванадиевых концентратов:
|
Медведёвский (7) Кусинский (2) |
Fe 57,70 60,00 |
TiO2 11,50 7,25 |
V2O5 0,95 1,00 |
|
|
МпО |
SiO2 |
А120з |
MgO |
CaO |
|
1,05 |
2,00 |
1,50 |
0,85 |
|
|
0,95 |
3,00 |
1,93 |
2,00 |
2,50 |
Поскольку отношение Fe/TiO2 в железо-ванадиевых концентратах составляет 4...6, получение из них чугуна в доменных печах также практически невозможно [1,2].
Ранее [3] показана возможность пирометаллургического разделения компонентов титаномагнетитовых руд по двухстадийной схеме переработки, включающей стадию восстановления железа в твёрдой фазе и последующую плавку в электропечи продуктов твердофазного восстановления. По такой схеме, по-видимому, возможна переработка и железо-ванадиевых концентратов, полученных при обогащении титаномагнетитовых руд.
Для реализации этой схемы необходимо изучить последовательность превращений в оксидах восстанавливаемых металлов, определить температуру восстановления разных металлов, определить необходимую продолжительность выдержки для возможно более полного восстановления железа. Решение этих вопросов явилось целью данной работы.
Концентраты 1 и 2 в измельчённом до фракции -1 мм состоянии смешивали с порошком восстановителя - чешуйчатым графитом. Смеси тщательно перемешивали и брикетировали. Брикеты (таблетки) разной массы нагревали во взвешивающей муфельной печи до 1200 °C со скоростью 10 °С/мин и выдерживали в течение 1, 2 или 3 часов при температуре 1000, 1100, 1200 °C. На дери-ватографе Q-1500D провели термический анализ поведения концентрата 1 при восстановительном нагреве с той же скоростью до 1500 °C. Кроме того, осуществили изотермическую выдержку таблеток в течение 3-х часов при температуре 1300 °C.
После охлаждения таблеток изготавливали шлифы. Анализ химического состава исходного концентрата, металлических и оксидных новообразований в рудных зернах восстановленных образцов проводили с использованием электронного микроскопа JSM-6460LV, оборудованного волновым и энергодисперсионным анализаторами. Исходные фазы, а также фазы, полученные после выдержки при температуре 900 °C и 1300 °C, подвергали рентгенофазовому анализу на дифрактометре ДРОН-4.
Результаты изменения массы образцов в процессе нагрева представлены на рис. 1.
Из представленных данных следует, что характер изменения массы при восстановительном
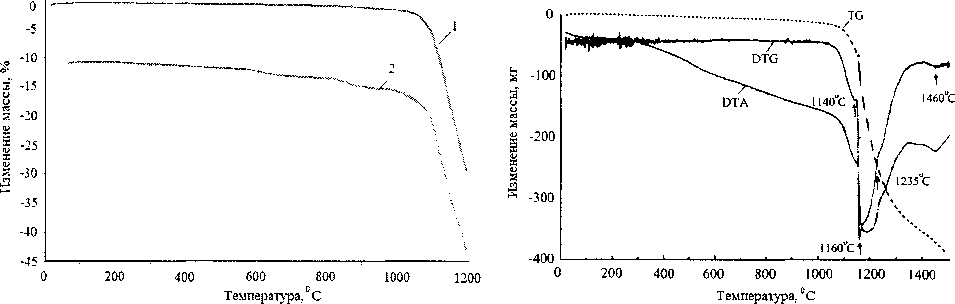
Рис. 1. Изменение массы образца при восстановительном обжиге концентратов 1 и 2 в муфельной печи (а) и концентрата 1 в печи дериватографа (б)
нагреве обоих концентратов практически одинаков. Некоторое отличие заключается в незначительном изменении массы концентрата 2 в температурных интервалах 620...700 °C и 850...930 °C. По-видимому, потеря массы при этих значениях температуры обусловлена удалением кристаллохимической влаги из водных силикатов нерудной фазы, а разница в поведении концентратов вызвана более высоким содержанием пустой породы в концентрате 2 [4].
Изучение шлифов показало, что в исходном концентрате присутствуют зерна магнетита и ти-таномагнетита, в подчиненном количестве имеются зерна ильменита (рис. 2). Ванадий находится в растворе в зёрнах магнетита, титаномагнетита и ильменита. При этом в зернах ильменита, как показали результаты рентгеноспектрального анализа, содержание ванадия меньше по сравнению с зёрнами титаномагнетита и магнетита. Примесными элементами в рудных зёрнах являются также хром и марганец. Пустая порода представлена силикатами группы серпентина-хлорита Mg3[Si2O5](OH)4 -(Mg,Al,Fe)3[Si2O5](OH)4.
В зёрнах титаномагнетита, подвергшихся восстановительному обжигу, сначала происходит распад твёрдого раствора с обособлением магнетита, ильменита и силикатов, а при более высокой температуре восстанавливается железо магнетита и ильменита, ильменит обедняется железом и превращается в дититанат железа FeO-2TiO2 (рис. 3, табл. 1).
В результате восстановительного обжига при 900 °C в титаномагнетитовых зернах выявляется структура распада, образованная выделениями магнетита, ильменита и силикатов. Следует отметить, что в ильменит практически полностью переходит марганец, а хром и ванадий остаются в магнетите. Металлического железа при данных условиях не обнаруживается. Рентгенофазовый анализ образца обнаруживает небольшое смеще-
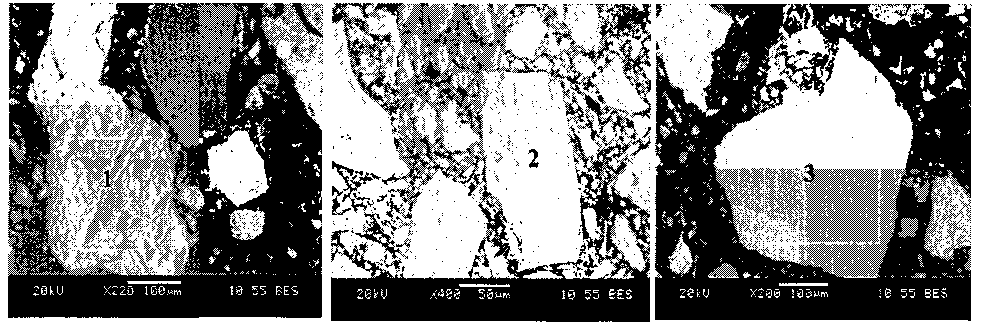
а) б) в)
Рис. 2. Вид и состав (содержание элементов, % мае.) рудных зёрен концентрата:
|
Площадь анализа: |
О |
AI |
Мд |
Ti |
V |
Сг |
Мп |
Fe |
|
1, титаномагнетит |
17,80 |
0,24 |
— |
3,58 |
0,83 |
0,67 |
0,54 |
69,02 |
|
2, магнетит |
19,81 |
0,25 |
— |
0,61 |
— |
0,46 |
74,23 |
|
|
3, ильменит |
25,98 |
— |
0,54 |
28,87 |
0,29 |
— |
0,62 |
40,93 |
Таблица 1
Состав фаз в зерне титаномагнетита после восстановительного обжига
|
Анализ в точках, фаза |
Содержание элементов, % мае. |
|||||||||||
|
О |
1 Mg |
Al |
1 Si |
| Са |
| Ti |
| Мп |
V |
Сг |
Fe |
С |
I Na |
|
|
Рис. 3, а |
||||||||||||
|
1, ильменит |
26,04 |
2,57 |
33,91 |
0,66 |
36,82 |
|||||||
|
2, магнетит |
20,00 |
0,65 |
2,93 |
0,91 |
0,63 |
76,42 |
||||||
|
3, силикат |
35,90 |
6,02 |
5,94 |
23,58 |
8,90 |
1,79 |
17,88 |
|||||
|
4, силикат |
35,97 |
18,78 |
1,35 |
29,18 |
0,32 |
0,46 |
13,94 |
|||||
|
5, силикат |
37,10 |
9,25 |
1,94 |
26,96 |
16,79 |
0,63 |
7,32 |
|||||
|
6, ильменит |
25,05 |
33,03 |
0,94 |
40,98 |
||||||||
|
7, ильменит |
25,92 |
2,20 |
32,52 |
0,74 |
38,62 |
|||||||
|
8, магнетит |
20,18 |
1,45 |
0,75 |
0,69 |
78,37 |
|||||||
|
Рис. 3 |
,6 |
|||||||||||
|
1, дититанат |
28,35 |
3,10 |
1,81 |
0,22 |
46,00 |
1,10 |
5,81 |
1,54 |
11,95 |
|||
|
2, ильменит |
23,23 |
2,43 |
5,55 |
12,49 |
2,69 |
5,89 |
12,65 |
35,08 |
||||
|
3, силикат |
37,94 |
0,68 |
9,28 |
24,42 |
5,52 |
3,27 |
0,76 |
0,40 |
6,34 |
2,92 |
||
|
4, магнетит |
24,46 |
75,55 |
||||||||||
|
5, магнетит |
27,78 |
0,78 |
71,22 |
|||||||||
|
6, силикат |
39,96 |
1,85 |
9,12 |
21,09 |
10,61 |
2,26 |
1,09 |
8,20 |
1,70 |
|||
|
7, чугун |
0,39 |
94,84 |
4,77 |
|||||||||
|
8, силикат |
40,51 |
0,71 |
7,98 |
20,94 |
7,29 |
3,07 |
0,76 |
11,41 |
1,62 |
|||
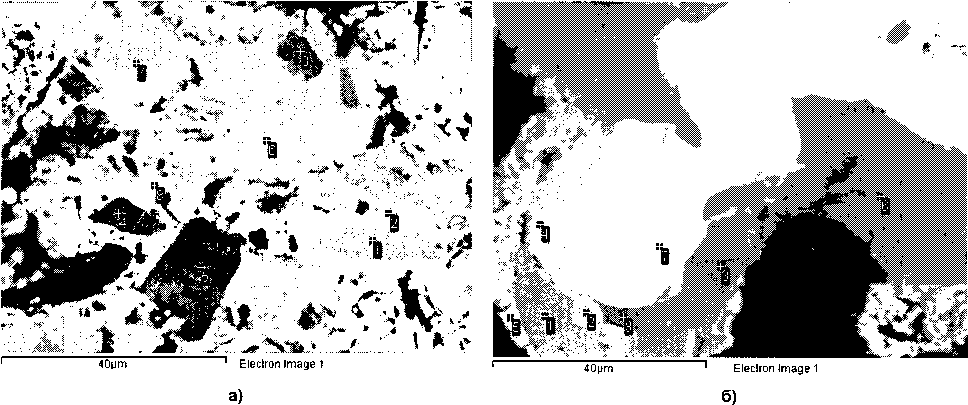
Рис. 3. Преобразования в зерне титаномагнетита после восстановительного обжига при температуре 900 °C (а) и 1300 °C (б)
ние пиков магнетита, что свидетельствует об изменении параметров его решётки.
После восстановительного обжига при 1300 °C образец сильно металлизируется. В первичных зёрнах титаномагнетита происходит восстановление железа из ранее выделившихся фаз магнетита и ильменита. Восстановление железа из ильменита протекает по реакции
2FeTiO3 + С = Fe + FeO2TiG2 + СО, в результате протекания которой появляются новообразования дититаната железа.
Авторы [5, 6] предполагают, что параллельно с восстановлением железа из ильменита имеет место взаимодействие ильменита со шпинелидом ванадия:
FeOTiO2 + Fe¥2O4 = V2TiO5 +2FeO.
Образования V2O3TiO2, в котором содержание ванадия больше содержания титана, нашими экспериментами не подтверждается. В то же время результаты рентгеноспектрального анализа показали, что ванадий после восстановительного обжига образца при 1300 °C действительно связан с оксидами титана и не обнаруживается ни в остаточном магнетите, ни в металлической фазе. Аналогичным образом ведёт себя и хром, который, как и ванадий, связан с оксидами титана.
Оксидная фаза, сопряжённая с металлической фазой, представлена недовосстановленным магнетитом, дититанатом железа и силикатами.
Рентгенофазовый анализ концентрата после восстановительного обжига при 1300 °C подтвердил присутствие в продуктах восстановле-
Таблица 2
Фазовый состав концентрата после обжига при температуре 1300 °C
Сопоставление результатов исследований фазового состава, микрорентгеноспектрального анализа и анализа дериватограммы свидетельствует о том, что:
-
1) восстановление железа из железо-ванадиевых концентратов твёрдым углеродом в условиях динамического нагрева со скоростью 10 °С/мин начинается при температуре 1080... 1110 °C;
-
2) при температуре 1215 °C начинается восстановление титана. Как было ранее показано термодинамическим расчётом [13], восстановление титана в этих условиях происходит преимущественно с образованием его низших оксидов и достигает максимальной скорости при температуре 1235 °C. При температуре 1420 °C происходит, по-видимому, восстановление титана до его карбидов [13], которое достигает максимальной скорости при температуре порядка 1460 °C;
-
3) восстановление железа в процессе нагрева концентрата со скоростью 10°С/мин не завершается даже при достижении температуры 1500 °C. Для завершения процесса восстановления железа необходима выдержка реагентов при высокой температуре.
Изменение массы концентратов в зависимости от времени и температуры восстановительного обжига представлено на рис. 4. Горизонтальные линии здесь соответствуют полному восстановлению железа согласно расчёту материального баланса.
Как следует из представленных данных, скорость восстановления железа из концентратов твердым углеродом зависит от температуры. Выдержка концентрата при температуре 1000 °C в течение 140 минут хотя и привела к развитию восстановительного процесса, но не позволила восстановить все железо. При температуре 1100, 1200 и 1300 °C происходит полное восстановление железа за 130, 45 и 30 минут соответственно. При нагреве до 1300 °C, как показал рентгеноспектральный анализ, происходит и частичное восстановление титана. Поэтому целесообразной является, по-видимому, выдержка при 1200 °C в течение 45 минут, что позволит сократить время по сравнению с необходимой выдержкой при температуре 1100 °C и предотвратить восстановление титана.
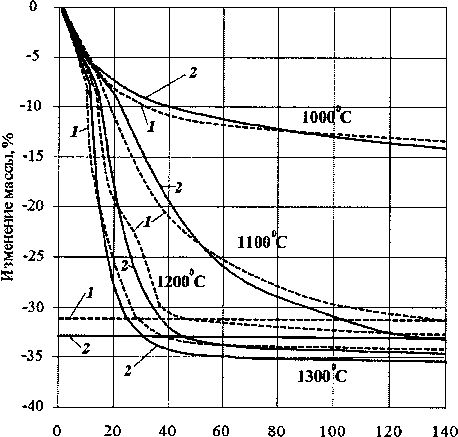
Время выдержки, мин
Рис. 4. Изменения массы концентратов 1 и 2 при восстановительном обжиге в зависимости от времени и температуры
Таким образом, изучена последовательность преобразований в рудных зёрнах железо-ванадиевых концентратов, определена температура начала восстановления железа и титана, выявлен температурный интервал и оценена необходимая продолжительность выдержки для селективного восстановления железа при твердофазной металлизации концентратов.
Список литературы Твердофазная металлизация железо-ванадиевых концентратов, получаемых из титаномагнетитовых руд
- Резниченко, В.А. Комплексное использование сырья в технологии тугоплавких металлов/B. А. Резниченко, А.А. Палант, В.И. Соловьев. -М.: Наука, 1988. -240 с.
- Пирометаллургическая переработка комплексных руд/Л.И. Леонтьев, Н.А. Ватолин, С.В. Шаврин и др. -М.: Металлургия, 1997. -431 с.
- Рощин, А.В. Оценка возможности пирометаллургического разделения компонентов титаномагнетитовых руд/А.В. Рощин, Н.В. Мальков, В.Е. Рощин//Электрометаллургия. -2006. -№ 8. -C. 23-28. 4.
- Рощин, А.В. Химическое взаимодействие твердого углерода с твердыми вкрапленными рудами/А.В. Рощин, В.Е. Рощин//Известия РАН. Металлы. -2003. -С. 3-9. 5.
- Резниченко, В.А. Электротермия титановых руд/В.А. Резниченко. -М.: Наука, 1969. -207 с.
- Влияние соды на фазовые превращения при восстановлении титаномагнетитового концентрата водородом/Г.Б. Садыхов, Л.О. Наумова, В.А. Резниченко и др.//Известия РАН Металлы. -1994. -№ 1. -С. 9-16.
- Powder Diffraction File International Centre for Diffraction Data (PDF-2, ICPDS, 74-748).
- Powder Diffraction File International Centre for Diffraction Data (PDF-2, ICPDS, 76-2372).
- Powder Diffraction File International Centre for Diffraction Data (PDF-2, ICPDS, 6-696).
- Powder Diffraction File International Centre for Diffraction Data (PDF-2, ICPDS, 3-411).
- Powder Diffraction File International Centre for Diffraction Data (PDF-2, ICPDS, 25-306).
- Powder Diffraction File International Centre for Diffraction Data (PDF-2, ICPDS, 71-1067).


