Твердофазное нанодисперсное получение и оценка свойств комплекса марганца с диэтилентриаминпентауксусной кислотой как контрастного препарата для магнитно-резонансной томографии
Автор: Белянин М.Л., Федущак Т.А., Филимонов В.Д., Бородин О.Ю., Чурин А.А., Усов В.Ю.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 2 т.23, 2008 года.
Бесплатный доступ
Статья посвящена разработке метода твердофазного синтеза парамагнитного контрастного препарата - комплекса марганца (II) с диэтилентриаминпентауксусной кислотой (MnNa2H-ДТПА, сокращенно Mn-ДТПА, мангапентетат) и доклиническому изучению его физико-химических и котннтрастирующих свойств. Комплекс Mn-ДТПА был получен из порошкообразных MnCO3 и H5-ДТПА в твердой фазе путем высокоскоростного нандиспергирования с одновременным смешиванием (планетарная мельница), с получением частиц 50-300 нм nm) при добавлении минимальных объемов водного дистиллята (до 10 мл на 0,5M MnCO3). Из исходного порошкового мангапентетата (MnNa2H-ДТПА) были затем получены и исследованы по физико-химическим свойствам, а также in vivo растворы с содержанием мангапентетата 0,5M, 0,75M и 1,0M. Величины LD50 для различных растворов мангапентетата составили соответственно 14,1±4,5 мл/кг веса для 0,5M, 13,4±3,7 мл/кг веса для 0,75M и 12,3±3,9 мл/кг веса для 1,0M. Морфологических изменений в организме крыс и мышей на протяжении вплоть до 2 недель наблюдения после введения 0,2 мМ мангапентетата на кг веса - не наблюдалось. Вязкость мангапентетата (сантистокс) зависела от его содержания в растворе ([Mn-ДТПА], как М/л) как Вязкость=0,171*e([Mn-ДТПА]/0,461) + 0,827, и заметно уступала вязкости рентгеновских контрастных препаратов - омнипака и урографина. Таким образом, твердофазный синтез мангапентетата в нанопорошке из MnCO3 и H5-ДТПА позволяет получить высококачественный контрастный препарат-парамагнетик - MnNa2H-ДТПА для получения различных инъекционных форм для внутривенного контрастирования при МРТ.
Твердофазный синтез, мангапентетат, мр-томография, парамагнитное контрастирование
Короткий адрес: https://sciup.org/14918852
IDR: 14918852 | УДК: 616-006.48
Solid-nanophase synthesis and evaluation of manganese (II) complex with diethylentriaminpentaacetic acid as contrast agent for magnetic resonance imaging
The authorsve developed a technique for synthesis of the paramagnetic complex of manganese (II) with diethylendiaminpentaacetate and tested it's physicochemical properties and in vivo preclinically. Mn(II)-DTPA complex was obtained from MnCO3 and H5-DTPA in solid phase by high-speed mixing pre-prepared nanoparticles (as little as 50-300 nm) and adding minor volumes of water (up to 10 ml per 0,5 M of MnCO3). Later on 0,5 M, 0,75 M and 1,0 M solutions of the mangapentetate (MnNa2H-DTPA) were tested in vivo in rats and in rabbits. The authors conclude that solid-phase synthesis of mangapentetate from MnCO3 and H5-DTPA is a reliable technique for production of this paramagnetic contrast agent.
Текст научной статьи Твердофазное нанодисперсное получение и оценка свойств комплекса марганца с диэтилентриаминпентауксусной кислотой как контрастного препарата для магнитно-резонансной томографии
Получение новых контрастных препаратов – парамагнетиков является в течение последнего десятилетия одним из важнейших путей повышения диагностической эффективности магнитно-резонансной томографии (МРТ) [1]. На сегодня основными препаратами – парамагнетиками, широко используемыми в практике МРТ, являются комплексы Gd(III) с ДТПА и сходными с ДТПА органическими хелатами [2]. Определенное распространение получили также препараты на основе микрочастиц оксида железа (SPIO – SuperParamagnetic Iron Oxide nanoparticles) [3], а также комплекс Mn(II) с дипиридоксальдифосфатом («Тесласкан», GE Medical) [4]. Промышленное производство отечественных контрастных препаратов для МРТ в России и СНГ на сегодня пока отсутствует. Ранее мы показали в эксперименте нетоксичность и возможность использования для парамагнитного контрастирования при МРТ комплекса Mn(II)-ДТПА - мангапентетата (« ™ Пентаманг») [5]. Поскольку реакция получения мангапентетата не требует высокой температуры и проходит до конца, а константа прочности мангапентетата достаточно велика и составляет 15,9 при pH 6,4-7,2 [6], мы оценили возможность получения мангапентетата в твердой фазе при смешении ультрадисперсных нанопорошков исходных компонент с последующим дополнительным диспергированием. Полученный в результате мангапентетат в различных концентрациях – от 0,5 М до 1,75 М был изучен в эксперименте в качестве парамагнитного контрастного препарата для МРТ.
МАТЕРИАЛ И МЕТОДЫ
Получение мангапентетата проводилось первоначально в твердой нанофазе путем одновременного механодиспергирования и смешивания исходных компонент при температуре 35-50°C. Получение мангапентетата осуществляли в один этап по реакции: MnCO3+H5-ДТПА+Na2CO3 ^ MnNa2H-ДТПА +CO2+H2O.
В ходе получения мангапентетата к 0,5 моль (60,18 г) порошкообразного карбоната марганца (MnCO3; процентное содержание в пересчете на Mn 95,5 %) добавляли 0,5 моль (196,65 г) диэтилентриа-минопентауксусной кислоты (H5-ДТПА), 0,5 моль (53,0 г) карбоната натрия безводного, полученную смесь измельчали в шаровой мельнице в течение 2 часов с добавлением H2O в объеме 5-10 мл, достигая в результате размера микрочастиц 50-300 нм. В итоге получали 242 г (98,6 %) микропорошка MnNa2H-ДТПА, который затем растворяли в физрастворе с получением растворов в диапазоне концентраций 0,5-1,75 М. За счет одновременного добавления гидроокиси натрия pH раствора устанавливалось в пределах 6,4-6,8.
Полученные растворы автоклавировались при температуре 140°C и затем фильтровались через мембранные микрофильтры «Millipore» (США); размер пор менее 0,22 мкм, диаметр сечения фильтра 30 мм. Фильтрация через микрофильтр с порами менее 0,22 мкм оказывалось достаточной для получения совершенно стерильного раствора для внутривенного введения: ни в одном случае не было выявлено признаков наличия микробиологических загрязнений. Затем препарат помещался в стандартные «пенициллиновые» флаконы по 10 мл под резиновой пробкой с закатыванием и повторным автоклавированием в течение часа и использовался как для физико-химических исследований, так и для экспериментов на лабораторных животных, в частности для оценки токсичности при внутривенном введении различных концентраций мангапентетата в водных растворах.
Контроль чистоты полученного раствора проводился по данным ВЭЖХ с помощью хроматографов «Миллихром» и «Цвет-4000» (НПФ «Цвет», Россия).
С помощью общепринятых лабораторных методов [7] оценивались также плотность, вязкость и осмоляльность 0,5M мангапентетата. При этом вязкость раствора как важнейший параметр, определяющий возможности быстрой внутрисосудистой инъекции контрастного препарата, оценивалась во всем интервале концентраций 0,5 М-1,75 М. Для сравнения также определялись в тех же условиях показатели вязкости широко используемых для рентгенангиогра-фических исследований и внутривенной урографии препаратов – йогексола и урографина.
Определение спин-решеточной релаксивности R1 мангапентетата и препарата сравнения – гадопентета-та проводилось с использованием неантропоморфных стеклянных фантомов, содержащих растворы контрастного препарата, различного разведения, по 33
H. Petersson et al. [8]. Все исследования были проведены с помощью резистивного низкопольного МР-томографа Магнетом Опен (Сименс Медикал). Для определения Т1, спин-эхо исследования проводились в Т1-взвешенном режиме, при времени эхо (TE), зафиксированном на величине TE=25 мс, при величинах времени повторения (TR) длительностью 250 мс, 500 мс, 750 мс, 1000 мс, 1500 мс и 2000 мс. Срезы МРТ при этом составляли в толщину 10 мм, при межсрезовом расстоянии 2 мм. На срезах в средней части фантомов выделялись зоны размером более 50 вокселов, и количественно определялась интенсивность Т1-взв. изображения в них. Строилась зависимость интенсивности Т1-взв. изображения от TR для каждого флакона, которая затем аппроксимировалась по методу наименьших квадратов, к следующему уравнению:
IT1-SE = A · [1 – e(–TR/T1)], где IT1-SE – интенсивность Т1-взвешенного изображения, A – интенсивность Т1-взв. изображения при TR=T1, TR – время повторения. Как было доказано ранее [H. Petersson et al. 1988], применение такого уравнения для аппроксимации зависимости IT1-SE от TR не дает ошибки более 2-4%, что вполне удовлетворительно для фантомной оценки релак-сивности. В результате были получены величины T1 для фантомов, содержащих контраст-парамагнетик в концентрациях 0,5-16 мМ. По этим данным строилась зависимость
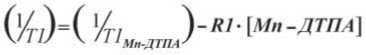
где R1 как раз и представляет собой искомую величину релаксивности контрастного препарата – парамагнетика.
Кроме того также были выполнены визуализа-ционные эксперименты с фантомами, содержащими раствор мангапентетата в 0,9% NaCl в количествах, близких к таковым, достигаемым в тканях при введении внутривенно – в интервале концентраций 0,25-8 мМ/л.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Мангапентетат представляет собой комплекс марганца (II) с динатрийдиэтилентриаминпентауксусной кислотой (рис. 1), обладающий высокой стойкостью в физрастворе и плазме при pH 5,5-8,0 (константа стойкости = 15,9 [Досон 1991]).
По данным хроматографического исследования, в составе готового раствора мангапентетата присутствовал только собственно Mn-ДТПА, а также незначительное количество свободного ДТПА, от 0,5% до 2%, считая относительно количества комплекса Mn-ДТПА. Примесей тяжелых металлов, других токсических или балластных соединений обнаружено не было. При хроматографическом анализе препарата спустя 34
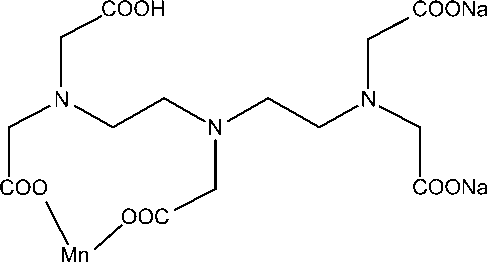
Рис. 1. Структурная формула мангапентетата (MnNa2H-ДТПА)
Таблица 1
Основные физические свойства раствора Пентаманга (мангапентетата 0,5 М) по сравнению с препаратом сравнения – 0,5 М Гадопентетатом
|
Показатель |
мангапентетат 0,5 М |
гадопентетат 0,5 М |
|
Осмоляльность, мОсмоль / (кг H2O), при 37°С |
1947±12 |
1955±15 |
|
Вязкость, мПа*с, при 37°С |
2,77±0,07 |
2,90±0,05 |
|
Релаксивность R1, ммоль-1*с-1, при B0 = 0,20 Т |
3,69±0,35 |
3,95±0,12 |
-
3, 6 и 12 мес не было отмечено признаков появления свободного Mn (II) в определяемых концентрациях или иных изменений состава препарата, что позволяет говорить о его стабильности в течение этого времени при комнатной температуре.
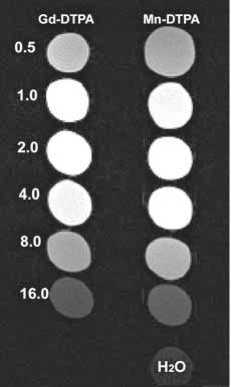
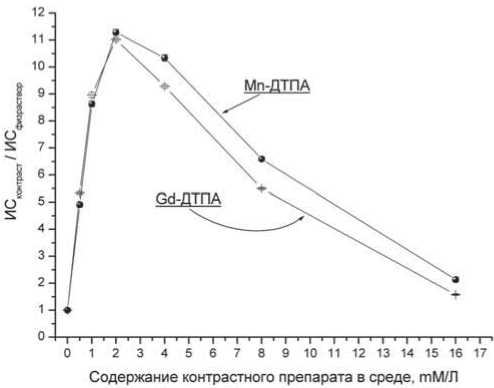
Показатели осмоляльности 0,5 М раствора ман-гапентетата и другие его физические показатели представлены в табл. 1. Релаксивность мангапенте-тата, определенная с помощью низкопольного МР-томографа при исследовании фантомов с различными концентрациями манагпентетата, примерно соответствующими таковым в тканях при клинических исследованиях с обычными дозировками парамагнетиков (0,1 мМ/10 кг веса тела), оказалась весьма близкой к показателю препарата сравнения – гадопентетата, несколько уступая ей (табл. 1). При этом визуально картина фантомов (рис. 2 а) не отличалась, а зависимость интенсивностей Т1-взвешенного изображения от концентрации (рис. 2 б) для этих двух препаратов также была весьма близка.
Плотность пентаманга 1,0 М составила 1,214 г/л, а во всем диапазоне концентраций зависела от содержания мангапентетата в физрастворе как [Плотность] = 1,01+0,233*[Mn-ДТПА] (r=0,978, p=0,00073). Зависимость вязкости раствора мангапентетата от
а)
б)
Рис. 2. (а) МР-томограмма фантома с различными концентрациями мангапентетата в физрастворе в Т1-взвешенном режиме (время повторения = 400 мс, время эхо = 20 мс). (б) – результаты количественной оценки изменений интенсивности Т1-взвешенного изображения этого фантома. Фантом с растворами мангапентетата (MnNa2H-ДТПА) и гадопентетата (Gd-ДТПА) в концентрациях 0 – 16 mM/л
токсические эффекты раствора мангапентетата обусловлены по сути не только препаратом как таковым, но и одновременным введением объемов жидкости, сопоставимым с объемом циркулирующей крови крыс.
Фармакологические характеристики и визуализа-ционные свойства мангапен-тетата как парамагнитного контрастного препарата при получении его в жидкой фазе были детально изучены ранее и опубликованы [5]. Полученные здесь результаты позволяют говорить, что нанодиспергирование как технология получения мангапентетата позволяет концентрации представлена на рис. 3. Можно видеть, что вплоть до концентрации 1,25 М вязкость раствора мангапентетата находится в пределах, обеспечивающих нетрудную внутривенную инъекцию с необходимой скоростью – до 4-5 мл/с, необходимых обычно для ангиографического исследования [9].
При исследовании токсичности растворов манга-пентетата in vivo оказалось, что отсутствует прямая зависимость величины LD50 от количества вводимого мангапентетата. Так, LD50 при внутривенном введении у крыс составила 14,1±4,5 мл/кг для 0,5 М раствора, 13,4±3,7 мл/кг для 0,75 М раствора и 12,3±3,9 мл/кг для 1,0 М раствора мангапентетата. Это позволяет предполагать, что мангапентетат во всех формах представляет собой соединение, относящееся к группе 4 препаратов по ГОСТ 12.1.007–76 (малотоксичные вещества), и
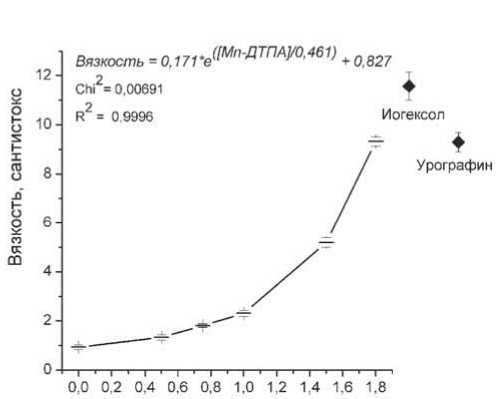
Мп(П)-ДТПА, М/л
Рис. 3 Зависимость вязкости водного раствора мангапентетата от его концентрации при 20°С. Для сравнения приведены также показатели вязкости для широко используемых для ангиографии рентгеноконтрастных препаратов – омнипака (иогексола) и урографина произвести этот контраст – парамагнетик в любой необходимой концентрации инъекционного раствора, а получаемые формы препарата по параметрам острой токсичности позволяют отнести их все к группе препаратов 4. В настоящее время ведется исследование острых токсических свойств пентаманга в полном соответствии с требованиями Фармкомитета России. Однако уже теперь обоснованно считать, что нанодиспергирование – практически приемлемая технология получения парамагнитных контрастных препаратов на основе комплексов марганца с ДТПА. Получаемые при этом препараты мангапентетата обеспечивают значительное усиление Т1-взвешенных МРТ изображений в качестве парамагнитного контраста в эксперименте.
Список литературы Твердофазное нанодисперсное получение и оценка свойств комплекса марганца с диэтилентриаминпентауксусной кислотой как контрастного препарата для магнитно-резонансной томографии
- Синицын В.Е., Корниенко В.Н., Никитин В.Г. и др. Применение Омнискана (гадодиамида) в магнитнорезонансных исследованиях центральной нервной системы.//Вест. рентгенол. радиол.-1995. -№ 4: -С. 5-11.
- Runge V.M., Muroff L.R., Jinkins J.R. Central nervous system: review of clinical use of contrast media.//Top Magn Reson Imaging. -2001. -V. 12. -№ 4. -P. 231-263.
- Bulte J.W., Kraitchman D.L. Iron oxide MR contrast agents for molecular and cellular imaging.//NMR Biomed. -2004. -V. 17. -№ 7. -P. 484-499.
- Rocklage, S.M.; Cacheris W.P.; Quay S.C. et al. Manganese (II) N,N'-dipyridoxylethylenediamine-N,N'-diacetate 5,5'-bis(phosphate). Synthesis and characterization of a paramagnetic chelate for magnetic resonance imaging enhancement.//Inorg.Chem. -1989. -V. 28. -P. 477-485.
- Усов В.Ю., Белянин М.Л., Бородин О.Ю. и др. Применение Mn-диэтилентриаминпентаацетата (ДТПА) для парамагнитного контрастирования при магнитно-резонансной томографии -результаты доклинических исследований и сравнения с Gd-ДТПА.//Мед. визуализация. -2007. -№ 4. -C. 134-142.
- Досон Р., Эллиот Д., Эллиот У., Джонс К. Справочник биохимика. М.: Мир. 1991; 338.
- Касаткин А. Г. Основные процессы и аппараты химической технологии. М.: Химия. 1998.
- Petersson H., Slone R.M., Spanier S. et al. Musculoskeletal tumors: T1 and T2 relaxation times.//Radiology. -1988. -167. -P. 783-785.
- Кармазановский Г. Г. Компьютерная томография -основа мощи современной рентгенологии.//Мед. визуализация. -2005. -№ 6. -C. 139-145.


