Участие адренорецепторов в регуляции роста эмбриональной сетчатки
Автор: Лопатин Алексей Игоревич, Пасатецкая Наталья Анатольевна, Удовенко Екатерина Григорьевна, Лопатина Екатерина Валентиновна
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 3 т.20, 2023 года.
Бесплатный доступ
В настоящее время изучаются перспективы применения адреноблокаторов в терапии ретинопатии недоношенных, а биогенные амины используются для инотропной поддержки при выхаживании детей с низкой и экстремально низкой массой тела. Цель исследования - изучить вклад адренорецепторов в регуляцию роста эмбриональной сетчатки в опытах in vitro. В работе использован метод органотипической культуры ткани сетчатки. Объектами исследования являлись эксплантаты ткани сетчатки 10-12-дневных куриных эмбрионов. В условиях органотипического культивирования ткани сетчатки обнаружен трофотропный эффект норадреналина (10-12 М). Этот эффект реализовывался при участии ог1-адренорецепторов. Ингибиторный анализ показал, что ретинотоксический эффект высоких концентраций катехоламинов основан на активации Д-адренорецепторов. В прямых экспериментах на уровне in vitro зарегистрирован ретенопротективный эффект пропаранолола. Для подтверждения перспектив применения пропранолола при лечении ретинопатий новорожденных необходимы дополнительные исследования на моделях in vivo. Особое внимание необходимо уделить реакциям со стороны сердечно-сосудистой системы, поскольку есть данные о провоцировании брадикардии и гипотензии при использовании пропранолола у новорожденных. Сочетание экспериментов in vitro и in vivo позволит корректно рассчитать дозы изучаемого препарата и минимизировать возможные побочные эффекты от его применения в дальнейшем.
Ретинопатия недоношенных, адренорецепторы, органотипическая культура ткани, катехоламины
Короткий адрес: https://sciup.org/142238797
IDR: 142238797 | УДК: 612.843.15
Participation of adrenoreceptors in the regulation of the growth of the embryonic retina
Currently, prospects for the use of adrenoblockers in the treatment of retinopathy of prematurity are being studied, and biogenic amines are used for inotropic support for inotropic support when caring for children with low and extremely low body weight. The aim of the investigation; to study the contribution of adrenoreceptors to the regulation of the growth of the embryonic retina in in vitro experiments. In the work was used the method of organotypic culture of retina tissue. The objects of the study were explants of retina tissue of 10-12-day-old chicken embryos. The trophotropic effect of norepinephrine (10-12 M) was detected In the conditions of the organotypic cultivation of retina tissue. This effect was realized with the participation of or1-adrenergic receptors. Inhibitory analysis showed that the retinotoxic effect of high concentrations of catecholamines is based on the activation of Д-adrenergic receptors. In direct experiments at the in vitro level, the retinoprotective effect of propranolol was registered. To confirm the prospects of using propranolol in the treatment of neonatal retinopathy, additional studies on in vivo models are needed. Particular attention should be paid to reactions from the cardiovascular system, since there is evidence of provoking bradycardia when using propranolol in newborns. The combination of in vitro and in vivo experiments will make it possible to correctly calculate the doses of the studied drug and minimize possible side effects from its use in the future.
Текст научной статьи Участие адренорецепторов в регуляции роста эмбриональной сетчатки
Ретинопатия недоношенных - одно из наиболее тяжелых заболеваний, приводящих к неустранимой слепоте с раннего детского возраста. Степень зрелости организма ребенка, как правило, определяет частоту развития и тяжесть заболевания. С 2011 г. в России принято выхаживать младенца с возраста 22 недель, если его масса тела составляет более 500 г, и длина тела более 35 см [1]. Исходя из вышесказанного, в настоящее время осуществляется активный поиск адекватных моделей, позволяющих исследовать физиологические механизмы ретинопротекции. Сетчатка глаза куриного эмбриона является уникальным экспериментальным объектом, поскольку содержит все типы клеток, которые находятся в сетчатке человека. Сетчатка и сам орган зрения играют ведущую роль в жизнеобеспечении птенцов кур (цыплят) после вылупления из яйца. Куры относятся к выводковым птицам, им свойственно зрелорождение, бинокулярное цветное зрение и такое явление как импритинг. Гестационный возраст 10-12-дневного куриного эмбриона соответствует 19-24 неделе пренатального развития человека. В период эмбриогенеза ткань сетчатки формируется путем регуляции координации пролиферации клеток-предшественников различными нейротрансмиттерами, включая моноамины [2]. При выхаживании младенцев с низкой и экстремальной низкой массой тела для инотропной поддержки применяют катехоламины. Вклад катехоламинов в регуляцию роста эмбриональной сетчатки изучен мало.
ЦЕЛЬ РАБОТЫ
Изучить вклад адренорецепторов в регуляцию роста эмбриональной сетчатки в опытах in vitro .
МЕТОДИКА ИССЛЕДОВАНИЯ
В работе использован метод органотипической культуры ткани сетчатки. Объектами исследования являлись эксплантаты ткани сетчатки 10-12-дневных куриных эмбрионов. Каждая серия экспериментов включала в себя 40 контрольных и 40 экспериментальных эксплантатов на каждую исследованную концентрацию действующих веществ. Фрагменты ткани сетчатки размером около 1 мм помещали в стерильные чашки Петри диаметром 40 мм на коллагеновую подложку и культивировали в СО2-инкубаторе (Binder, Германия) при 37 оС и 5 % СО2 в течение 3 суток. Состав питательной среды описан ранее [3]. В питательную среду экспериментальных эксплантатов добавляли адреналин и норадреналин, пропранолол, урапидил согласно протоколу эксперимента. Для количественной оценки степени роста эксплантатов применяли морфометрический метод. Морфометрический критерий «индекс площади» (ИП) рассчитывали как отношение общей площади эксплантата к площади исходной зоны. Значение ИП контрольных эксплантатов принимали за 100 %. Статистическую обработку результатов проводили с помощью программы «Statistica 10.0». При сравнении контрольной и экспериментальной групп использовали t-критерий Стьюдента для двух независимых выборок. Различия считались достоверными при р < 0,05. Результаты представлены в виде среднее арифметическое ± стандартное отклонение (M ± а).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Влияние адреналина на рост экплантатов ткани сетчатки исследовали в диапазоне концентраци от 10-4 до 10-12 М. Трофотропного действия препарата не обнаружено. В высоких концентрациях (10-4 и 10-5 М) адреналин оказывал ретинотоксический эффект.
ИП экспериментальных эксплантатов был ниже контрольного значения на 95,0 ± 2,0 % ( n = 40, р < 0,001) и 35 ± 5,0 % ( n = 40, р = 0,01) (рис. 1).
При исследовании влияния норадреналина (10 -4 -10-12 М) на рост эксплантатов ткани сетчатки обнаружен трофотропный эффект препарата в дозе 10-12 М. ИП был выше контрольного значения на 40 ± 6,0 % ( n = 40, р = 0,01). В высоких концентрациях (10-410-5 М) норадреналин, так же как и адреналин, угнетал рост эксплантатов исследуемой ткани (рис. 2).
Для изучения механизма трофотропного и ретинотоксического действия катехоламинов в питательную среду экспериментальных чашек Петри вводили неселективный в -адреноблокатор пропранолол и селективный а 1 -адреноблокатор урапидил. Предварительно оценили влияние блокаторов на рост эксплантатов ткани сетчатки.
Пропранолол в диапазоне концентраций от 10-4 до 10-10 М проявлял дозозависимое действие. В концентрации 10-4 М препарат практически полностью угнетал рост экспериментальных эксплантатов, ИП был ниже контрольного значения на 95,0 ± 1,8 % ( n = 40, р < 0,01). При введении в питательную среду пропранолола в концентрации 10-6 М ИП экспериментальных эксплантатов был ниже контрольного значения на 32,0 ± 5,9 % ( n = 40, р = 0,014). В следующей части работы в -адреноблокатор использовали в максимальной концентрации, которая не влияет на рост эксплантатов ткани сетчатки (10-8 М).
Урапидил в концентрациях 10-4-10-8 М на рост эксплантатов ткани сетчатки не влиял. ИП не отличался от контрольного значения. Поэтому в следующих сериях экспериментов для изучения механизма трофотропного действия катехоламинов блокатор применяли в концентрации 10-4 М.
Для оценки механизма трофотропного действия норадреналина эксплантаты ткани сетчатки культивировали в питательной среде, содержащей норадреналин (10-12 М) и пропранолол (10-8 М) или урапи-дил (10-4 М). Стимулирующее рост эксплантатов действие норадреналина сохранялось в присутствии в-адреноблокатора. ИП был на 37,0 ± 6,0 % (n = 40, р = 0,02) выше контрольного значения и не отличался от ИП эксплантатов, культивируемых только в присутствии норадреналина (10-12 М). При введении в питательную среду совместно урапидила и норадреналина, трофотропное действие последнего отсутствовало. ИП экспериментальных эксплантатов не отличался от контрольного значения (рис. 3). Оценку ретинотоксического эффекта катехоламинов проводили при культивировании эксплантатов в питательной среде, содержащей катехоламины в концентрации 10-5 М и пропранолол (10-8 М). Ретинотоксический эффект как адреналина, так и норадреналина на фоне β-адрено-блокатора отсутствовал (рис. 4).
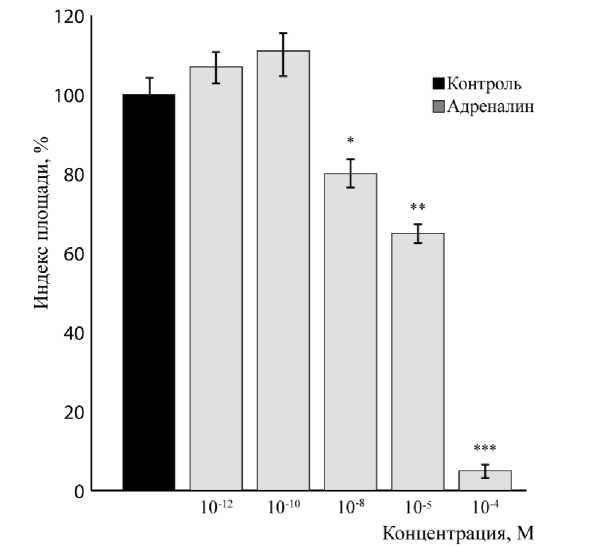
Рис. 1. Влияние адреналина на рост эксплантатов ткани сетчатки: * - p < 0,05; ** - p < 0,01, *** - p < 0,001 по сравнению с контрольным значением
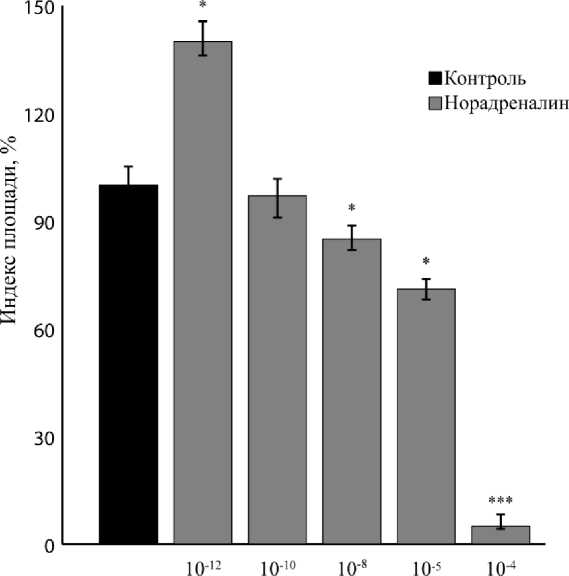
Концентрация, М
Рис. 2. Норадреналин дозозависимо регулирует рост эксплантатов ткани сетчатки: * - p < 0,05, *** - p < 0,001 по сравнению с контрольным значением
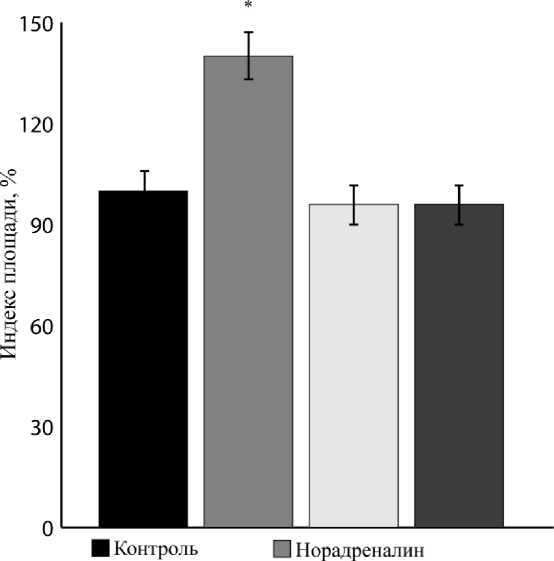
□ Урапидил ■ Норадреналин+Урапидил
Рис. 3. Трофотропный эффект норадреналина (10-2 М) опосредован активацией а і -адренорецепторов: * - p < 0,05 по сравнению с контрольным значением
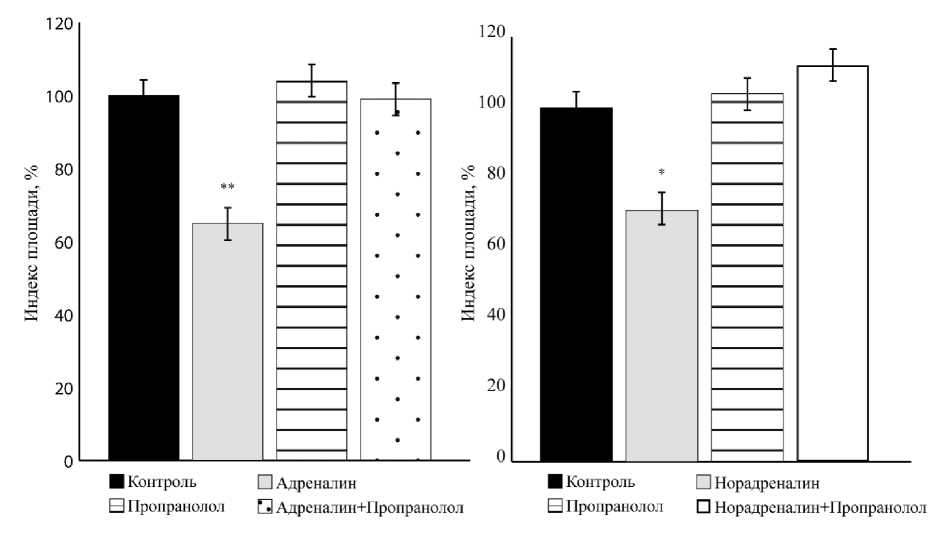
Рис. 4. Пропранолол нивелирует ретинотоксический эффект катехоламинов:
* - p < 0,05, ** - p < 0,01 по сравнению с контрольным значением
Поскольку сетчатка является тканью с высокой метаболической потребностью, неудивительно, что нарушение гемодинамики сетчатки играет критическую роль в патогенезе ряда глазных болезней. Патогенез ретинопатии недоношенных связан с нару- шением образования новых сосудов сетчатки и изменением уже сформировавшихся сосудистых трактов. Наблюдается прекращение образования сосудов в аваскулярных зонах сетчатки, а новообразованные сосуды начинают прорастать в стекловидное тело [4].
При классическом течении заболевания высокие результаты демонстрирует применение лазерко-агуляции. Однако эта терапия разрушает части сетчатки и может привести к серьезным осложнениям в более позднем возрасте. В связи с этим разрабатываются альтернативные подходы к лечению заболевания: консервативное лечение при помощи внутриглазных инъекций блокатора фактора роста эндотелия (VEGF), основного индуктора неоангиогенеза. Изучаются ангиогенные свойства моноаминов.
Не смотря на пристальное внимание к процессам неоангиогенеза, как ведущему патологическому фактору заболевания, нельзя игнорировать влияние препаратов на клетки сетчатки. Возможность модуляции нейропротекции в терапии ретинопатии может снизить риски оперативного лечения, а в связи с этим уменьшить осложнения анестезиологического и хирургического вмешательства. Особую роль в ретино-протекции могут играть моноамины. Доказано, что в эмбриональный период развития катехоламины проявляют трофотропные свойства и стимулируют рост ткани сердца [5] и кости [6]. Механизм трофо-тропного действие катехоламинов тканеспецифичен и реализуется как через β -, так и через α -адрено-рецепторы. Полученные ранее результаты показали, что β -адренорецепторы не вовлечены в реализацию ретиностимулирующего действия норадреналина [7].
В сетчатке зарегистрированы все типы адренорецепторов: α 1 , α 2 , β 1 , β 2 , β 3 [8]. α 1 -адрено-рецепторы локализованы преимущественно в сосудах сетчатки [9], во внешнем плексиформном слое сетчатки крысы и пигментном эпителии сетчатки крупного рогатого скота, кролика, мыши и человека, где они модулируют транспорт K+ и Cl- и электрические токи [10].
Результаты in vivo исследований влияния α 1 -адре-нергических агонистов на регуляцию сосудистого сопротивления и перфузию сетчатки противоречивы, что затрудняет однозначные выводы о функциональной роли α 1 -адренорецепторов [8]. Показано, что стимуляция α-адренергических рецепторов катехоламинами усиливает васкулогенез, пролиферацию и миграцию эндотелиальных клеток [11]. Вопрос об участии α 1 -адренорецепторов в регуляции ретиноге-неза остается открытым. В нашем исследовании впервые показано, что трофотропное действие низких концентраций норадреналина реализуется через α 1 -адренорецепторы.
β-адренорецепторы локализованы практически во всех слоях сетчатки и играют важную роль в функционировании сосудов и нейронов сетчатки [8]. Стрессовые состояния, такие как гипоксия, резко увеличивают уровень катехоламинов в сетчатке. Считается, что активация β-адренорецепторы усиливает регуляцию индуцируемого гипоксией фактора-1 (HIF-1) и VEGF. Блокатор β-адренорецепторов, пропранолол, эффективно ингибировал повышение экспрессии VEGF, вызванное гипоксией, и сопровождающий его неоваскулярный ответ в сетчатке [4]. Ана- логичным образом, пропранолол, вводимый подкожно, снижал уровни VEGF и HIF-1 в мышиной модели кислород-индуцированной ретинопатии (OIR). В связи с этим в настоящее время активно исследуется возможность применения пропранолола в терапии ретинопатиии новорожденных. Пероральное введение препарата не было успешным, поскольку, не смотря на снижение прогрессирования заболевания, сопровождалось развитием брадикардии и гипотензии. В результате исследование было прекращено по причине роста смертности в группе лечения [12].
Были разработаны глазные микрокапли с пропранололом 0,1%, которые протестированы в многоцентровом пилотном клиническом исследовании для анализа безопасности и эффективности лечения недоношенных новорожденных со 2-й стадией ретинопатии. Однако второй этап этого исследования был прекращен, поскольку у четверых из 19 новорожденных наблюдалось прогрессирование до 2-й или 3-й стадии с дополнительным заболеванием [13]. Следовательно, несмотря на некоторые успехи, вопрос безопасности применения пропранолола для лечения ретинопатии остается открытым.
В нашем исследовании зарегистрировано ретинопротекторное действие пропранолола на фоне высоких концентрации катехоламинов.
ЗАКЛЮЧЕНИЕ
Применение метода органотипической культуры ткани позволяет детально оценить физиологическую активность изучаемых веществ, поскольку отсутствуют влияния со стороны систем целого организма. Поскольку, биогенные амины используются для инотропной поддержки при выхаживании детей с низкой и экстремально низкой массой тела. Для подтверждения перспектив применения пропранолола при лечении ретинопатий новорожденных необходимы дополнительные исследования на моделях in vivo . Особое внимание необходимо уделить реакциям со стороны сердечно-сосудистой системы. Сочетание экспериментов in vitro и in vivo позволит корректно рассчитать дозы изучаемого препарата и минимизировать возможные побочные эффекты от его применения в дальнейшем.
Список литературы Участие адренорецепторов в регуляции роста эмбриональной сетчатки
- Симаходский А. С., Горелик Ю. В., Горелик К. Д. и др. Смертность детей, родившихся на ранних сроках гестации,-непреодолимый барьер или резерв снижения младенческой смертности? Вопросы современной педиатрии. 2020;19(5):340–345. https://doi.org/10.15690/vsp.v19i5.2209.
- Martins R. A., Pearson R. A. Control of cell prolifera-tion by neurotransmitters in the developing vertebrate retina. Brain Res. 2008;4(1192):37–60. https://doi.org/ 10.1016/ j.brainres.2007.04.076.
- Пасатецкая Н. А., Лопатин А. И., Кипенко А. В., Лопатина Е. В. Ремоделирование костной ткани: возможный вклад адреналина. Волгоградский научно-медицинский журнал. 2017;4(56):47–50.
- Bancalari A., Schade R. Update in the Treatment of Retinopathy of Prematurity. Am J Perinatol. 2022;39(1):22–30. https://doi.org/ 10.1055/s-0040-1713181.
- Lopatina E. V., Kipenko A. V., Pasatetskaya N. A. et al. Modulation of the transducer function of Na+,K+-ATPase: new mechanism of heart remodeling. Can J Physiol Pharmacol. 2016;94(10):1110–1116. https://doi.org/ 10.1139/cjpp-2015-0577.
- Пасатецкая Н. А., Лопатин А. И., Климшин С. И. и др. Норадреналин регулирует остеогенез в эмбриональный период развития. Гены и клетки. 2021;16(4):50–53. https://doi.org/10.23868/202112006.
- Лопатина Е. В., Пеннияйнен В. А., Цырлин В. А. Исследование влияния норадреналина и селективных b1-адре-ноблокаторов на рост эксплантатов ткани сетчатки. Бюллетень экспериментальной биологии и медицины. 2012; 153(1):56–58.
- Ruan Y., Böhmer T., Jiang S., Gericke A. The Role of Adrenoceptors in the Retina. Cells. 2020;9(12):2594. https://doi.org/ 10.3390/cells9122594.
- Bohmer T., Manicam C. The alpha1b-adrenoceptor subtype mediates adrenergic vasoconstriction in mouse retinal arterioles with damaged endothelium. Br. J. Pharmacol. 2014;171:3858–3867. https://doi.org/ 10.1111/bph.12743.
- Skarphedinsdottir S. B., Eysteinsson T., Árnason S. S. Mechanisms of Ion Transport Across the Mouse Retinal Pigment Epithelium Measured In Vitro. Invest Ophthalmol Vis Sci. 2020;61(6):31. https://doi.org/ 10.1167/iovs.61.6.31.
- Tilan J., Kitlinska J. Sympathetic Neurotransmitters and Tumor Angiogenesis-Link between Stress and Cancer Progression. J Oncol. 2010; 2010:539706. https://doi.org/ 10.1155/2010/539706.
- Filippi L., Cavallaro G., Bagnoli P. et al. Oral propran-olol for retinopathy of prematurity: risks, safety concerns, and perspectives. J Pediatr. 2013;163(6):1570–1577. https://doi.org/ 10.1016/j.jpeds.2013.07.049.
- Filippi L., Cavallaro G. Propranolol 0.1% eye micro-drops in newborns with retinopathy of prematurity: A pilot clini-cal trial. Pediatric Res. 2017;81: 307–314. https://doi.org/ 10.1038/pr.2016.230.


