Участвуют ли жировые тела щек в постнатальном гемопоэзе?
Автор: Марков Игорь Иванович, Буланов Сергей Иванович, Моисеева Татьяна Васильевна
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.23, 2015 года.
Бесплатный доступ
Изучена гистоструктура жировых тел щек, извлеченных при аутопсии новорожденных, детей и взрослых людей обоего пола. Цель исследования - доказать участие жировых тел щек в постнатальном гемопоэзе. Полученные данные позволяют считать, что жировые тела щек являются органами, функционирующими на протяжении всего постнатального периода онтогенеза человека. У новорожденных и детей грудного возраста в жировых телах щек происходит активный внутрисосудистый эритро - и миелопоэз.
Жировые тела щек, постнатальный онтогенез, гемопоэз
Короткий адрес: https://sciup.org/143177058
IDR: 143177058
Do suctorial pads participate in postnatal haemopoiesis?
The paper presents the study of the histostructure of suctorial pads extracted postmortem from neonates, children and adults of both sexes. The aim of the research is to the participation of suctoriak pads are organs which function throughout the entire postnatal period of human ontogenesis. Neonates and nursing infants have active intrascular erythro-and myelopoesis of suctoriak pads.
Текст научной статьи Участвуют ли жировые тела щек в постнатальном гемопоэзе?
Введение. В перинатальном периоде развития ребенка основным органом кроветворения является костный мозг [1]. Однако в этот период у многих млекопитающих кроветворение еще сохраняет эмбриональный характер [2]: его очаги обнаруживаются в тимусе [ 3 ], в печени [4] в селезенке [5] и даже в брыжейке тонкой кишки [6]. Нередко подобная ситуация отмечается и у новорожденных детей [7]. Более того, у них в периферической крови наблюдается лейкоцитоз с выраженной лимфопенией и нейтрофильным гранулоцитом [1, 10 ] при индексе Шагана – 0,4 [2 ]. Очевидно, что эритроциты способствуют снижению у новорожденных детей иммунореактивности [ 11-13 ], а «аварийная» линия защиты у них формируются нейтрофильными гранулоцитами, принадлежащими к неспецифическим факторам иммунитета [14]. В работе [15] впервые были опубликованы данные об эритропоэзе в жировых телах щек новорожденных детей. Однако продолжается ли эритропоэз в жировых телах щек и в более поздние сроки постнатального онтогенеза или он ограничен только неонатальным периодом до настоящего времени остается неясным.
Цель исследования – доказать участие жировых тел щек человека в постнатальном гемопоэзе.
Материал и методы исследования. В работе использован аутопсийный материал жировых тел щек новорожденных детей (п=5), детей грудного возраста (п=3) и биопсийный материал жировых тел щек людей I периода зрелого (п=5) и пожилого (п=5) возрастов.
При аутопсиях жировые тела щек полностью извлекались после линейных разрезов кожи по линии, соединяющей угол рта и мочку ушной раковины. Биопсийный материал получен во время хирургических операций в челюстно-лицевой области. После фиксации материала в 10% нейтральном формалине (5-7 суток) готовились серийные парафиновые срезы для окраски гемо-токсилином и эозином, по Ван Гизону, азур II-эозином и парарозанилином и толуидиновым синим. Микропрепараты изучались под микроскопом drica ДМ1000 и фотографировались цифровой видеокамерой.
Результаты исследования и их обсуждение. Жировые тела щек справа и слева обнажались после линейных разрезов кожи по линиям, соединяющие мочки ушных раковин с углами рта. Скуловые дуги распиливались и удалялись после отделения от них височных фасций. Жевательные мышцы удалялись вместе со скуловыми дугами и фрагментами ветвей нижней челюсти. Масса жировых тел была удивительно постоянна и не коррелировала с массой тела субъекта. Основная часть жировых тел щек представляется в виде желоба с вертикальной осью, открытого в заднем отделе, имеющего боковую и срединную поверхности, выпуклые спереди и вогнутые сзади. Топографически в основной части жировых тел необходимо выделить три отдела: нижний – ску- ловой, верхний – латерально - пазушный и латеральный – орбитальный. Нижний скуловой отдел снаружи прилежит к жировой клетчатке щечной области, вверху – большой скуловой мышце, а спереди – ограничен ротовыми ветвями лицевого нерва. Снаружи к скуловому отделу прилежит выводной проток околоушной слюнной железы, окруженный жировой клетчаткой. Проток делает резкий под прямым углом изгиб, проникает в жевательно-щечную ямку и затем перфорирует щечную мышцу. Верхний – латерально-пазушный и латерально-орбитальный отделы жировых тел продолжаются вверх и на уровне глазниц переходят в височные отростки тел. Основная часть жировых тел щек является постоянным образованием и была обнаружена в 100% случаев (рис. 1).
По гистоструктуре щечная область представляет собой два отчетливо выраженных слоя тканей: 1 – поверхностный, расположенный под кожей (надфасциальный) и 2 – глубокий (подфасциальный или подапоневротический). Первый слой объединен с подкожно-жировой клетчаткой височной и околоушной областей, второй – с жировым телом щеки.
Жировые тела щек окружены тонкой соединительно-тканевой капсулой, которая легко и полностью снимается. Капсула имеет достаточно постоянную толщину, как на аутопсийных препаратах новорожденных детей, так и на биопсийных препаратах людей I зрелого возраста - от 60, 5 + 12,2 мм (растянутая капсула) до 106,8 +14,7 мм (собранная в складки). Жевательная и щечная мышца в области жирового тела щеки без всяких границ переходят друг в друга. Слизистая оболочка щеки и щечная мышца интимно соединены между собой, а пучки щечной мышцы проникают в паренхиму жирового тела. Щечная мышца у новорожденных детей развита чрезвычайно слабо и находится непосредственно под слизистой оболочкой щеки. Она начинается широким основанием от наружных поверхностей верхней и нижних челюстей напротив альвеол моляров, а сзади - от крыловидно-нижнечелюстных связок и направляется к углу рта. Здесь она сливается внизу и вверху с круговой мышцей рта. Сзади щечная мышца прикрывается жевательной мышцей, от которой она отделена крыловидно-нижнечелюстным отростком жирового тела. В щечных отделах преддверия рта щечная мышца находится в глубине мягких тканей на нижней челюсти. Ее пучки идут сзади от крыло-челюстного шва, сверху – от альвеолярного отростка верхней челюсти, снизу - от тела нижней челюсти, латеральнее наружной косой линии в зоне нижнее-челюстного кармана, на участке, ограниченном медиально-альвеолярным гребнем. В мышечных пучках щечной мышцы мало рыхлой соединительной ткани, поэтому сарколеммы пер- вичных мышечных волокон плотно контактируют друг с другом, а их продолговатые вытяжные ядра располагаются непосредственно под сарколеммой. Средний диаметр мионов составлял 10,2 +0,5 мкм и их поперечная исчерченность была выражена чрезвычайно слабо. В многочисленных участках щечной мышцы на всех препаратах наблюдались различные стадии формирования эктопических очагов эритропоэза. Вначале ее мышечные волокна окончательно теряли поперечную исчерченность и фрагментировались, а ядра утрачивали вытянутую форму и становились округлыми или овальными (рис. 2). Измененные мышечные ядра располагались внутри мышечных волокон беспорядочно, смещаясь на периферию и в дальнейшем, очевидно, исчезали из них. Поэтому часть мышечных волокон и на поперечных, и на продольных срезах была лишена ядер (рис. 3). В других участках щечной мышцы контуры, фрагментов трансформированных мионов выглядели более четкими, а между ними возникали многочисленные связи в виде сарколеммальных мостиков. Затем за счет сарколеммальных связей и длинных отростков реликулярных клеток целые группы фрагментарно трансформированных ми-онов оказывались изолированными от интактных участков щечной мышцы (рис. 4). Этот процесс изоляции фрагментов трансформированных ми-онов завершался формированием значительных по диаметру вазоидов (от 300,0 – 600,0 мкм). Стенка их была образована длинными отростками ретикулярных клеток, но в отдельных участках она могла прерываться при полном отсутствии базальной мембраны (рис. 5). Просвет вазои-дов был заполнен в одних случаях фрагментами трансформированных миоцитов и форменными элементами крови, в других случаях - эритробластическими островками и эритроцитами, в третьих - полипотентными стволовыми клетками; в четвертых – только нейрофильными гранулоцитами (рис. 5,6,7,8). В большинстве препаратов к стенке вазоидов снаружи интимно прилегали фрагменты трансформированных миоцитов, возможно, и участвующих в структурной организации ее стенки (рис. 9). Окончательно сформированные вазоиды, в просвете которых определялись только форменные элементы крови – эритроциты и лейкоциты, становились составной частью микрососудистого русла жировых тел щек (рис. 10).
В красном костном мозге млекопитающих основными структурами, обеспечивающими гемопоэз являются синусоиды.
Они формируются в пренатальном периоде онтогенеза, но активно начинают функционировать только после рождения. Структуры, подобные синусоидам красного костного мозга, формируются постнатальном периоде и в жировых телах щек
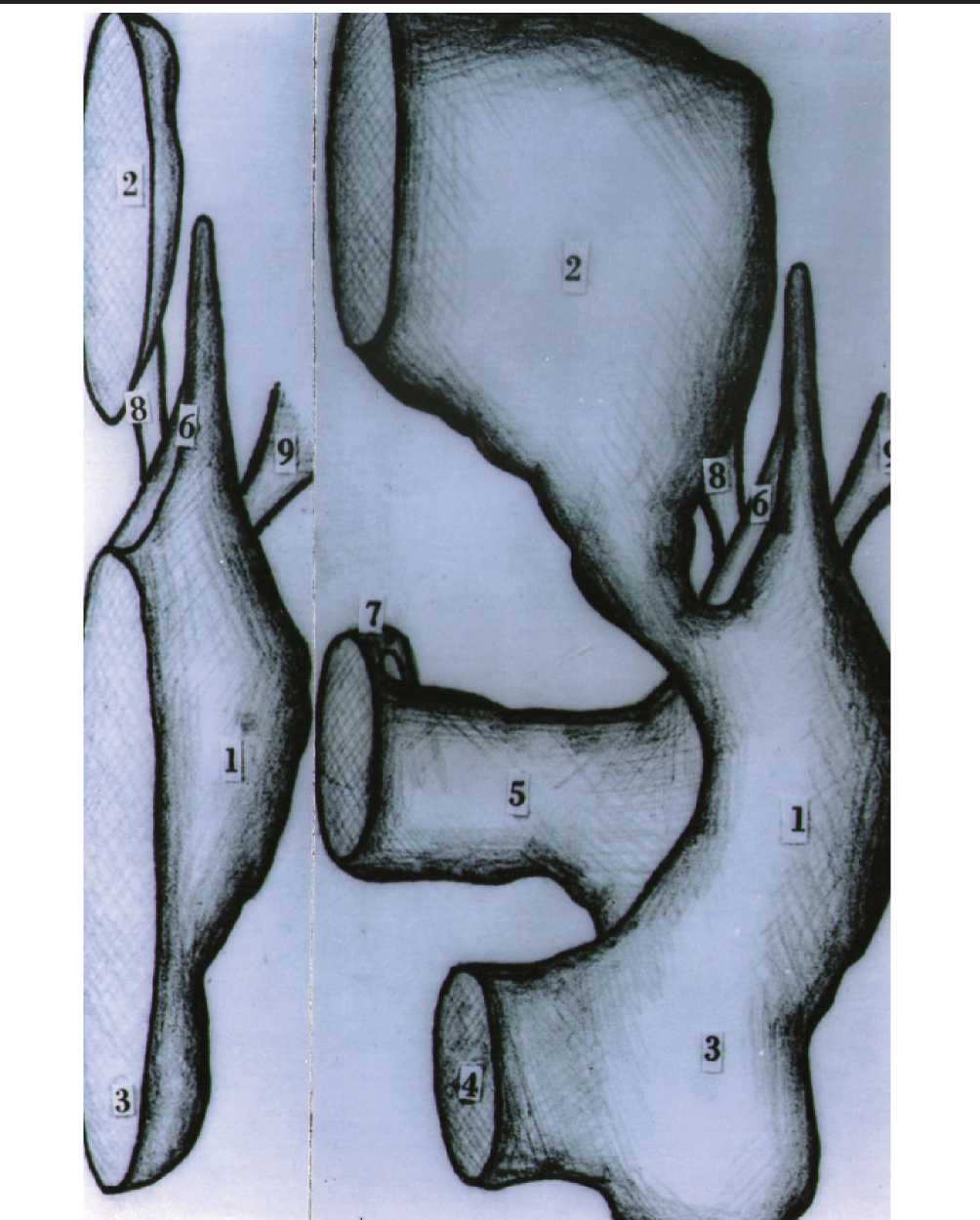
Рис. 1. Схема жирового тела щеки новорожденного ребенка 1, 3 – основная часть; 2 – поверхностный височный отросток; 4 – жевательный отросток; 5 – крыловиднонижнечелюстной отросток; 6 – глубокий височный отросток; 7 – межкрыловидный отросток; 8 0 крыло-небный отросток; 9 – нижнее-глазничный отросток. а – вид спереди; б – вид снаружи. Реконструкция с макропрепаратов.
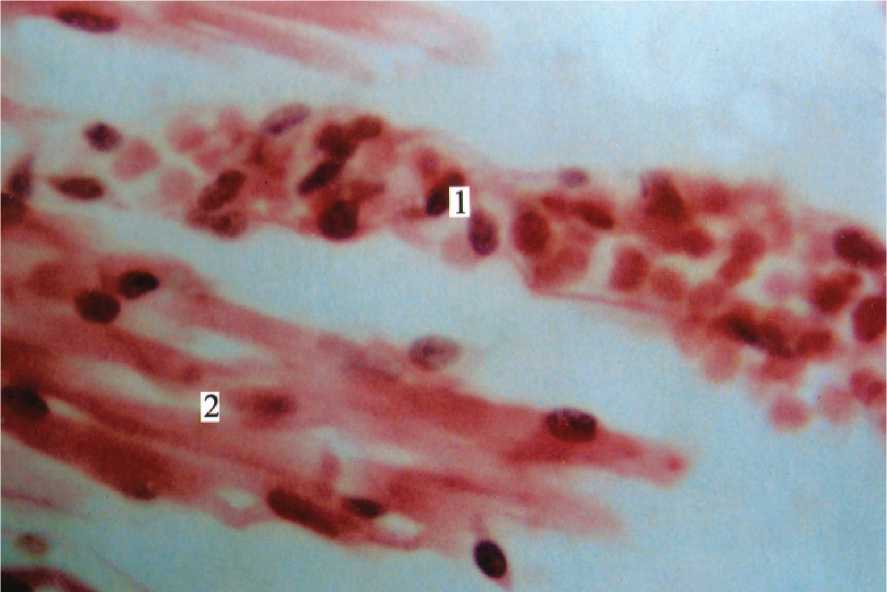
Рис. 2. Форменные элементы крови (1) и фрагмент щечной мышцы (2). Новорожденный ребенок. Окраска гематоксилином и эозином. Цв. 400
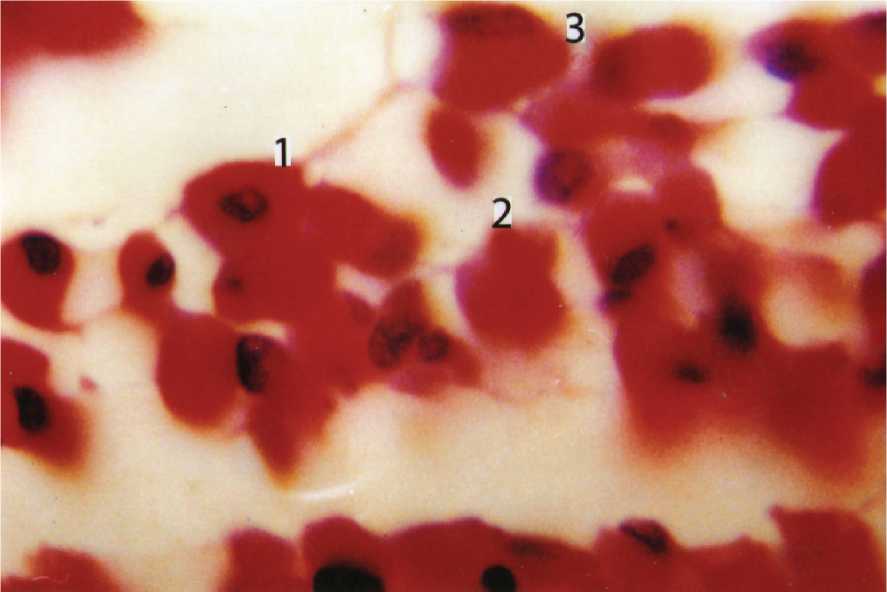
Рис. 3. Фрагменты трансформированных первичных мышечных волокон (1, 2, 3) щечной мышцы. Новорожденный ребенок. Окраска гематоксилином и эозином. Цв. 900.
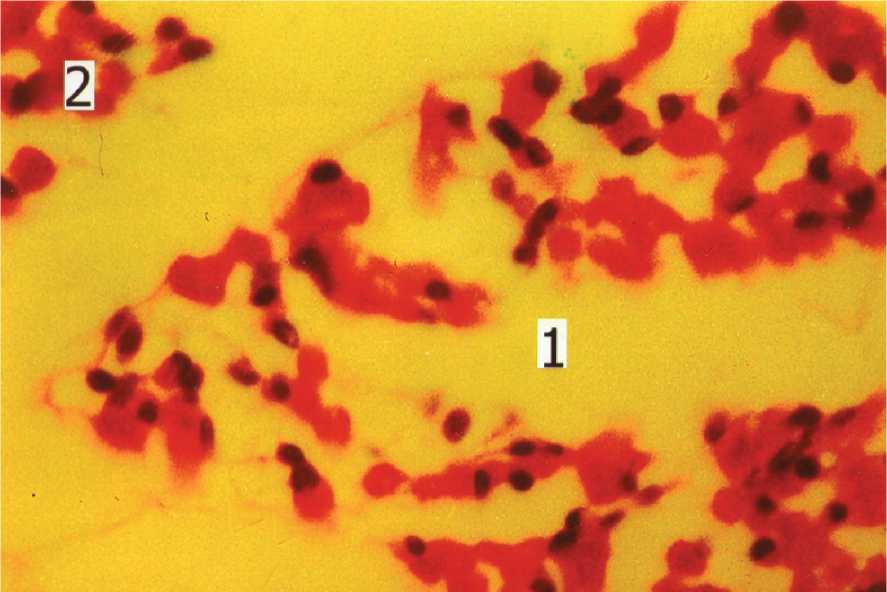
Рис. 4. Изоляция фрагментов трансформированных первичных мышечных волокон (1) от интактных участков щечной мышцы. Биопсия жирового тела щеки. Мужчина 27 лет. Окраска парарозанилином и толуидиновым синим. Цв. 900.
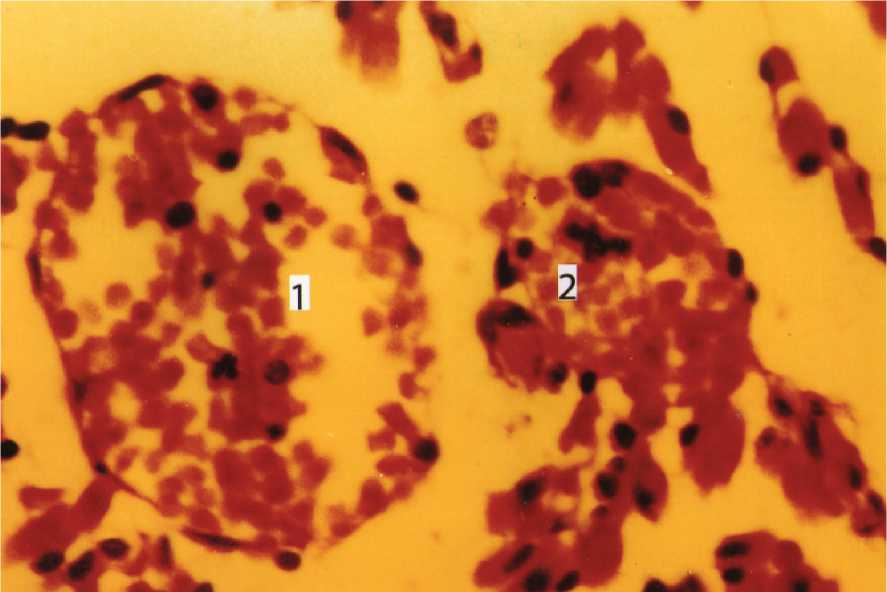
Рис. 5. Вазонды (1, 2) в жировом теле щеки. Биопсийный материал. Мужчина 32 лет.
Окраска гематоксилином и эозином. Цв. 400
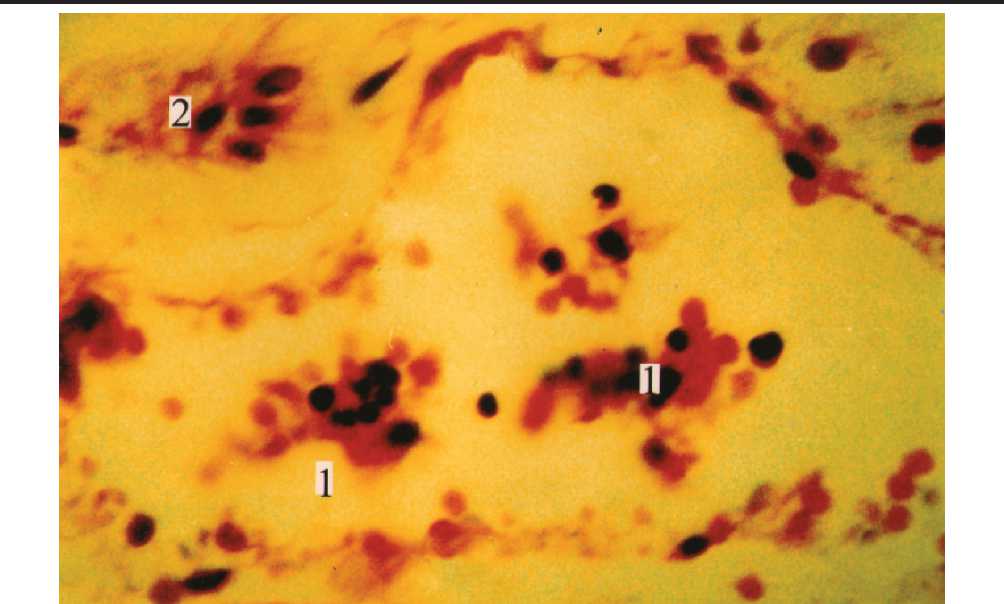
Рис. 6. Эритробластические островки (1) в просвете вазонда. 2) трансформированные мионы щечной мышцы. Новорожденный ребенок. Окраска гематоксилином и эозином. Цв.600
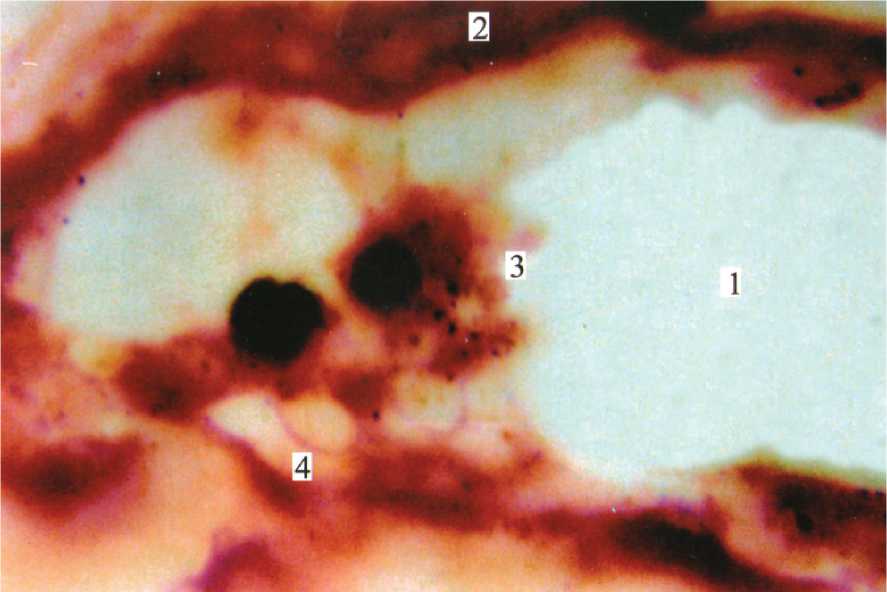
Рис. 7. Полипотентные стволовые клетки (3) и адипоциты (4) в просвете вазонда (1) 2) стенка вазонда. Биопсийный материал. Женщина 40 лет. Окраска парарозанилином и толуидиновым синим. Цв. 900
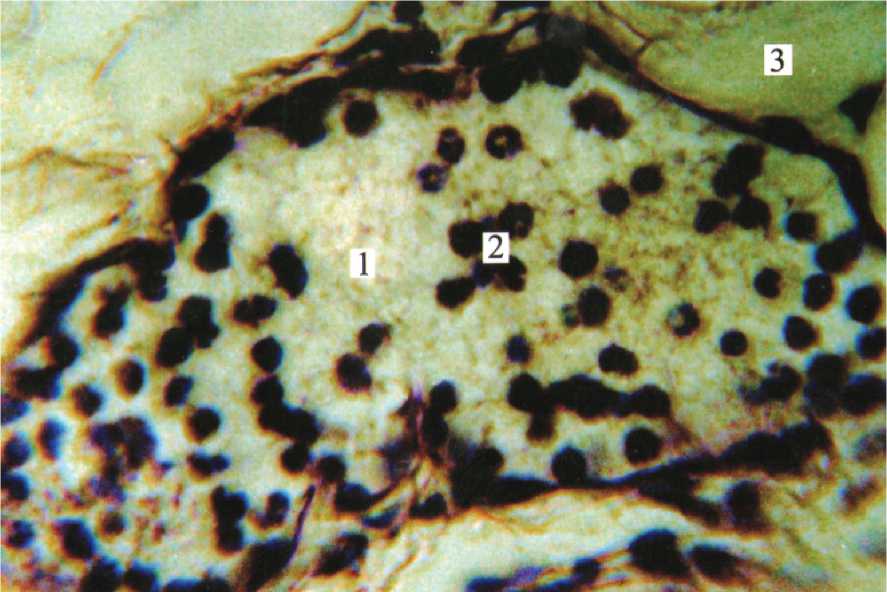
Рис. 8. Гранулопоэз (2) в просвете вазонда (2) жирового тела щеки. Ребенок 1,5 лет.
Окраска по Ван Гипоиз. Цв.600
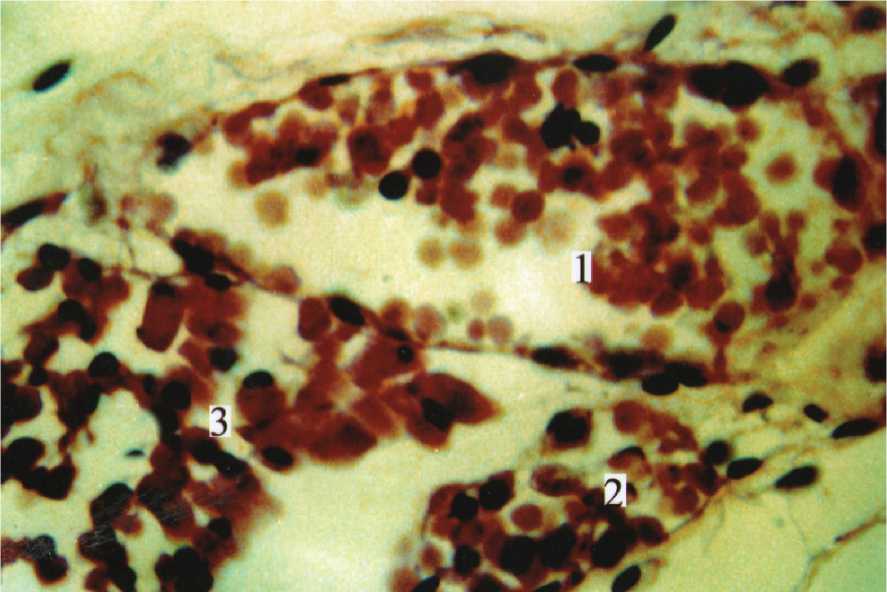
Рис. 9. Вазонд (1) и трансфомированные фрагменты щечной мышцы (2,3) в жировом теле щеки. Биопсийный материал. Женщина 37 лет. Окраска гематоксилином и эозином. Цв.600
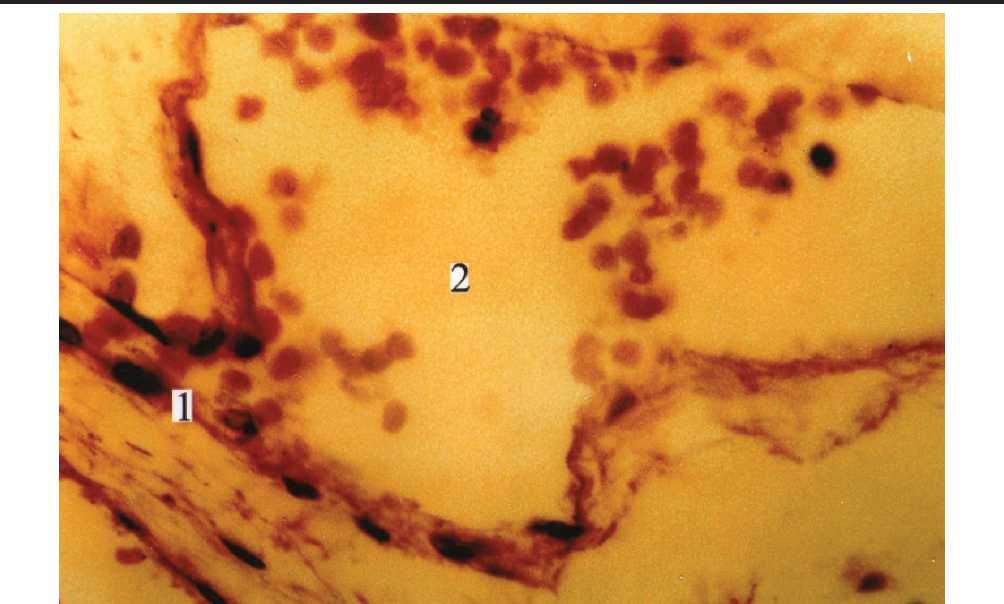
Рис. 10. Гемокапилляр (1) и вазонд (2) жирового тела щеки. Биопсийный материал.
Женщина 23 лет. Окраска гематоксилином и эозином. Цв.600.
человека. В их формировании принимают участие так же и трансформированные фрагменты щечных мышц. В костном мозге клетки предшественники, собранные в грозди [16] и окруженные фибробластами и эндотелиоцитами, должны пробить себе путь в синусоиды, а из них – в общую циркуляцию. В жировых телах щек происходит совершенно иной процесс формирования очагов гемопоэза. Он базируется на трансформации отдельных фрагментов щечных мышц, их изоляции на формировании вазоидов с эритро- и гранулопоэзом в просвете и дальнейшим включением их в общую циркуляцию. Вопрос о метаплазии первичных мышечных волокон в элементы крови и соединительной ткани дискутируется с середины ХIХ века [17]. Так И.И.Мечников [18] считал, что фагоциты могут происходить из мышечных волокон, а В.П. Вейцман [19], - что синцитиальный апотелий поперечнополосатых мышц, обладает большим потенциалом и поэтому все новообразованные сосуды и соединительная ткань могут развиваться так же и непосредственно из первичных мышечных волокон. Эти положения, хотя и соответствуют трансформационной клеточной теории Г.Э.Корицкого [20], не получили до настоящего времени ни широкого признания, ни отрицательной оценки.
Список литературы Участвуют ли жировые тела щек в постнатальном гемопоэзе?
- Тур А.Ф. Гематология детского возраста / А.Ф.Тур//Л.Медгиз, 1957, 312с.
- Шаган Б.Ф. Основы учения о новорожденном ребенке /Б.Ф.Шаган// М.Медиз, 1959, 331 с.
- Ивановская Т.Е. Функциональная морфология вилочковой железы /Т.Е.Ивановская, Т.Ф.Когой //Арх.патол., 1968, № 10, с.3-11.
- Fried W. The inflyence of and sex on erythropoietin tires plasma and tissue homogenates of hypoxis rat / W.Fried etal//Exp. Hematol, 1982, v. 10, № 5, р.472-477.
- Назаров С.Б. Динамика становления эритроидного ростка кроветворных органов белых крыс в онтогенезе/ С.Б.Назаров// Физиол.журн., 1992, № 3, с.54-59.
- Мичурина Т.В. Строение эктопических очагов кроветворения у мышей /Т.В.Мичурина, Г.П.Садыкова и др.//Арх.анат., 1985 № 7, с.62-69.
- Владимировская Е.Б. Регуляция кровотворения и иммуногенеза в перинатальный период/ Е.Б.Владимирская, Н.Н.Володин и др.// Педиатрия, 1997, № 4, с.76-82.
- Моршакова Е.Ф. Эритропоэз и его регуляция в эмбриональном, фетальном и неонотальном периодах/Е.Ф.Маоршакова, А.Д.Павлов// Рос. вестн.перинатол.,педиатр., 1999, № 3, с.12-16.
- Феер Е. Руководство по детским болезням/ Е.Феер// М.Госиздат, 1930, 885с.
- Шиллер И.Г. Картина крови и ее клиническое значение/И.Н.Шиллер//М.Медицина, 1989,272с.
- Козлов В.А. Иммунорегуляторные клетки нелимфоцитарной природы/ В.А.Козлов, И.Г.Цырлова//Докл. АН СССР, 1984, № 1, с.247-249.
- Цырлова И.Г. Иммуносупрессивный эффект популяции клеток с различной эритропоэтической активностью у зародышей и новорожденных мышей/И.Г.Цырлова, В.В.Чеглякова//Онтогенез, 1985, № 2, с.143-148.
- Прокопенко Л. Г. Эритроциты как модуляторы иммунных реакций/ Л.Г.Прокопенко, Л.Е.Сиплая// Усп.физиол.наук, 1992, № 4, с.89-106.
- Мовэт Г.З. Воспаление, иммунитет,гиперчувствительность/ Г.З.Мовэт// М.Медицина (пер.с англ.), 1975, 560с.
- Марков А.И. Эритропоэз в жировых телах щек человека/ А.И.Марков и др.// Морфологические ведомости, 2004, №.3-4, с.55-57.
- Натан Д. Г. Регуляция кровотворения/ Д. Г. Натан, К.А. Зифф// Гематол., трансфузиол., 1994, № 2, с.3-4.
- Waldeger W. Uber die Veranberung der guergestreiften Muskeln bei Entrundung und dem Typhusprozess sowie uber die Regeneration derselben nach Substanzdrfecten/ W.Waldeger// Virch.Arch., 1865, Bd.34, P.473-514
- Мечников И.И. Atrophie des muscles pendant la transformation des Babracies/ И.И.Чечников// Annal.del Ynsf/Pasteur, 1892, Vol.6, p.1-12.
- Вейцман В.Р. Об ангиоматозном превращении мышечной ткани /В.В.Вейцман// Сов.хирургия, 1934, № 7, с.760-767.
- Налетов Н.А. Основы трансформационной клеточной теории /Н.А.Налетов// Арх.патол., 1993, № 7, с.79-80.


