Ultrasound-guided interventional procedures - effective method of tumor morphological verification
Author: Utin K.G., Vazhenin A.V., Yatsev S.V.
Journal: Сибирский онкологический журнал @siboncoj
Section: Опыт работы онкологических учреждений
Article in issue: 4 (28), 2008.
Free access
From 2001 to 2006, 767 ultrasound-guided interventional procedures were performed, out of them there were 43 (5,6 %) with curative intent. Multi-functional digital ultrasound scan (HP Image Point NX) with the kit of multi-frequency sensors was used for making biopsies. All interventional procedures were done using mechanical needles with 14G in diameter. Specimens for pathomorphological examination were obtained in 68,2-97,5 % of cases.
Ultrasonography, punctual biopsy, morphological verification, cancer
Short address: https://sciup.org/14054879
IDR: 14054879 | UDC: 616-006-076
Интервенционные вмешательства под контролем ультрасонографии - эффективный метод морфологической верификации опухолевого процесса
С 2001 по 2006 г. проведено 767 интервенционных процедур под контролем ультрасонографии, из которых 43 (5,6 %) манипуляции носили лечебных характер. Для выполнения биопсий использовался многофункциональный цифровой ультразвуковой сканер «HP Image Point HX» c прилагающимся набором мультичастотных датчиков с пункционными насадками. Все интервенционные вмешательства производились механическими иглами диаметром 14 G, режущего типа. Материал для патоморфологического исследования получен в 68,2-97,5 % случаев.
Text of the scientific article Ultrasound-guided interventional procedures - effective method of tumor morphological verification
Интервенционные вмешательства под контролем ультрасонографии (УСГ) – эффективный медицинский инструмент для малоинвазивного установления диагноза или проведения лечебных мероприятий. Компьютерная или магнитная резонансная томография могут быть также использованы для проведения подобных процедур, но УСГ является более предпочтительной методикой, преимущества которой состоят в сочетании высокой информативности, достаточной доступности и рентабельности. Кроме того, оборудование для УСГ является мобильным и не обладает радиоактивной опасностью [4, 10, 12].
В Челябинском областном онкологическом диспансере в отделении ультразвуковой диагностики малоинвазивные интервенционные вмешательства под контролем УСГ проводятся с 2001 г. Накоплен определенный опыт применения данной методики в различных клинических ситуациях, с 2001 по 2006 г. проведено 767 интервенционных процедур, из них 43 (5,6 %) носили лечебный характер. Из диагностических инвазивных вмешательств с забором тканей основную часть занимают биопсии предстательной железы – 320 (41,7 %) случаев, затем по частоте следуют биопсии молочной железы – 132 (17,2 %), печени – 111 (14,5 %), органов малого таза – 49 (6,4 %), забрюшинного пространства – 32 (4,2 %). Около 80 наблюдений (11 %) приходится на биопсии других локализаций (переднее средостение, грудная клетка, мягкие ткани, орбита и т.д.).

Рис. 1. Механическая игла для проведения трансректальной биопсии предстательной железы с пункционной насадкой
Манипуляция проводилась в процедурном кабинете отделения эндоскопической и ультразвуковой диагностики, с использованием внутривенного, местного или смешанного обезболивания. Все малоинвазивные вмешательства, проводимые в брюшной полости или забрюшинном пространстве, осуществлялись после соответствующей подготовки кишечника. Для выполнения намеченных мероприятий использовался многофункциональный цифровой ультразвуковой сканер «HP Image Point HX» c прилагающимся набором мультичастотных датчиков и пункционных насадок. Все интервенционные вмешательства производились механическими иглами диаметром 14 G, режущего типа (рис. 1).
Основным малоинвазивным методом, проводимым в нашей клинике, была трансректальная режущая биопсия предстательной железы под контролем УСГ. Рак простаты, выявляемый клинически, в обязательном порядке требует морфологического подтверждения, тем более что в последнее время считается необходимым использование системы Gleason (1966), различающей пять градаций и основанной на степени организации клеток опухоли в виде четко различимых железистых структур. Эти данные являются важными диагностическими и прогностическими критериями, на основании которых определяется дальнейшая тактика лечения. В 312 (97,5 %) случаях получен материал для гистологического исследования. У 143 (45,8 %) пациентов была диагностирована доброкачественная гиперплазия предстательной железы, у 153 (49,0 %) – аденокарцинома различной степени дифференцировки. Другие гистологические формы рака предстательной железы встречались крайне редко.
По литературным данным известно, что в 70 % случаев рак предстательной железы развивается в периферической зоне, где характерной особенностью наличия злокачественного роста является наличие зоны или очага пониженной эхогенности [2, 3, 6]. Однако, анализируя свой материал, мы с такой закономерностью не встретились. На наш взгляд, не важно, определяется или нет объемное образование или подозрительный участок в измененной структуре железы (на фоне наличия аденоматозных узлов, кист, участков фиброза), необходимо лишь технически правильно произвести манипуляцию, т.е. резецировать «веерообразно» под контролем УСГ по три или более фрагментов из каждой доли [5]. Необходимым условием также является по возможности избегать проведения биопсии из уретральной зоны или междолевой борозды, так как это может способствовать не только возникновению гематурии, но и появлению выраженного болевого синдрома.
Биопсия молочной железы под контролем ультразвуковой сонографии была проведена 132 больным, гистоморфологическое заключение получено в 90 (68,2 %) случаях. Всем женщинам малоинвазивная манипуляция проводилась под местной анестезией, в амбулаторных условиях. Основной целью было взятие ткани опухоли для иммуно-гистохимического исследования и определения наличия специфических рецепторов к женским половым гормонам. Это во многом определяло дальнейшую тактику лечения пациенток с доказанным раком молочной железы. В большинстве случаев (75,6 %) был выявлен низкодифференцированный инфильтрирующий протоковый рак. Некоторые исследователи отмечают недостаточную визуализацию кончика иглы, малое количество клеточного субстрата при проведении тонкоигольной пункционной биопсии с целью дифференциальной диагностики образований молочных желез [1]. Мы же столкнулись с рядом других проблем. При использовании механических режущих игл диаметром 14 G при значительной подвижности органа и большой плотности очага интереса возникают огромные трудности с забором опухолевой ткани. Поэтому мы согласны с мнением ряда отечественных и зарубежных авторов и считаем целесообразным применять для этих целей автоматические иглы [8, 9, 11, 14].
Информативным методом дифференциальной диагностики патологических очаговых процессов в печени является биопсия под ультразвуковой визуализацией [4, 10, 13]. В нашем диспансере за пять лет было проведено 111 режущих биопсий печени, из которых в 84,5 % случаев получено гистологическое заключение. В 50,5 % случаев диагностированы метастазы рака в паренхиму печени из различных первичных очагов, большую часть которых составила аденокарцинома. Первичный гепатоцеллюлярный рак или холангиокарцинома были выявлены у 5,3 % больных. Низкодифференцированный рак с неизвестным первичным очагом был доказан в 4,2 % случаев. У 33,6 % больных после биопсии печени под контролем УСГ были диагностированы доброкачественные изменения (гепатиты различной степени активности, имитирующие очаговое поражение; дистрофические изменения, характерные для жирового гепатоза). Доброкачественные опухоли (гемангиома, печеночноклеточная или светлоклеточная аденома) доказаны в 6,3 % случаев.
Большой интерес вызывают интервенционные вмешательства на органах забрюшинного пространства. В нашей клинике были проведены 32 режущие биопсии под контролем ультразвука. У 30 (93,7 %) пациентов получено гистологическое заключение. Биопсия проводилась под смешанным обезболиванием методом «свободной руки». Положение больного выбиралось при предварительном ультразвуковом осмотре на предмет возможности проведения данной манипуляции. Больной находился в положении тела на спине или на боку, в зависимости от локализации очага интереса. По воз-
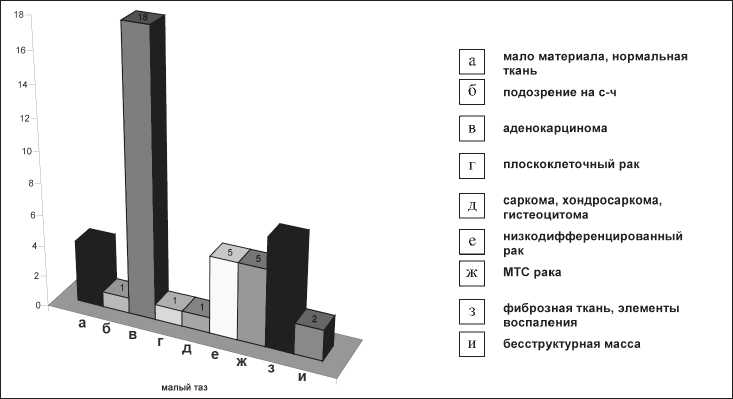
Рис. 2. Морфологическая характеристика биопсии органов малого таза под УСГ
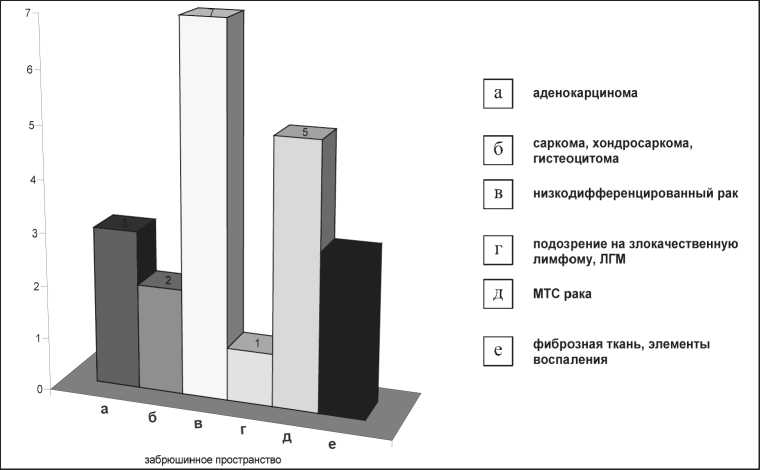
Рис. 3. Морфологическая характеристика результатов биопсии забрюшинного пространства под УСГ
Необходимо отметить, что фиксированные объемные образования больших размеров (более 50–70 мм), расположенные забрюшинно, можно пунктировать даже механическими режущими иглами под УСГ контролем. Однако, по нашему мнению, подвижные при дыхании, меньшие по размеру, расположенные рядом с жизненно важными структурами и сосудами образования, невозможно пунктировать «толстыми» механическими иглами, а необходимо использовать тонкоигольную режущую биопсию в автоматическом режиме. Хотя при проведении биопсии под контролем УСГ можно проследить как траекторию введения иглы, так и прицельное ее попадание в очаг интереса, при попытке биопсии небольшой (до 30–50 мм) забрюшинной опухоли, которая «флотирует» при дыхании, создается очевидная угроза ранения рядом расположенного паренхиматозного органа (почки, селезенки, печени) или травматизации сосудистого пучка. Это происходит потому, что наличие капсулы и плотность очага интереса не позволяют в механическом режиме (отсутствие скорости забора материала, недостаточная острота кончика иглы и режущей части) взять достаточное количество материала. У 4 пациентов мы попытались взять биопсию из очагов меньше 50 мм, из них в 2 случаях очаги располагались в почке, в одном – в области верхнего полюса правой почки (надпочечника), в одном – в проекции хвоста поджелудочной железы. Только в одном случае удалось получить достаточное количество материала для гистологического исследования. В данном случае более оправдано применение тонкоигольной пункционной или режущей биопсии в автоматическом режиме.
Таким образом, малоинвазивные вмешательства под контролем УСГ являются высокоэффективными диагностическими методиками и в большинстве случаев позволяют установить истинную распространенность опухолевого процесса, стадию заболевания и, следовательно, правильно выбрать дальнейшую тактику лечения опухолевой патологии.


