Ультразвуковая диагностика неокклюзионной ишемии кишечника при панкреонекрозе
Автор: Алексеечкина О.А., Хамидова Л.Т., Владимирова Е.С., Титова Г.П., Гришин А.В.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Медицинская визуализация
Статья в выпуске: 6 т.15, 2025 года.
Бесплатный доступ
Актуальность. Известно, что острый тяжёлый панкреатит (ОТП) сопровождается нарушениями водно–электролитного обмена с развитием дегидратации, гиперкоагуляции, гипоперфузии внутренних органов, что приводит к закономерному поражению микроциркуляторного русла кишечной стенки, способствует развитию неокклюзионной ишемии кишечника и сопровождается высоким риском сепсиса и летального исхода. Цель: выявить особенности ультразвуковой диагностики неокклюзионной ишемии кишечника при остром тяжёлом панкреатите и сопоставить с морфологическими данными аутопсии. Материалы и методы. Проанализированы результаты ультразвукового исследования кишечника у 25 пациентов с острым тяжёлым панкреатитом. Критерии включения: острый тяжёлый панкреатит, оценка степени тяжести пациентов по шкале SOFA – 5–12 баллов, APACHE 2 – 15–38 баллов. Исследование органов брюшной полости проводили на ультразвуковых приборах среднего класса (SAMSUNG HS-60 RUS), конвексным 3,5 мГц и линейным 7,5 мГц датчиками. По срокам возникновения ишемических изменений кишечника выделены две группы больных: 1 группа – ишемия кишечника в ранние сроки (до 7 суток с момента заболевания) – 18 человек, 2 группа – в поздние сроки (от 7 суток и позднее) – 7 пациентов. Морфологические и гистологические исследования выполнены в 22 случаях. Результаты. По данным УЗИ у всех пациентов с ОТП с первых суток нахождения в стационаре были выявлены признаки пареза кишечника с расширением просвета тонкой кишки до 3,5 см, перистальтика отсутствовала. Ткани брыжейки средней эхогенности были слоистой структуры. На 3–7 сутки с момента поступления в стационар при УЗИ на фоне пареза кишечника выявлены изменения стенок тонкой кишки: лоцировался спазмированный фрагмент тонкой кишки без перистальтики, распластанный на инфильтрированной брыжейке повышенной эхогенности, в 3-х случаях в режиме ЦДК кровоток в стенках тонкой кишки не получен, в 8 случаях прослеживался артериальный кровоток только по брыжеечному краю кишки. В поздние сроки (7–21 сутки) выявлены признаки отёка стенки тонкой кишки с единичными мелкими гиперэхогенными включениями в структуре стенок (пузырьками газа). Изменения толстой кишки с утолщением стенок различных отделов до 7–10 мм, структура стенки пониженной эхогенности с инфильтрацией подслизистого слоя. В режиме ЦДК получить артериальный спектр не удалось. Гистологические изменения в слизистой оболочке кишечника варьировали от острых некробиотических до завершённых некротических. Так, в одних участках толстой или тонкой кишок преобладали острые сосудистые изменения с кровоизлияниями в слизистой оболочке толстой кишки, в других были завершённые некрозы слизистой оболочки с полным нарушением строения. Заключение. Ультразвуковое исследование с применением цветного допплеровского картирования, проводимое в динамике, даёт возможность оценки состояния стенок тонкой и толстой кишок, что позволяет сделать вывод о наличии воспалительных или ишемических изменений в стенках тонкой и толстой кишки.
Неокклюзионная ишемия кишечника, панкреонекроз, ультразвуковая диагностика, острый панкреатит, допплерография, ишемия тонкой кишки, ишемия толстой кишки, осложнения панкреатита, кишечная непроходимость, морфология
Короткий адрес: https://sciup.org/143185469
IDR: 143185469 | УДК: 616.37-002-06:616.34-005.1-073.43 | DOI: 10.20340/vmi-rvz.2025.6.MIM.1
Ultrasound diagnosis of non-occlusive intestinal ischemia in pancreatic necrosis
Relevance. It is known that acute severe pancreatitis (ASP) is accompanied by water-electrolyte metabolism disorders with the development of dehydration, hypercoagulation, hypoperfusion of internal organs, which leads to a natural lesion of the microcirculatory bed of the intestinal wall, contributes to the development of non-occlusive intestinal ischemia and is accompanied by a high risk of sepsis and death. Objective: to identify the features of ultrasound diagnostics of non-occlusive intestinal ischemia in acute severe pancreatitis and compare with morphological data of autopsy. Materials and methods. The results of intestinal ultrasound examination in 25 patients with acute severe pancreatitis were analyzed. Inclusion criteria: acute severe pancreatitis, assessment of the severity of patients according to the SOFA scale - 5-12 points, APACHE 2 - 15-38 points. Abdominal examination was performed using a mid-range ultrasound device (SAMSUNG HS-60 RUS) with a 3.5 MHz convex and 7.5 MHz linear transducers. Two groups of patients were divided based on the timing of intestinal ischemic changes: Group 1 — early intestinal ischemia (up to 7 days after the onset of the disease) — 18 patients; Group 2 — late intestinal ischemia (from 7 days onward) — 7 patients. Morphological and histological studies were performed in 22 cases. Results. According to ultrasound data, all patients with OLT showed signs of intestinal paresis with small intestinal lumen dilation up to 3.5 cm and no peristalsis from the first day of hospital stay. Mesenteric tissues were of medium echogenicity and had a layered structure. On days 3–7 from the moment of admission to the hospital, ultrasound examination revealed changes in the walls of the small intestine against the background of intestinal paresis: a spasmodic fragment of the small intestine without peristalsis was located, flattened on the infiltrated mesentery of increased echogenicity. In 3 cases, blood flow in the walls of the small intestine was not obtained in the color Doppler mode, in 8 cases, arterial blood flow was traced only along the mesenteric edge of the intestine. In the later stages (7–21 days), signs of edema of the small intestinal wall with single small hyperechoic inclusions in the wall structure (gas bubbles) were revealed. Changes in the colon with thickening of the walls of various sections up to 7–10 mm, wall structure of decreased echogenicity with infiltration of the submucosal layer. It was not possible to obtain an arterial spectrum in the color Doppler mode. Histological changes in the intestinal mucosa ranged from acute necrobiotic to complete necrotic. Thus, in some areas of the colon and small intestine, acute vascular changes with hemorrhages in the colonic mucosa predominated, while in others, complete mucosal necrosis with complete structural disruption was observed. Conclusion. Dynamic color Doppler ultrasound allows for the assessment of the condition of the small and large intestinal walls, which allows for the determination of the presence of inflammatory or ischemic changes in the walls of the small and large intestines.
Текст научной статьи Ультразвуковая диагностика неокклюзионной ишемии кишечника при панкреонекрозе
Conflict of interests. The author declares that there is no conflict of interest.
Financing. The authors state that there is no external funding for the study.
Compliance with ethical principles. The authors confirm that they respect the rights of the people participated in the study, including obtaining informed consent when it is necessary.
Cite as: Alekseechkina O.A., Khamidova L.T., Vladimirova E.S., Titova G.P., Grishin A.V. Ultrasound diagnosis of non-occlusive intestinal ischemia in pancreatic necrosis. Bulletin of the Medical Institute “REAVIZ”: Rehabilitation, Doctor and Health. 2025;15(6):295–303.
АКТУАЛЬНОСТЬ
Острый тяжёлый панкреатит (ОТП) остаётся актуальной проблемой в неотложной абдоминальной хирургии. Несмотря на определённые достижения в области хирургической тактики, а также в реаниматологии, результаты лечения пациентов с ОТП остаются неудовлетворительными [1–7]. Известно, что ОТП сопровождается нарушениями водно– электролитного обмена с развитием дегидратации, гиперкоагуляции, усугубляющих тканевую гипоксию и гипоперфузию внутренних органов. Эти нарушения приводят к закономерному поражению микро-циркуляторного русла кишечной стенки, повреждению барьерной функции, развитию инфекционных осложнений, приводящих к развитию полиорганной недостаточности [5, 6, 8–11].
В ранние сроки происходит формирование динамической кишечной непроходимости с повышением внутрикишечного давления в тонкой кишке за счёт газообразующего эффекта патогенной микрофлоры [5]. Инфильтрация забрюшинной клетчатки и клетчатки связочного аппарата брюшной полости панкреатогенным экссудатом способствует развитию неокклюзионной ишемии кишечника, вследствие блокады проведения нервного импульса на высоте ферментной токсемии с реактивным отёком клетчатки [12]. Изменения стенки толстой кишки, такие как ишемия, перфорация при тяжёлом пан-креонекрозе возникают в 15% случаев и ассоциированы с летальностью более 50% [4, 6, 9, 13, 14].
Диагностика этого состояния крайне сложна. Ишемические изменения в кишечной стенке маскируются выраженной интоксикацией, болевым синдромом, парезом кишечника на фоне панкреатогенного шока в первые трое суток с момента заболевания. В более поздние сроки, от 7 до 14 суток, ишемические изменения могут развиваться на фоне полиорганной дисфункции внутренних органов (ПОН), отягощающей состояние пациента и приводящей к тяжёлым осложнениям и летальным исходам.
ЦЕЛЬ: выявить особенности ультразвуковой диагностики неокклюзионной ишемии кишечника при остром тяжёлом панкреатите и сопоставить с морфологическими данными аутопсии.
МАТЕРИАЛЫ И МЕТОДЫ
За последние два года (2023–2024 гг.) в отделении реанимации проведены ультразвуковые исследования (УЗИ) у 150 пациентов с ОТП, что составило 30% от общего количества пациентов с острым пан- креатитом, поступивших в НИИ СП им. Н.В. Склифосовского.
Ультразвуковые признаки неокклюзионной ишемии кишечника выявлены у 25 (16%) из 150 пациентов с ОТП, в том числе у 6 женщин и 19 мужчин, в возрасте от 30 до 77 лет (табл. 1). Степень тяжести пациентов с ОТП на момент поступления в стацио- нар по шкале SOFA соответствовала 5–13 баллам, по шкале APACHE-2 – 15–38 баллам.
По срокам возникновения ишемических изменений кишечника выделены две группы пациентов: 1 группа – ишемия кишечника в ранние сроки (до 7 суток с момента заболевания) – 18 человек, 2 группа – в поздние сроки (от 7 суток и позднее) – 7 человек.
Таблица 1. Распределение пациентов с панкреонекрозом по полу, возрасту, оценке степени тяжести и проведённым оперативным вмешательствам (n=25)
Table 1. Distribution of patients with pancreatic necrosis by gender, age, severity assessment and surgical interventions performed (n=25)
|
Показатель |
Группа 1 n=18 (72%) |
Группа 2 n=7 (28%) |
Всего n=25 (100%) |
|
|
Пол |
М, чел. (%) |
13 (72%) |
7 |
20 (80%) |
|
Ж, чел. (%) |
5 (27%) |
0 |
5 (20%) |
|
|
Возраст |
М, лет |
53,3 (30–77) |
55,6 (35–84) |
– |
|
Ж, лет |
52,5 (40–65) |
– |
– |
|
|
Оценка тяжести состояния |
SOFA, баллы |
5–13 |
7–9 |
– |
|
APACHE-2, баллы |
15–38 |
12–25 |
– |
|
|
Проводимые оперативные вмешательства |
Дренирование брюшной полости |
18 |
7 |
25 |
|
Дренирование сальниковой сумки |
10 |
2 |
12 |
|
|
Дренирование зон панкреатогенной деструкции |
18 |
7 |
25 |
|
|
Эмболизация селезеночной артерии |
3 |
– |
3 |
|
|
Открытая операция |
1 |
1 |
2 |
|
|
Всего |
50 |
17 |
67 |
|
Всем пациентам с ОТП выполняли ультразвуковые исследования органов брюшной полости, забрюшинного пространства.
Ультразвуковые показатели верифицированы c данными аутопсии. Морфологические и гистологические исследования проведены в 72 случаях (за последние 2 года), неокклюзионные изменения кровообращения в стенках толстой и тонкой кишок выявлены у 22 (30%) пациентов. В 4 случаях ультразвуковые данные ишемии кишечной стенки морфологически не подтверждены.
По данным аутопсии в ранние сроки (от 3 до 7 суток) неокклюзионная ишемия кишечной стенки выявлена в 15 случаях, в поздние (от 7 до 21 суток) – в 7 случаях.
Исследование органов брюшной полости проводили на ультразвуковых приборах среднего класса (SAMSUNG HS-60 RUS), конвексным 3,5 мГц и линейным 7,5 мГц датчиками: исследовали на наличие свободной жидкости в брюшной полости, оценивали состояние печени, желчного пузыря, поджелудочной железы и связочного аппарата брюшной полости, забрюшинную клетчатку на предмет распространения деструктивного процесса. Также проводили УЗИ с применением допплерографии для выявления кровотока в тканях брыжейки и стенках тонкой и толстой кишок.
Петли тонкой кишки визуализировали при установке датчика слева продольно в мезо- и гипога-стрии. Оценивали диаметр тонкой кишки, содержимое, перистальтику, толщину стенок в разных от- делах тонкой кишки, складки слизистой. Исследовали толстую кишку: оценивали состояние гаустр, толщину и структуру стенок, клетчатку параколон справа и слева. Исследовали интраорганный кровоток в стенках тонкой и толстой кишок. После получения адекватной ультразвуковой картины фрагмента кишки в В-режиме, в стенках тонкой кишки чаще, по брыжеечному краю в режиме ЦДК в стенке тонкой кишки фиксировали наличие артериального кровотока в мелких сосудах.
Оценивали состояние брыжейки тонкой кишки, прослеживали слоистость тканей брыжейки, в режиме ЦДК визуализировали сосудистый пучок.
Гистологическое и гистохимическое изучение кишечной стенки тонкой и толстой кишок проводили после фиксации материала в 10% формалине, заливки в парафин с окраской парафиновых срезов гематоксином и эозином, окраска МСБ на фибрин. Микросъемку проводили на фото насадке Leica EC-3.
РЕЗУЛЬТАТЫ
У 18 пациентов с выявленными признаками ишемии кишечника в ранние сроки (3–5 сутки) с момента заболевания при УЗИ регистрировали выраженный отёк и некроз поджелудочной железы с формированием острых жидкостных скоплений в связочном аппарате и забрюшинном пространстве. В 7 случаях ишемические изменения кишечника выявлены в поздние сроки (7–21 сутки) на стадии секвестрации и расплавления зон деструкции в сальниковой сумке, в тканях желудочно-ободочной связки, в клет- чатке параколон и формирования органной дисфункции.
У всех пациентов с ОТП с первых суток нахождения в стационаре были выявлены признаки пареза кишечника, что выражалось в расширении просвета тонкой кишки, преимущественно в левых отделах брюшной полости диаметром 2,5–3,4 см, стенки не утолщены, в просвете жидкостное содержимое, перистальтика резко замедлена, либо отсутствовала (рис. 1).
На 3–7 сутки с момента поступления в стационар у трёх пациентов при УЗИ на фоне пареза кишечника выявлены изменения со стороны тонкой кишки: лоцировался спазмированный фрагмент тонкой кишки без перистальтики, распластанный на инфильтрированной брыжейке повышенной эхогенности, в режиме ЦДК кровоток в брыжеечном крае тонкой кишки не получен (рис. 2). В других отделах брюшной полости петли тонкой кишки умеренно расширены, в просвете с жидкостным содержимым, складки слизистой прослеживались, перистальтика не определялась, ткани брыжейки средней эхогенности слоистой структуры.
В четырёх случаях при УЗИ выявлен фрагмент тонкой кишки с отёчными стенками – структура пониженной эхогенности, также на инфильтрированной брыжейке, в режиме ЦДК кровоток по брыжеечному краю прослеживался.
У восьми пациентов с отёчными стенками тонкой кишки в режиме ЦДК прослеживался артериальный кровоток по брыжеечному краю кишки. В стенках противобрыжеечного края кровоток определить ни в одном случае не удалось. У этих пациентов при УЗИ отмечали фрагментарно утолщение стенок толстой кишки в разных отделах.
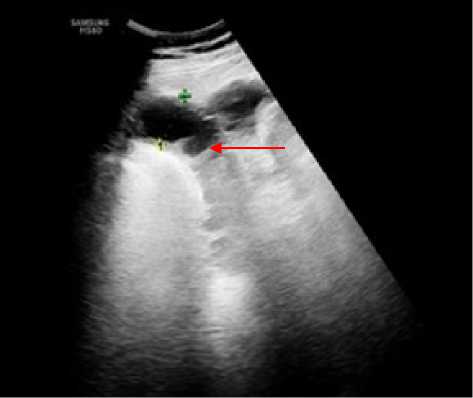
Рисунок 1. Эхограмма расширенного фрагмента тонкой кишки, прослеживаются складки слизистой, в просвете жидкостное содержимое
Figure 1. Echogram of a dilated fragment of the small intestine, mucosal folds are visible, and there is liquid content in the lumen.
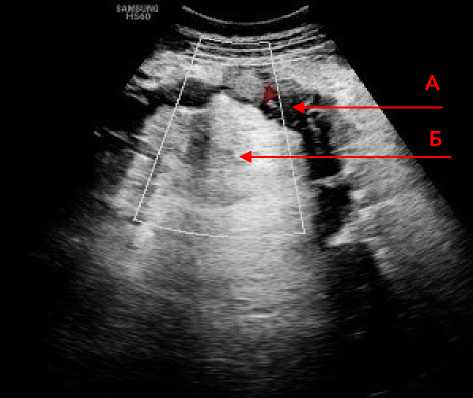
Рисунок 2. Эхограмма фрагмента тонкой кишки ( А ), распластанной на инфильтрированной брыжейке ( Б ) – воспалительный инфильтрат с вовлечением брыжейки и фрагмента тонкой кишки Figure 2. Echogram of a fragment of the small intestine ( A ), spread on the infiltrated mesentery ( Б ) – inflammatory infiltrate involving the mesentery and a fragment of the small intestine
В поздние сроки (7–21 сутки) в трёх случаях лоцировался фрагмент тонкой кишки с отёком стенки пониженной эхогенности с мелкими гиперэхогенными включениями в структуре – пузырьками газа (рис. 3).
В трёх случаях были выявлены изменения только в толстой кишке в виде фрагментарного утолщения стенок с инфильтрацией подслизистого слоя в разных отделах толстой кишки.
Всего в 12 случаях из 25 в разные сроки (7–21 сутки) с момента поступления в стационар имелись изменения в стенках толстой кишки в виде утолщения стенок различных отделов толстой кишки, чаще всего, сигмовидной и слепой, что выражалось в утолщении стенок до 7–10 мм, структура стенки пониженной эхогенности с инфильтрацией подслизистого слоя повышенной эхогенности, просвет кишки был сужен. В режиме ЦДК получить артериальный спектр не удалось. Выявленные изменения стенок толстой кишки были расценены как воспалительные на фоне деструктивных изменений забрюшинной клетчатки (рис. 4).
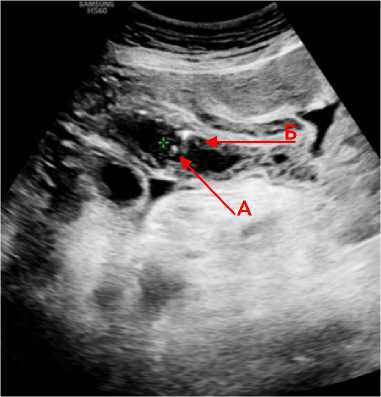
Рисунок 3. Эхограмма фрагмента подвздошной кишки с отёком стенки ( А ) и мелкими гиперэхогенными включениями в структуре стенки ( Б )
Figure 3. Echogram of a fragment of the ileum with wall edema ( A ) and small hyperechoic inclusions in the wall structure ( Б )
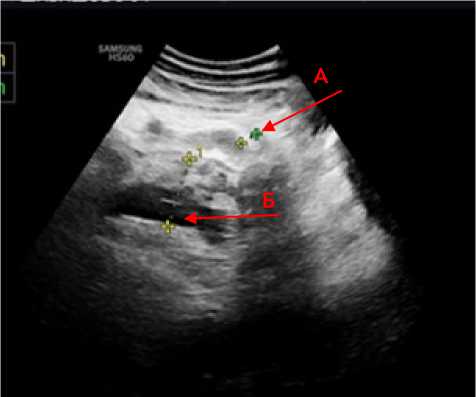
Рисунок 4. Эхограмма фрагмента толстой кишки с утолщенными стенками ( А ) на фоне деструктивных изменений клетчатки параколон ( Б )
Figure 4. Echogram of a fragment of the colon with thickened walls ( A ) against the background of destructive changes in the paracolonic tissue ( Б )
У четырёх пациентов с выявленными изменениями стенок тонкой кишки с подозрением на неокклюзионную ишемию кишечника при УЗИ на 5–7 сутки с момента заболевания, на аутопсии патологии со стороны тонкой кишки не выявлено, результаты исследования явились ложноположительными. Их анализ показал, что основанием подозревать наличие ишемии в двух наблюдениях послужил спазмированный фрагмент тонкой кишки на инфильтрированной брыжейке и в двух – отёчные стенки кишки без кровотока в режиме ЦДК.
У одного из пациентов с выявленными гиперэхогенными включениями в структуре стенки тонкой кишки наблюдались изменения толстой кишки на всём протяжении в виде утолщения стенок до 1,0 см с инфильтрацией подслизистого слоя, что было расценено нами как псевдомембранозный колит. Однако диагноз не подтвердился, анализы на токсины А и В Clostridium dificile отрицательные. По поводу выявленных изменений в стенках тонкой кишки пациент был взят на лапаротомию, интраоперационно изменений со стороны тонкой и толстой кишки и висцеральной брюшины не выявлено. Пациенту проведено УЗИ в послеоперационном периоде через 2 и 4 дня, изменения в стенках тонкой кишки не определялись, что указывает на возможность обратимости ишемических изменений при восстановлении гемодинамики.
При анализе умерших от панкреонекроза за последние два года в 22 (30%) наблюдениях из 72 были обнаружены сегментарные ишемически-некротические поражения кишечника. Они выявлялись изолировано в тонкой, толстой кишках или в сочетании при отсутствии нарушения кровообра- щения в устье, основном стволе и крупных ветвях в системе верхней и нижней брыжеечных артерий. Неокклюзионные сегментарные нарушения кровообращения кишечника были обнаружены в ранние (до 7 суток) сроки заболевания в 15 из 22 наблюдений на фоне ферментной токсемии, нарушений гемодинамики и полиорганной недостаточности.
Макроскопические проявления неокклюзионных сегментарных повреждений кишечника интраоперационно и на аутопсии крайне скудны. На секции выявляли сегмент толстой или тонкой кишки изолированно или в сочетании (подвздошная и слепая кишка), которые имели синюшный вид разной интенсивности, блестящий серозный покров, умеренный отёк стенки и прилежащей клетчатки брыжейки (рис. 5А).
Наибольшие изменения видны со стороны слизистой оболочки тонкой кишки с преимущественной локализацией по противобрыжеечному краю, отличались очаговым или сливным характером, подчёркнутым или стертым рисунком складок до полного их уплощения, отёком, геморрагиями или гнойнонекротическим детритом на поверхности (рис. 5).
Гистологически в одних участках толстой кишки преобладают острые сосудистые изменения с кровоизлияниями в слизистой оболочке, некрозом поверхностного эпителия и крипт в толстой кишке, в других завершённый некроз слизистой оболочки с полным нарушением строения, клеточным детритом на поверхности с отторжением последнего и формированием эрозивно-язвенных дефектов при наличии фибриновых тромбов кровеносных сосудов слизистой оболочки и подслизистой основы (рис. 6, В–Г).
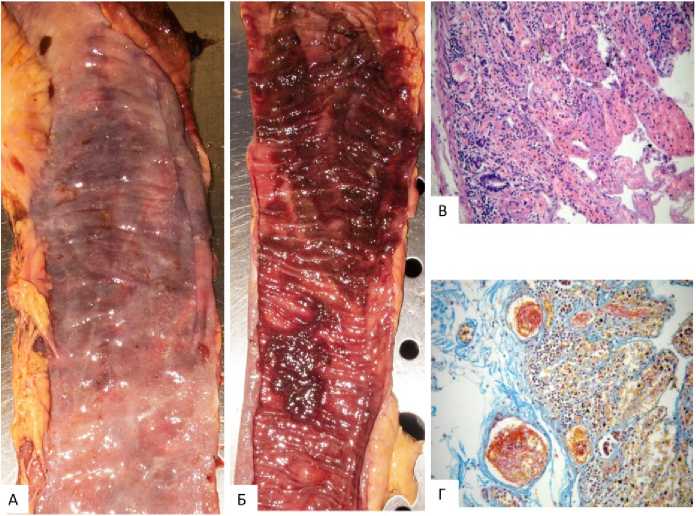
Рисунок 5. Макроскопические (А, Б) и гистологические (В, Г) изменения в тонкой кишке при панкреонекрозе: А – крупноочаговая синюшная поверхность серозного слоя; Б – очаговые кровоизлияния с нарушением строения складок слизистой оболочки (СО); В – диффузные кровоизлияния в собственной слое СО, незавершенный некроз, окраска гематоксилином и эозином, ув. ×200; Г – полное нарушение строения кишечных ворсин, тромбы в сосудах СО и подслизистой основы, окраска МСБ, ув. ×200
Figure 5. Macroscopic (A, Б) and histological (В, Г) changes in the small intestine in pancreatic necrosis: A – large-focal cyanotic surface of the serous layer; Б – focal hemorrhages with disruption of the structure of the mucosal folds (MM); В – diffuse hemorrhages in the proper layer of the MM, incomplete necrosis, hematoxylin and eosin staining, ×200 magnification; Г – complete disruption of the structure of the intestinal villi, thrombi in the vessels of the MM and submucosa, MSB staining, ×200 magnification
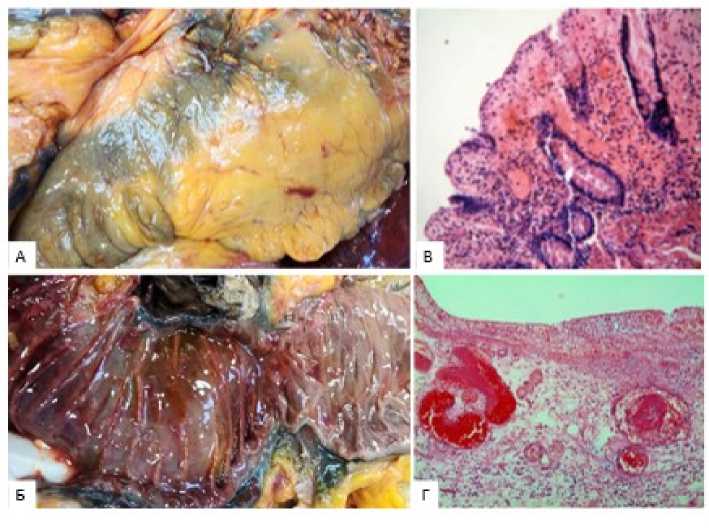
Рисунок 6. Макроскопические (А, Б) и гистологические (В, Г) изменения в толстой кишки при панкреонекрозе: А – гладкий, блестящий серозный слой; Б – отёк, пятнистые кровоизлияния в слизистой оболочке (СО); В – диффузные кровоизлияния в собственном слое СО; Г – некроз СО, отёк подслизистого слоя (ПС), тромбы в сосудах ПС; окраска гематоксилином и эозином, ув. ×200-100
Figure 6. Macroscopic (A, B) and histological (C, D) changes in the colon with pancreatic necrosis: A – smooth, shiny serous layer; Б – edema, spotty hemorrhages in the mucosa (SM); В – diffuse hemorrhages in the lamina propria (SL); Г – necrosis of the SM, edema of the submucosa (SM), thrombi in the SL vessels; hematoxylin and eosin staining, magnification ×200-100
Таким образом, проведённые нами УЗ исследования желудочно-кишечного тракта с применением допплерографии, позволили выявить ишемические изменения в стенках тонкой кишки:
– спазмированный фрагмент тонкой кишки без перистальтики на инфильтрированной брыжейке с отсутствием кровотока в стенках,
-
- наличие единичных мелких гиперэхогенных включений в структуре стенки тонкой кишки пониженной эхогенности.
Со стороны толстой кишки выявлено утолщение стенок до 0,8–1,0 см, повышение эхогенности подслизистого слоя, отсутствие кровотока в структуре стенки, сегментарность изменений толстой кишки.
Диагностическая чувствительность, специфичность и эффективность УЗ диагностики неокклюзионных нарушений кровообращения кишечника у пациентов с ОТП составили соответственно 68,7%, 97% и 94%.
ОБСУЖДЕНИЕ
У больных ОТП довольно часто диагностируют и описывают патологические изменения толстой кишки, такие как ишемия, перфорация, образование свищей. По литературным данным, ультразвуковые признаки в виде утолщения стенок толстой кишки 6–9 мм за счёт всех слоёв были подтверждены данными КТ с контрастированием, изменения особо выражены в проксимальной и средней трети поперечной ободочной кишки [4, 6, 8, 15]. Морфологически среди умерших от панкреонекроза макро- и микроскопические изменения в стенках тонкой кишки описаны в 60% случаев. Наиболее выраженные изменения зафиксированы в слизистой и подслизистом слое. Выявленные морфологические изменения в стенках тонкой кишки обусловливали нарушение барьерной функции слизистой тонкой кишки и являлись субстратом энтеральной недостаточности, приводящей к синдрому мальабсорбции при панкреонекрозе [12, 14, 16].
Сравнительная оценка ультразвуковых данных с морфологическими изменениями в стенках тонкой кишки в литературе не освещалась.
Проведённые нами УЗ исследования желудочнокишечного тракта с применением допплерографии позволили выявить ишемические изменения в стенках толстой и тонкой кишок. Ультразвуковые данные были подтверждены морфологически и гистологически. Изменения в слизистой оболочке кишечника варьируют от острых некробиотических до завершённых некротических. В одних участках толстой или тонкой кишок преобладают острые сосудистые изменения с кровоизлияниями в слизистой оболочке, в других – завершённый некроз слизистой оболочки с полным нарушением строения стенки и формированием эрозивно-язвенных дефектов.
Таким образом, ультразвуковое исследование с применением цветного допплеровского картирования, проводимое в динамике, даёт возможность оценки состояния стенок тонкой и толстой кишок, что позволяет сделать вывод о наличии воспалительных или ишемических изменений в стенках кишечника. Выявление УЗ признаков ишемии, особенно нарастающих в процессе динамического УЗ наблюдения, должно служить основанием для выполнения диагностической видеолапароскопии.
ВЫВОДЫ
Ультразвуковые признаки неокклюзионной ишемии тонкой кишки характеризуются формированием инфильтрата брыжейки с распластанным фрагментом тонкой кишки, в режиме ЦДК без кровотока в её стенках, обнаруженные в ранние сроки заболевания. А наличие мелких гиперэхогенных включений в структуре стенки тонкой кишки в поздние сроки заболевания подтверждается данными гистологического исследования.
Ультразвуковое исследование в динамике с применением цветного допплеровского картирования дает возможность оценки состояния стенок тонкой и толстой кишок, что позволяет прогнозировать течение воспалительного процесса и определяет тактику ведения пациентов.


