Ультразвуковая оценка сегментарных показателей функции аорты и сонных артерий у здоровых детей первого года жизни
Автор: Синельников Ю.С., Орехова Е.Н., Матановская Татьяна Владимировна
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Врожденные пороки сердца
Статья в выпуске: 1 т.24, 2020 года.
Бесплатный доступ
Цель. Изучить ультразвуковые показатели сегментарной функции аорты и сонных артерий у здоровых детей первого года жизни. Методы. Проведено обследование 114 здоровых детей возрасте от 1 до 12 мес., 52,6% - мальчики, площадь поверхности тела - 0,35 ± 0,8 м2. Эхокардиографическое исследование проводили на аппарате Аcuson S 2000 (Siemens Medical Systems, Маунтин-Вью, США) с использованием визуализации вектора скорости движения. На уровне восходящего и брюшного отделов аорты и в общих сонных артериях оценивали: максимальный и минимальный диаметры, циркумференциальную деформацию и скорость деформации, фракцию изменения площади, артериальную жесткость (Р2). Результаты. Максимальные и минимальные диаметры оцениваемых сегментов аорты и общих сонных артерий, фракция изменения площади аорты и общих сонных артерий, циркумференциальная деформация и скорость деформации аорты и общих сонных артерий коррелируют с площадью поверхности тела, возрастом, ударным индексом левого желудочка, индексом массы миокарда левого желудочка. Ни один изученный параметр артериальной функции не коррелирует в обследованной возрастной группе с полом, артериальным давлением, фракцией выброса левого желудочка. Самые большие значения циркумференциальной деформации определялись в общих сонных артериях 7,85 ± 2,8% (по сравнению с циркумференциальной деформацией восходящего отдела аорты 5,4 ± 0,98%, р = 0,0001, с циркумференциальной деформацией брюшного отдела аорты 6,7 ± 1,8%, р = 0,03). Циркумференциальная скорость деформации в общих сонных артериях (0,84 ± 0,22 с-1) выше, чем на уровне брюшного отдела аорты (0,67 ± 0,24 с-1, р = 0,001), но ниже, чем в восходящем отделе аорты (1,3 ± 0,3 с-1, р = 0,00001). Выводы. Показатели сегментарной функции аорты и общей сонной артерии могут быть использованы как нормативные у детей первого года жизни. Параметры функции аорты и общей сонной артерии зависят от возраста и площади поверхности тела.
Аорта, общая сонная артерия, скорость деформации, циркумференциальная деформация
Короткий адрес: https://sciup.org/142230721
IDR: 142230721 | DOI: 10.21688/1681-3472-2020-1-37-44
Ultrasonographic evaluation of segmental function of the aorta an d carotid arteries in healthy infants
Aim. To study the ultrasonographic parameters of segmental function and mechanics of the aorta and carotid arteries in healthy infants. Methods. We observed 114 healthy infants (age range, 1-12 months; boys 52.6%; mean body surface area (BSA): 0.35 ± 0.8 m2). Echocardiography was performed with an Acuson S 2000 (Siemens Medical Systems, Mountain View, CA, USA) using vector velocity imaging (VVI). The following parameters were estimated at the level of the ascending and abdominal aorta and in the common carotid arteries (CCA): maximum and minimum diameters (mm); circumferential strain (CS, %) and circumferential strain rate (CSR, s-1); fraction area change (FAC, %); arterial stiffness (£2). Results. The maximum and minimum diameters of the examined segments of the aorta and CCA, FAC of the aorta and CCA, CS and CSR of the aorta and CCA showed a correlation with BSA, age, LV stroke index, and LV myocardial mass index. None of the estimated parameters showed a correlation with sex, arterial blood pressure, or left ventricular ejection fraction. The highest CS values were found in CCA 7.85 ± 2.8% [compared with 5.4 ± 0.98% (p = 0.0001) in the ascending aorta and 6.7 ± 1.8 % (p = 0.03) in the abdominal aorta). CSR in the CCA (0.84 ± 0.22 s-1) was significantly higher than that at the abdominal aorta level (0.67 ± 0.24 s-1, p = 0.001), but lower than that in the ascending aorta (1.3 ± 0.3 s-1, p = 0.00001). Conclusion. The parameters of segmental function of the aorta and common carotid artery obtained in our research can serve as normative reference for children in the first year of life. The functional parameters of the aorta and common carotid artery depend on the age and BSA.
Текст научной статьи Ультразвуковая оценка сегментарных показателей функции аорты и сонных артерий у здоровых детей первого года жизни
Синельников Ю.С., Орехова Е.Н. , Матановская Т.В. Ультразвуковая оценка сегментарных показателей функции аорты и сонных артерий у здоровых детей первого года жизни Патология кровообращения и кардиохирургия. 2020;24(1):37-44. http://
Ю.С. Синельников, https://orcid. org/0000-0002-6819-2980
Е.Н. Орехова, https://orcid. org/0000-0002-7097-8771 Т.В. Матановская, https://orcid. org/0000-0002-2277-8935
Функциональные нарушения артериальной стенки являются первым проявлением структурных изменений и предшествуют клинической манифестации сердечно-сосудистых заболеваний. Нормальные упруго-эластические свойства аорты — важнейшая составляющая гемодинамики, обеспечивающая как кондуитную (проводниковую), так и буферную функцию артериального русла. Вопросы оценки геометрических и функциональных изменений аорты, брахиоцефальных артерий хорошо изучены у взрослых, а оценка индекса артериальной жесткости (β1) — общепризнанный маркер структурных характеристик артерий, влияющий на сердечно-сосудистый риск [1]. Некоторые врожденные пороки сердца, связанные с обструкцией дуги аорты (коарктация), двустворчатый аортальный клапан с нарушением функции (стеноз или недостаточность) и даже без нарушения функции ассоциированы с ремоделированием сосудистого русла, что проявляется повышенной частотой сердечно-сосудистых событий во взрослом возрасте (раннее развитие артериальной гипертонии, инфаркты, инсульты, аневризмы восходящего отдела аорты, мозговых артерий). Кроме того, у детей с воспалительными и аутоиммунными заболеваниями артерий (неспецифический аор-тоартериит, синдром Такаясу, болезнь Кавасаки), хромосомными заболеваниями (синдром Шере-шевского – Тернера, синдром Вильямса), наследственными дисплазиями соединительной ткани (синдром Марфана, синдром Элерса – Данлоса) также нарушаются структурно-функциональные свойства артерий. Раннее выявление дисфункции артериальной стенки у этой категории детей было бы полезным диагностическим дополнением к стандартному обследованию. Однако большинство методик, использующихся как для оценки локальных изменений геометрии и функции артериальной стенки, так и региональных изменений артериальной функции (каротидно-феморальная скорость распространения пульсовой волны) неприменимо или трудновыполнимо у детей раннего возраста.
Двумерная (2D) ультразвуковая визуализация циркумференциальной сосудистой деформации (изменение длины ткани при максимальной деформации по окружности в систолу относительно начальной длины) с использованием визуализации вектора скорости движения (vector velocity imaging, VVI) — это относительно новая методика, которая применяется в исследованиях артерий и непосредственно характеризует механику сосуда, его упруго-эластические свойства [2–4]. Очевидные преимущества оценки циркумференциаль-ной деформации состоят в том, что показатель отражает локальную (в выбранной зоне интереса) окружностную эластичность (процент максимального «удлинения» волокон артериальной стенки и скорости этого удлинения при максимальном растяжении), тогда как традиционно оцениваемый показатель артериальной жесткости (β1) является косвенным расчетным параметром, учитывающим изменение внутреннего диаметра просвета артерии в радиальном (не окружностном) направлении [2, 4]. Y. Oishi и соавт. предложили на основе цир-кумференциальной деформации проводить расчет артериальной жесткости (β2) [3]. В литературе представлена широкая валидация этого показателя и изучение его диагностической и прогностической ценности у взрослых [2, 4–6]. Однако у детей исследования деформации и артериальной жесткости единичны, а у детей первого года жизни не проводились. Учитывая потенциал циркумферен-циальной деформации и жесткости, необходимо получить нормативные значения у детей первого года жизни.
Методы
Работа проведена в Федеральном центре сердечно-сосудистой хирургии имени С.Г. Суханова (г. Пермь). Обследовано 114 здоровых детей возрасте от 1 до 12 мес. (в среднем 5,30 ± 3,81 мес.), 60 мальчиков (52,6%), с площадью поверхности тела (ППТ) 0,35 ± 0,8 м2 (от 0,23 до 0,55 м2, общие данные представлены ниже).
|
Показатель, n = 114 |
M ± SD [min; max; Me] |
|
Площадь поверхности тела, м2 |
0,35 ± 0,80 [0,23; 0,55; 0,34] |
|
Рост, см |
61,86 ± 8,07 [52,00; 80,00; 59,50] |
|
Вес, кг |
6,86 ± 2,20 [3,60; 12,00; 6,40] |
|
Пол мужской, % |
52,6 |
|
Систолическое артериальное давление, мм рт. ст. |
80,1 ± 7,3 [80,0; 100,0; 90,0] |
|
Диастолическое артериальное давление, мм рт. ст. |
47,6 ± 4,5 [40,0; 60,0; 50,0] |
|
Частота сердечных сокращений, уд./мин |
112,2 ± 16,4 [96,0; 160,0; 107,0] |
|
Конечный систолический размер ЛЖ, мм |
15,8 ± 2,3 [11,7; 20,3; 15,5] |
|
Конечный диастолический размер ЛЖ, мм |
23,7 ± 3,6 [17,6; 33,0; 22,4] |
|
Ударный индекс ЛЖ, мм |
33,6 ± 5,7 [26,0; 47,0; 31,6] |
|
Фракция выброса ЛЖ, % |
69,6 ± 2,1 [65,0; 74,0; 69,5] |
|
Индекс массы миокарда ЛЖ, г/м2 |
28,8 ± 2,0 [25,0; 32,0; 29,0] |
|
Продольная деформация ЛЖ, % |
-19,7 ± 1,9 [-23,0; -16,0; -19,8] |
|
Скорость продольной деформации ЛЖ, с-1 |
-0,80 ± 0,25 [-0,59; -1,23; -0,90] |
Примечание. ЛЖ — левый желудочек
Исследование одобрено локальным этическим комитетом учреждения, и письменное информированное согласие получено от родителей обследованных детей. Эхокардиографию проводили секторным датчиком 10V4 на аппарате Аcuson S 2000 (Siemens Medical Systems, Маунтин-Вью, США) с использованием визуализации вектора скорости движения для изучения продольной деформации левого желудочка (ЛЖ), циркумференциальной деформации и скорости деформации аорты и общих сонных артерий (ОСА) [3, 5, 7]. Из эхокардиографических данных с применением стандартизированных методик оценивали конечные систолический и диастолический размеры левого желудочка, ударный объем индексировали к ППТ с оценкой ударного индекса, индекса массы миокарда, фракции выброса, продольной деформацией ЛЖ [8–10]. Получены в В-режиме c использованием датчика 18L6HD и сохранены в формате DICOM для постобработки следующие данные: из парастернального доступа изображения восходящего отдела аорты по короткой оси на уровне ствола легочной артерии, из субкостального доступа изображения короткой оси брюшного отдела аорты на инфраре-нальном уровне, поперечные срезы обеих общих сонных артерий, проксимальнее бифуркации. Предварительное сканирование внутренних, наружных, общих сонных и позвоночных артерий выполнено для исключения аневризм, врожденных мальформаций. Основные морфометрические параметры аорты и ОСА на изучаемых уровнях представлены ниже.
|
Показатель, n = 114 |
M ± SD [min, max, Me] |
|
Максимальный диаметр восходящего отдела аорты, |
9,8 ± 1,4 [7,9; 11,7; 10,0] |
|
мм |
|
|
Минимальный диаметр восходящего отдела аорты, |
9,00 ± 1,25 [7,40; 10,80; 9,00] |
|
мм |
|
|
Максимальный диаметр брюшного отдела аорты, мм |
7,70 ± 0,48 [6,90; 8,40; 7,75] |
|
Минимальный диаметр брюшного отдела аорты, мм |
6,47 ± 0,54 [5,60; 7,90; 6,70] |
|
Максимальный диаметр общей сонной артерии, мм |
3,67 ± 0,48 [2,90; 4,40; 3,75] |
|
Минимальный диаметр общей сонной артерии, мм |
3,10 ± 0,46 [2,30; 3,80; 3,10] |
Для оценки функциональных сосудистых характеристик на уровне восходящего и брюшного отделов аорты и в обеих ОСА оценивали фракцию изменения площади артерии (ФИП) и артериальную жесткость (β2) [3,5, 7]. ФИП рассчитывали как процентное изменение площади поперечного сечения изучаемого сегмента аорты или ОСА между систолой и диастолой (наибольшая площадь поперечного сечения артерии — наименьшая площадь поперечного сечения артерии) / (наибольшая площадь поперечного сечения артерии) × 100) [5, 7]. Для расчета артериальной жесткости использована формула: ln (систолическое артериальное давление / диастолическое артериальное давление) / циркумферен-циальная деформация [3]. Циркумференциальная деформация и скорость деформации представлены как среднее значение пиковой деформации и скорости деформации от шести сегментов на каждом изучаемом уровне аорты и от каждой ОСА (пример получения данных о механике ОСА представлен на рисунке ) [3]. Полученные значения циркумференци-альной деформации и скорость деформации ОСА и стандартные отклонения от циркумференциальной деформации и скорости деформации ОСА проанализированы в каждом случае, а затем усреднены, таким образом представленные в работе значения — результат усреднения данных от обеих общих сонных артерий [4].
Статистический анализ
Статистический анализ проводили с использованием программы Statistica 12.0. Полученные данные представлены в виде среднего значения ± стандартное отклонение, максимального, минимального значения и медианы. Нулевая гипотеза о соответствии нормальности распределения проверялась с использованием теста Шапиро – Уилка. Непрерывные переменные сравнивались с использованием t-критерия Стьюдента. Связи между переменными изучены с использованием ранговой корреляции Спирмена. Статистически значимым считалось p<0,05. Внутри- и межисследовательская разница для локальных измерений деформации и скорости деформации восходящего и брюшного отделов аорты оценены двумя независимыми исследователями с использованием 30 случайно выбранных примеров из обследованной группы.
Результаты
Все полученные эхокардиографические данные соответствовали нормативным по возрасту и ППТ [8,9]. Максимальный (Rs = 0,88, р = 0,0001) и минимальный (Rs = 0,9, р = 0,0001) диаметры восходящего отдела аорты, ФИП восходящего отдела аорты (Rs = 0,53, р = 0,003), циркумферен-циальная деформация восходящего отдела аорты (Rs = 0,73, р = 0,0001) и скорость деформации восходящего отдела аорты (Rs = 0,47, р = 0,008), артериальную жесткость (β2) восходящего отдела аорты статистически значимо прямо коррелировали с возрастом обследованных детей. Обнаружена обратная умеренная связь ЧСС и ФИП (Rs = -0,51, р = 0,003), ЧСС и циркумференциаль-ной деформации, скорости деформации восходящего отдела аорты (Rs = -0,6, р = 0,001 и Rs = -0,41, р = 0,02 соответственно). Не выявлено связи диаметров восходящего отдела аорты, ФИП, циркумференциальной деформации, скорости деформации с систолическим и диастолическим артериальным давлением, полом, конечными систолическим и диастолическим размерами, фракцией выброса ЛЖ. Индекс массы миокарда ЛЖ показал умеренную прямую связь с артериальной жесткостью (β2) восходящего отдела аорты (Rs = 0,58, р = 0,001). Обнаружена умеренная связь продольной деформации ЛЖ и артериальной жесткости (β2) восходящего отдела аорты (Rs = 0,5 р = 0,01), а также ударного индекса ЛЖ и циркумференциальной деформации восходящего отдела аорты (Rs = 0,52, р = 0,02).
Показатели циркумференциальной механики (циркумференциальная деформация, скорость деформации) и функции (ФИП, артериальная жесткость (β2)) брюшного отдела аорты были больше, чем в восходящем отделе аорты (цир-кумференциальная деформация восходящего отдела аорты 5,4 ± 0,98% против циркумферен-циальной деформации брюшного отдела аорты 6,7 ± 1,8%, р = 0,01; ФИП восходящего отдела аорты 22 ± 2,1% против ФИП брюшного отдела аорты 24,6 ± 2%, р = 0,001; артериальная жесткость (β2) восходящего отдела аорты 3,4 ± 0,73 против артериальной жесткости (β2) брюшного отдела аорты 3,8 ± 0,9, р = 0,04). Однако скорость циркумференциальной деформации в восходящем отделе аорты (1,3 ± 0,3 с-1) была значимо выше, чем в брюшном отделе аорты (0,67 ± 0,24 с-1, р = 0,001). Также определялась прямая связь возраста ребенка и ФИП (Rs = 0,51, р = 0,002), обратная корреляция ЧСС и циркумфе-ренциальной деформации (Rs = -0,58, р = 0,01), ЧСС и скорости деформации на уровне брюшного отдела аорты (Rs = -0,36, р = 0,02).
Из всех обследованных артериальных сегментов самые большие значения циркумференци-альной деформации определялись в ОСА 7,85 ± 2,8% (в восходящем отделе аорты 5,4 ± 0,98%, р = 0,0001, в брюшном отделе аорты 6,7 ± 1,8%, р = 0,03). Циркумференциальная скорость деформации в ОСА (0,84 ± 0,22 с-1) была выше, чем на уровне брюшного отдела аорты (0,67 ± 0,24 с-1, р = 0,001), но ниже, чем в восходящем отделе аорты (1,3 ± 0,3 с-1, р = 0,00001). Также ФИП (16,2 ± 2,19%) и артериальная жесткость (2,96 ± 0,9) ОСА были статистически значимо ниже, чем в восходящем отделе аорты (22 ± 2,1%, р = 0,0001 и 3,4 ± 0,73, р = 0,04 соответственно) и в брюшном отделе аорты (24,6 ± 2,0%, р = 0,0001 и 3,8 ± 0,9, р = 0,0001 соответственно). Чем выше была ЧСС у обследованных детей, тем ниже ФИП ОСА (Rs = -0,47, р = 0,008), деформация ОСА (Rs = -0,42, р = 0,019) и скорость деформации ОСА (Rs = -0,44, р = 0,013). Чем больше был возраст ребенка, тем выше ФИП ОСА (Rs = 0,47, р = 0,09), деформация ОСА (Rs = 0,7, р = 0,001) и скорость деформации (Rs = 0,8, р = 0,0001). Выявлена прямая связь ППТ и деформации ОСА (Rs = 0,66, р = 0,01), ППТ и скорости деформации (Rs = 0,7, р = 0,001). Положительная умеренная корреляция определялась между ударным индексом ЛЖ и деформацией ОСА (Rs = 0,51, р = 0,03), ударным индексом ЛЖ и скоростью деформации (Rs = 0,47, р = 0,02), индексом массы миокарда ЛЖ и артериальной жесткостью (β2) ОСА (Rs = 0,57, р = 0,001). Не выявлено связи ФИП, деформации, скорости деформации и артериальной жесткости (β2) ОСА с полом, систолическим и диастолическим артериальным давлением, размерами и фракцией выброса ЛЖ. Данные ультразвуковые параметры функции оцениваемых сегментов аорты и общей сонной артерии представлены ниже.
|
Показатель, n = 114 |
M ± SD [min, max, Me] |
|
Фракция изменения площади восходящего отдела аорты, % |
22,0 ± 2,1 [19,0; 25,0; 22,0] |
|
Циркумференциальная деформация восходящего отдела аорты, % |
5,40 ± 0,98 [3,30; 6,80; 5,90] |
|
Скорость циркумференциальной деформации восходящего отдела аорты, с-1 |
1,3 ± 0,3 [0,8; 1,9; 1,3] |
|
Артериальная жесткость восходящего отдела аорты |
3,4 0 ± 0,73 [1,80; 4,40; 3,49] |
|
Фракция изменения площади брюшного отдела аорты, % |
24,6 ± 2,0 [21,0; 27,0; 25,0] |
|
Циркумференциальная деформация брюшного отдела аорты, % |
6,7 ± 1,8 [4,0; 12,0; 6,8] |
|
Скорость циркумференциальной деформации брюшного отдела аорты, с-1 |
0,67 ± 0,24 [0,27; 1,20; 0,70] |
|
Артериальная жесткость брюшного отдела аорты |
3,8 ± 0,9 [1,6; 5,6; 3,8] |
|
Фракция изменения площади общей сонной артерии, % |
16,20 ± 2,19 [12,00; 19,00; 16,50] |
|
Циркумференциальная деформация общей сонной артерии, % |
7,85 ± 2,80 [5,00; 16,50; 7,30] |
|
Скорость циркумференциальной деформации общей сонной артерии, с-1 |
0,84 ± 0,22 [0,54; 1,60; 0,80] |
|
Артериальная жесткость общей сонной артерии |
2,96 ± 0,90 [1,27; 5,00; 3,00] |
С помощью статистической методики Блэнда – Альтмана выполнен анализ согласованности результатов при повторных измерениях (внутри- и межоператорской воспроизводимости) локальной аортальной циркумференциальной деформации. Полученные результаты свидетельствуют о хорошей воспроизводимости получаемых результатов: вну-триоператорская разница измерений для деформации в восходящем отделе аорты составила 0,1% от средней деформации (Bias 0,016; 95% доверительный интервал (ДИ) -0,04… 0,07; R2 0,95), межоператорская 0,5% от средней деформации (Bias 0,05; 95% ДИ -0,17… 0,27; R2 0,89), внутриоператорская для скорости деформации в восходящем отделе аорты: -0,1% от средней скорости деформации (Bias -0,016; 95% ДИ -0,02… 0,06; R2 0,96), межоператорская -0,5% от средней деформации (Bias 0,05; 95% ДИ -0,17…
0,27; R2 0,89), для брюшного отдела аорты внутрио-ператорская разница 0,3% от средней деформации (Bias 0,31; 95% ДИ -0,05… 0,57; R2 0,91), межоператорская 0,39% от средней деформации (Bias 0,39; 95% ДИ -0,08… 0,69; R2 0,85), внутриоператорская для скорости деформации в брюшном отделе аорты: 0,13% от средней скорости деформации (Bias 0,13; 95% ДИ -0,18… 0,44; R2 0,88), межоператорская 0,39% (Bias 0,39; 95% ДИ 0,08… 0,7; R2 0,79).
Обсуждение
В этом исследовании мы представили локальные значения функциональных параметров аорты и ОСА, полученные с помощью визуализации вектора скорости движения, у детей первого года жизни. С учетом опубликованных данных, это исследование является первым у здоровых детей раннего возраста с целью получения диапазона нормальных значений циркум-ференциальной механики аорты и ОСА и обнаружения связей между этими параметрами, геометрией и функцией ЛЖ. Неинвазивность, доступность, простота получения данных, воспроизводимость, отсутствие лучевой нагрузки делают ультразвуковую методику изучения сегментарной функции артериальной стенки идеальной для динамического наблюдения за пациентами с двустворчатым аортальным клапаном, после коррекции коарктации аорты, операции артериального переключения, у пациентов с синдромом Марфана и при широком спектре врожденных и приобретенных пороков сердца, генетических аномалий и мальформаций у детей.
Согласно полученным данным, скорость циркум-ференциальной деформации в восходящем отделе аорты у детей первого года жизни максимальная (по сравнению со скоростью деформации в брюшном отделе аорты и ОСА), хотя самые большие показатели циркумференциальной деформации выявляются в ОСА, а ФИП и артериальная жесткость (β2) — в брюшном отделе аорты. Эти данные демонстрируют особенности биомеханики аорты и ОСА у детей первого года жизни и связаны со структурой и геометрией артериальной стенки каждого оцениваемого сегмента. Так, максимальная жесткость, выявленная на этом уровне, объясняется тем, что в норме на уровне брюшного отдела коллагеновых волокон больше, а содержание эластина от восходящего к брюшному отделу аорты уменьшается. Максимально высокие
Циркумференциальная деформация и скорость деформации брюшного отдела аорты
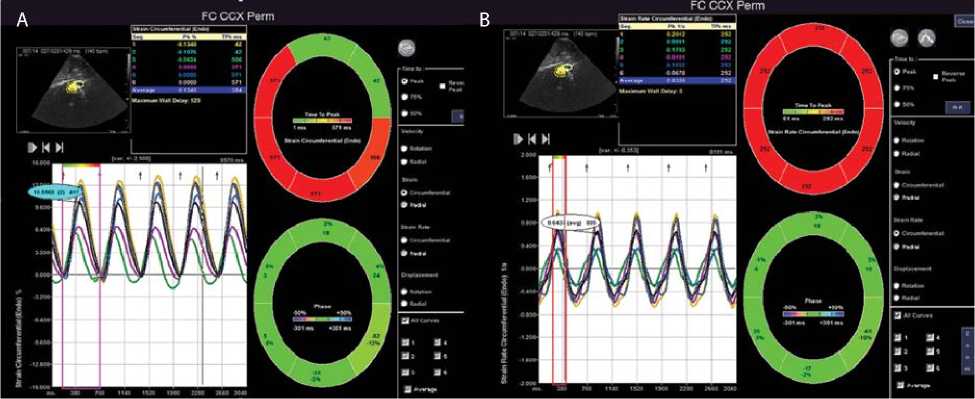
Примечание. Данные о циркумференциальной деформации брюшного отдела аорты обследованного здорового ребенка (мальчик), 7 мес., площадь поверхности тела 0,39 м2. Артериальное давление 90/50 мм рт. ст. Изображение аорты на инфраренальном уровне по короткой оси: программное обеспечение после оконтуривания самостоятельно делит артерию на 6 сегментов и данные о деформации каждого сегмента, а также усредненные данные от всех сегментов представляет в виде таблицы и графика. Схематичная круговая диаграмма с использованием цветовых маркеров «время – деформация» представляет отчет о времени до достижения пиковой деформации каждым сегментом, максимальное отклонение и усредненные значения также указаны в таблице. Циркумференциальная деформация брюшного отдела аорты в нашем примере 10,5% (A). Данные о скорости деформации брюшного отдела аорты (аналогичная показателям деформации схема представления данных). В нашем примере скорость деформации 0,64 с-1 (B)
значения скорости деформации восходящего отдела аорты объясняются биомеханикой деформации и геометрией восходящего отдела аорты (для адекватного демпфирования при распространении пульсовой волны в восходящем отделе аорты скорость деформации максимальная). Самые высокие показатели каротидной циркумференциальной деформации в ОСА объясняются структурными характеристиками: в отличие от аорты, общие сонные относятся к мышечно-эластическому типу артерии, поэтому циркумфе-ренциальная деформация здесь больше, чем в аорте. Также важным обнаружением у обследованных нами здоровых детей было отсутствие связи между линейными размерами и фракцией выброса ЛЖ с показателями функции аорты и ОСА, тогда как индекс массы миокарда ЛЖ прямо коррелировал с артериальной жесткостью (β2) восходящего отдела аорты и ОСА, а ударный индекс ЛЖ — с циркумференциальной деформацией восходящего отдела аорты. Эти данные свидетельствуют о ведущей роли возрастания массы миокарда и ударного объема ЛЖ в возрастной дина- мике биомеханических свойств аорты и общих сонных артерий.
S. Yuda и соавт. изучили показатели деформации ОСА в циркумференциальном направлении и артериальной жесткости у здоровых взрослых и получили данные о диапазоне нормальных значений — 6,7 ± 2,1 и 5,5 ± 1,3% соответственно [11]. По нашим данным, параметры деформации ОСА у детей первого года жизни выше, а показатель жесткости ОСА ниже, чем у здоровых взрослых.
S. Curcio и соавт. показали, что различия артериальной жесткости у здоровых детей, связанные с полом, ППТ и уровнем артериального давления, начинают обнаруживаться между 8 и 14 годами [12]. Мы выявили, что показатели артериальной жесткости даже в нормативном диапазоне у детей первого года жизни закономерно увеличиваются с каждым месяцем жизни и повышением ППТ. G.S. Reusz и соавт. сообщили о сильной корреляции между возрастом и каротидно-феморальной скорости распространения пульсовой волны в большом многоцентровом исследовании, включаю- щем более 1 000 участников [13]. Но, как и в работе S. Curcio и соавт., нам не удалось выявить гендерных различий среди изученных параметров у обследованных детей. Возможное объяснение этих результатов состоит в том, что связанные с полом изменения проявляются в более старших возрастных группах.
В исследовании Z. Bu и соавт. артериальная жесткость (β2) в восходящем отделе аорты у здоровых взрослых лиц 7,4 ± 2,3 %, что выше, чем выявленные нами значения у детей первого года жизни (5,40 ± 0,98) [7]. Следует помнить, что при расчете артериальной жесткости (β2) используются не только параметры деформации, но и значения систолического и диастолического артериального давления, которые в норме у детей существенно ниже, чем у взрослых.
К сожалению, наше исследование ограничено относительно небольшим размером выборки. Мы оценивали биомеханику восходящего и брюшного отделов аорты на локальном уровне, что не дает представления о региональных сосудистых свойствах. Также возможна вариабельность получения данных в зависимости от программного обеспечения. Невозможно получение короткой оси аорты на уровне дуги и нисходящего отдела аорты с использованием трансторакального ультразвукового исследования. Однако с учетом потенциальной пользы и простоты получения данных о биомеханике аорты и ОСА у детей с первых месяцев жизни накопление фактических показателей представляется важной диагностической задачей. Интегральный подход оценки локальной геометрии и функции аорты и ОСА в нашем исследовании позволяет более полно понять особенности желудочково-артериальной сопряженности раннего детского возраста, оценить взаимодействие структурных и функциональных параметров. Значения сегментарной циркумференциальной механики аорты и ОСА могут стать ранними маркерами артериальной дисфункции у детей с ВПС и помочь оптимизировать стратегии динамического наблюдения и лечения.
Выводы
Полученные в работе показатели сегментарной функции аорты и общей сонной артерии могут быть использованы как нормативные у детей первого года жизни. Параметры функции аорты и общей сонной артерии зависят от возраста и площади поверхности тела. Основные особенности биомеханики аорты и
ОСА у здоровых детей первого года жизни отражают структурные и геометрические особенности артериальной стенки в зоне оценки: максимальная окруж-ностная деформация в ОСА, максимальная скорость деформации в восходящем отделе аорты, максимальная артериальная жесткость в брюшном отделе аорты.
Список литературы Ультразвуковая оценка сегментарных показателей функции аорты и сонных артерий у здоровых детей первого года жизни
- Saito M., Okayama H., Inoue K., Yoshii T., Hiasa G., Sumimoto T., Nishimura K., Ogimoto A., Higaki J. Carotid arterial circumferential strain by two-dimensional speckle tracking: a novel parameter of arterial elasticity. Hypertens Res. 2012;35(9):897-902. https://doi. org/ DOI: 10.1038/hr.2012.39 PMID: 22495610
- Rosenberg A.J., Lane-Cordova A.D., Wee S.O., White D.W., Hilgenkamp T.I.M., Fernhall B., Baynard T. Healthy aging and carotid performance: strain measures and p-stiffness index. Hypertens Res. 2018;41(9):748-55. https:// DOI: 10.1038/s41440-018-0065-x PMID: 29968848
- Oishi Y., Mizuguchi Y., Miyoshi H., Iuchi A., Nagase N., Oki T. A novel approach to assess aortic stiffness related to changes in aging using a two-dimensional strain imaging. Echocardiography. 2008;25(9):941-5. DOI: 10.1111/j.1540-8175.2008.00725.x PMID: 18771548
- Kim S.A., Lee K.H., Won H.Y., Park S., Chung J.H., Jang Y., Ha J.W. Quantitative assessment of aortic elasticity with aging using velocity-vector imaging and its histologic correlation. Arterioscler Thromb Vasc Biol. 2013;33(6):1306-12. DOI: 10.1161/ATVBAHA.113.301312 PMID: 23580144
- Teixeira R., Viera M.J., Goncalves A. Ultrasonographic vascular mechanics to assess arterial stiffness: a review. Eur Heart J Cardiovasc Imaging. 2016;17(3):233-46. DOI: 10.1093/ehici/iev287 PMID: 26546802


