Уровень оксидативного стресса в эндотелиальных клетках, культивируемых в присутствии митомицина С
Автор: Синицкий М.Ю., Синицкая А.В., Шишкова Д.К., Асанов М.А., Хуторная М.В., Понасенко А.В.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Экспериментальные исследования
Статья в выпуске: 3 т.37, 2022 года.
Бесплатный доступ
Обоснование. Атеросклероз - одна из ведущих патологий сердечно-сосудистой системы. Показано, что одним из факторов риска данного заболевания является повреждение ДНК эндотелиальных клеток, приводящее к эндотелиальной дисфункции и вызванное воздействием на клетки мутагена митомицина С (ММС). ММС оказывает алкилирующее действие на ДНК и вовлечен в процесс формирования оксидативного стресса, также являющегося фактором риска развития атеросклероза.Цель исследования: оценить уровень маркеров оксидативного стресса в культурах первичных эндотелиальных клеток человека, экспонированных мутагеном алкилирующего механизма действия ММС.Материал и методы. Материалом исследования послужили коммерческие культуры первичных эндотелиальных клеток коронарной (HCAEC) и внутренней грудной (HITAEC) артерий человека, культивируемые в присутствии 500 нг/мл ММС (экспериментальная группа) и без мутагенной нагрузки (контрольная группа). Уровень активных форм кислорода, азота и 8-OH-дезоксигуанозина (8-OHdG) определяли в культуральной среде методом иммуноферментного анализа (ИФА). Относительную длину теломерных участков ДНК эндотелиальных клеток, а также экспрессию генов TERT и POT1 оценивали с помощью метода количественной полимеразной цепной реакции (кПЦР) с детекцией продуктов амплификации в режиме реального времени. Статистическую обработку результатов исследования проводили в программе GraphPad Prism 9.Результаты. В результате проведенной работы установлено, что концентрация активных форм кислорода, реактивных форм азота (NO2 -, NO3 -, NO2 -/NO3 -) и 8-OHdG статистически значимо не различалась в экспериментальной и контрольной группах клеток HCAEC и HITAEC. При этом в экспонированных ММС клетках HCAEC и HITAEC отмечено уменьшение относительной длины теломерных участков ДНК по сравнению с неэкспонированным контролем (10,97 против 27,03 в клетках HCAEC, p = 0,002 и 9,12 против 25,64 в клетках HITAEC, p = 0,001). Кроме того, в экспонированных ММС клетках HCAEC установлено 1,75-кратное повышение экспрессии гена POT1 относительно контроля (p = 0,019). Ген TERT не экспрессировался ни в одной из изученных групп.Заключение. Мутаген алкилирующего механизма действия ММС в эксперименте in vitro не вызывает выраженный оксидативный стресс в культурах первичных эндотелиальных клеток человека. Формирование эндотелиальной дисфункции, ассоциированной с экспозицией клеток ММС, обусловлено, главным образом, генотоксическим стрессом, связанным с алкилированием ДНК эндотелиальных клеток.
Эндотелиальная дисфункция, оксидативный стресс, мутагенез, атерогенез, теломеры, теломераза
Короткий адрес: https://sciup.org/149141427
IDR: 149141427 | УДК: 577.152.1:611-018.74:57.086.83 | DOI: 10.29001/2073-8552-2022-37-3-121-127
Oxidative stress in the endothelial cell culture exposed to mitomycin C
Background. Atherosclerosis is one of the leading cardiovascular pathologies. Evidence suggests that DNA damage caused by endothelial cell exposure to mitomycin C (MMC) leads to endothelial dysfunction and is the risk factor for this disease. MMC is an alkylating mutagen involved in the development of oxidative stress, which is also a risk factor for atherosclerosis. Aim. To access the levels of oxidative stress markers in the primary human endothelial cell culture exposed to alkylating mutagen MMC. Material and Methods. Commercially available primary cultures of endothelial cells obtained from human coronary artery (HCAEC) and human internal thoracic artery (HITAEC) were used in the study. The cells were cultivated in the presence of 500 ng/mL MMC (experimental group) and without mutagenic load (control group). The levels of reactive oxygen species, reactive nitrogen species, and 8-OH-deoxyguanosine (8-OHdG) in cell growth media were assessed by enzyme-linked immunosorbent assay. The relative telomere length and expression of TERT and POT1 genes were accessed in endothelial cells by quantitative polymerase chain reaction. Statistical analysis of data was performed using GraphPad Prism 9 software. Results. There were no differences in the concentrations of reactive oxygen species, reactive nitrogen species (NO2 -, NO3 -, NO2 -/NO3 -), and 8-OHdG in HCAEC and HITAEC cultures exposed to MMC compared to the corresponding parameters in the non-exposed controls. At the same time, HCAEC and HITAEC exposed to MMC were characterized by a decrease in the relative telomere length compared to control (10.97 vs. 27.03 in HCAEC, p = 0.002 and 9.12 vs. 25.64 in HITAEC, p = 0.001). Moreover, we discovered 1.75-fold increase in the expression of POT1 gene in the experimental HCAEC compared to control (p = 0.019). No expression of TERT gene was observed in study groups. Conclusions. Alkylating mutagen MMC did not induce any pronounced oxidative stress in the primary human endothelial cells in vitro. The development of endothelial dysfunction caused by MMC exposure was triggered mainly by DNA alkylation resulting in the genotoxic stress in the endothelial cells.
Текст научной статьи Уровень оксидативного стресса в эндотелиальных клетках, культивируемых в присутствии митомицина С
Согласно статистике, патологии сердечно-сосудистой системы на настоящий момент занимают лидирующую позицию в структуре заболеваемости и смертности как во всем мире, так и в России, с тенденцией к росту в 2030 г. до 23 млн случаев. При этом причиной абсолютного большинства смертей среди всех патологий сердечно-сосудистого континуума является атеросклероз [1], представляющий собой мультифакторное воспалительное заболевание, в основе которого лежит развитие эндотелиальной дисфункции, факторами риска которой является гиперхолистеремия, артериальная гипертензия, сахарный диабет, курение и ряд других [2]; обсуждается также роль повреждения ДНК в атерогенезе [3].
В последнее десятилетие активно изучалась связь между воспалением, оксидативным стрессом, мутагенезом и атерогенезом [3]. Так, известно, что некоторые факторы риска развития атеросклероза (например, сахарный диабет и курение), а также ряд экзогенных токсических веществ способствуют образованию активных форм кислорода в сосудистом русле, участвующих в атерогене-зе [4]. Отмечается повышенный уровень ароматических ДНК-аддуктов, являющихся маркерами оксидативного стресса, в клетках атеросклеротических бляшек, таких как макрофаги, гладкомышечные и эндотелиальные клетки, по сравнению со здоровыми тканями [5]. В экспериментальных работах показано, что экспозиция культур первичных эндотелиальных клеток человека мутагеном митомицином С (ММС) приводит к выраженному воспалительному ответу и развитию эндотелиальной дисфункции [6]. Известно, что ММС способен вызвать генотоксический стресс за счет образования поперечных сшивок молекулы ДНК в результате реакции N-алкилирования, что приводит в конечном итоге к нарушению процессов транскрипции, трансляции и гибели клеток путем апоптоза [7]. Кроме этого, ММС способен вызвать и оксида-тивный стресс за счет циклического одноэлектронного восстановления молекулы ММС с последующим окислением молекулярным кислородом, в результате чего образуется супероксидный радикал – чрезвычайно активная частица, относящаяся к активным формам кислорода. Активные формы кислорода оказывают повреждающее действие на различные типы биологических молекул, таких как ДНК, липиды и белки, что приводит к инактивации ферментов, повреждению ДНК, дисфункции и гибели клеток [8]. Таким образом, понимание ведущего механизма действия ММС на эндотелиальные клетки, приводящего к развитию эндотелиальной дисфункции, является чрезвычайно актуальным для современной сосудистой биологии и внесет вклад в понимание фундаментальных аспектов атерогенеза.
Цель исследования: оценить уровень маркеров окси-дативного стресса в культурах первичных эндотелиальных клеток человека, экспонированных мутагеном алкилирующего механизма действия ММС.
Материал и методы
Материалом исследования послужили коммерческие культуры первичных эндотелиальных клеток коронарной (Human Coronary Artery Endothelial Cells, HCAEC) и внутренней грудной (Human Internal Thoracic Endothelial Cells, HITAEC) артерий (Cell Applications, США). Данные клеточные линии были выбраны в связи с их разной по-ражаемостью атеросклерозом: так, атеросклеротическое поражение коронарной артерии встречается наиболее часто, в том время как внутренняя грудная артерия практически не подвержена атеросклерозу [9]. Все работы с клеточными культурами проводили в асептических условиях. Клетки культивировали в условиях повышенной влажности, 5%-го содержания CO2 и при температуре 37 ˚C в среде для роста клеток Human MesoEndo Cell Growth Medium (Cell Applications, США) до достижения 80% конфлюентности, после чего пересевали в 6-лу-ночные культуральные планшеты, содержащие по 2 мл среды для роста клеток в каждой лунке, и культивировали еще сутки. После окончания культивирования старую среду для роста клеток удаляли и приливали в каждую лунку 2 мл свежей среды, содержащей 500 нг/мл алкилирующего мутагена ММС (AppliChem, Испания) (экспериментальная группа) или 0,9% раствор NaCl (контрольная группа). Экспериментальные и контрольные планшеты культивировали в стандартных условиях в течение 6 ч, после этого проводили замену культуральной среды на чистую и культивировали клетки еще сутки, после чего выводили из эксперимента. Выбор концентрации ММС и времени культивирования в условиях мутагенной нагрузки был обусловлен имеющимися рекомендациями по моделированию мутагенеза in vitro и результатами собственных исследований [6].
Относительная длина теломерных (ОДТ) участков ДНК оценивалась методом количественной полимеразной цепной реакции (кПЦР) с детекцией продуктов амплификации в режиме реального времени с использованием SYBR Green праймеров, изготовленных компанией ЗАО «Евроген» (Москва, Россия). В качестве референса был использован ген HBG1 . Характеристика праймеров, использованных для оценки ОДТ, представлена в таблице 1.
Таблица 1. Характеристика праймеров, использованных для оценки относительной длины теломер
Table 1. Characteristics of primes used for relative telomere length assessment
Праймер Primer
Telo
HBG1
Последовательность Sequence
F:GGTTTTTGAGGGTGAGGGTGAGGGTGAGGGTGA GGGT
R:TCCCGACTATCCCTATCCCTATCCCTATCCCTATCC CTA
F:GCTTCTGACACAACTGTGTTCACTAGC R:CACCAACTTCATCCACGTTCACC
Примечание: ОДТ – относительная длина теломер, F – прямой праймер, R – обратный праймер.
Note: RLT – relative telomere length, F – forward primer, R – reverse primer.
Из экспериментальных и контрольных клеток HCAEC и HITAEC выделяли геномную ДНК по стандартному протоколу фенол-хлороформной экстракции и оценивали ее качество на спектрофотометре NanoDrop 2000 (Thermo Scientific, США). ПЦР проводили на амплификаторе ViiA 7 (Applied Biosystems, США) в 96-луночном планшете, включающем в себя изучаемые образцы, пять стандартов с двукратным разведением и отрицательный контроль, анализируемые в трех технических повторах. Для проведения амплификации на каждый образец готовили по 10 мкл реакционной смеси, содержащей 5 мкл мастер-микса PowerUp SYBR Green Master Mix (Applied Biosystems, США), по 500 нМ прямого и обратного праймеров (ЗАО «Евроген», Москва) и 5 мкл раствора геномной ДНК (либо деионизированной воды в случае с отрицательным контролем). Амплификацию проводили по следующей программе: 2 мин при 50 °C (1 цикл), 2 мин при 95 °C (1 цикл), 15 с при 95 °C и 60 с при 60 °C (40 циклов). ОДТ рассчитывалась по следующей формуле:
ОДТ = [2 Ct (Telo) /2 Ct (HBG1) ] –1 [10].
Для оценки экспрессии генов POT1 и TERT было проведено выделение общей РНК из эндотелиальных клеток при помощи коммерческого набора RNeasy Plus Universal Mini Kit (Qiagen, Германия) по протоколу производителя. Количество и чистота выделенной РНК определяли на спектрофотометре NanoDrop 2000 (Thermo Scientific, США), а ее качество – на флуориметре Qubit
4 (Invitrogen, США) путем оценки индекса RIQ (RNA Integrity and Quality) с использованием набора реагентов Qubit RNA IQ Assay Kit (Invitrogen, США). Далее на основе выделенной РНК с помощью реакции обратной транскрипции и набора High Capacity cDNA Reverse Transcription Kit (Applied Biosystems, США) была синтезирована молекула комплиментарной ДНК (кДНК). Генная экспрессия оценивалась с помощью метода кПЦР с использованием SYBR Green праймеров, изготовленных компанией ЗАО «Евроген» (Москва, Россия), на амплификаторе ViiA 7 (Applied Biosystems, США). Нормирование результатов ПЦР проводилось с помощью трех референсных генов на ампли-фикаторе ViiA 7 (Applied Biosystems, США), таблица 2.
Таблица 2. Характеристика праймеров, использованных для оценки генной экспрессии
Table 2. Characteristics of primers used for gene expression assessment
|
Праймер Primer |
Последовательность Sequence |
|
POT1 |
F:GCAAAAGGAGTATTCTAACAAACAG R:TCACGCTTACACCAAAATCG |
|
TERT |
F:TTTCTGGAGCTGGTTGGGAA R:GAAGAGCCTGAGCAGCTCGA |
|
HPRT1 |
F:TTGCTTTCCTTGGTCAGGCA R:TCGTGGGGTCCTTTTCACCA |
|
GAPDH |
F:AGCCACATCGCTCAGACAC R:GCCCAATACGACCAAATCC |
|
B2M |
F:TCCATCCGACATTGAAGTTG R:CGGCAGGCATACTCATCTT |
Примечание: F – прямой праймер, R – обратный праймер.
Note: F – forward primer, R – reverse primer.
Методика приготовления реакционной смеси и программа амплификации были аналогичны описанным в разделе по оценке ОДТ. Уровень экспрессии генов POT1 и TERT рассчитывали по методу ΔCt (Уровень экспрессии = 2Ct [среднее геометрическое референсных генов] -Ct [ген интереса]) и выражали в виде условных единиц (у. е.). Оценку генной экспрессии проводили в строгом соответствии с существующими стандартами [11].
Статистический анализ результатов исследования выполняли в программе StatSoft STATISTICA 10. Для количественных показателей рассчитывали медиану ( m ) и межквартильный размах (IQR), сравнение двух независимых групп проводили с помощью U- критерия Манна – Уитни. Различия между группами считали статистически значимыми при значениях p < 0,05.
Результаты
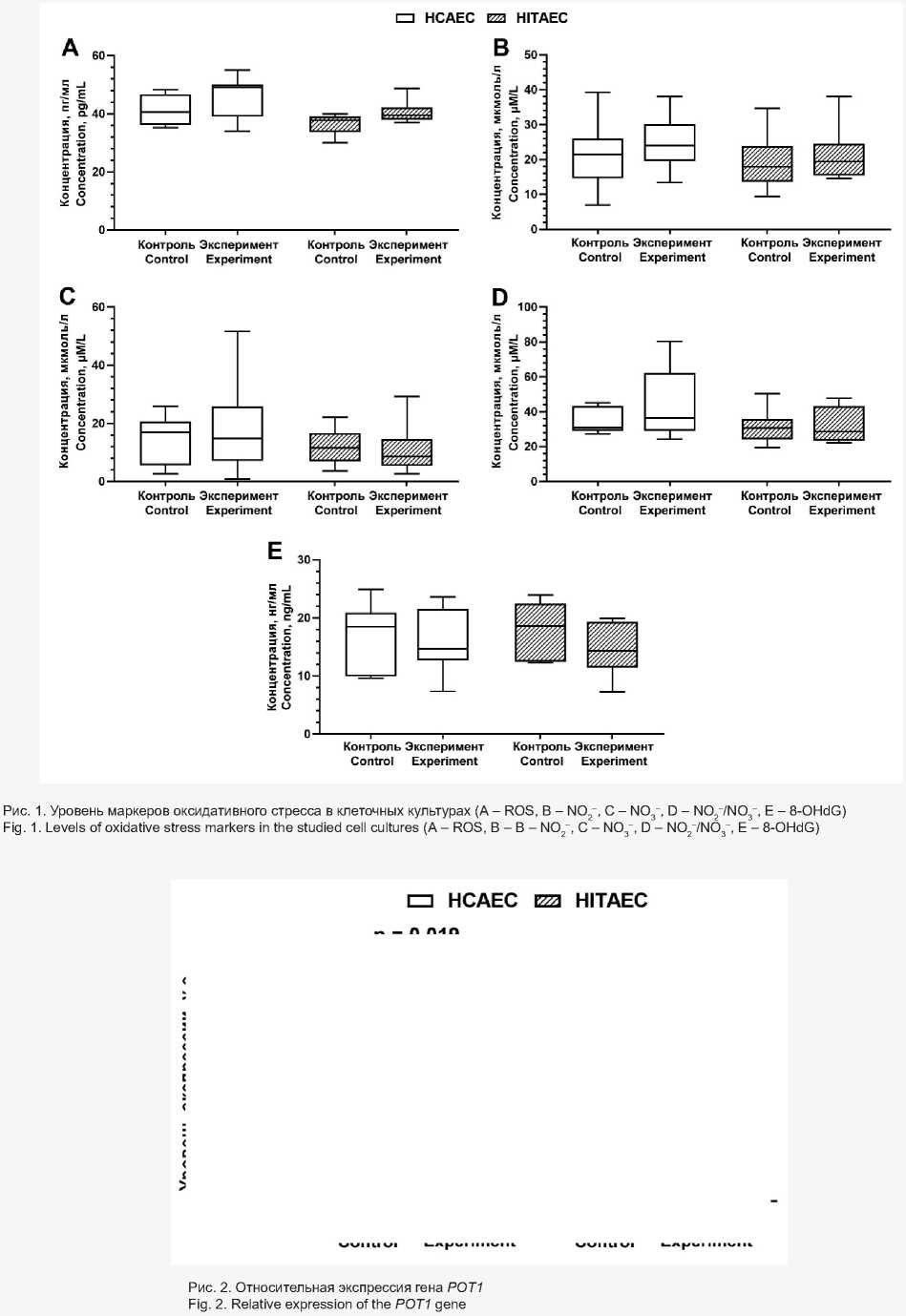
В результате оценки уровня маркеров оксидативно-го стресса в клеточных культурах, таких как ROS, NO2–, NO3–, NO2–/NO3– и 8-OHdG, не обнаружено статистически значимого изменения изученных показателей в клетках HCAEC и HITAEC, экспонированных ММС, по сравнению с контрольной группой (рис. 1).
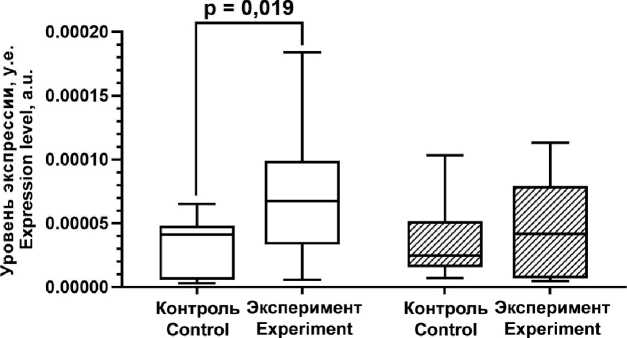
Одновременно с этим в экспонированных ММС клетках HCAEC и HITAEC было отмечено уменьшение ОДТ по сравнению с неэкспонированным контролем (10,97 против 27,03 в клетках HCAEC, p = 0,002 и 9,12 против 25,64 в клетках HITAEC, p = 0,001). Кроме того, в клетках HCAEC было обнаружено статистически значимое 1,75-кратное увеличение уровня экспрессии гена POT1 (Protection Of
Telomeres 1) на уровне p = 0,019, в то время как в клетках HITAEC данный ген экспрессировался на одинаковом уровне и в экспериментальной, и в контрольной группах (рис. 2). Ген TERT (Telomerase Reverse Transcriptase) в изученных клеточных культурах не экспрессировался.
Обсуждение
Вместе с тем токсическое действие ММС на биологические молекулы, в том числе и на ДНК, может проявляться и посредством активации оксидативного стресса, в результате чего происходит образование гидроксильного радикала (•OH), который вовлечен в большинство путей оксидативного повреждения молекулы ДНК [13]. Образование •OH зачастую сопровождается активацией NO-синтаз, стимулирующих образование оксида азота (•NO), который может взаимодействовать с анион-ради-калом с образованием достаточно мощного окислителя пероксинитрита (ONOO-), относящегося к реактивным формам азота и также участвующего в повреждении ДНК [14]. Для оценки свободнорадикального повреждения ДНК наиболее часто используется такой маркер, как 8-OHdG [15].
В результате проведенного нами исследования в эндотелиальных клетках различных артерий, in vitro экспонированных мутагеном алкилирующего механизма действия ММС, не выявлено повышения активных форм кислорода, реактивных форм азота и 8-OHdG по сравнению с неэкспонированным контролем. Вместе с тем существующие исследования на моделях лабораторных животных показывают, что пораженная атеросклерозом аорта характеризуется уменьшением уровня оксидатив-ных повреждений ДНК от интимы к адвентиции, при этом в интиме уровень 8-OHdG в 2,8 раза выше, чем в медии, что объясняется хронической экспозицией эндотелиального монослоя сосудов мутагенами окружающей среды, циркулирующими в кровотоке [5].
Несмотря на отсутствие повышения уровня свободных радикалов в экспонированных ММС клеточных культурах, в нашем эксперименте было обнаружено значительное снижение ОДТ эндотелиальных клеток из экспериментальной группы. Длина теломер поддерживается за счет фермента теломеразы, кодируемого геном TERT . Показано, что изменение длины теломер ассоциировано с воспалением и оксидативным стрессом [16].
Оксидативный стресс способствует разрушению теломерных участков хромосом в процессе клеточного деления in vitro и также стимулирует выработку провоспалительных цитокинов [17]. Интересно, что в нашем эксперименте в экспонированных ММС эндотелиальных клетках наблюдается снижение ОДТ с одновременным отсутствием выраженного оксидативного стресса (уровень активных форм кислорода, реактивных форм азота и 8-OHdG в экспериментальной и контрольной группах находился на одном и том же уровне). Вероятным объяснением этого может служить деградация теломерных участков ДНК в результате прямого действия ММС, а также воздействие на теломеры провоспалительных цитокинов, активно синтезирующихся в результате экспозиции клеточных культур ММС и участвующих в клеточном старении, при котором также отмечается уменьшение длины теломер [18]. Наблюдаемое в экспонированных ММС клетках HCAEC (более чувствительных к действию ММС в сравнении с клетками HITAEC) повышение экспрессии гена POT1, кодирующего белок, защищающий теломеры от повреждения за счет подавления ATR-сигнального пути и привлечения теломеразы к теломерам для их восстановления [19], вероятно, является компенсаторным механизмом на действие мутагена, играющим важную физиологическую роль, заключающуюся в поддержании стабильности хромосом эндотелиальных клеток, культивируемых в условиях генотоксической нагрузки. Необходимо отметить, что нам не удалось оценить экспрессию гена TERT в изученных группах, что, вероятно, связанно с чрезвычайно низким уровнем экспрессии теломеразы в зрелых клетках [20].
Следует отметить, что представленное исследование имеет ряд ограничений. В частности, результаты, полученные в ходе эксперимента in vitro , должны быть проверены в экспериментах на лабораторных животных для того, чтобы смоделировать изучаемые эффекты не только в клеточных культурах, но и в условиях живого организма. Использование in vivo моделей позволит смоделировать хроническую экспозицию клеток мутагеном.
Заключение
В результате проведения исследования установлено, что мутаген алкилирующего механизма действия ММС в эксперименте in vitro не вызывает выраженный оксидатив-ный стресс в культурах первичных эндотелиальных клеток человека. Формирование эндотелиальной дисфункции, ассоциированной с экспозицией клеток ММС, обусловлено, главным образом, генотоксическим стрессом, связанным с алкилированием ДНК эндотелиальных клеток.
Список литературы Уровень оксидативного стресса в эндотелиальных клетках, культивируемых в присутствии митомицина С
- Global, regional, and national age-sex-specific mortality for 282 causes of death in 195 countries and territories, 1980-2017: A systematic analysis for the Global Burden of Disease Study 2017. Lancet. 2018;392(10159):1736-1788. DOI: 10.1016/S0140-6736(18)32203-7.
- Libby P. The changing landscape of atherosclerosis. Nature. 2021;592(7855):524-533. DOI: 10.1038/s41586-021-03392-8.
- Кутихин А.Г., Синицкий М.Ю., Понасенко А.В. Роль мутагенеза в развитии атеросклероза. Комплексные проблемы сердечно-сосуди-стыхзаболеваний. 2017;(1):92-101. DOI: 10.17802/2306-1278-20171-92-101. Kutikhin A.G., Sinitsky M.Y., Ponasenko A.V. The role of mutagenesis in atherosclerosis. Complex Issues of Cardiovascular Diseases. 2017;(1):92-101. (In Russ.). DOI: 10.17802/2306-1278-2017-1-92-101.
- Borghini A., Cervelli T., Galli A., Andreassi M.G. DNA modifications in atherosclerosis: From the past to the future. Atherosclerosis. 2013;230(2):202-209. DOI: 10.1016/j.atherosclerosis.2013.07.038.
- Nair J., De Flora S., Izzotti A., Bartsch H. Lipid peroxidation-derived etheno-DNA adducts in human atherosclerotic lesions. Mutat. Res. 2007;621(1-2):95-105. DOI: 10.1016/j.mrfmmm.2007.02.013.
- Синицкий М.Ю., Цепокина А.В., Кутихин А.Г., Шишкова Д.К., Понасенко А.В. Профиль генной экспрессии в эндотелиальных клетках, культивируемых в присутствии митомицина С. Биомедицинская химия. 2021;67(3):130-136. DOI: 10.18097/PBMC20216702130. Sinitsky M.Y., Tsepokina A.V., Kutikhin A.G., Shishkova D.K., Ponasenko A.V. The gene expression signature in endothelial cells exposed to mitomycin C. Biomedical Chemistry. 2021;67(3):130-136. (In Russ.). DOI: 10.18097/PBMC20216702130.
- Lee Y.J., Park S.J., Ciccone S.L., Kim C.R., Lee S.H. An in vivo analysis of MMC-induced DNA damage and its repair. Carcinogenesis. 2006;27(3):446-453. DOI: 10.1093/carcin/bgi254.
- Klaunig J.E., Wang Z., Pu X., Zhou S. Oxidative stress and oxidative damage in chemical carcinogenesis. Toxicol. Appl. Pharmacol. 2011;254(2):86-99. DOI: 10.1016/j.taap.2009.11.028.
- Sims F.H. A comparison of coronary and internal mammary arteries and implications of the results in the etiology of atherosclerosis. Am. Heart J. 1983;105(4):560-566.
- Cawthon R.M. Telomere measurement by quantitative PCR. Nucleic Acids Res. 2002;30(10):e47. DOI: 10.1093/nar/30.10.e47.
- Bustin S.A., Benes V., Garson J.A., Hellemans J., Huggett J., Kubista M. et al. The MIQE guidelines: Minimum information for publication of quantitative real-time PCR experiments. Clin. Chem. 2009;55(4):611-622. DOI: 10.1373/clinchem.2008.112797.
- Gnad-Vogt S.U., Hofheinz R.D., Saussele S., Kreil S., Willer A., Willeke F. et al. Pegylated liposomal doxorubicin and mitomycin C in combination with infusional 5-fluorouracil and sodium folinic acid in the treatment of advanced gastric cancer: Results of a phase II trial. Anticancer Drugs. 2005;16(4):435-440. DOI: 10.1097/00001813-200504000-00010.
- Cadet J., Davies K.J.A., Medeiros M.H., Di Mascio P., Wagner J.R. Formation and repair of oxidatively generated damage in cellular DNA. Free Radic. Biol. Med. 2017;107:13-34. DOI: 10.1016/j.freerad-biomed.2016.12.049.
- Radi R. Peroxynitrite, a stealthy biological oxidant. J. Biol. Chem. 2013;288(37):26464-26472. DOI: 10.1074/jbc.R113.472936.
- Shekaftik O.S., Nasirzadeh N. 8-Hydroxy-2'-deoxyguanosine (8-OHdG) as a biomarker of oxidative DNA damage induced by occupational exposure to nanomaterials: А systematic review. Nanotoxicology. 2021;15(6):850-864. DOI: 10.1080/17435390.2021.1936254.
- Kiecolt-Glaser J.K., Epel E.S., Belury M.A., Andridge R., Lin J., Glaser R. et al. Omega-3 fatty acids, oxidative stress, and leukocyte telomere length: A randomized controlled trial. Brain Behav. Immun. 2013;28:16-24. DOI: 10.1016/j.bbi.2012.09.004.
- Lipcsey M., Soderberg E., Basu S., Larsson A., Sjolin J., Astrom M. et al. F2-isoprostane, inflammation, cardiac function and oxygenation in the endotoxaemic pig. Prostaglandins Leukot. Essent. Fatty Acids. 2008;78(3):209-217. DOI: 10.1016/j.plefa.2008.01.006.
- Wang L., Yu X., Liu J.P. Telomere damage response and low-grade inflammation. Adv. Exp. Med. Biol. 2017;1024:213-224. DOI: 10.1007/978-981-10-5987-2_10.
- Aramburu T., Plucinsky S., Skordalakes E. POT1-TPP1 telomere length regulation and disease. Comput. Struct. Biotechnol. J. 2020;18:1939-1946. DOI: 10.1016/j.csbj.2020.06.040.
- Zvereva M.I., Shcherbakova D.M., Dontsova O.A. Telomerase: Structure, functions, and activity regulation. Biochemistry (Mosc.). 2010;75(13):1563-1583. DOI: 10.1134/s0006297910130055.


