Ускоренное отторжение иммуногенной опухоли у мышей при ингибировании активности индоламин-2,3-диоксигеназы этилпируватом
Автор: Васильева Е.Д., Каледин В.И., Николин В.П., Попова Н.А., Кирилюк И.А., Григорьев И.а
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 1 (49), 2012 года.
Бесплатный доступ
Индоламин-2,3-диоксигеназа (ИДО) - недавно обнаруженный фермент, который катаболизирует триптофан, что создает локаль- ный дефицит этой незаменимой аминокислоты и подавляет пролиферацию и функцию иммунных лимфоцитов в данном регионе. Поэтому ингибиторы активности ИДО могут способствовать преодолению иммунорезистентности опухолей. В эксперименте на мышах линии С3НА, иммунизированных несингенной опухолью Г-29, изучали влияние системного и местного введения ингиби- тора ИДО этилпирувата на частоту и скорость отторжения повторных трансплантатов Г-29. Оба способа введения этилпирувата увеличивали частоту и ускоряли регрессиию опухолей по сравнению с контролем. Таким образом, ингибиторы активности ИДО, ослабляющие иммунорезистентность опухолей, могут оказаться полезными в плане увеличения эффективности противоопухо- левой терапии.
Индоламин-2, 3-диоксигеназа, этилпируват, гепатома г-29, регрессия опухоли
Короткий адрес: https://sciup.org/14056184
IDR: 14056184 | УДК: 616-006:612.017.1:577.155]-092.9
Enhanced immunogenic tumor rejection in mice when inhibiting activity of indoleamine 2,3-dioxygenase with ethyl pyruvate
Indoleamine-2,3-dioxygenase (IDO) is a recently founded enzyme that catalyzes tryptophan, thus causing local deficiency of this essential amino acid and inhibiting proliferation and function of immune lymphocytes in the given region. Inhibitors of IDO activity, therefore, can contribute to tumor immunoresistance breaking. The influence of systemic and local administration of IDO inhibitor (ethyl pyruvate) on the frequency and the rate of rejection of H-29 repeated grafts was studied on C3HA-line mice immunized with H-29 tumor cells. Both methods of ethyl pyruvate administration increased the frequency and enhanced tumor regression as compared to the control. Thus, IDO activity inhibitors can be useful for increasing anti-tumor efficiency
Текст научной статьи Ускоренное отторжение иммуногенной опухоли у мышей при ингибировании активности индоламин-2,3-диоксигеназы этилпируватом
После того как в 1998 г. было показано, что неотторжение аллогенных зародышей материнским организмом каким-то образом связано с катаболизмом триптофана [13], появилось большое количество публикаций, посвященных изучению механизма этого явления. Было обнаружено, что присутствующий в клетках трофобласта фермент индоламин-2,3-диоксигеназа (ИДО), катаболи-зирующий триптофан по кинурениновому пути, создает его локальный дефицит при избытке ток- сичных для Т-лимфоцитов продуктов катаболизма [4, 11]. Экспериментальное подавление активности ИДО у беременных мышей приводило к отторжению аллогенных, но не сингенных зародышей [13]. Для онкологов эти исследования открывают путь к пониманию того, каким образом заведомо иммуногенные опухоли избегают или могут избегать иммунологической атаки со стороны организма. Действительно, оказалось, что ИДО экспрессируется в клетках многих опухолей и в инфильтрирующих их макрофагах, причем высокая активность фермента в этих случаях, как правило, ассоциируется с плохим прогнозом [6, 12, 14]. Ингибиторы активности ИДО сами по себе снижают скорость роста таких опухолей [15], а в сочетании с воздействием химиопрепаратов в ряде случаев усиливают терапевтический эффект последних [8]. В качестве ингибитора ИДО обычно используют синтетический аналог триптофана 1-метил-D-триптофан, который вводят хронически в суточной дозе до 800 мг/кг массы тела животных [8]. Поскольку для преодоления обусловленной ИДО иммунорезистентности опухоли необходимо подавить активность фермента только в ее клетках и в инфильтрирующих опухоль макрофагах, дозу ингибитора можно значительно снизить, если вводить препарат местно в зону опухоли. Кроме того, в последнее время обнаружен ряд новых соединений, способных ингибировать активность ИДО [7], среди которых наше внимание привлек применяющийся в клинике сравнительно дешевый и малотоксичный противовоспалительный агент этилпируват [5, 9, 10]. В представленной работе, выполненной на модели заведомо иммуногенной несингенной опухоли мышей, мы показали, что хроническое системное или местное введение этилпирувата в район локализации опухоли приводит к ее ускоренному отторжению по сравнению с контролем.
Материал и методы
В работе использованы мыши линии С3НА и перевиваемая опухоль Гепатокарцинома-29 (Г-29) [1]. Опухоль происходит от мыши линии СВА, но прививается у 100 % мышей линии С3HA, у значительной части которых в последующем прекращает рост и регрессирует. При подготовке эксперимента в мышцы бедра самцам С3НА трансплантировали по 5×105 клеток Г-29 и месяц особей, у которых опухоль прогрессивно росла, выбраковывали, а отторгнувшим опухоль иммунным мышам прививали ее повторно значительно большей дозой клеток (в 5, а потом и в 10 раз). После этого животных распределяли по 2 группам, мышам одной группы вводили для ингибирования ИДО этилпируват, другую использовали в качестве контроля.
В эксперименте с системным введением этилпи-рувата последний растворяли в физиологическом растворе Рингера (5 мг/мл) и вводили мышам по 0,2 мл внутрибрюшинно 2 раза в сут на протяжении
20 сут. Контрольным мышам физраствор не вводили. В опыте с местным применением 0,1 мл 1 % раствора этилпирувата вводили внутримышечно в район локализации опухолевых клеток 1 раз в день на протяжении первых 10 сут после перевивки опухоли. Контрольным животным аналогично вводили 0,1 мл физраствора. Опухоли периодически пальпировали, измеряли с помощью штангенциркуля и регистрировали момент их исчезновения. Эксперимент заканчивали через 10 сут после регрессии последней опухоли в опытной группе.
Достоверность различий между опытом и контролем по проценту мышей с регрессировавшими опухолями оценивали по φ-критерию с помощью arc sin-преобразования Фишера.
Результаты и обсуждение
В нашей предыдущей работе при первичной трансплантации опухоли ГА-1 несингенным мышам С3НА ингибирование ИДО 1-метил-D-триптофаном привело не к торможению, а к стимуляции ее роста [2]. Полученный эффект кажется парадоксальным, однако только на первый взгляд. Дело в том, что впервые трансплантированная опухоль развивается в условиях так называемой патологической иммунной привилегии [3], при которой иммунный ответ на новообразование имеет сложную природу и наряду с тормозящим может оказывать и стимулирующее влияние. В этом случае ингибирование ИДО может приводить к активации не только Т-киллеров и Т-хелперов, но и Т-регуляторов, способствующих формированию толерантности и, как следствие, усилению роста опухоли. Напротив, в клинической онкологии обычно имеют дело с опухолями, иммунологические отношения которых с организмом хозяина уже определились и которые с помощью ИДО подавляют только эффекторное звено иммунного ответа. Поэтому и в экспериментах, имеющих целью изучение возможности воздействия на рост опухолей с помощью ингибиторов ИДО, очевидно, следует использовать предыммунизированных животных.
В представленной работе мы выполнили такое исследование, использовав в качестве реципиентов опухоли мышей, которым эта опухоль была перевита ранее и у которых она отторглась. При планировании первого эксперимента перевили опухоль Г-29 40 интактным 4-месячным мышам линии С3HA в мышцы бедра дозой 5×105 клеток.
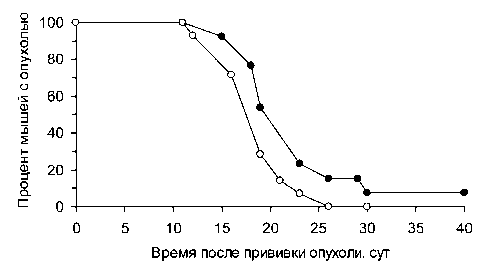
Рис. 1. Динамика регрессии трансплантатов опухоли Г-29 у мышей линии С3HA при системном введении ингибитора индоламин-2,3-диоксигеназы этилпирувата (светлые кружки) и в контроле (темные кружки)
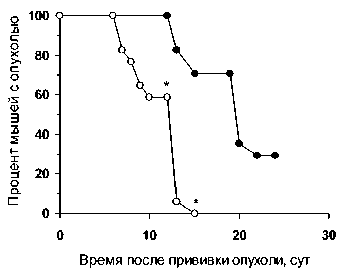
Рис. 2. Динамика регрессии трансплантатов опухоли Г-29 у мышей линии С3HA при местном введении ингибитора индоламин-2,3-диоксигеназы этилпирувата (светлые кружки) или физиологического раствора (темные кружки). Примечание: * – различия статистически значимы по сравнению с группой контроля (p<001)
Через неделю опухоли появились у всех животных, после чего у 13 из них они продолжали расти, а у 27 прекратили рост и постепенно регрессировали. Мышей с опухолями выбраковали, а всем животным, у которых опухоль отторглась, ее перевили повторно в то же бедро, но значительно (в 5 раз) большей дозой опухолевых клеток. Сразу после этого мышей разделили на 2 группы и 13 животных контрольной группы оставили без воздействия, а 14 подопытным стали 2 раза в сут вводить этилпи-руват, как описано в разделе «Материал и методы». Препарат вводили на протяжении 20 сут без перерывов; при разовой дозе 40 мг/кг это составило на курс около 1,6 г/кг массы тела животных. К 10-м сут после перевивки опухоли возникли у 100 % мышей обеих групп, после чего начали регресси- ровать – сначала (в течение 4 сут) с одинаковой, а затем с несколько большей скоростью в опыте по сравнению с контролем (рис. 1). К 26-м сут после перевивки в подопытной группе опухоли регрессировали у всех животных, тогда как в контрольной еще оставались 2 мыши с опухолями, из которых одна со временем регрессировала, а другая возобновила рост.
Через месяц после отторжения опухолей выживших мышей использовали повторно, для чего им трансплантировали еще большую, чем ранее (5×106), дозу клеток опухоли Г-29. После этого леченых и нелеченых мышей распределили поровну между опытной и контрольной группами нового эксперимента, добавив к ним по 4–5 появившихся к тому времени мышей с регрессировавшими опухолями, и начали лечение путем ежедневного местного введения этилпирувата или физраствора.
На 6-й день после перевивки опухоли появились у всех животных в обеих группах, при этом их средний объем был равен 0,30 ± 0,031 см3 в контроле и 0,20 ± 0,045 см3в опытной группе. Еще через 2 сут объем опухолей составлял – 0,23 ± 0,031 см3 и 0,15 ± 0,34 см3 соответственно (различия недостоверны). В дальнейшем опухоли постепенно уменьшались в обеих группах, но переставали прощупываться (полностью регрессировали) раньше и у большего числа мышей, которым вводили этилпируват, чем у контрольных животных (рис. 2). В обоих экспериментах этилпируват не оказывал на мышей сколько-нибудь заметного токсического действия, как при системном, так и при местном введении к концу курса масса их тела снизилась менее чем на 4 % по сравнению с исходной.
Таким образом, полученные результаты показывают, что у мышей, предыммунизированных опухолью, хроническое системное или местное введение этилпирувата в нетоксичной дозе приводит к ускоренному отторжению повторных трансплантатов этой опухоли. В настоящей работе (в особенности в первом эксперименте) мы применяли этилпируват по громоздкой схеме, применявшейся предложившими его в качестве ингибитора ИДО авторами [13]. Между тем в литературе имеется указание на то, что этилпируват используется как пищевая добавка, что предполагает сохранение по крайней мере какой-то его активности при приеме per os. Необходимо выяснить, относится ли это к способности этилпирувата ингибировать активность
ИДО, или эта способность проявляется только при парентеральном введении препарата. В дальнейшем нужно сосредоточиться на выяснении вопроса о возможности и перспективах использования его (и/или других ингибиторов ИДО) в сочетании с применяющимися в клинике препаратами для терапии опухолей.


