Успешное применение ресинхронизирующей терапии в лечении вторичной (аритмогенной) дилатационной кардиомиопатии у детей младшего возраста после кардиохирургических вмешательств
Автор: Кандинский Максим Леонидович, Ефимочкин Григорий Алексеевич, Латкин Михаил Владимирович, Клычева Оксана Валерьевна, Кохтычева Оксана Владимировна, Таран Елена Александровна, Борисков Максим Валентинович, Порханов Владимир Алексеевич
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Случай из практики
Статья в выпуске: 1 т.30, 2015 года.
Бесплатный доступ
Представлен клинический случай успешной имплантации кардиоресинхронизатора (CRT-P). Детям младшего возраста была проведена хирургическая коррекция врожденного порока сердца дефекта межжелудочковой перегородки (ДМЖП). В связи с развившейся интраоперационно полной поперечной блокадой сердца имплантирован искусственный водитель ритма (ИВР). В дальнейшем прогрессирующая дилатация полостей сердца, снижение фракции выброса левого желудочка (ФВ ЛЖ), отсутствие эффекта от медикаментозной терапии и нарастание явлений сердечной недостаточности потребовали имплантации CRT-P.
Ресинхронизирующая терапия, аритмогенная дилатационная кардиомиопатия, дети младшего возраста, кардиохирургические вмешательства
Короткий адрес: https://sciup.org/14919995
IDR: 14919995 | УДК: 616.12-008.313.2
Successful cardiac resynchronization therapy for treatment of secondary (arrhythmogenic) dilated cardiomyopathy in young children after cardiac surgery
The article presents clinical cases of successful implantation of cardiac resynchronization device (CRT-P). Young children received surgical correction of congenital ventricular septal defect (VSD). Due to the intraoperative development of complete atrioventricular heart block, the electric cardiac pacemaker (ECP) was implanted. The following progression of dilatation of the cardiac cavities, decrease in the left ventricular ejection fraction (LV EF), inefficacy of drug therapy, and the worsening of heart failure required CRT-P implantation.
Текст научной статьи Успешное применение ресинхронизирующей терапии в лечении вторичной (аритмогенной) дилатационной кардиомиопатии у детей младшего возраста после кардиохирургических вмешательств
Вторичная дилатационная (аритмогенная) кардиомиопатия у детей после имплантации ИВР встречается достаточно редко. В мультицентровом исследовании Американского колледжа кардиологов [1] у 27 пациентов из 73 после предшествующего кардиохирургического вмешательства развилась полная поперечная блокада, которая потребовала имплантации ИВР, и 11 из них в последующем потребовалась имплантация CRT–P. Критерии имплантации были типичны: выраженные нарушения функции системного желудочка (снижение фракции выброса в динамике ниже 35%) и удлинение интервала QRS более 120 мс [2]. Основным исследованием в определении показаний для имплантации CRT–P служит эхокардиография (исследование PROSPECT Европейского общества кардиологов) [3], хотя и оно указывает на то, что очень важна грамотная оценка состояния пациента в динамике.
Мы описываем двух пациентов: 15 мес. (больной Р., мальчик) и 34 мес. (больная У., девочка), сопоставимого веса (5,6 и 7 кг соответственно), которым выполнялись операции по поводу ДМЖП в возрасте 5 и 7 мес. соответ- ственно. Анатомия порока в обоих случаях сходна: ДМЖП перимембранозный приточный, прикрыт структурами трикуспидального клапана, размером 8 мм, с хорошими показателями сердечной деятельности: до операции ФВ ЛЖ у обоих больных более 65%, умеренная дилатация ЛЖ – конечный диастолический размер (КДР) ЛЖ 29 и 26 мм соответственно. В обоих случаях выполнено типичное оперативное вмешательство: стандартное искусственное кровообращение (ИК), стандартное время ИК (41 и 62 мин), стандартное время ишемии миокарда (20 и 25 мин), для защиты миокарда на время пережатия аорты использовался стандартный раствор “Кустодиол” 20 мл/ кг. У обоих пациентов полная поперечная блокада развилась интраоперационно, эпизодов восстановления проведения по атриовентрикулярному (АВ) соединению не было. В обоих случаях проводилась временная предсердно-желудочковая электрокардиостимуляция (ЭКС) в течение 7 суток, периодов изменения характера нарушений ритма не отмечалось, сохранялась постоянная полная поперечная АВ-блокада. Обоим пациентам на 7-е сутки после первичной операции был имплантирован двух-
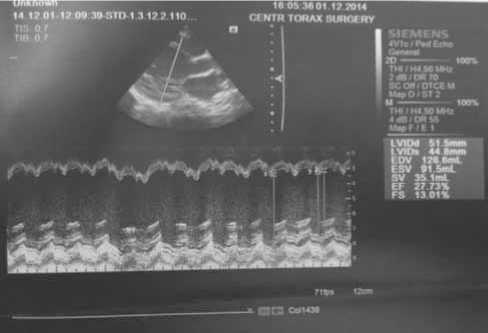
Рис. 1. Эхо-КС сканы пациента У. до имплантации CRT-P
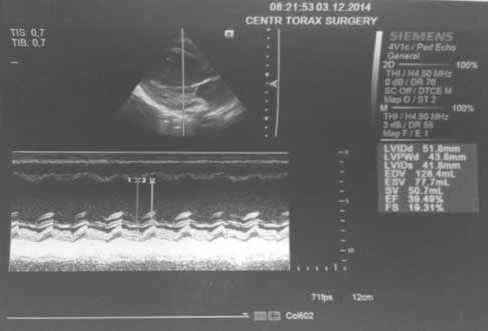
Рис. 2. Эхо-КС сканы пациента У. после имплантации CRT-P
камерный частотно-адаптивный электрокардиостимулятор Altrua S502 DR (Boston Scientific) в режиме DDDR. Данные эхокардиоскопии (Эхо-КС) на момент выписки из стационара были идентичны: ФВ ЛЖ – более 65%, отсутствовала дилатация ЛЖ, в обоих случаях имел место дискинез межжелудочковой перегородки.
У пациентки У. на контрольном осмотре через 9 мес. после оперативного лечения жалоб не было, по данным Эхо-КС, ФВ ЛЖ – 75%, КДР ЛЖ – 26 мм (норма), сохранялся дискинез МЖП; при тестировании ЭКС нарушений в работе стимулятора не выявлено, порог стимуляции предсердного электрода 1,4 В, желудочкого – 1,0 В. Через 10 мес. после операции появились жалобы на утомляемость, по данным Эхо-КС, ФВ ЛЖ – 75%, КДР ЛЖ – 35 мм (дилатирован), выраженный дискинез МЖП; при тестировании ЭКС нарушений в работе стимулятора не выявлено, пороги стимуляции прежние. Учитывая дилатацию ЛЖ, режим стимуляции изменен на VVIR. При осмотре через 11 мес. после операции жалоб нет, по данным Эхо-КС, ФВ ЛЖ – 75%, КДР ЛЖ – 43 мм (прогрессирующая дилатация), выраженный дискинез МЖП; при тестировании ЭКС нарушений в работе стимулятора не выявлено, порог стимуляции предсердий – 1,4 В, желудочков – 0,9 В. Учитывая отсутствие эффекта от смены режима стимуляции, возвращен режим DDDR. В динамике наблюдения через 14 мес. после операции жалоб нет, по данным Эхо-КС, ФВ ЛЖ – 63% (верхняя граница нормы), КДР ЛЖ – 45 мм (прогрессирующая дилатация), выраженный дискинез МЖП, появилась недостаточность на трикуспидальном клапане; при тестировании ЭКС нарушений в работе стимулятора не выявлено, порог стимуляции предсердий – 1,8 В, желудочков – 1,2 В (V). На контрольном осмотре через 25 мес. после операции жалобы на одышку в горизонтальном положении, потливость, утомляемость, по данным Эхо-КС, ФВ ЛЖ снижена до 50%, КДР ЛЖ – 53 мм (прогрессирующая дилатация), КДО ЛЖ – 139 мл, дилатация ЛП – до 30 мм, выраженный диски-нез МЖП; при тестировании ЭКС нарушений в работе стимулятора не выявлено, порог стимуляции желудочков – 1,5 В, порог стимуляции предсердий – 1,0 В (V). Учитывая клинику сердечной недостаточности, больной назначена медикаментозная терапия – дигоксин, спиронолактон, каптоприл. На контрольном осмотре через 26 мес.
после операции сохранялись прежние жалобы, на фоне медикаментозной терапии без динамики, по данным Эхо-КС, ФВ ЛЖ критически снижена до 27%, КДР ЛЖ – 54 мм (выраженная дилатация), КДО ЛЖ – 134 мл, дилатация ЛП – до 35 мм, выраженный дискинез МЖП; при тестировании ЭКС нарушений в работе стимулятора не выявлено. Учитывая отсутствие эффекта от медикаментозной терапии и нарастание явлений сердечной недостаточности, принято решение о проведении кардиоресинхрони-зирующей терапии. Выставлен диагноз: Вторичная (арит-могенная) дилатационная кардиомиопатия со снижением глобальной сократимости ЛЖ.
Через 27 мес. после первичной пластики межжелудочкового дефекта из переднебоковой торакотомии в бессосудистой зоне ЛЖ имплантирован электрод MyoDextm 108T (St. Jude Medical) – 54 cм, в ложе предыдущего ЭКС установлен CRT-P Consulta™ C3TR01(Medtronic) DR в режиме biDDDR.
Через 3 дня после начала ресинхронизирующей терапии исчезли жалобы, эхокардиоскопия через 7 суток после операции выявила уменьшение степени дилатации ЛЖ (КДР 48 мм) и повышение ФВ ЛЖ до 39% (рис. 1, 2).
Ухудшение состояния пациента Р. произошло в более короткий срок. На контрольном осмотре через 1,5 мес. после оперативного лечения жалоб не было, по данным Эхо-КС, умеренно снижена ФВ ЛЖ – 55%, КДР ЛЖ – 32 мм (умеренно дилатирован), отмечается дискинез МЖП; при тестировании ЭКС нарушений в работе стимулятора не выявлено, порог стимуляции предсердий 0,8 В, желудочков – 0,8 В. Через 4 мес. после операции картина была полностью идентична, но на следующем плановом осмотре через 10 мес. после первичной операции выявлена резкая дилатация ЛЖ (КДР 57 мм), снижение ФВ ЛЖ до 50% и увеличение КДО ЛЖ до 159 (!!!) мл. Назначена медикаментозная терапия, рекомендован следующий осмотр через 1 мес., однако на 18-е сутки больной поступил в экстренном порядке с клиникой декомпенсированной сердечной недостаточности в НИИ-ККБ № 1. При Эхо-КС выявлено резкое снижение ФВ ЛЖ до 32%, прогрессирование степени дилатации ЛЖ до 58 мм; отмечался выраженный дискинез МЖП и появление недостаточности на трикуспидальном клапане 2–3-й степени с градиентом 40–45 мм рт. ст. Выставлен диагноз: Вторич-
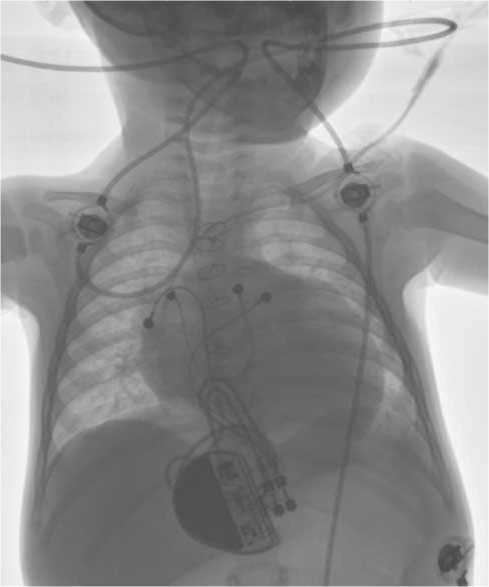
Рис. 3. Рентгенограммы пациента Р. с имплантированным двухкамерным ЭКС
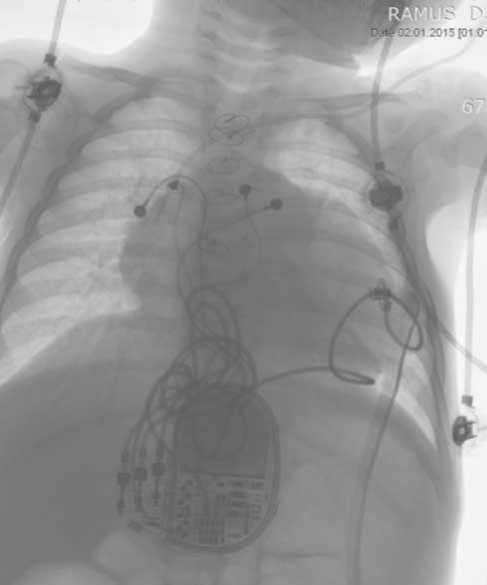
Рис. 4. Рентгенограммы пациента Р. после смены на CRT-P
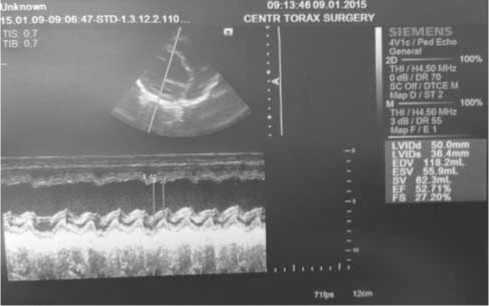
Рис. 6. Эхо-КС сканы пациента Р. после имплантации CRT-P
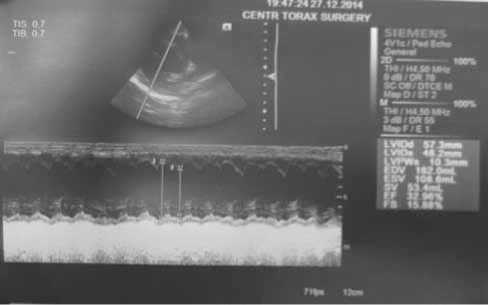
Рис. 5. Эхо-КС сканы пациента Р. до имплантации CRT-P
ная (аритмогенная) дилатационная кардиомиопатия со снижением глобальной сократимости ЛЖ, умеренная легочная гипертензия. Как и в первом случае, принято решение о проведении кардиоресинхронизирующей терапии.
Через 10 мес. после первичной пластики межжелудочкового дефекта из переднебоковой торакотомии в бессосудистой зоне ЛЖ имплантирован электрод MyoDextm 108T(St. Jude Medical) – 54 cм, в ложе предыдущего ЭКС установлен CRT-P Consulta™ C3TR01 (Medtronic) DR в режиме biDDDR.
Через 8 суток после начала ресинхронизирующей терапии исчезли жалобы, Эхо-КС на 12-е сутки после операции выявила уменьшение степени дилатации ЛЖ (КДР 43 мм) и повышение ФВ ЛЖ до 52% (рис. 3–6).
Почему же мы решили столь подробно описать историю заболевания каждого ребенка? С той лишь целью, чтобы показать полную независимость времени декомпенсации от исходного состояния больного, сроков динамического наблюдения, режима и состояния ЭКС, степени дилатации желудочка и уровня снижения ФВ. Как видно из вышеприведенного описания, резкое падение ФВ с появлением клиники заболевания возможно, по сути, в любое время и у любого больного с ятрогенной полной поперечной блокадой и имплантированным электрокардиостимулятором. В этом свете, возможно, стоит расши- рить показания к более раннему началу кардиоресинх-ронизирующей терапии, а не ждать падения ФВ ЛЖ до критических 30–35%? По достижении этого значения степень дилатации ЛЖ является запредельной, и ожидать восстановления размеров левого сердца до возрастной нормы, по меньшей мере, не оправданно. Более того, единственной альтернативой у таких пациентов является трансплантация сердца, что в нашей стране сопряжено со значительными трудностями. Имеющиеся 5- и 10летние результаты наблюдения пациентов показывают [4, 5], что трансплантация требуется в этот период времени незначительному их количеству, более того, кардиоресин-хронизирующая терапия применяется и после трансплантации сердца для улучшения функции миокарда.
Мы считаем, что данная методика позволяет преодолеть критическую декомпенсированную сердечную недостаточность и является хорошей альтернативой единственному возможному кардиохирургическому методу помощи таким детям – трансплантации сердца. Возраст пациента также не является ограничивающим фактором.
Список литературы Успешное применение ресинхронизирующей терапии в лечении вторичной (аритмогенной) дилатационной кардиомиопатии у детей младшего возраста после кардиохирургических вмешательств
- Dubin A.M., Janousek J., Rhee E. et al. Resynchronization therapy in pediatric and congenital heart disease patients. An International MultiCenter Study//J. Am. Coll. Cardiology. -2005. -Vol. 46, No. 12. -P. 2277-2283.
- Avari J.N., Rhee E.K. Cardiac resynchronization therapy for pediatric heart failure//Heart Rhythm. -2008. -Vol. 5, No. 10. -P. 1476-1478.
- Cleland J.G., Abdellah A.T., Khaleva O. et al. Clinical trials update from the European Society of Cardiology Congress 2007: 3CPO, ALOFT, PROSPECT and statins for heart failure//Eur. J. Heart Fail. -2007. -Vol. 9. -P. 1070-1073.
- Cecchin F., Frangini P.A., Brown D.W. et al. Cardiac resynchronization therapy (and multisite pacing) in pediatrics and congenital heart disease: five years experience in a single institution//J. Cardiovasc. Electrophysiol. -2009. -Vol. 20. -P. 58-65.
- Thamboa J.-B., Santosb P.D., Bordacharb P. Cardiac resynchronization therapy in patients with congenital heart disease//Arch. Cardiovasc. Disease. -2011. -Vol. 104. -P. 410-416.


